原發骨髓大B細胞淋巴瘤一例并文獻復習
郭淑萍 金 鑫 陳志爐 蔣慧芳
原發骨髓淋巴瘤(primary bone marrow lymphoma,PBML)臨床上較為罕見,主要表現為淋巴瘤侵犯骨髓而無全身淋巴結腫大及其他結外器官受累。由于該病起病急、臨床表現不典型,診斷難度大,對臨床及病理醫生均具有一定的挑戰。原發骨髓大B細胞淋巴瘤則更罕見,目前尚無統一的專家治療共識。現將本院血液科確診并獲得理想療效的1例原發骨髓大B細胞淋巴瘤的診治情況報道如下。
1 病例資料
患者,女,48歲。2016年11月28日因婦科檢查前查血常規提示:白細胞8.9×109/L,中性粒細胞百分比24.2%,單核細胞百分比31.4%,嗜堿粒細胞百分比17.7%,血紅蛋白109g/L,血小板238×109/L,鏡檢看到幼稚細胞。患者無發熱,無乏力,無牙齦出血,無咳嗽咳痰,無胸悶氣急等不適。查體:輕度貧血貌,余查體未見明顯異常。肝腎功能正常,超聲心動圖檢查未見明顯異常。2016年11月29日行骨髓常規(插頁圖1):骨髓增生活躍;淋巴細胞系統增生活躍,可見一類形態明顯異常的淋巴細胞,約占10%,考慮淋巴瘤細胞可能;全片巨核細胞38個,其中產血小板巨核細胞10個,產血小板板功能可。骨髓常規結論:涂片可見一類異常細胞,形態學考慮淋巴系統腫瘤可能;骨髓免疫分型(插頁圖2):CD45設門中可見一群CD45高表達,SSC大、FSC大細胞群,占10.62%,主要表達 CD19、CD20、CD22、DR、CD25、FMC7,限制性表達輕鏈LAM;結論:CD45設門可見異常B淋巴細胞,考慮大B細胞腫瘤。骨髓活檢病理(插頁圖3):骨髓造血組織增生活躍,粒紅比例尚可,紅系各期可見,粒系多為中晚幼及桿狀核,巨核細胞及少量分化成熟的漿細胞散在排列,另見少量異形的淋巴細胞呈小簇狀排列,特殊染色無殊,免疫組化:CD3(-),CD20(+),PAX-5(+),CD79α(+),CD235α(-),CD138(-),MPO(-),CyclinD1(-)。結論:(骨髓活檢)骨髓造血組織增生活躍,伴見少量異形的B淋巴細胞,結合臨床首先考慮B細胞淋巴瘤累及骨髓。外周血細胞學分析:CD45設門中可見一群CD45高表達,側散射(SSC)大、前散射(FSC)大細胞群 20.45%,主要表達CD19、CD20、CD22,限制性表達輕鏈LAM,考慮大B細胞腫瘤。急淋常見15種融合基因(dupMLL,MLL/AF4,MLL/AF6,BCR/ABL(p190),MLL/AF1P,MLL/AFX,MLL/ENL,BCR/ABL(p210),E2A/PBX1,TEL/AML1,SIL/TAL1,TLS/ERG,E2A/HLF,TEL/ABL,HOX11)均陰性。熒光原位雜交(FISH)檢查:IGH基因位點擴增陽性,C-MYC基因位點重排陽性,BCL-2、BCL-6基因檢測結果均為陰性。骨髓染色體檢查:46,XX。Ig基因重排:檢測到 IgVH、IgK 和IgL基因發生重排。雙側頸部、雙側鎖骨上、雙側腋下、雙側腹股溝及腹膜后B超未見明顯腫大淋巴結。2016年12月1日浙江省醫學檢查診療中心全身PET-CT檢查:(1)掃描區域全身彌漫性氟脫氧葡萄糖(FDG)代謝增高,標準攝入值(SUV)最大值約4.2,未見明顯骨質破壞,結合病理,淋巴瘤浸潤考慮;(2)雙側頸部多發淋巴結,FDG代謝輕度增高,首先考慮炎性病變。患者診斷大B細胞淋巴瘤(原發骨髓),Ann Arbor分期:IVA期,年齡調整的國際預后指數(aaIPI)評分:1分。
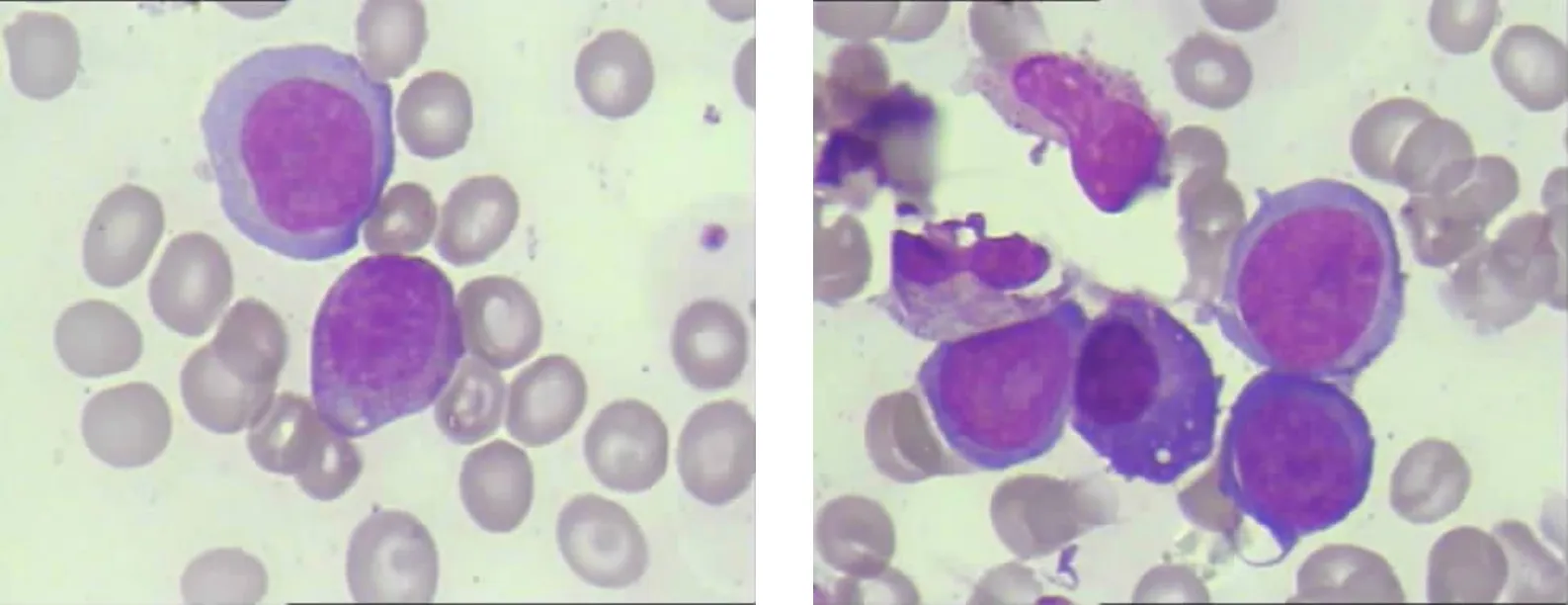
圖1 原發骨髓的大B細胞淋巴瘤患者骨髓常規涂片結果:骨髓增生活躍,淋巴細胞系統增生活躍,可見一類形態明顯異常的淋巴細胞,該類細胞胞體大,胞漿豐富,著色淡藍,漿中未見明顯顆粒,核染色質均勻,部分可見模糊核仁,考慮淋巴瘤細胞可能。(瑞特-吉姆薩染色 ×400)
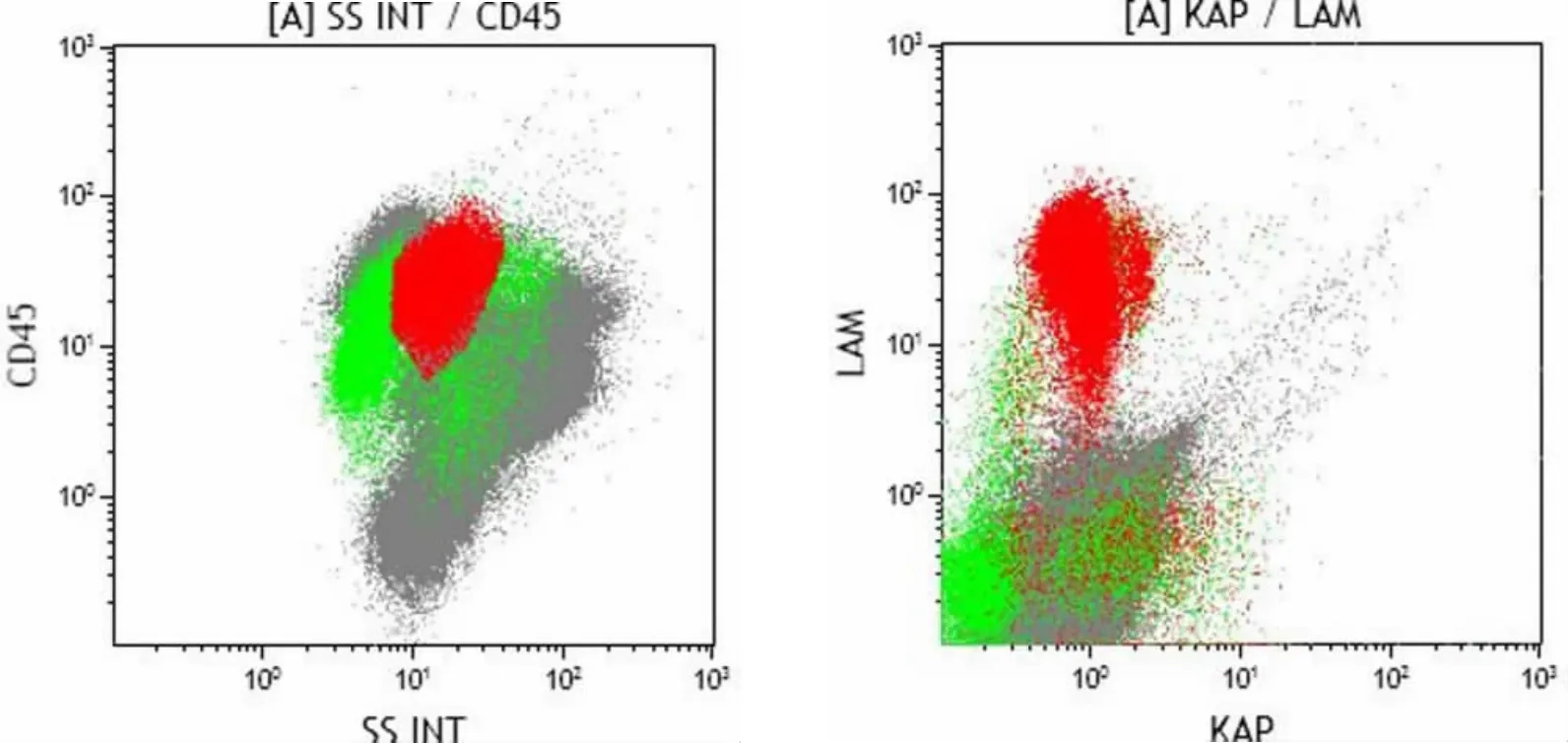
圖2 原發骨髓的大B細胞淋巴瘤患者骨髓免疫分型:CD45設門中可見一群CD45高表達,SCC大、FSC大的細胞群,占10.62%,在所檢測抗原中主要表達CD19,CD20,CD22,DR,CD25,FMC7,限制性表達輕鏈LAM,考慮B細胞腫瘤。
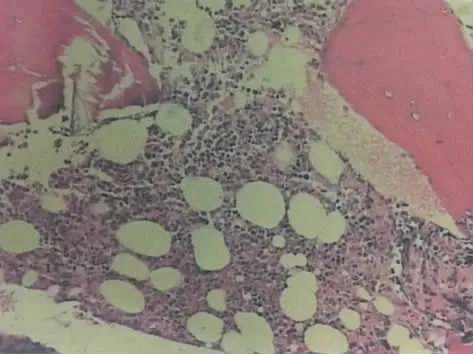
圖3 原發骨髓的大B細胞淋巴瘤患者骨髓活檢病理結果:骨髓造血組織活躍,粒紅比例尚可,紅系各期可見,粒系多為中晚幼及桿狀核,巨核細胞及少量分化成熟的漿細胞散在排列,另見少量異形的淋巴細胞呈小簇狀排列,特色染色無殊,免疫組化:CD3(-),CD20(+),CD79a(+),CD235α(-),CD138(-),MPO(-),CyclinD1(-)。(瑞氏染色及免疫組化染色 ×400)
2016年12月7日開始給予患者R-CHOP方案,具體用藥:美羅華600mg d0+環磷酰胺1000mg d1+長春地辛4mg d1+多柔比星(阿霉素)70mg d1+潑尼松90mg d1-5,化療后血象恢復正常,復查骨髓提示緩解。2017年1月5日再次給予患者R-CHOP方案化療(劑量及用法同上),患者化療后出現胸悶氣急,考慮化療藥物相關,完善冠脈CTA示右冠狀動脈近段、左前降支近段非鈣化斑塊,相應管腔輕度狹窄。2017年2月11日行第3次R-CHOP方案化療(考慮患者冠狀動脈粥樣硬化,更改阿霉素為脂質體阿霉素40mg d1,余同前),化療過程順利。2017年3月7日復查骨髓穿刺常規提示:骨髓增生明顯活躍,淋巴細胞系統增生欠活躍,分類200細胞中未見形態明顯異常的淋巴細胞。免疫分型提示:殘留腫瘤細胞<0.01%。骨髓活檢提示:骨髓造血組織增生活躍,粒紅比例增大,紅系各期可見,粒系多為中晚幼及桿狀核、巨核細胞及少量分化成熟的淋巴漿細胞散在排列。特殊染色無殊。(骨髓活檢)骨髓造血組織增生活躍。免疫組化:CD3(-),CD20(-),CD45RO(+),CD79α(+),CD235α(+),CD138(+),MPO(+)。患者經濟情況一般,胸悶氣促未再發作,不予以脂質體阿霉素化療。2017年3月15日給予患者行第4次化療,更改為R-EPOCH方案,具體用藥:利妥昔單抗600mg d0+依托泊苷40mg q12h+多柔比星15mg d1-4+環磷酰胺1.1g d5+強的松100mg d1-5。患者此次化療后骨髓抑制期較長,故第5次化療時間延遲至2017年5月2日行第5周期R-EPOCH方案,劑量同第4周期。2017年6月7日行第6周期REPOCH化療,劑量同上,化療后評估病情緩解。患者目前疾病確診1.5年,化療6個周期后,療效評估完全緩解(CR),到目前化療結束接近1年,每3月復查病情穩定,無淋巴瘤復發跡象。
2 討論
非霍奇金淋巴瘤常以無痛性淋巴結腫大起病,隨著疾病進展,可出現骨髓及中樞神經系統累及,亦可原發骨髓及中樞神經系統。原發骨髓的淋巴瘤(primary bone marrow lymphoma,PBML) 是一類罕見的血液系統惡性腫瘤(除外慢性淋巴細胞白血病/小淋巴細胞淋巴瘤),病情進展較快,預后差[1]。目前發病機制尚未完全清楚,缺乏特異性臨床表現和明確診斷標準。外周血淋巴細胞無量與質的改變,體檢及影像學檢查排除顱內腫瘤、胸腔、腹腔淋巴結及肝臟脾臟腫大,結合早期骨髓活檢對診斷有較為重要的意義,盡早給予利妥昔單抗的聯合化療能提高患者生存質量,延長患者生存期[2]。
檢索文獻,國內外報道例數均較少,其中個例報道為主。高靜等[2]報告3例原發骨髓淋巴瘤,第1例73歲女性因“乏力納差、間斷發熱4個月”入院,經骨髓涂片及免疫分型診斷為PBML,給予R-CHOP方案化療4個療程達完全緩解(CR);第2例60歲女性因“頭暈乏力10天”入院,經骨髓涂片及骨髓活檢,確診為PBML,患者放棄治療,3月后死亡;第3例72歲男性因“頭暈乏力伴間斷牙齦出血2年”入院,經骨髓涂片及骨髓活檢確診PBML,經2個療程COP(環磷酰胺+長春地辛+潑尼松)和6個療程CHOP(環磷酰胺+長春地辛+表柔比星+潑尼松)方案化療,血常規及骨髓常規恢復正常,之后回家休養,半年后復發死亡。Chang等[3]總結12例PBML患者發病中位年齡62.5歲,9例出現不明原因的發熱,2例為全血細胞減少,其余有不同程度血小板減少和貧血,9例測定有8例血β2微球蛋白中增高。Martinez等[4]報道的21例PBML患者大部分出現貧血、血小板減少。由此可見,對于不明原因發熱或血常規異常(特別是貧血、血小板減少)患者,應盡早行骨髓穿刺及活檢以排除此病。
PBML常無典型淋巴結腫大及肝脾侵犯,僅表現血常規異常,如不行骨髓檢查常不能明確診斷,易誤診及漏診。目前臨床常用的檢測淋巴瘤骨髓侵犯方法有骨髓液穿刺涂片及骨髓活檢術,而診斷骨髓侵犯時骨髓活檢陽性率明顯高于骨髓涂片[5-6]。Martinez等[4]總結的15例B細胞淋巴瘤骨髓侵犯中8例為彌漫性浸潤,6例為結節性浸潤,1例為間質性浸潤;劉慧敏等[7]報道的3例彌漫大B細胞淋巴瘤骨髓侵犯均為彌漫性浸潤;高靜等[2]報道的3例PBML骨髓活檢均為彌漫性浸潤。可見,PBML在骨髓侵犯常表現為彌漫性浸潤,也可表現為結節性浸潤,而間質性浸潤少見。骨髓涂片免疫組織化學、骨髓活組織檢查骨髓受累情況與患者性別、年齡、Karnofsky評分、B癥狀、結外累及、乳酸脫氫酶、血小板數、血紅蛋白含量、中性粒細胞數、淋巴細胞數、臨床分期無相關性(均P>0.05),而兩種檢測方法間存在相關性[8]。對于PBML,骨髓活檢在早期診斷中發揮重要作用,故血常規異常患者初診時,骨髓涂片是必要的,骨髓活檢同時也是需要的。
臨床上,PBML罕見,但淋巴瘤骨髓浸潤(bone marrow infiltration,BMI)較為常見,淋巴瘤 BMI的患者已經發展為Ⅳ期,確定BMI對制訂治療方案有重要意義。出現BMI等預后不良等因素時,對年輕患者應選擇的治療方法是使用大劑量的造血干細胞移植。因此,BMI的準確評估對惡性淋巴瘤的治療、預后具有重要意義[9]。無論是PBML還是BMI,骨髓常規及活檢均為局部檢查,存在局限性,可出現假陰性結果,此時需完善骨顯像檢查,當然全身PET-CT檢查更有意義。關于PBML治療,Chang等[3]報道12例PBML中,4例未經治療,均在1個月內死亡;4例CHOP方案治療,中位生存期為13個月;4例分別接受R-CHOP和R-COP(美羅華+環磷酰胺+長春新堿+潑尼松)均達CR。Bhagat等[10]報道1例PBML接受1個R-CHOP療程和7個療程R-CVP,4個療程后達CR;1例接受8個療程CHOP,治療過程中達到持續CR,但停藥2個月后復發。Qian等[11]報道1例PBML給予6個療程R-CHOP達CR。劉慧敏等[7]報道的3例PBML中,1例診斷后2個月死亡,1例接受R-CHOP方案7個療程達完全緩解(CR),1例RCHOP和R-EPOCH共4個療程達CR。Yi等[12]報道了1例原發肱骨的B淋巴母細胞淋巴瘤,以右側肘關節疼痛、發熱、血細胞減少和脾大起病,無淋巴結侵犯;PET-CT掃描提示右側肱骨遠端的18F-氟脫氧葡萄糖攝取升高,外科手術切除病灶,術后病理確診B淋巴母細胞淋巴瘤,按急性淋巴細胞白血病方案化療,獲得完全緩解,但4個月后復發。上述治療結果表明,PBML惡性度高,疾病進展快,易復發,不治療數月內死亡,化療可控制疾病進展,甚至達到完全緩解。但相比單獨化療,給予利妥昔單抗的聯合化療方法可以達到CR,且不易復發。
目前提出診斷PBML至少應包括2個基本條件:(1)單獨的骨髓浸潤;(2)體檢及影像學資料證實排除顱內腫瘤、胸腔及腹腔淋巴結、肝臟脾臟增大及其他髓外浸潤表現[3]。本文中的患者符合此2個條件,患者行骨髓常規及活檢明確淋巴瘤骨髓浸潤,行全身PET-CT檢查,除外全身骨髓外部位浸潤,故PBML診斷成立,但因骨髓組織無法行更多免疫標記,所以無法進一步明確是哪種類型的大B細胞淋巴瘤。治療上,目前國內外報道病例,以R-CHOP方案為主,也有采用R-COP等方案化療,結果提示以美羅華為基礎的治療方案,效果更佳,不易復發[4]。本例患者經1次R-CHOP方案化療,達到骨髓緩解,繼續2次R-CHOP方案化療,復查骨髓緩解,之后行3次R-EPOCH方案化療,化療結束評估疾病緩解。患者目前已停化療1年,疾病仍處于緩解狀態,繼續隨訪觀察。

