化合物化學式計算的幾種常見考查方式
張新中
(江蘇省邗江中學 225009)
化合物化學式的計算是高中學生必須掌握的一項基本技能,在高考和各地的模擬試卷中也屢屢出現.常見的考查方式有以下幾種.
一、利用反應列方程進行計算
例1 某科研小組采集到兩種銅礦標本,經地理老師辨認為孔雀石和石青,老師說其化學組成均可表示為xCuCO3·yCu(OH)2,屬于天然碳酸鹽類銅礦.
(1)為了準確測定兩種礦石的化學組成,該小組同學將兩種礦石分別與足量鹽酸反應,孔雀石耗用的鹽酸的物質的量與生成的CO2的物質的量之比為4∶1;石青則為3∶1.請確定它們的化學組成,孔雀石:____;石青:____.
(2)現取兩份等質量的兩種礦石的混合物樣品,一份加入過量鹽酸,生成CO26.6 g;對另一份樣品加熱使其完全分解,得到CuO 20g,則混合物中孔雀石和石青的物質的量之比為____.
解析(1)xCuCO3·yCu(OH)2與鹽酸反應的化學方程式為xCuCO3·yCu(OH)2+2(x+y)HCl→(x+y)CuCl2+xCO2↑+(x+2y)H2O
根據孔雀石耗用的鹽酸與生成的CO2的物質的量比為4∶1,可得:2(x+y)∶x=4∶1,解得x∶y=1∶1,故孔雀石的化學式可表示為CuCO3·Cu(OH)2.
根據石青耗用的鹽酸與生成的CO2的物質的量比為3∶1,可得:2(x+y)∶x=3∶1,解得x=2y,故石青的化學式可表示為2CuCO3·Cu(OH)2.
根據C守恒得:a+2b=0.15 mol
根據Cu守恒得:2a+3b=0.25 mol
解得a=0.05 mol,b=0.05 mol.
故該混合物中孔雀石和石青的物質的量之比為:
0.05 mol∶0.05 mol=1∶1
答案:(1)CuCO3·Cu(OH)2;2CuCO3·Cu(OH)2(2)1∶1
點評本題根據銅礦與鹽酸反應消耗鹽酸的物質的量與生成的CO2的物質的量之比計算化學式,只要寫出化學方程式,找出相應物質的物質的量,列方程即可解答.本題的關鍵在于化學方程式的書寫,題目比較簡單.
二、利用三大守恒進行計算
例2 某結晶水合物含有兩種陽離子和一種陰離子.稱取兩份質量均為 10.00 g的該結晶水合物,分別制成溶液.

②另一份加入足量的BaCl2溶液,生成不溶于稀硝酸白色沉淀,經過濾、洗滌、干燥稱其質量為11.65 g.
(1)該結晶水合物中含有的兩種陽離子是____和____,陰離子是____.
(2)試通過計算確定該結晶水合物的化學式(寫出計算過程,注意解題規范).
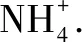
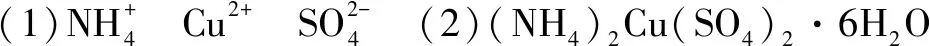
點評本題先根據反應現象推斷出物質中的離子,然后根據題中給出的物質的物質的量,計算出已知離子的物質的量,再根據電荷守恒計算出剩余離子的物質的量,最后得出物質的化學式.本題的關鍵在于應用電荷守恒計算最后一種離子的物質的量.
三、利用分解產物的比例進行計算
例3 實驗所制得的堿式碳酸銅的組成可表示為:xCuCO3·yCu(OH)2·zH2O,要測定其組成,甲同學設計的實驗方案中需要如下五個步驟:①稱取12.0 g的樣品;②高溫分解;③測出生成CO2的質量為2.2 g;④測出生成水蒸氣的質量為1.8 g;⑤稱量生成CuO的質量為8.0 g.而乙同學認為除步驟②外,實驗只需測定4個量中的部分數據即可,則合理的組合為____(填序號,寫一組即可).根據你的選擇,計算出堿式碳酸銅的組成,寫出計算過程.
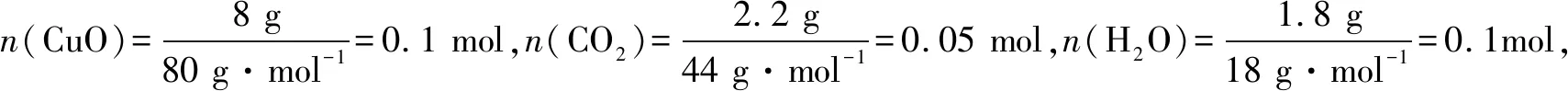
答案:③④⑤,①③④,①③⑤,①④⑤(任寫一種) CuCO3·Cu(OH)2·H2O
點評本題根據分解產物的物質的量之比寫出鹽的氧化物表示形式,然后改寫為鹽的形式.本題的關鍵在于理解用氧化物的形式表示鹽的組成;要注意的是分解生成的水不是鹽中的結晶水.
四、利用熱重分析圖進行計算
例4 鈷及其化合物廣泛應用于磁性材料、電池材料及超硬材料等領域.
(1)CoxNi(1-x)Fe2O4(其中Co、Ni的化合價均為+2價)可用作H2O2分解的催化劑,具有較高的活性.
① 該催化劑中鐵元素的化合價為____.
② 圖1表示兩種不同方法制得的催化劑CoxNi(1-x)Fe2O4在10℃時催化分解6%的H2O2溶液的相對初始速率隨x變化曲線.由圖中信息可知:____法制取得到的催化劑活性更高;Co2+、Ni2+兩種離子中催化效果更好的是____.
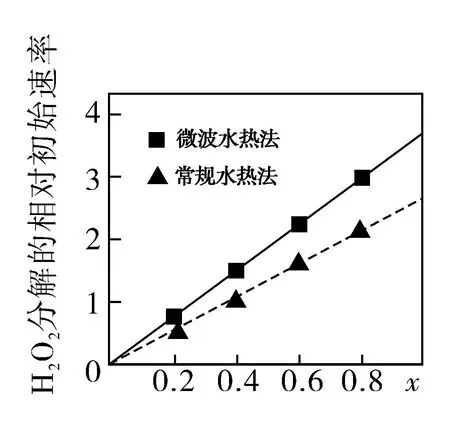
圖1

圖2
(2) 草酸鈷是制備鈷氧化物的重要原料.圖2為二水合草酸鈷(CoC2O4·2H2O)在空氣中受熱的質量變化曲線,曲線中300℃及以上所得固體均為鈷氧化物.
① 通過計算確定C點剩余固體的化學成分為____(填化學式).寫出B點對應的物質與O2在225~300℃的條件下發生反應的化學方程式:____.
② 取一定質量的二水合草酸鈷分解后的鈷氧化物(其中Co的化合價為+2、+3價),用480 mL 5 mol·L-1鹽酸恰好完全溶解固體,得到CoCl2溶液和4.48 L(標準狀況)黃綠色氣體.試確定該鈷氧化物的化學式.
解析(1)①該催化劑中Co、Ni均為+2價,O為-2價,所以Fe元素的化合價是[8-(2x+2-2x)]/2=+3.②反應速率越快,則催化劑的催化活性越高,根據圖像可知,x相同時微波水熱法初始反應速率大于常規水熱法,所以微波水熱法制取得到的催化劑活性更高;隨x增大,初始速率增大,而x增大,Co2+的比例增大,所以Co2+的催化效果更好.
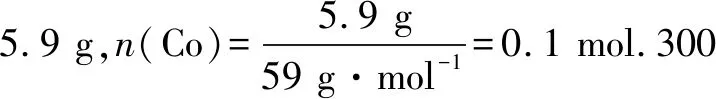
答案:(1)①+3 ②微波水熱 Co2+

②Co5O6(過程見解析)
點評本題(2)①根據化合物在受熱時的質量變化計算不同階段的化學式.解答這類題的一般思路是:(1)失重一般是先失水,再失非金屬氧化物;(2)晶體中金屬質量不再減少,仍在m余中;(3)失重最后一般為金屬氧化物,由質量守恒得m氧,由n金屬∶n氧,即可求出失重后物質的化學式.解題的關鍵在于弄清物質質量變化的原因,從而計算出變化物質的物質的量.
五、利用滴定實驗數據進行計算
例5 堿式次氯酸鎂[Mga(ClO)b(OH)c·xH2O]是一種有開發價值的微溶于水的無機抗菌劑.為確定堿式次氯酸鎂的組成,進行如下實驗:

(1)步驟①需要用到的指示劑是____.
(2)步驟②若滴定管在使用前未用EDTA標準溶液潤洗,測得的Mg2+物質的量將____(填“偏高”“偏低”或“不變”).
(3)通過計算確定堿式次氯酸鎂的化學式(寫出計算過程).
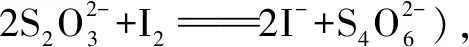
解析(1)I2遇淀粉顯藍色,當Na2S2O3將I2完全消耗時,溶液的藍色褪去,故選擇淀粉作指示劑.
(2)若滴定管沒有潤洗,則其濃度變小,與Mg2+反應時,EDTA的消耗量增多,所得Mg2+的量偏高.

答案:(1)淀粉溶液 (2)偏高
n(Mg2+)=0.020 00 mol·L-1×25.00×10-3L×1 000 mL/25.00 mL=2.000×10-2mol
根據電荷守恒,可得:
n(OH-)=2n(Mg2+)-n(ClO-)=2×2.000×10-2mol-1.000×10-2mol=3.000×10-2mol
m(H2O)=1.685 g-1.000×10-2mol×51.5 g·mol-1-2.000×10-2mol×24 g·mol-1-3.000×10-2mol×17 g·mol-1=0.180 g
n(Mg2+)∶n(ClO-)∶n(OH-)∶n(H2O)
=2.000×10-2mol∶1.000×10-2mol∶3.000×
10-2mol∶1.000×10-2mol=2∶1∶3∶1
則堿式次氯酸鎂的化學式為Mg2ClO(OH)3·H2O.
點評本題利用滴定實驗測定出ClO-、Mg2+的物質的量,再利用電荷守恒和質量守恒計算出OH-和H2O的量,最后確定出化學式.解題的關鍵在于根據滴定實驗找出關系式,從而進行計算.

