ABS塑料化學鍍銅研究
高萬旭,葉 健,李全良
(周口師范學院 化學化工學院,河南 周口 466000)
0 引言
化學鍍金屬能使非金屬物質具有金屬物質所擁有的特性,如:易導電性、易導熱性、延展性、光澤性等。化學鍍自1948年開始發展到如今已經成為表面處理的主要技術之一[1]。化學鍍應用極其廣泛,在其觀賞性方面、電子通訊、功能性方面、硬件加工、電腦行業、防護性方面、石油和天然氣、織物金屬化、航空航天等都有應用[2-4]。化學鍍的生產成本低,對環境的污染小,方法簡單等優點成為表面處理技術的重點研究對象。
對比與其他材料表層金屬化的方式,化學鍍的方式既簡單又經濟,在工業化發展迅速的今天成為了工業上一項重要的化工工藝。實驗室中的化學鍍銅實驗大部分是應用分析純試劑進行的,但在工業生產時,除了放大效應的影響外,還會由于工業級試劑的純度和雜質影響生產產品的質量[5]。本實驗全部采用工業級試劑,用甲醛作還原劑、酒石酸鉀鈉作絡合劑,以ABS塑料為載體,在其表面還原溶液中絡合的銅離子形成均勻致密的銅層。研究工業級試劑進行化學鍍銅工藝并確定最佳工藝對于在工業上應用化學鍍銅這種重要工藝具有現實意義。
1 實驗部分
1.1 儀器與試劑
儀器:PHS-3C型酸度計(上海理達儀器廠);DF-101S集熱式恒溫加熱磁力攪拌器(河南碩杰儀器設備有限公司);電子分析天平(上海卓精電子科技有限公司);燒杯;玻璃棒等。
試劑:三氧化鉻、工業硫酸、氯化亞錫、鹽酸(約37%)、硝酸銀、氨水、五水硫酸銅、甲醛(36%~38%)、氫氧化鈉、酒石酸鉀鈉、EDTA、乙醇、七水硫酸鎳、65%稀硝酸(以上全部為工業級試劑)。
1.2 工藝流程
ABS塑料表面化學鍍銅的工藝流程為:ABS塑料件—除去應力—應力檢查—除油—水洗—粗化—水洗—還原—水洗—敏化—水洗—活化—還原—水洗—化學鍍銅。
1.3 實驗過程
1.3.1 粗化
粗化是利用硫酸和鉻酸的混合溶液微蝕塑料基體,經過氧化處理在表面形成微觀下的粗糙不平的凹孔或孔洞,增大表面的附著力使離子更容易吸附,并且能夠增添基體表面積。配置溶液:三氧化鉻 350~400 g/L,硫酸 210~240 mL/L,溫度在328 K下,加熱時間25 min。
1.3.2 敏化
敏化是在粗化后的塑料表面形成一層還原性的物質。常用的物質為氯化亞錫,此道工序能在之后的活化反應中發生氧化還原反應,在塑料的表面形成金屬薄層。配置溶液:氯化亞錫20 g/L,鹽酸45 mL/L,控制溫度為303 K,加熱時間為15 min。
1.3.3 活化
將經過敏化處理的ABS塑料浸入到硝酸銀溶液后,氧化性較強的Ag+在其表面發生還原反應,生成Ag微粒,這些Ag擁有催化活性,銅沉淀以這些Ag微粒為結晶中心,使ABS塑料的表面能夠很快沉淀一層金屬銅[8]。溶液配置:硝酸銀6 g/L,氨水滴加至溶液剛好澄清,大約需要8~10 mL,控制溫度 303 K,加熱時間 10~15 min。
1.3.4 化學鍍銅
五水硫酸銅 12 g/L,甲醛(36%~38%)16 mL/L,酒石酸鉀鈉60 g/L,七水硫酸鎳1.2 g/L,氫氧化鈉約7 g/L,pH約11~12。硫酸鎳可以增大鍍銅層的結合力,增加鍍銅層的光澤性,減少在鍍銅時塑料表面發生反應產生的氣泡等優點。控制溫度范圍 303~313 K,加熱時間 25~30 min。
2 結果與討論
2.1 鍍銅液的組成
在實驗中需加入EDTA起絡合作用[6],乙醇作為穩定劑起到穩定溶液的作用。工業級的EDTA和乙醇中含有更多的雜質,乙醇本身就起到穩定劑的作用,在鍍液中主反應難以進行,在不使用EDTA和乙醇的情況下組成鍍銅液進行實驗。實驗結果顯示仍然可以完成鍍銅,鍍銅液也相對穩定,最終確定的鍍銅液組成為五水硫酸銅、酒石酸鉀鈉、甲醛、氫氧化鈉、七水硫酸鎳這5種物質。并且這五種物質的質量與實驗室級試劑配比鍍銅的溶液的質量也有不同,對不同物質質量對于沉積速率的影響也做了實驗,取最佳質量配制鍍銅液。
2.2 五水硫酸銅的質量濃度對銅沉積速率的影響
在粗化、敏化、活化的最佳處理條件下,選擇酒石酸鉀鈉的質量濃度為60 g/L,甲醛 (36%~38%)的體積濃度為16 mL/L,七水硫酸鎳的質量濃度為1.2 g/L,氫氧化鈉的質量濃度大約7 g/L,pH約11~12,所以氫氧化鈉還需邊檢測pH邊添加,不能直接加入。然后改變五水硫酸銅的質量濃度,結果如圖1所示,伴隨著五水硫酸銅的加入,沉銅速率逐漸加快,當其質量濃度增加到12 g/L時,沉銅速率由快速增加轉變為緩慢增加,超過15 g/L后沉銅速率由緩慢增加變為緩慢減少。所以五水硫酸銅的質量濃度應在12~15 g/L之間進行取值,但實驗結果顯示,增加五水硫酸銅的質量濃度會使鍍銅液的穩定性變差,所以最后將五水硫酸銅的質量濃度設定在12 g/L。
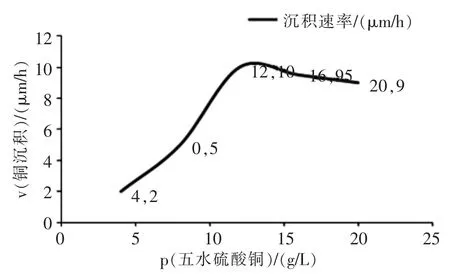
圖1 五水硫酸銅的質量濃度對銅沉積速率的影響
2.3 甲醛的體積濃度對銅沉積速率的影響
在第2.2節的工藝前提下,選取五水硫酸銅的質量濃度為12 g/L,在其他的變量不變的情況下,以甲醛的體積濃度為變量,當增加甲醛的體積濃度時,沉銅速率先是快速增長,當超過16 mL/L時,銅的沉積速率曲線增加程度開始減緩,如圖2所示。所以增加甲醛的體積濃度意義不大,而且浪費試劑,故此實驗選擇甲醛的體積濃度為16 mL/L。
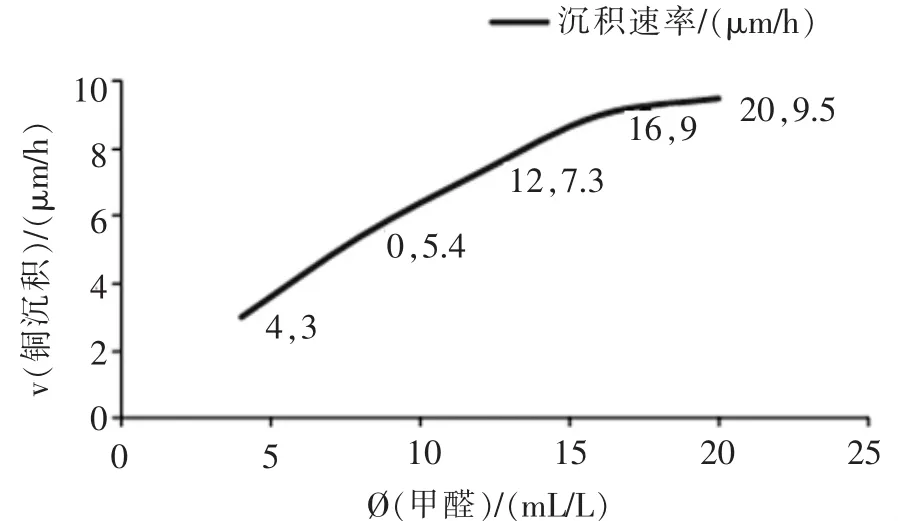
圖2 甲醛的體積濃度對銅沉積速率的影響
2.4 酒石酸鉀鈉的質量濃度對銅沉積速率的影響
加入甲醛的體積濃度為16 mL/L后,依然保持其他變量不變,改變酒石酸鉀鈉的質量濃度,實驗的結果與實驗室級試劑略有不同。使用工業級試劑,當酒石酸鉀鈉的質量濃度低于40 g/L時沒有銅沉淀出現,高于40 g/L后,銅的沉積速率逐漸增加,增加到60 g/L時銅的沉積速率開始緩慢的下降,如圖3所示,而且隨著酒石酸鉀鈉繼續的增加鍍銅液穩定性開始降低。相比于實驗室級試劑,工業級的酒石酸鉀鈉加入的量更多,而且加入的量不足時反應不會進行。因此將酒石酸鉀鈉的質量濃度定為60 g/L。
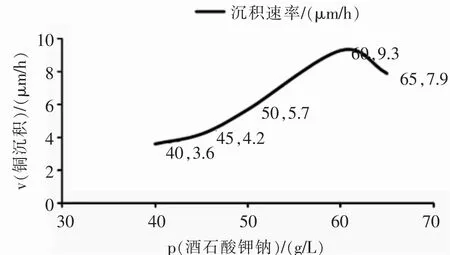
圖3 酒石酸鉀鈉的質量濃度對銅沉積速率的影響
2.5 化學鍍液的pH對銅沉積速率及鍍層的質量外觀的影響
在第2.4節的工藝前提下,選擇酒石酸鉀鈉的質量濃度為60 g/L,改變鍍銅液的pH,觀察在不同的pH下銅的沉積速率和鍍層的質量外觀有何差別,結果如表1所示。鍍銅液的pH低于11時不能形成良好的鍍層,銅的沉積速率隨著pH的升高而增大,但是溶液中還存在著副反應,當pH高于12時,鍍銅液的穩定性會因為銅的沉積速率過快而下降,導致溶液中銅的自催化反應,影響鍍液的后續使用,也影響塑料表面的鍍銅質量,鍍銅層結合力弱容易溶解。本實驗選擇鍍銅液的pH 為 11~12。

表1 化學鍍液的pH對鍍層的質量外觀的影響
3 結論
本實驗全部使用工業級試劑,通過以上試驗可以得到在工業上進行ABS塑料表面化學鍍銅生產的最佳工藝條件。即:粗化溫度328 K,粗化時間25 min;敏化溫度303 K,敏化時間15 min;活化溫度303 K,活化時間10~15 min;化學鍍銅液的配制采用五水硫酸銅12 g/L、甲醛 (36%~38%)16 mL/L、酒石酸鉀鈉60 g/L、七水硫酸鎳1.2 g/L、氫氧化鈉大約 7 g/L、pH 大約在 11~12,化學鍍溫度 303~313 K,化學鍍時間 25~30 min。

