轉化生長因子β1/Smad信號通路與早發性卵巢功能不全相關性研究
趙銳 劉宴君 高步嬋 許小翠
早發性卵巢功能不全是卵巢功能下降的進展后果,除了功能障礙更有器質性病變。嚴格來講這種病理損害在現有醫療技術階段,是不可逆的。對臨床病例進行統計分析發現,由于現代社會對女性生存造成的壓力等一系列原因,患有早發性卵巢功能不全的患者年齡階段顯著年輕化,嚴重影響女性生活質量的同時,還擴大了不孕癥的患者群,正是這種不良影響引起了臨床醫生以及科研人員的警惕,使得加速早發性卵巢功能發病機制研究進展的需求提上日程。
一、早發性卵巢功能不全
1.早發性卵巢功能不全概念:早發性卵巢功能不全(primary ovarian insufficiency,POI),曾名卵巢早衰,定義為,年齡小于40歲女性的卵巢功能退化的臨床綜合征[1]。臨床癥狀以過早的更年期表現常見,如:月經稀發,盜汗,心悸,情緒急躁,陰道干澀,性欲低下等。診斷標準為:(1)稀發月經或停經至少4個月。(2)檢測時間間隔>4周,連續兩次卵泡刺激素值FSH>25 U/L(對比參照IMS的診斷閾值FSH>40 U/L,ESHR的診斷標準更具有臨床診療意義)[2]。早發性卵巢功能不足以低雌激素,高卵泡刺激素,以及高黃體生成素分泌為臨床指標的特點。作為臨床疑難癥,早發性卵巢功能不全治愈率低,治療效果差,危害女性健康,嚴重降低生活質量,其可能導致的不孕癥對有生育需求的女性來說更是災難性的打擊。早在2008年據不完全數據統計顯示,早發性卵巢功能不全在女性群體中的患病率為百分之一,且近年來患者年輕化顯著,降低生活質量,嚴重危害女性健康。經臨床實驗觀察總結,可以確定POI的發病與遺傳因素[3]、免疫因素[4]、手術、化療、放療、酶缺陷、精神心理因素及吸煙[5]等密切相關。關于致病因素具體導致早發性卵巢功能不全發生的機制仍未有一個明確的說法,科研人員試圖從信號通路的水平來進一步探究,TGFβ/Smad信號通路就是受關注較多的一個角度。
二、TGFβ/Smad信號通路
1.轉化生長因子-β(TGF-β):轉化生長因子-β超家族是一類具有自分泌、旁分泌功能的細胞因子。目前研究發現其至少由35種細胞因子組成,包括五大亞型:轉化生長因子-β亞型(TGF-β1、TGF-β2、TGF-β3)、生長和分化因子(至少9個成員)、骨形態發生蛋白(20個成員)、激活素(含激活素A、激活素AB、激活素B)及抑制素(抑制素A、抑制素B)等[6]。TGF-β1是廣受認可的多功能因子,參與胚胎發育,細胞的生長與分化,創傷修復,機體免疫,血管生成,腫瘤的形成以及炎癥等各項進程[7]。轉化生長因子-β亞型中TGF-β1、TGF-β2共同作用于TGFβ/Smad信號通路,并在信號傳導中有著決定性的作用。
2.Smads蛋白家族:Smad蛋白是轉化生長因子-β的直接作用底物,在哺乳動物中共發現8種蛋白,從結構和功能上主要可以分為3個亞族:5種配體蛋白(R-SMADs;Smad1/2/3/5/9)是TGF-β1的直接效應分子,1種通用型蛋白(Co-SMAD;Smad4),是信號在通路中傳導時,所有轉化生長因子-β超家族的信號分子進入細胞核之前必需結合的蛋白,和2種抑制蛋白(I-SMADs:Smad6、Smad7)是TGFβ信號傳導的抑制劑[8]。參與卵巢功能調控的smad蛋白是smad2、smad3、smad4、smad6、smad7。
3.TGF-β1/Smad的信號傳導:TGFβ/Smad信號通路是近年來的明星通路,其在卵巢功能方面的作用得到廣泛的認可,信號的傳導是一個復雜的且受到多方干預的過程:首先,活化的超家族配體信號分子識別TGF-β2型受體并與之結合,TGF-β2自身磷酸化后以募集式與TGFβ1結合形成二聚體復合物而具有激酶活性。此時已經活化的TGFβ1將其底物smad2/3磷酸化,將信號傳到磷酸化的受體,并與Smad4結合將TGFβ的信號由胞漿傳遞到胞核內,作用于特定的基因啟動子,與許多輔助活化因子和輔助抑制因子協同作用調節靶基因的轉錄[9-10]。I-Smad則與R-smads競爭結合活化TGF-β1的機會,阻斷信息的傳導[11]。
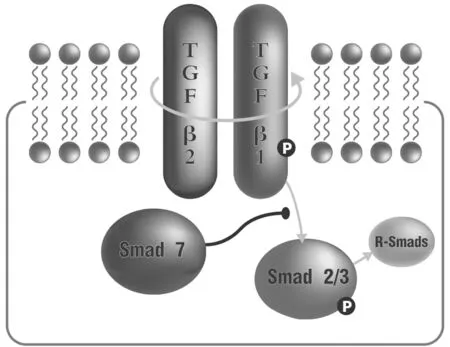
圖1 TGF-β1/Smad信號通路傳導示意圖
三、TGF-β1/Smad信號通路與早發性卵巢功能不全
TGF-β1/Smad信號通路在生命體中廣泛的參于細胞的各項生命活動,參與介導組織與器官的正常生長和發育,在正常卵巢組織中有完整的TGF-β1/Smad信號通路,其中各個信號分子對顆粒細胞的分化與凋亡有著多層次的影響,并且干預卵泡的生長發育與排出,TGF-β1,smad2、smad3等的異常表達均會引起卵巢功能的異常。
1.TGF-β1異常表達對卵巢功能的影響:異常的TGF-β1表達導致卵泡發育障礙、無排卵。對雷公藤制備的大鼠模型進行鏡下觀察發現組織形態學的變化:卵泡膜細胞層增厚,而顆粒層數減少,排列致密、染色加深且間質增加;除此之外,更有閉鎖卵泡數目增多,黃體數目減少,無優勢卵泡等一系列卵巢功能下降的表現。對比空白組TGF-β1在卵巢顆粒細胞及間質細胞的表達,模型組的TGF-β1過表達明顯。故路帥等認為,雷公藤導致卵泡發育障礙的機制與TGF-β1在顆粒細胞中的高表達有著因果關系,而其中機制與TGF-β1介導竇卵泡顆粒細胞的凋亡有著密切的相關性[12-13]。在劉慧萍的試驗中,免疫性因素所致的卵巢早衰小鼠模型卵泡中顆粒細胞TGF-β1蛋白表達明顯減弱,HE檢測發現卵泡閉鎖顯著增加,再次提示TGF-β1的非正常表達對卵巢功能有負面影響[14]。胡興文等人在對比TGF-β1在卵泡液和血清中TGF-β1的濃度時發現,前者明顯低于后者,故推測TGF-β1沒有卵巢源性,并產生了TGF-β1對卵母細胞的發育成熟有抑制作用的猜想[15]。對不孕癥患者顆粒細胞進行離體培養發現,TGF-β1對顆粒細胞卵丘擴展相關基因PTX3、TNFAIP有促進作用,并呈濃度梯度正相關以及作用時間正相關[16]。
2.TGF-β1/Smad信號通路對卵巢功能的影響:TGF-β1在信號傳導中通過對直接作用底物smad蛋白的影響參與調節雌激素的生成,對維持卵巢內環境穩態有著重要影響。早在2001年,呂時銘等[17]將人顆粒細胞離體培養,發現在無卵泡刺激素干預條件下TGF-β1可以使顆粒細胞分泌雌二醇,且適當濃度的TGF-β1可以增強fsh促進雌二醇分泌的效果。而卵泡刺激素FSH對Smad2/Smad3有激活作用,且依賴TGF-β2調節TGF-β1/Smad信號通路調控卵巢功能[18]。2008年Zheng等人的實驗在驗證了這一點的同時,還說明了TGF-β1通過抑制參與雄激素轉化為E2的關鍵酶來抑制顆粒細胞中E2的合成[19]。除此之外,大量實驗研究表明,TGF-β1/Smad信號通路同時介導顆粒細胞的凋亡以及卵泡的生發,而其具體作用分子是smads家族各成員蛋白。應用基因敲除技術,研究人員發現單獨對雌性小鼠去除Smad3基因[20-21]將導致穩定動情周期的缺失,卵泡發育的紊亂,顆粒細胞凋亡的增加,進而導致卵泡閉鎖的增加,對生育功能并無明顯影響,然而在同時敲除Smad2與Smad3這一對基因時[22],雌性大鼠則喪失生育功能。應用siRNA轉染手段研究顯示,Smad2和Smad3分別參與TGF-β1上調和PGE的生成,進而參與卵巢調控排卵的發生和發展[23]。Yu[24]等使用Cyp19-Cre小鼠,對其排卵前卵泡中的顆粒細胞特異性地清除Smad4,結果導致卵泡閉鎖的增加,進一步分析發現,Smad4的缺失降低了Nppc和Npr2的表達,使其維持卵母細胞減數分裂阻滯的作用減弱,損害女性生育功能[25]。
三、總結
TGF-β1/Smad信號通路在卵巢的發生發育中有著非常重要的作用,任何一個信號分子對卵巢功能產生的影響都是復雜而多方的。TGF-β1通過對顆粒細胞的影響干預雌激素的生成,同時提高受體對fsh的敏感性,增強雌激素分泌效果,除此之外其在信號通路中通過對底物Smad蛋白影響對顆粒細胞的發育以及卵泡的發育排出都有著不同程度的影響。對于不同病因造成的早發性卵巢功能不全模型的觀察提示我們TGF-β1的過高表達或者過低表達都會產生卵巢功能方面的障礙:尤為明顯的化療源性POI模型中卵巢組織的TGF-β1高表達以及免疫性因素導致的POI模型中TGF-β1低表達。我們可大體推測這種現象與TGF-β1對顆粒細胞的發生發育以及凋亡有聯系,然而其中具體機理仍未有一個明確化的理論學說。信號在整條信號通路的傳導受多個分子的調控和干預,而任何一個信號分子的上調或者下降導致的結果是多個作用疊加而導致的,我們應當從更加細致的角度來客觀評價TGF-β1在整條信號通路中的影響,以詮釋整條信號通路與疾病的相關性,例如基因角度。

