國產聚乙二醇化干擾素α治療HBeAg陽性慢性乙型肝炎患者療效研究*
袁春暉,李春雨,李紅麗,趙紅娜,王文紅,孟慶旭,張中學
研究發現,CHB患者肝病進展程度往往與血清HBV DNA載量相關[1,2]。因此,治療HBV感染時應以抑制HBV持續復制為主要目的[3]。聚乙二醇化干擾素α(peg-IFN-α)具有免疫調節和抗病毒作用,療程肯定,病毒學應答率(SVR)較高,是被推薦的HBeAg陽性CHB患者的一線治療方案[4,5]。目前,IFN-α可分為peg-IFN-α-2a/2b兩類,研究結果顯示,兩種干擾素對慢性丙型肝炎(CHC)治療效果基本一致,但有報道認為peg-IFN-α-2a更具有治療優勢[6,7]。因此,我們選擇了500例HBeAg陽性CHB患者為研究對象,分別采用peg-IFN-α-2b和peg-IFN-α-2a治療,通過隨訪觀察比較了兩種IFN-α的治療效果,現將結果報道如下。
1 資料與方法
1.1 臨床資料 2015年1月~2017年12月我院和保定市傳染病醫院肝病科收治的HBeAg陽性CHB患者500例,男362例,女138例;年齡18~39歲,平均年齡為(28.5±10.5)歲。均符合《慢性乙型肝炎防治指南》[8](2015版)的診斷標準,納入患者治療前均未接受過抗病毒或胸腺素等免疫調節藥物治療。排除標準:①合并HEV、HAV、HCV和HIV等多重病毒感染者;②合并自身免疫性肝病或藥物性肝損傷患者;③妊娠或哺乳期婦女;④血清HBsAg和抗-HBs同時陽性或HBeAg和抗-HBe同時陽性者;⑤肝功能衰竭或患有失代償期肝病者。本研究經醫院醫學倫理委員會批準,患者簽署知情同意書。
1.2 治療方法 將患者分成兩組。在A組150例患者,給予peg-IFNα-2b(廈門特寶生物工程股份有限公司,國藥準字:S20160001)1~1.5 μg·kg-1皮下注射,1次/w,治療24~48 w;在B組350例患者,給予聚乙二醇干擾素α-2a(派羅欣,上海羅氏制藥有限公司,國藥準字:J20040038)180μg皮下注射,1次/w,治療24~48 w。在治療結束后,對兩組患者隨訪24 w。
1.3 臨床檢測 使用日本OLYMPUS AU2700自動生化分析儀檢測血生化指標(北京康思潤業生物技術有限公司);采用ELISA法定量檢測血清HBeAg、抗-HBe、HBsAg(美國雅培公司),血清HBeAg為0~1 s/co即為陰性,抗-HBe>1 s/co為陽性,血清HBsAg<0.05 IU/m L為陰性,血清抗-HBs>10 mIU/m L即為陽性;采用實時熒光定量PCR法檢測血清HBV DNA(上海江萊生物科技有限公司),血清HBV DNA 定量<1×103拷貝 /毫升為陰性;采用直接測序法檢測HBV基因型(北京康為世紀生物科技有限公司)。
1.4 療效考核標準 參考《指南》[8],停止治療后,希望獲得持久的血清HBsAg消失,伴或不伴HBsAg血清學轉換,或獲得持續病毒學應答、血清ALT復常和出現HBeAg血清學轉換為完全應答。
1.5 統計學方法 應用SPSS 22.0統計軟件進行數據分析,計量資料以(±s)表示,采用 t檢驗,計數資料采用x2檢驗。P<0.05被認為差異具有統計學意義。
2 結果
2.1 兩組基線資料比較 兩組基線病毒學、血清學和生化學資料間差異無統計學意義(P>0.05,表1)。
2.2 兩組感染HBV基因型比較 兩組HBV基因型比較,差異無統計學意義(P>0.05,表2)。
表1 兩組CHB患者基線資料(±s)比較

表1 兩組CHB患者基線資料(±s)比較
例數 HBV DNA(lg cps/ml) ALT(u/L) 體質指數 HBeAg(lg s/co) HBsAg(IU/ml)A 組 150 6.1±0.7 81.1±29.8 22.1±2.9 3.1±0.6 4.4±0.6 B 組 350 6.2±0.6 80.7±27.9 21.9±2.9 3.1±0.1 4.4±0.6 x2/t值 0.767 0.137 0.484 0.575 0.177 P值 0.444 0.891 0.629 0.566 0.86
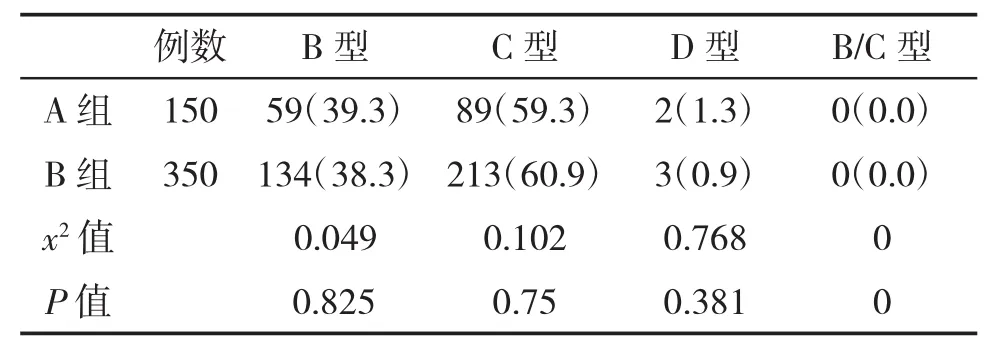
表2 兩組HBV基因型分布(%)比較
2.3 兩組治療結束時和隨訪24周時療效比較 在治療結束和隨訪結束時,兩組療效無顯著性差異(P>0.05,表3);在隨訪 24 周時,peg-IFN-α-2b 和peg-IFN-α-2a治療組分別有12例(8.0%)和23例(6.6%)病情復發。
2.4 兩組安全性分析 無論是注射進口還是國產干擾素后,主要的不良反應包括乏力、頭痛、肌肉酸痛、脫發和血細胞減少等,但兩組各種不良反應發生率并無顯著差異(P>0.05,表4)。對于發生白細胞減少病例,給予粒細胞集落刺激因子注射后,完成治療,而對個別血小板減少病例,則將干擾素劑量減半后,維持治療至結束。
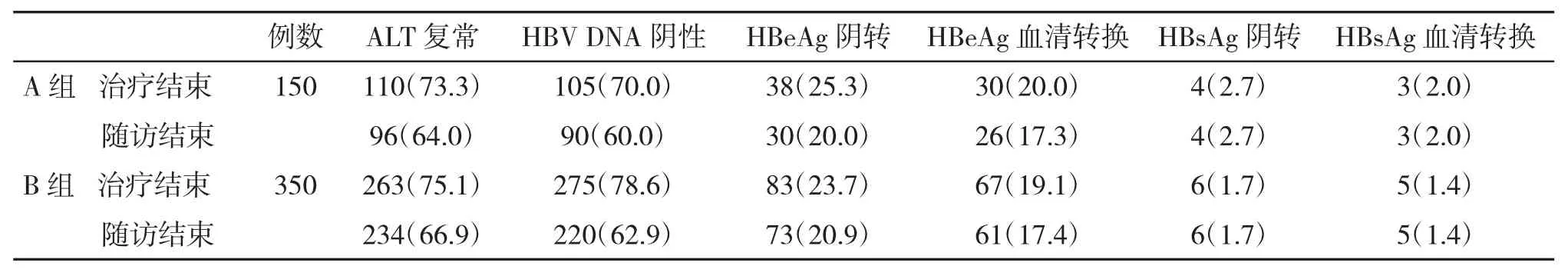
表3 兩組療效(%)比較
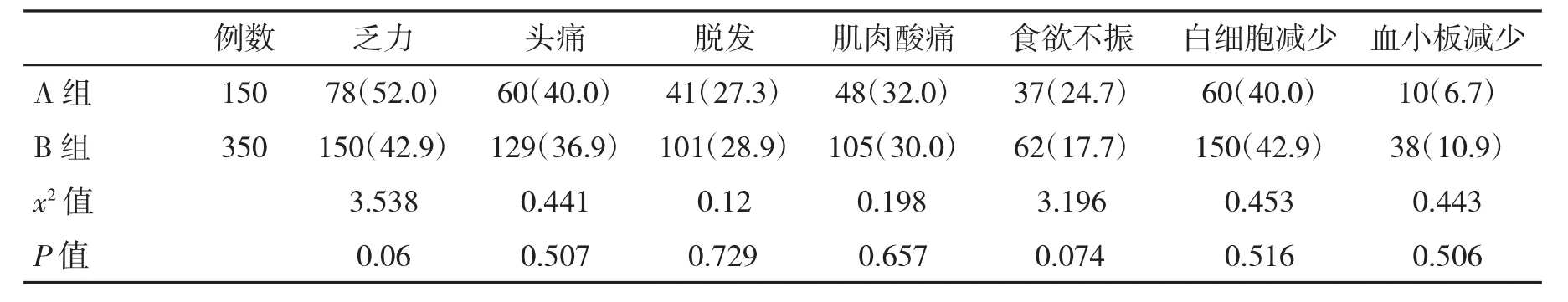
表4 兩組主要不良反應(%)比較
3 討論
CHB可發展為肝硬化甚至肝癌。Peg-IFN-α是目前抗病毒治療CHB患者的一線藥物。CHB患者經peg-IFN-α治療后能獲得較高的病毒學和血清免疫學應答率[9,10],對HBeAg陽性CHB患者也可獲得較好的療效。我國2015年版《慢性乙型肝炎防治指南》指出,在部分合適的CHB患者,可以選擇Peg-IFN-α治療,以盡可能地獲得臨床治愈的效果[8]。另外,國內[11,12]有研究表明,采用 Peg-IFN-α治療CHB患者,可明顯降低肝硬化和肝癌的發生率,起到預防肝癌的效果。目前,Peg-IFN-α可分為Peg-IFN-α-2a和 Peg-IFN-α-2b兩種,其中,Peg-IFN-α-2a是聚乙二醇化干擾素,是一種長效干擾素,可與細胞表面的特異性α受體結合,即可在細胞內誘導信號傳遞,并激活基因的轉錄,起到抑制病毒復制,調節免疫功能的作用,是臨床治療CHB和慢性丙型肝炎(CHC)患者的常用藥物[13]。Peg-IFN-α-2b是一種 IFN-α-2b與聚乙二醇(40kDY型)結合所得的長效干擾素,可用于治療CHC和血清HBeAg陽性的CHB患者。國產干擾素α-2b與Peg-IFN-α-2a的抗病毒作用機制基本一致[6]。國內外在對 CHC患者的治療研究[14,15]表明,Y型Peg-IFN-α-2b與peg-IFN-α-2a可達到相似的治療效果,且安全性也相似。
由于peg-IFN-α治療的療效可能會受到多種因素的影響,如HBV DNA基因型的影響等。本研究結果顯示,兩組患者基線資料差異均無統計學意義(P>0.05),初步排除了其他因素對本研究治療結果的干擾。國外研究[16,17]結果報道稱,PEG-IFNα-2a和PEG-IFNα-2b治療CHB患者,在獲得SVR和不可檢測的血清HBV DNA水平方面無顯著性差異。本研究結果也表明,兩組HBV DNA檢測不到發生率間差異無統計學意義(P>0.05),驗證了上述結果。有研究[18,19]報道稱,Toll樣受體可能參與了抑制HBV DNA復制的過程,而HBeAg可以阻止該受體的激活。因此,HBeAg的高表達可能會引起HBV DNA復制的活躍。同時,HBeAg又是HBV DNA的編碼產物。因此,隨著CHB患者體內HBV DNA高復制,其體內的HBeAg往往呈高表達狀態。多數學者將HBeAg血清學轉換作為提示CHB患者病情穩定的重要指標。本研究結果顯示,peg-IFN-α-2b治療組HBeAg血清學轉換率與IFN-α-2a治療組間差異無統計學意義(P>0.05)。國內相關研究[20]結果也表明,兩種藥物治療的血清學轉換率并無明顯差異,與本研究結果一致。抗病毒治療CHB患者過程中,通常是首先發生HBV DNA陰轉,繼而隨著 HBeAg水平降低及發生血清學轉換,最后才能實現血清HBsAg水平的降低和消失。應用進口Peg-IFNα持續治療1年后,CHB患者HBsAg血清學轉換率可達到11%。本研究結果顯示,在隨訪24周末,peg-IFNα-2b治療組HBsAg血清轉換率為2.0%,而peg-IFNα-2a治療組為1.4%,均低于既往研究結果,可能與治療時間還不夠長有關。本研究結果還顯示,兩組HBeAg血清學轉換率均隨治療時間的延長而升高,表明Peg-IFNα類藥物治療后,其免疫學應答效應的持久性。本研究結果顯示,兩組不良事件主要包括乏力、頭痛、肌肉酸痛和血細胞減少等,但兩組不良事件發生率差異無統計學意義(P>0.05),提示兩種藥物治療的安全性較為相似。
雖然Peg-IFNα治療可提高CHB患者病毒學和生化學應答率,但迄今為止,還缺乏徹底治愈CHB患者的方法。越來越多的研究開始嘗試研制新型藥物治療CHB患者,包括靶向HBV感染的特效藥物及各種免疫調節劑等,并開始研究采用新型的治療方案如Peg-IFNα與其他免疫調節劑(如HBV疫苗)聯合的治療方案,以期能夠早日實現臨床治愈CHB患者。

