卵巢巧克力囊腫術后聯合諾雷得治療的應用研究
林佳


[摘要]目的 探討卵巢巧克力囊腫術后聯合諾雷得治療的應用研究。方法 選取我院婦科治療的50例腹腔鏡治療的卵巢巧克力囊腫患者,收集時間2016年1月~2017年12月,根據治療方式,分為孕三烯酮組及諾雷得組,觀察治療后的疼痛評分的改善、月經量的改變及巧克力囊腫復發情況。結果治療前的諾雷得組及孕三烯酮組患者的疼痛評分無明顯的差異,諾雷得組治療后3個月、6個月、12個月的疼痛評分均明顯的低于孕三烯酮組(P<0.05);治療后的諾雷得組患者的月經增多率明顯低于孕三烯酮組(P<0.05),治療后的諾雷得組患者的月經正常率及月經減少率與孕三烯酮組無明顯的差異(P>0.05);治療3個月后,兩組患者的巧克力囊腫復發率無明顯的差異(P>0.05),治療6個月后,諾雷得組患者的卵巢巧克力囊腫的復發率均明顯低于孕三烯酮組(P<0.05)。結論 腹腔鏡術后聯合諾雷得治療能夠顯著改善疼痛表現,改善月經異常表現并降低巧克力囊腫的復發率。
[關鍵詞]巧克力囊腫;諾雷得;腹腔鏡;疼痛評分
[中圖分類號]R713.6
[文獻標識碼]A
[文章編號]2095-0616(2019)02-93-03
卵巢巧克力囊腫的發生率仍然具有一定的上升趨勢,流行病學研究提示,臨床上卵巢巧克力囊腫的發生率可達262~484/1萬人左右[1-2]。手術治療是目前臨床上治療卵巢巧克力囊腫的主要方式,腹腔鏡手術的創傷小,對于卵巢巧克力囊腫的治療效果較為肯定,其能夠顯著改善患者的短期內臨床癥狀,改善痛經及非近期下腹痛等臨床癥狀[3-5]。但單純腹腔鏡手術治療的局限性同樣較為明顯,單純腹腔鏡手術治療后的患者的復發率仍然較高,治療后的患者痛經表現仍然存在[6]。孕三烯酮能夠通過拮抗孕激素受體,降低孕激素受體激活導致的腺體細胞的持續性增殖效應;諾雷得能夠通過通過抑制下丘腦-垂體軸,抑制卵泡刺激素(FSH)及黃體生成素(LH)的釋放,減輕卵巢囊腫部位病灶組織的腺體的增殖速度[7-8]。為了指導臨床卵巢巧克力囊腫的診療不,本次研究收集了相關臨床病例,探討了腹腔鏡聯合孕三烯酮或者諾雷得治療的臨床效果,現報道如下。
1 資料與方法
1.1 一般資料
選取我院婦科治療的50例卵巢巧克力囊腫患者,收集時間2016年1月~2017年12月,根據治療方式分為孕三烯酮組及諾雷得組,其中對照組26例,年齡28~41歲,平均(34.3±3.5)歲,受教育年限(11.5±4.2)年,病程0.4~1.7年,平均(0.79±0.13)年;觀察組24例,年齡26~50歲,平均(35.5±2.9)歲,受教育年限(11.3±2.9)年,病程0.3~1.7年,平均(0.83±0.12)年。兩組患者在年齡范圍、病程或者受教育程度等方面均差異無統計學意義(P>0.05),具有可比性。
1.2 納入排除標準
1.2.1 納入標準(1)卵巢巧克力囊腫患者,同時需要滿足下列幾個條件:CA125>40U/L,超聲檢查提示盆腔附件區域包塊,合并有明顯的月經期下腹痛或者下腹不適;(2)得到了家屬的簽字同意。
1.2.2 排除標準(1)合并有不同程度的高血壓;
(2)并有基礎性的糖尿病;(3)合并有代謝性或者免疫系統疾病。
1.3 治療方法
所有患者均采用腹腔鏡手術治療,在此基礎上孕三烯酮組:腹腔鏡治療術后3個月開始,口服孕三烯酮(H20080256,華潤紫竹藥業),2.5mg,口服,每周2次,連續治療3~6個月;諾雷得組:腹腔鏡術后聯合GnRH-a(南京凱基生物科技有限公司,H20048594),3.75mg,每28天一次,皮下注射,連續治療3~6個月。
1.4 評估標準
疼痛評分的評估方法:在紙上或尺上劃出10cm長的直線,按毫米劃格,一端為無痛,另一端為極痛,患者根據自身的疼痛體驗情況選擇相應的節點,重復兩次,取平均值。
巧克力囊腫復發的評估:CA125>40U/L,超聲檢查提示盆腔附件區域包塊,合并有明顯的月經期下腹痛或者下腹不適,滿足以上2個或者2個以上可以診斷為巧克力囊腫復發。
1.5 統計學處理
采用統計學軟件SPSS16.0對數據進行統計分析,計量資料以(x±s)表示,采用t檢驗,計數資料以百分數(%)表示,采用χ2檢驗。P<0.05為差異有統計學意義。
2結果
2.1 治療后的兩組患者的疼痛評分的改善情況比較
治療前的諾雷得組及孕三烯酮組患者的疼痛評分無明顯的差異,諾雷得組治療后3、6、12個月的疼痛評分均明顯低于治療前,孕三烯酮組治療后3、6、12個月的疼痛評分均明顯低于治療前;諾雷得組治療后3、6、12個月的疼痛評分均明顯的低于孕三烯酮組。見表1。
2.2 治療后的兩組患者的月經量的改變情況比較
治療后的諾雷得組患者的月經增多率明顯低于孕三烯酮組(P<0.05),治療后的諾雷得組患者的月經正常率及月經減少率與孕三烯酮組無明顯的差異(P>0.05)。見表2。
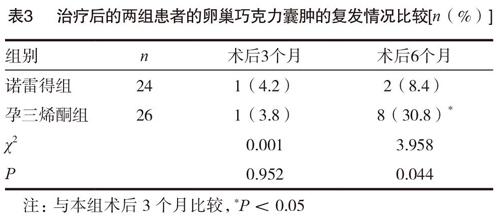
2.3 治療后的兩組患者的卵巢巧克力囊腫的復發情況比較
治療3個月后,兩組患者的巧克力囊腫復發率無明顯的差異(P>0.05),諾雷得組患者的卵巢巧克力囊腫的6個月的復發率率與3個月無明顯的差異(χ2=1.492,P=0.221),治療6個月后,孕三烯酮組患者的卵巢巧克力囊腫的6個月的復發率明顯高于3個月(χ2=25.484,P=0.018);治療6個月后,諾雷得組患者的卵巢巧克力囊腫的復發率均明顯低于孕三烯酮組(P<0.05)。見表3。
3 討論
腹腔鏡手術治療在卵巢巧克力囊腫的臨床治療方面發揮了重要的作用,其對于卵巢囊腫部位的病灶的清除效果較為理想[9]。但鑒于卵巢巧克力囊腫病灶組織中腺體細胞的浸潤性生長特點,腹腔鏡手術治療難以徹底清除病灶組織,術后異位癥腺體細胞的增殖和浸潤性生長表現仍然較為明顯[10-11]。通過對于圍手術期的輔助性用藥,能夠降低腹腔鏡術后卵巢巧克力囊腫的復發風險,抑制異位癥腺體細胞的持續性增殖。孕三烯酮能夠通過對于孕激素受體的拮抗作用,進而輔助腹腔鏡治療卵巢巧克力囊腫[12-13]。但包括孕三烯酮輔助治療在內的相關治療措施,雖然能夠降低術后的復發率,但治療后的患者的痛經表現仍然較為明顯,治療后的不孕的風險仍然較高[14]。
諾雷得能夠通過對于下丘腦-垂體軸的調節作用,抑制FSH或者LH的持續性釋放,降低卵巢巧克力囊腫病灶組織中腺體細胞的增殖,促進異位癥腺體細胞的凋亡,進而減輕其浸潤性臨床癥狀[15]。本次研究中諾雷得輔助腹腔鏡治療后,患者的疼痛表現明顯的改善,諾雷得治療后的疼痛評分的改善主要考慮與諾雷得對于術后腺體細胞的凋亡及新生血管的促萎縮作用有關。王會先[16]研究者也認為,諾雷得輔助腹腔鏡治療后,卵巢巧克力囊腫患者的疼痛評分可平均下降25%以上,同時諾雷得治療后的妊娠成功率可上升10%以上。諾雷得治療后的月經增多率明顯的下降,提示諾雷得輔助治療對于患者月經周期的改善作用,這主要考慮與諾雷得對于患者術后性激素水平的穩定作用有關。治療3個月后、6個月后,諾雷得組患者的卵巢巧克力囊腫的復發率均明顯低于孕三烯酮組,進一步提示了諾雷得的輔助治療價值,這主要由于諾雷得能夠進一步抑制異位癥組織中內膜腺體細胞的變形能力,抑制腺體細胞再生和浸潤臨近組織導致的卵巢囊腫的復發。
綜上所述,腹腔鏡術后聯合諾雷得治療能夠顯著改善疼痛表現,改善月經異常表現并降低巧克力囊腫的復發率。
[參考文獻]
[1] Minas V,Dada T.Laparoscopic treatment of endometriosis and effects on quality of life:A retrospective study using the short form EHP-5 endometriosis specific questionnaire[J].Journal of Obstetrics and Gynaecology,2014,34(4):336-340.
[2] Deguara CS,Liu B,Davis C.Measured symptomatic and psychological outcomes in women undergoing laparoscopic surgery for endometriosis[J].Current Opinion in Obstetricsand Gynecology,2013,25(4):299-301.
[3]孫彥,車艷辭.腹腔鏡手術聯合藥物治療子宮內膜異位癥臨床效果的Meta分析[J].現代婦產科進展,2015,24(1):37-39.
[4]王彧,范可心.腹腔鏡手術與開腹手術治療子宮內膜異位癥性不孕的療效比較[J].中國婦幼保健,2014,29(4):630-632.
[5]李強.腹腔鏡下卵巢巧克力囊腫剝除術后輔以不同藥物治療對患者性激素及預后效果分析[J].中國醫藥科學,2017,7(22):19-22.
[6] Menakaya U,Reid S,Lu C,et al.Performance ofultrasound-based endometriosis staging system(UBESS) for predicting level of complexity of laparoscopic surgery for endometriosis[J].Ultrasound in Obstetrics & Gynecology,2016,48(6):786-795.
[7]吳俞虹,陳錦紅.注射用醋酸亮丙瑞林微球對子宮內膜異位癥患者腹腔鏡術后的影響[J].中國衛生標準管理,2015,6(28):96-97.
[8]殷婉萍,吳少敏,黎佩瑩.腹腔鏡手術聯合GnRh-a藥物治療子宮內膜異位伴不孕的臨床研究[J].海南醫學,2017,28(22):3666-3668.
[9] Yeung P.The Laparoscopic Management of Endometriosis in Patients with Pelvic Pain[J].Obstetrics and Gynecology Clinics of North America,2014,41(3):371-383.
[10] Shah P,Adlakha A. Laparoscopic management of moderate:Severe endometriosis[J].Journal of Minimal Access Surgery,2014,10(1):27-29.
[11]王芳芳,傅朝霞,袁慶新.子宮內膜異位癥患者腹腔鏡術后應用GnRH-a的效果分析[J].中國生化藥物雜志,2014,34(7):108-110.
[12]周小玲,陳文慧,黎雪玲.腹腔鏡術聯合藥物治療子宮內膜異位癥伴不孕患者的療效及對妊娠結局、不良反應的影響[J].右江民族醫學院學報,2017,39(4):272-275.
[13]鐘健.腹腔鏡手術聯合藥物治療卵巢囊腫的臨床效果[J].中國當代醫藥,2018,25(4):116-118.
[14]潘偉,俞磊.促性腺激素釋放激素激動劑聯合孕三烯酮在子宮內膜異位癥腹腔鏡術后的臨床應用[J].中國臨床研究,2016,29(4):549-551.
[15]楊曉瓊,杜小琴.腹腔鏡手術聯合戈舍瑞林治療子宮內膜異位癥合并不孕癥的療效及對血清MMP-9、TIMP-1水平的影響[J].中國婦幼保健,2017,32(18):4486-4489.
[16]王會先.腹腔鏡手術聯合促性腺激素釋放激素激動劑治療浸潤型子宮內膜異位癥的效果觀察[J].中國綜合臨床,2014,30(6):666-668.

