電流-時間曲線法測定魚露中的苯乙胺
趙曉娟,周嬋媛,張 敏,陳海光,白衛東
(1.仲愷農業工程學院輕工食品學院,廣東 廣州 510225;2.廣州市廣式傳統食品加工與安全控制重點實驗室,廣東 廣州 510225)
苯乙胺又稱β-苯乙胺,是一種芳香族生物胺,廣泛存在于巧克力、牛奶、肉和葡萄酒中[1-2]。在人體內,苯乙胺是一種生物堿與單胺類神經遞質,能夠提升細胞外液中多巴胺的水平,同時抑制多巴胺神經活化,用于治療抑郁癥。苯乙胺作為重要的醫藥中間體,主要用于合成興奮藥、抗抑郁藥、迷幻劑、神入感激發劑、降食欲劑、支氣管擴張藥等。但人體若攝入過量的苯乙胺,則可能出現惡心、失眠、頭暈和頭痛等不良反應。因此,必須控制從食品中攝入的苯乙胺量,建立苯乙胺的快速、簡便、靈敏的檢測方法具有重要的現實意義。
目前食品中苯乙胺及其他生物胺的檢測方法主要有[3]:色譜法[4-12]、毛細管電泳法[13-16]和生物傳感器法[17-22]等。其中,色譜法由于具有分離效率高、選擇性好、準確可靠等優點而應用最為廣泛,但色譜法的樣品前處理操作繁瑣而耗時,尤其高效液相色譜法在測定生物胺時通常需要進行衍生化反應[4,23],大量化學試劑的使用可能會給環境和人體造成一定的危害。
本研究通過優化電極修飾方法、電化學測試方法和測試條件,建立一種苯乙胺的電化學檢測方法,并利用干擾性、重復性和加標回收實驗等對檢測方法進行評價,旨在建立一種成本低、簡便快速測定苯乙胺含量的方法,為魚露等食品中生物胺的快速檢測及質量控制提供依據。
1 材料與方法
1.1 材料與試劑
魚露 市購;苯乙胺、酪胺、組胺、精胺、亞精胺、腐胺、尸胺、色胺 美國Sigma-Aldrich公司;L-半胱氨酸(L-cysteine,Cys)、氯金酸、殼聚糖 國藥集團化學試劑有限公司;氫氧化鈉、硼氫化鈉 天津福晨化學試劑廠;所用試劑均為分析純;實驗用水均為超純水(電阻率18.2 MΩ·cm)。
1.2 儀器與設備
CHI660E電化學工作站 北京華科普天儀器有限公司;三電極系統:工作電極為金電極(AuE,Φ=2 mm)或修飾的AuE,參比電極為Ag/AgCl電極(飽和KCl溶液),輔助電極為鉑絲電極 上海辰華儀器有限公司;金薄膜微電極(gold thin-film microelectrode,AuME)(由工作(Φ=1 mm)、參比和輔助電極組成) 西班牙Micrux公司;BSA124S電子天平 賽多利斯科學儀器(北京)有限公司;RE-52AA旋轉蒸發儀 上海亞榮生化儀器廠。
1.3 方法
1.3.1 納米金(AuNPs)的制備
AuNPs的制備參照文獻[24-26]方法。所用的玻璃器皿均用HNO3-HCl(1∶3,V/V)混合酸洗滌干凈。稱取適量殼聚糖,溶解在1.0%乙酸溶液中,配成2 mg/mL的溶液30 mL,在電磁攪拌下加入15 mL 10 mmol/L的氯金酸溶液,攪拌30 min,然后在攪拌下逐滴加入6 mL新配制的0.1 mol/L硼氫化鈉溶液,繼續攪拌,直至溶液變為透明的酒紅色,并置于4 ℃冰箱中保存備用。
1.3.2 電極處理
1.3.2.1 AuE的處理
將AuE依次用粒徑為1.0、0.3 μm和0.05 μm的α-Al2O3粉在專用拋光絨毛墊上拋光,每一步均用超純水洗凈,然后依次在HNO3(1+1)、無水乙醇和水中超聲清洗。將預處理后的電極置于0.5 mol/L硫酸溶液中,在-0.3~1.5 V電位區間內,以50 mV/s 的掃描速率進行循環伏安電化學處理,直到獲得穩定的循環伏安響應為止。
1.3.2.2 AuME的處理
將3 μL的0.1 mol/L硫酸溶液滴加在AuME表面,-1.5~1.5 V電位區間內,以0.1 V/s的掃描速率循環伏安處理10 圈,用水淋洗后室溫晾干備用。
1.3.3 修飾電極的制備
分別利用AuNPs和Cys對AuE進行修飾。將3 μL的AuNPs溶膠滴涂在AuE表面,室溫晾干后,即得到納米金修飾金電極(AuNPs/AuE)。將AuE浸入0.1 mol/L Cys的HCl溶液(0.05 mol/L)中,于4 ℃自組裝12 h,取出電極用水淋洗后得到Cys修飾電極(Cys/AuE)。
1.3.4 樣品處理
魚露樣品的處理參照GB 5009.208—2016《食品中生物胺的測定》[27]中的萃取方法。取約15 mL魚露于干凈的小燒杯中,用0.22 μm醋酸纖維濾膜過濾于50 mL燒杯中,在所得濾液中加入氯化鈉使溶液飽和。量取10.0 mL飽和溶液于50 mL離心管中,用1.0 mol/L NaOH溶液調節pH值至12,再加入5 mL正丁醇-三氯甲烷(1∶1,V/V)混合液,旋渦振蕩5 min,于3 600 r/min離心10 min,取上層有機相,且需重復2 次,合并2 次溶液。將混合液置于60 ℃水浴蒸至近干,然后用氮氣吹干。最后加入1 mL pH 12.7的NaOH溶液使殘留物溶解,所得溶液即待測溶液。
1.3.5 測試方法
基于AuE的測試體系是將三電極系統置于pH 12.7的NaOH空白溶液中,在磁力攪拌器均勻快速攪拌下,用積分脈沖安培(integrated pulsed amperometric detection,IPA)法[28](E2電位0.5 V)和電流-時間(I-t)曲線法(初始電位0.1 V)分別進行掃描,待基線穩定后,用微量注射器注入一定量的苯乙胺溶液,再掃描至穩定,測量出響應的電流差(各濃度苯乙胺溶液的響應電流值與NaOH空白溶液的響應電流值之差)。
基于AuME的測試體系是將NaOH空白溶液和不同濃度的苯乙胺溶液依次滴加在電極表面進行掃描。
2 結果與分析
2.1 IPA法測定條件優化
2.1.1 工作電極的選擇
工作電極的形狀和尺寸對其測試性能有重要影響。利用IPA法考察不同濃度的苯乙胺溶液在AuE和AuME上的電化學響應。結果發現,用AuE進行測定時操作簡單方便,基線穩定,1.66×10-6mol/L苯乙胺具有明顯響應,測試靈敏度較高,且響應電流隨著苯乙胺濃度的增加而增加。當用AuME進行測定時,1.0×10-6mol/L和1.0×10-5mol/L苯乙胺溶液與NaOH空白溶液的響應曲線幾乎重疊,說明AuME對低濃度苯乙胺溶液無響應,雖然1.0×10-3mol/L苯乙胺在AuME上具有明顯響應,但基線一直下降,不穩定。因此,選用AuE作為IPA法測定的工作電極。
2.1.2 電極修飾方法的選擇
Cys分子能通過巰基定向自組裝在AuE的表面,其分子中的氨基和羧基兩種活性官能團能增加修飾電極的電催化活性。AuNPs具有大的比表面積和良好的導電性,能增加電極表面的氧化還原反應位點,提高修飾電極的靈敏度,是目前應用最為廣泛的一種金屬納米材料。本研究分別采用Cys和AuNPs對AuE進行修飾,比較AuE和制備的Cys/AuE和AuNPs/AuE對不同濃度苯乙胺溶液的測試效果。由圖1A可知,3 種電極測定苯乙胺的響應電流差由大到小依次為:AuE、Cys/AuE、AuNPs/AuE。由圖1B可知,AuNPs/AuE在NaOH空白溶液中掃描時基線達到穩定所需的時間較長,主要是由于利用IPA法掃描過程中,電位的變化引起電極表面AuNPs的穩定性發生改變;而Cys/AuE與AuE測定苯乙胺的安培響應曲線變化趨勢近乎相同,穩定性均良好,說明與AuE相比,利用Cys修飾AuE對苯乙胺的測試效果沒有顯著影響和改善。因此,選擇AuE進行測試。
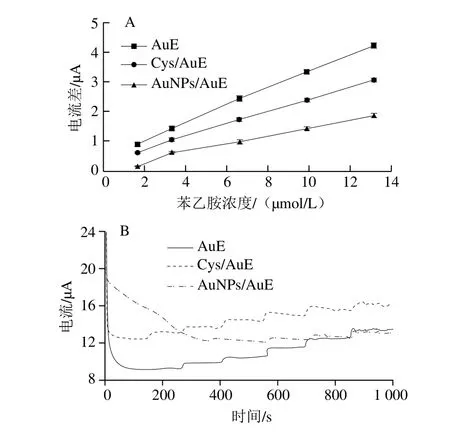
圖1 不同電極測定苯乙胺的電流差比較圖(A)和IPA圖(B)Fig. 1 Comparison of current difference (A) and integrated pulsed amperometric responses (B) of phenethylamine on different electrodes
2.1.3 氧化峰電位和E2電位的確定
將AuE先后置于pH 12.7的NaOH和1.0×10-3mol/L苯乙胺溶液中,用流體力學調制伏安法[29-31]在0~0.9 V進行掃描,通過比較兩者的伏安曲線,確定苯乙胺的氧化峰電位在0.3~0.65 V之間。根據氧化峰電位,將IPA法的E2電位分別設置為0.3、0.4、0.45、0.5、0.55、0.6 V和0.65 V,運用IPA法測試8.32×10-7mol/L和1.66×10-6mol/L苯乙胺溶液,比較不同電位參數下AuE對于低濃度苯乙胺的響應情況,確定最優電位。如圖2所示,當E2電位為0.3~0.5 V時,測得的電流差值逐漸增大,在0.5 V時苯乙胺的電流響應達到最大值,然后電流差值隨著E2電位的增加而減小。因此,最優E2電位確定為0.5 V。

圖2 E2電位對苯乙胺電化學響應的影響Fig. 2 Effects of E2 potential on the electrochemical response of phenethylamine
2.1.4 IPA法標準曲線的建立
按照2.1.3節優化的E2電位,使用IPA法考察不同濃度苯乙胺在AuE上電流響應的變化。結果發現,隨著苯乙胺濃度的增加,IPA響應曲線呈階梯式上升。電流差ΔI與苯乙胺溶液濃度c在8.32×10-7~1.40×10-5mol/L范圍內呈良好的線性關系,線性回歸方程為:ΔI = 0.279 8c+0.389 3(r = 0.997),基于3 倍的信噪比,得到該法測定苯乙胺的檢出限為2.8×10-7mol/L。
2.1.5 干擾性實驗結果

圖3 IPA法測定3 種生物胺的電流差比較圖Fig. 3 Comparison of current difference of three kinds of biogenic amines on AuE by IPA
以1.66×10-6、3.32×10-6mol/L和6.62×10-6mol/L苯乙胺溶液為對照,采用IPA法考察相同濃度的酪胺、組胺對苯乙胺測定的干擾情況,結果如圖3所示。利用該法測試苯乙胺時,酪胺和組胺均有明顯響應,會對苯乙胺的測試結果產生干擾,食品中其他幾種常見的生物胺很可能也有干擾。因此,采用IPA法可以對食品中的組胺、酪胺和苯乙胺等生物胺的總量進行測定,但是該法不能對苯乙胺含量進行準確測定。
2.2 I-t曲線法
2.2.1 工作電極的選擇
運用I-t曲線法考察不同濃度苯乙胺溶液在AuE和AuME表面的電化學響應。結果發現,用I-t曲線法測定時,苯乙胺在兩種電極上的響應靈敏度均明顯高于IPA法。此外,與IPA法相似,AuE的響應基線穩定,能夠測定8.26×10-8mol/L苯乙胺溶液,測試靈敏度高于AuME,且響應電流差值隨著苯乙胺濃度的增加而增加。因此,選用AuE作為I-t曲線法測定的工作電極。
2.2.2 修飾方法的選擇
采用AuNPs對AuE進行修飾,比較AuE和AuNPs/AuE對8.26×10-8、2.49×10-7、5.8×10-7、9.08×10-7mol/L和1.23×10-6mol/L苯乙胺溶液的測試效果。結果發現,苯乙胺在AuE和AuNPs/AuE上I-t響應曲線的變化趨勢大致相同,穩定性良好,但是響應電流差的大小有明顯區別。相同濃度苯乙胺在AuNPs/AuE上的響應電流差明顯比AuE的大,隨著苯乙胺濃度的增加,電流差增大的幅度越明顯,說明AuNPs/AuE對苯乙胺具有良好的測試效果,AuNPs的修飾增加了AuE的響應靈敏度。因此,選擇AuNPs作為AuE的修飾材料。
2.2.3 初始電位的優化
I-t曲線法對苯乙胺的響應電位與IPA法不同,因此,首先需要測出苯乙胺溶液的開路電位,然后以開路電位為基礎,對I-t曲線法的初始電位進行優化。實驗測得1.0×10-6mol/L苯乙胺溶液的開路電位為0.083 V。根據開路電位,將I-t曲線法的初始電位分別設置為0.06、0.08、0.1、0.2 V和0.3 V,考察不同濃度苯乙胺在AuNPs/AuE上的響應情況,結果如圖4所示。初始電位的改變對苯乙胺的電流響應值具有顯著影響,與其他電位相比,當初始電位為0.1 V時,不同濃度苯乙胺在AuNPs/AuE上的響應電流值均最大。而當初始電位為0.3 V時,苯乙胺在電極表面沒有響應,隨著苯乙胺濃度的增加,掃描曲線無明顯變化。因此,選擇0.1 V作為I-t曲線法的最佳初始電位。
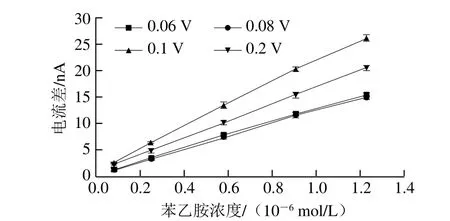
圖4 不同初始電位時苯乙胺在AuNPs/AuE上的電流差比較圖Fig. 4 Comparison of current difference of phenethylamine at different initial potentials on AuNPs/AuE
2.2.4 I-t曲線法標準曲線的建立
使用I-t曲線法考察不同濃度苯乙胺在AuNPs/AuE上電流響應的變化情況。結果顯示,隨著苯乙胺溶液濃度的增加,I-t曲線呈階梯式下降。苯乙胺在電極上的響應電流差-ΔI與濃度c在4.13×10-8~4.72×10-6mol/L范圍內呈良好的線性關系,線性回歸方程為:-ΔI= 7.783c+1.181(r = 0.997),該法對苯乙胺的檢出限為1.4×10-8mol/L(RSN= 3),雖然高于超高效液相色譜-串聯質譜法[32]的2.5×10-10mol/L,但明顯低于2.1節IPA法和文獻[4,15-16,28]報道的檢出限水平。該電化學檢測方法試劑用量少、靈敏度較高、成本低、簡便快速,可以與色譜法形成優勢互補,在苯乙胺的快速檢測領域發揮其應用價值。
2.2.5 干擾性實驗結果
采用I-t曲線法考察不同濃度的酪胺、組胺、精胺、亞精胺、腐胺、尸胺、色胺對測定苯乙胺的干擾情況。結果發現,除色胺外,相同濃度甚至10 倍于苯乙胺濃度的其余6 種生物胺對苯乙胺的測定均無明顯干擾。2.5×10-7、5.8×10-7、1.23×10-6mol/L苯乙胺和色胺的電化學響應如圖5所示。與苯乙胺相比,相同濃度色胺的響應電流差值明顯較小。由于色胺在水產品及其制品中含量相對較少,所以利用該法測定水產品及其制品中的苯乙胺時可不考慮色胺的影響。

圖5 I-t曲線法測定苯乙胺和色胺的電流差比較圖Fig. 5 Comparison of current difference of phenethylamine and tryptamine on AuNPs/AuE by I-t method
2.2.6 重復性實驗結果
用6支AuNPs/AuE對濃度為1.66×10-7、3.32×10-7mol/L的苯乙胺溶液分別進行測定,測得苯乙胺響應電流的相對標準偏差分別為4.7%和4.0%,表明AuNPs/AuE的重復性良好。
2.3 樣品分析與回收率的測定結果
將魚露調味品按照1.3.4節方法進行前處理,然后使用I-t曲線法進行測定。測得該魚露測試樣品液中苯乙胺濃度為1.85×10-7mol/L,經換算得出該魚露樣品中苯乙胺濃度為1.11×10-5mol/L。為驗證此方法的準確性,對魚露樣品進行加標回收實驗。魚露樣品中不同濃度(1.66×10-7、3.31×10-7mol/L)苯乙胺的加標回收率為90.0%~110.8%,其相對標準偏差分別為4.8%和6.2%。
3 結 論
本實驗采用IPA法和I-t曲線法測定苯乙胺,對工作電極、電極修飾方法、測定電位分別進行選擇和優化,并比較兩種方法的測定效果。結果表明:利用AuE和IPA法可以對食品中的組胺、酪胺和苯乙胺等生物胺的總量進行測定,但是該法不能對苯乙胺含量進行準確測定;采用膠體金修飾的AuE,在初始電位為0.1 V時,運用I-t曲線法測定苯乙胺具有良好的選擇性和較高的靈敏度,檢出限為1.4×10-8mol/L,測定魚露樣品中苯乙胺的加標回收率在90.0%~110.8%之間,該法適用于魚露樣品中苯乙胺的測定。

