柴黃口服液對靶動物雞安全性試驗研究
劉 毅張國榮耿智霞賈 興瞿紅穎劉 欣?宋婷婷劉 靜魏麗娟劉 欣史萬玉
(1.河北遠征藥業有限公司,石家莊050041;2.河北省獸藥工程技術研究中心,石家莊050041;3.黃驊市農業局,滄州061100;4.河北農業大學,保定071001)
我國大部分地區每年夏季都會出現持續性高溫、高濕天氣,如果外界環境溫、濕度過高,特別是通風不良等,雞體散熱困難,體內新陳代謝和生理機能紊亂,嚴重影響到雞的采食量、生產繁殖性能、飼料利用率以及產品質量下降,并可導致雞在短時間內大量死亡。長期以來,高溫、高濕給畜禽業帶來不可忽視的經濟損失[1-3],因此,如何有效的緩解由高溫、高濕引起的疾病,已經引起國內外學者們的高度重視,而進一步開發和研究能夠緩解或修復動物由高溫、高濕引起的疾病損傷的安全型藥物將對畜禽生產具有重要的現實意義。
柴黃口服液由柴胡、黃芩兩味藥材提取組成,具有清熱燥濕的作用,擬臨床用于預防高溫、高濕引起的雞群發熱,精神不振,食欲下降。為了全面評價本制劑在臨床上使用的安全性,研究根據《獸藥研究技術指導原則匯編》[4],通過靶動物安全試考察其用于靶動物雞的的安全性及安全劑量范圍,為臨床試驗給藥方案的制定提供依據。
1 材料與方法
1.1 材料
1.1.1 試驗動物及飼料 1日齡體重相差±5 g 的羅斯308 肉雛雞:購自河北大午農牧集團種禽公司,嚴格按照管理標準進行飼養。
飼料:購自河北大午農牧集團生產的雛雞全價飼料。
1.1.2 供試藥品及試劑 柴黃口服液:河北遠征藥業有限公司生(含量:每1 mL 相當于原生藥1 g,批號:150312)。
門冬氨酸氨基轉移酶試劑盒、丙氨酸氨基轉移酶試劑盒、尿素氮試劑盒、肌酐試劑盒購于北京北化康泰臨床試劑有限公司。
1.1.3 儀器設備 TBA-120FR 全自動生化分析儀(日本東芝);08-230-2C 型滑走切片機(日本愛爾瑪公司);S-35 型羽毛刀片(日本愛爾瑪公司)。
1.2 方法
1.2.1 動物分組與處理 根據《獸用中藥、天然藥物臨床試驗技術指導原則》中對靶動物安全試驗的分組要求,從新購進的1日齡體重相差±5 g 的羅斯308 肉雛雞中選取健康活潑的雛雞80 只,隨機分為四組,每組20 只。其中1~3 組為試驗組,分別在飲水中全程添加擬推薦劑量(1 mL/L)1 倍、3 倍和5倍的柴黃口服液;4 組為不用藥對照組,全程飲用新鮮自來水。試驗期6 周,每天觀察并記錄各組雞的臨床體征,每周末稱重1 次,6 周末試驗結束時心臟采血,用全自動血液細胞分析儀測定白細胞計數及分類、紅細胞計數、血紅蛋白含量測定各組雞的血液學指標,分離血清,用門冬氨酸氨基轉移酶試劑盒、丙氨酸氨基轉移酶試劑盒、尿素氮試劑盒和肌酐試劑盒測定AST、ALT、BUN 和CRE 等血液生化指標。同時進行剖檢,觀察各臟器有無眼觀和顯微結構上的變化。
1.2.2 檢測指標及方法 臨床體征變化觀察:試驗過程中,每天觀察并記錄各組雞的臨床體征,比較各組雞群之間有無異常變化。
體重測定:試驗過程中,每周末測定各組雞的體重變化情況,比較各組雞群之間的體重有無異常變化。
血液生理指標的測定:6 周末試驗結束時各組雞心臟采血,測定各組雞的血液生理指標的變化情況。
①紅細胞總數的測定 采用試管法,即將供檢血稀釋200 倍后,用血細胞計數板計數一定容積內的紅細胞數,最后計算出每升血液中的紅細胞數。紅細胞總數的計算公式:紅細胞總數(×1012個/L)=X/100×1012。式中的X為5 個中方格的紅細胞總數。
②白細胞總數的測定 采用試管法,即將供檢血稀釋20 倍后,用血細胞計數板計數一定容積內的白細胞數,最后計算出每升血液中的白細胞數。白細胞總數的計算公式:白細胞總數(×109個/L)=X×50×106。式中的X為4個大方格中的白細胞總數。
③血紅蛋白含量的測定 采用比色法。紅細胞遇酸溶解后會游離出血紅蛋白,并被酸化為褐色的酸性血紅素,稀釋后與標準比色柱比色,即可求得血紅蛋白的含量。
④淋巴細胞比例的測定 用未抗凝血,制作血涂片,姬姆薩染色法染色,采用白細胞胞分類法對白細胞計數,計算淋巴細胞比例。
血液生化指標的測定:試驗組在飲水中以推薦劑量的1 倍、3 倍、5 倍劑量加入柴黃口服液飲喂雛雞,對照組正常飲水,6 周后,剖殺取血液制備血清,測定肝功能指標門冬氨酸氨基轉移酶(AST)及丙氨酸氨基轉移酶(ALT)和腎臟功能指標尿素氮(BUN)、肌酐(CRE)。
剖檢變化觀察:6 周末試驗結束后,將各組雞進行剖檢,觀察其眼觀剖檢變化。
組織切片觀察:取肝臟、腎臟、脾臟、心臟固定,石蠟切片,H-E 染色并觀察。
1.3 數據處理及統計 應用SPSS17.0 軟件對數據進行單因素方差分析。
2 結果與分析
2.1 臨床表現 在整個試驗過程中,1 倍、3 倍、5倍劑量試驗組和對照組的雛雞,活潑好動,能自由攝食、飲水,糞便正常。整個試驗過程所有雛雞均存活,未出現中毒性臨床癥狀。
2.2 體重變化 由表1可知,肉雞在試驗期前3 周內各組間的平均體重均無顯著性差異(P>0.05)。只是在42日齡試驗結束時,1 倍劑量組和3 倍劑量組肉雞的體重均顯著高于5 倍劑量組和不用藥對照組(P<0.05);而1 倍劑量組和3 倍劑量組間,以及5 倍劑量組和對照組間均無顯著性差異(P>0.05) 。
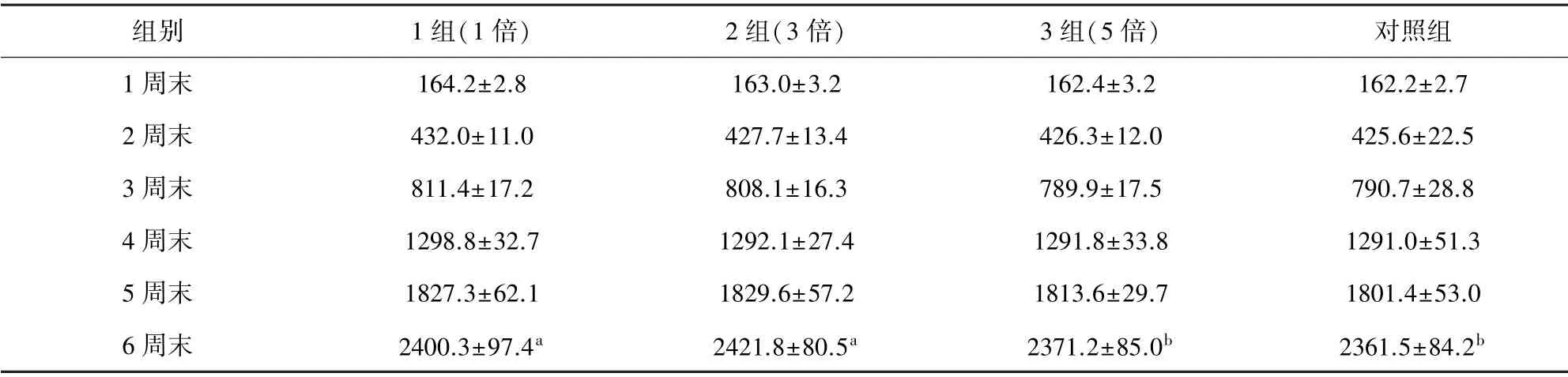
表1 試驗各組體重情況( ±SD) (g/只)Tab 1 Weight of each group in the trial( ±SD)
2.3 血液生理指標變化 由表2可知,各試驗組與對照組的紅細胞總數,血紅蛋白含量、白細胞總數均差異不顯著(P>0.05),各試驗組之間的淋巴細胞比例也均無顯著差異(P>0.05)。

表2 各組雛雞血液生理指標( ±SD)Tab 2 Blood physiological indexes of chickens in each group
2.4 血液生化指標變化情況 由表3可知,試驗組雛雞血清中門冬氨酸氨基轉移酶(AST)、丙氨酸氨基轉移酶(ALT)、尿素氮(BUN)和肌酐(CRE)的含量均與對照組差異不顯著(P>0.05 ),且各試驗組各劑量水平之間差異也不顯著(P>0.05)。

表3 對血液生化指標的影響( ±SD)Tab 3 The influence on blood biochemical indexes
2.5 大體剖檢變化 試驗結束時對各組雛雞進行剖檢觀察。結果發現,各組雞的臟器顏色,形狀,大小、位置等均未見異常變化。
2.6 主要臟器病理組織切片觀察 在進行上述剖檢檢查時,采集各組雞的心、肝、脾、腎等實質器官,制作石蠟切片,進行組織結構的顯微觀察。結果發現,各組織器官的細胞輪廓完整,排列有序;胞質豐滿,細胞核結構清晰,符合正常組織形態和結構特點,說明柴黃口服液對所采集組織無毒性作用(圖1~圖4)。
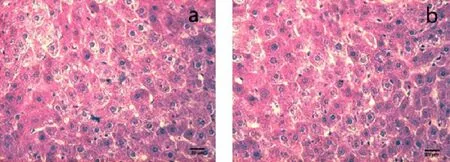
圖1 肝臟組織切片顯微結構Fig 1 Microstructure of liver tissue slices
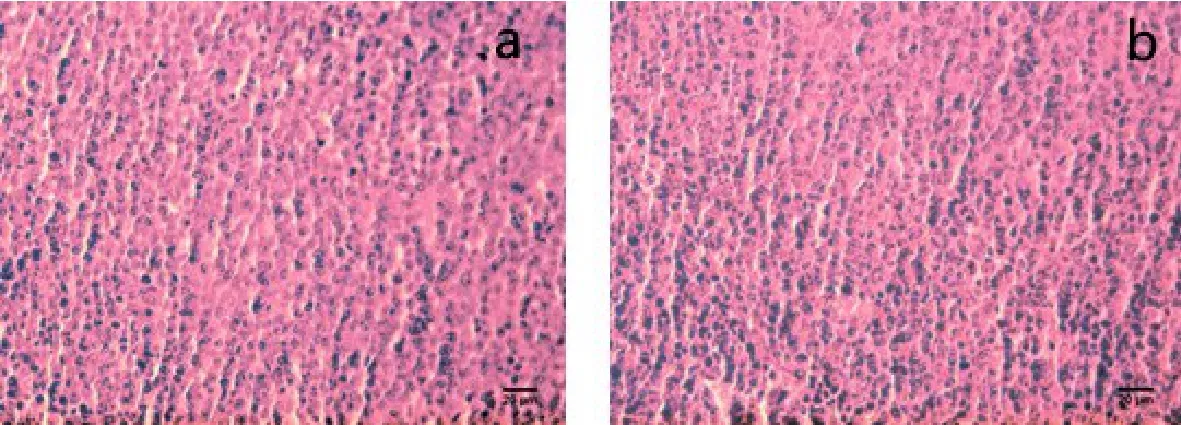
圖2 脾臟組織切片顯微結構Fig 2 Microstructure of splenic tissue section
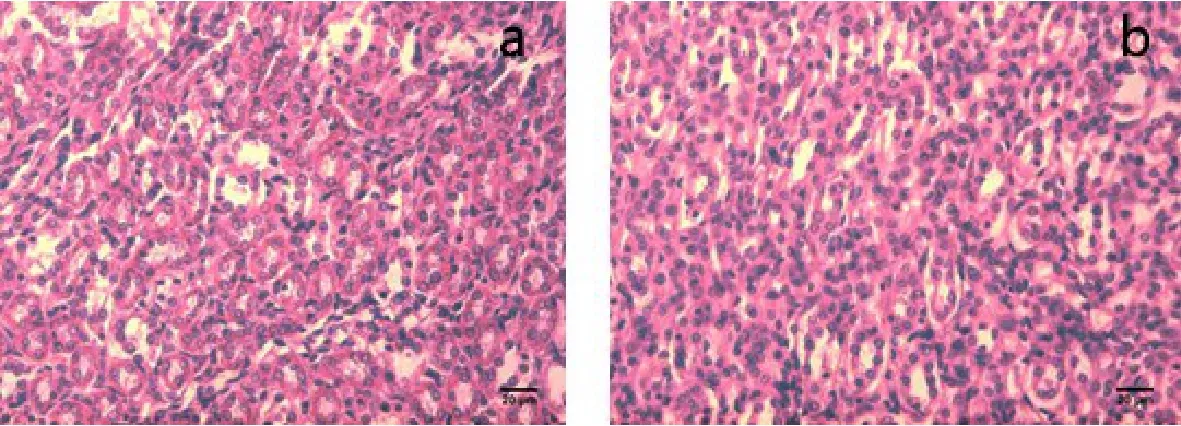
圖3 脾臟組織切片顯微結構Fig 3 Microstructure of splenic tissue section
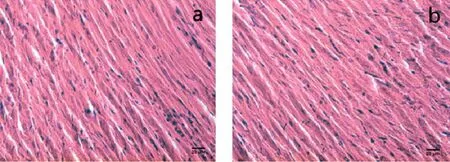
圖4 心臟組織切片顯微結構Fig 4 Microstructure of cardiac tissue slices
3 討論與結論
中獸醫學認為,雞群長時間處于高溫、高濕的環境中,熱邪極易侵襲機體,引起機體發熱。柴黃口服液由柴胡和黃芩配伍組成,方中柴胡可瀉半表半里之表熱[5],黃芩可瀉半表半里之里熱[6-7];柴胡升清陽,黃芩降濁火。二藥相合,升清降濁,調和表里,和解少陽,清少陽之邪熱。柴胡又長于開郁,黃芩又善于泄熱。兩藥相互為用,既可調肝膽之氣機,又可清泄內蘊之熱邪[8-10]。
靶動物安全性試驗是觀察不同劑量受試獸藥作用于靶動物后從有效作用到毒性作用,甚至到致死作用的動態變化的過程。該試驗旨在考察受試獸藥使用于靶動物的安全性及安全劑量范圍,為進一步臨床試驗給藥方案的制定提供依據。為觀察不同劑量柴黃口服液作用于靶動物后從有效作用到毒性作用的動態變化過程,而進行了本次試驗。采用與臨床應用相同的給藥途徑,給藥為全程給藥。結果發現:柴黃口服液三個劑量組雛雞狀態良好,生長正常,未出現中毒癥狀及死亡,血液生化生理指標、剖檢以及組織顯微結構等與對照組相比均無明顯差異。只是在42日齡試驗結束時,1 倍劑量組和3 倍劑量組肉雞的體重均顯著高于5 倍劑量組和不用藥對照組(P<0.05),這種變化并非受試藥物柴黃口服液的毒副作用,可能與柴黃口服液能夠清解雛雞脾胃濕熱,進一步調動脾胃功能,提高雛雞采食、消化和吸收有關。而5 倍劑量組卻并未提高雛雞的體重,可能與藥物濃度太高,超過柴黃口服液有效藥物濃度范圍有關。因此,柴黃口服液按照1 倍(1mL/L)、3 倍(3mL/L)、5 倍(5mL/L)推薦劑量,分別連續飲水給藥42 d,均對靶動物雞無明顯毒副作用。因此,柴黃口服液在臨床上以1mL/L在雞飲水中混飲是安全的。

