前蛋白轉化酶枯草溶菌素Kexin 9型抑制劑在缺血性卒中二級預防中的臨床應用專家共識
中國卒中學會
近30年來,我國卒中的患病率和發病率逐年攀升,已成為我國全因死亡的首要疾病[1-2]。2013年對全國31個省份進行的一項入戶調查顯示,我國卒中患病率為1115/10萬人年,發病率為247/10萬人年,死亡率為115/10萬人年,在各卒中亞型中,缺血性卒中約占70%[3]。缺血性卒中復發率高,流行病學數據顯示中國缺血性卒中患者1年內再發心腦血管事件發生率達11.8%,故有效的二級預防至關重要[4]。降脂治療是卒中二級預防的基石之一。強化降低膽固醇預防卒中(Stroke Prevention by Aggressive Reduction in Cholesterol Levels,SPARCL)研究顯示,對于非心源性缺血性卒中或TIA的患者,強化阿托伐他汀(80 mg/d)治療5年,可使患者卒中復發相對危險降低16%(HR0.84,95%CI0.71~0.99,P=0.03)[5]。在SPARCL研究的事后分析中,與LDL-C水平降幅度<50%相比,應用阿托伐他汀使LDL-C水平降幅超過50%的患者,其卒中復發風險顯著降低31%;且LDL-C降至<1.8 mmol/L與降至≥2.6 mmol/L相比,卒中復發風險顯著降低28%[6]。通過對支架與強化內科治療在顱內動脈狹窄患者預防復發性卒中(Stenting and Aggressive Medical Management for Preventing Recurrent Stroke in Intracranial Stenosis,SAMMPRIS)研究顯示,給予顱內動脈狹窄(70%~99%)患者單純強化藥物治療,嚴格接受降壓、降脂、降糖及抗血小板治療,患者獲益更大[7-8]。《中國缺血性卒中和短暫性腦缺血發作二級預防指南(2014)》推薦對于缺血性卒中或TIA的患者予高強度他汀類藥物長期治療,且推薦LDL-C應下降≥50%或LDL-C≤1.8 mmol/L[9]。而在實際臨床中,雖然我國缺血性卒中患者使用降脂治療的比例已高達79.6%,但LDL-C達標率(<1.8 mmol/L)僅為27.4%[10],降脂治療現狀不容樂觀。
前蛋白轉化酶枯草溶菌素Kexin 9型(proprotein convertase subtilisin/kexin type 9,PCSK9)是一種由肝細胞合成的蛋白質,它對于肝細胞表面低密度脂蛋白受體數量的調節起著至關重要的作用[11]。針對該蛋白靶點的新型降脂藥物——PCSK9抑制劑,通過選擇性結合PCSK9,上調低密度脂蛋白受體數量,從而能大幅度降低血液中LDL-C水平[11]。近年來一系列的研究結果也證明了PCSK9抑制劑在動脈粥樣硬化心血管疾病(atherosclerotic cardiovascular disease,ASCVD)(指有心肌梗死、非出血性卒中或癥狀性周圍動脈疾病史)二級預防中的作用[12-13]。鑒于目前我國缺血性卒中患者較高的心腦血管事件發生率,血脂達標不佳,在規范傳統降脂藥物治療同時,PCSK9抑制劑有望為臨床醫師提供額外的降脂方案選擇。因此,中國卒中學會組織國內本領域專家,對于最新的PCSK9抑制劑研究證據及國外PCSK9抑制劑相關指南及共識進行了梳理,征求多方建議,組織專家討論,制訂本共識,以指導和規范PCSK9抑制劑在我國缺血性卒中患者中的應用(本共識采用的證據強度及推薦級別參照中國卒中學會指南撰寫規范,表1)[14]。
1 PCSK9抑制劑關鍵醫學證據及國內外指南共識推薦
目前全球已獲批的PCSK9抑制劑主要是單克隆抗體依洛尤單抗(evolocumab)和阿利西尤單抗(alirocumab)。多項薈萃分析及臨床研究顯示,PCSK9抑制劑可以在單獨或在聯合他汀類藥物治療基礎上長期有效地降低LDL-C水平(降幅可達60%)[12-13,15-17]。其中一項薈萃分析納入25項PCSK9抑制劑療效和安全性的隨機對照研究,共12 200例患者,結果顯示,與安慰劑相比,依洛尤單抗(420 mg,每月1次)可顯著降低LDL-C達54.6%,和依折麥布相比,可顯著降低LDL-C達36.3%。使用依洛尤單抗(140 mg,每2周1次)效果相當或更加顯著。與安慰劑相比,阿利西尤單抗(50~150 mg,每2周1次)可顯著降低LDL-C達52.6%,和依折麥布相比,可顯著降低LDL-C達29.9%[15]。PCSK9抑制劑整體安全性及耐受性良好,主要的不良事件為注射部位局部反應,血清轉氨酶、膽紅素、肌酸激酶異常,肌肉相關不良事件,神經認知不良事件及出血性卒中,其發生率均與安慰劑相似[12-13,17-20]。依洛尤單抗對高膽固醇血癥長達5年的開放標簽(The Open-Label Study of Long-term Evaluation Against LDL-C,OSLER-1)研究共納入1324例患者,該研究在第一階段為開放標簽、隨機對照設計,患者按照2∶1比例隨機分配至依洛尤單抗聯合標準治療組或標準治療組(標準治療由醫師根據所在地臨床實踐制定,包括藥物治療、飲食及運動),共干預52周,隨后進入第二階段,所有患者均接受依洛尤單抗聯合標準治療,直到研究結束。在5年的研究期,依洛尤單抗420 mg,每月1次可持久降低LDL-C水平,第5年仍維持高達58%的降幅。嚴重不良事件發生率不超過10%,因不良事件停藥的患者不超過3%。潛在過敏反應發生率不到10%。且隨治療時間延長,任何不良事件發生率呈降低趨勢[21]。
PCSK9抑制劑的有效性證據主要來自兩項心血管結局研究。PCSK9抑制劑在高危人群中的心血管預后(Further Cardiovascular Outcomes Research with PCSK 9 Inhibition in Subjects with Elevated Risk,FOURIER)研究是一項多中心、隨機、雙盲、安慰劑對照研究,共納入27 564例40~85歲正在接受最優他汀治療,且LDL-C水平仍≥1.8 mol/L或非HDL-C≥2.6 mmol/L的ASCVD患者,并具有≥1個主要危險因素或≥2個次要危險因素[12]。基線時,患者距離上次心肌梗死或卒中的中位時間3.2~3.4年。兩組患者的LDL-C水平均為2.38 mg/dL,使用高強度和中等強度他汀類藥物治療的患者比例分別為69.3%和30.4%。將患者隨機分配到依洛尤單抗組(140 mg,每2周1次或420 mg,每月1次)或安慰劑組。中位隨訪2.2年。結果顯示,依洛尤單抗組的主要終點心血管死亡、心肌梗死、卒中、因不穩定性心絞痛住院或冠狀動脈血運重建的復合終點事件發生率比安慰劑組降低了15%(HR0.85,95%CI0.79~0.92,P<0.001),次要終點心血管死亡、心肌梗死和卒中的復合終點事件發生率比安慰劑組降低20%(HR0.80,95%CI0.73~0.88,P<0.001)。同時,依洛尤單抗治療使患者的心肌梗死相對危險顯著降低達27%,卒中相對危險顯著降低21%(其中缺血性卒中相對危險顯著降低達25%),冠狀動脈血運重建的相對危險降低22%,但對因不穩定性心絞痛住院、心血管死亡或因心功能能衰竭加重住院、任何原因導致的死亡無明顯影響。在FOURIER研究的卒中亞組中,對既往有卒中病史的5337例患者和無卒中病史的22 227例患者進行分析[22]。患者基線LDL-C水平分別為2.52 mmol/L和2.53 mmol/L,從發生卒中事件至隨機分組的時間<1年的比例分別為27%和26%。結果發現,與安慰劑相比,依洛尤單抗治療可以顯著降低非出血性卒中患者的主要終點事件相對危險達15%(13.9%vs14.6%,HR0.85,95%CI0.72~1.00,P=0.047),但對患者的心血管死亡、卒中復發無明顯影響。急性冠狀動脈綜合征應用阿利西尤單抗心血管預后評價(Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment With Alirocumab,ODYSSEY OUTCOMES)研究是阿利西尤單抗對急性冠狀動脈綜合征(acute coronary syndrome,ACS)患者心血管結局的一項多中心、隨機、雙盲、安慰劑對照研究,共納入18 924例≥40歲的隨機化前1~12個月因ACS住院(中位時間為2.6個月),LDL-C≥1.8 mmol/L,非HDL-C≥2.6 mmol/L或載脂蛋白B≥80 mg/dL,且正在接受高強度或最大耐受劑量他汀類治療的患者[13]。兩組患者的LDL-C水平均為2.38 mmol/L,88.8%的患者接受每日阿托伐他汀40~80 mg或瑞舒伐他汀20~40 mg治療。將患者隨機分配到阿利西尤單抗(75 mg,每2周1次,皮下注射)治療組或匹配安慰劑組。中位隨訪2.8年。結果顯示,阿利西尤單抗治療組的主要療效終點——冠狀動脈粥樣硬化性心臟病死亡、非致死性心肌梗死、致死性或非致死性缺血性卒中或因不穩定性心絞痛住院的復合終點事件發生率比安慰劑組降低15%(9.5%vs11.1%,HR0.85,95%CI0.78~0.93,P<0.001)。一項薈萃分析納入了54項PCSK9抑制劑干預性研究,共97 910例患者[23]。結果顯示,與安慰劑相比,PCSK9抑制劑可以顯著降低主要心血管不良事件相對危險達16%(HR0.84,95%CI0.79~0.89),非致死性心肌梗死相對危險達17%(HR0.83,95%CI0.74~0.93),任何卒中相對危險達25%(HR0.75,95%CI0.79~0.89)。

表1 中國卒中學會2017《指南制定指導手冊》中的推薦意見分類和證據等級
目前國際上多個指南共識對于PCSK9抑制劑的使用給予了推薦意見[24-26]。各指南共識對于推薦人群和起始治療閾值略有差別,但主要應用人群包括ASCVD和家族性高膽固醇血癥(familial hypercholesterolemia,FH)。詳細推薦見表2。
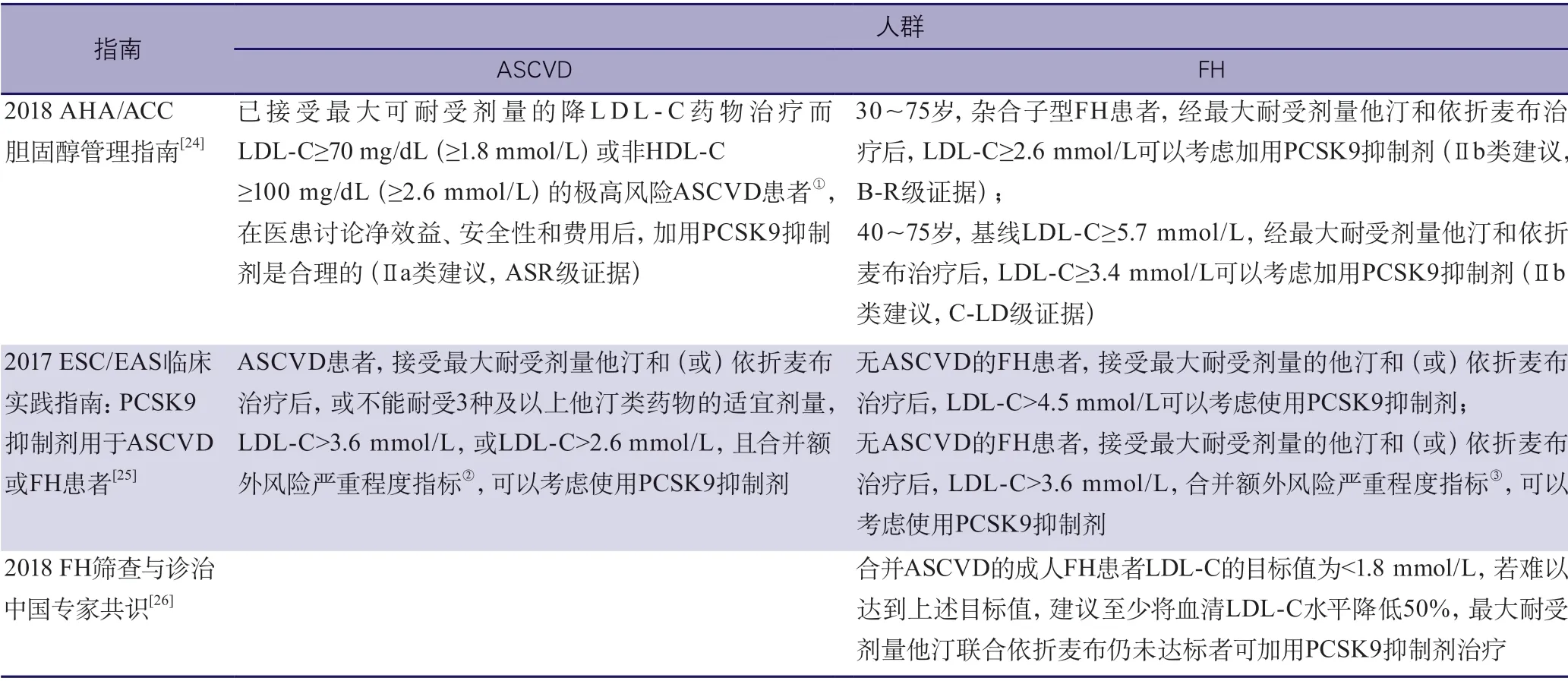
表2 其他指南對PCSK9抑制劑的應用推薦
2 推薦意見
(1)對于非心源性缺血性卒中患者,接受最優劑量他汀和(或)依折麥布治療后,但LDL-C水平仍≥1.8 mmol/L,在充分討論凈效益、安全性和費用后,可以聯合PCSK9抑制劑治療(Ⅱa類建議,B級證據)。
(2)對于缺血性卒中合并心肌梗死病史、癥狀性外周動脈疾病、顱內大動脈粥樣硬化性狹窄(狹窄率70%~99%)或合并多個危險因素*的患者,考慮需要長期嚴格控制LDL-C水平<1.8 mmol/L。對于這部分患者,當接受最優劑量他汀和(或)依折麥布治療后,LDL-C水平仍≥1.8 mmol/L,可積極啟用PCSK9抑制劑(Ⅱb類建議,B級證據)。
*危險因素包括:年齡>65歲、冠狀動脈旁路移植術史或非心肌梗死以外的經皮冠狀動脈介入治療史、糖尿病、高血壓、慢性腎臟病、吸煙、缺血性卒中發生在半年內。
(3)對于缺血性卒中合并FH,尤其是純合子型FH患者,當接受最優劑量他汀和依折麥布治療后,LDL-C水平仍≥1.8 mmol/L,可啟用PCSK9抑制劑(Ⅱb類建議,B級證據)。此外對于缺血性卒中患者,如果發現符合下列任意1項者要進入FH的篩查流程:①早發ASCVD(男性<55歲或女性<65歲);②成人血清LDL-C≥3.8 m mol/L,兒童血清LDL-C≥2.9 mmol/L,且能除外繼發性高脂血癥者;③有皮膚/腱黃素瘤或脂性角膜弓(<45歲);④一級親屬中有上述3種情況。
3 展望
降脂治療對于缺血性卒中的預后管理至關重要,而目前針對這一領域的研究結果依舊是有限的。缺血性卒中病因復雜,血脂在不同卒中亞型的發生發展中所起作用可能存在差別,不同卒中亞型降脂治療后獲益也可能不同。目前尚無大規模干預性研究探討強化降脂對卒中急性期的獲益與風險,而對于降脂目標及長期血脂管理亦無研究證據。此外,目前主要的研究均是針對他汀類降脂藥物,而非他汀類降脂治療藥物或聯合治療在缺血性卒中二級預防中的作用仍存在大量空白。
PCSK9抑制劑作為一種新型降脂藥物,通過降低缺血性卒中患者LDL-C水平從而降低心腦血管事件風險,目前已得到初步驗證,但未來仍需更多高質量研究進一步探索PCSK9抑制劑對缺血性卒中的有效性及安全性。尤其是針對缺血性卒中的病因多樣性及不同的卒中亞型、高危人群等做進一步的探索,例如合并顱內外大動脈狹窄、不穩定動脈粥樣硬化斑塊或動脈到動脈栓塞的患者。在使用時機方面,應全面評估缺血性卒中急性期的有效性及安全性。目前有關中國卒中患者的相關研究較少,終點結局事件主要為復合終點,未以卒中復發、神經功能預后等作為主要終點,未來需獲得更多中國人群數據。PCSK9抑制劑的誕生為臨床醫師與患者提供了新的降脂選擇,希望未來有更多的研究去進一步探索PCSK9抑制劑在缺血性卒中中的應用。
執筆作者:
李子孝,徐安定,劉麗萍,陳康寧
指南討論組專家名單(按姓氏拼音排列):
陳會生 中國人民解放軍北部戰區總醫院
陳康寧 重慶陸軍軍醫大學第一附屬醫院
董 強 復旦大學附屬華山醫院
韓 翔 復旦大學附屬華山醫院
何 俐 四川大學華西醫院
胡 波 華中科技大學同濟醫學院附屬協和醫院
黃立安 暨南大學附屬第一醫院
李子孝 首都醫科大學附屬北京天壇醫院
劉麗萍 首都醫科大學附屬北京天壇醫院
樓 敏 浙江大學醫學院附屬第二醫院
羅本燕 浙江大學醫學院附屬第一醫院
施 炯 首都醫科大學附屬北京天壇醫院
唐北沙 中南大學湘雅醫院
王 檸 福建醫科大學附屬第一醫院
王伊龍 首都醫科大學附屬北京天壇醫院
王擁軍 首都醫科大學附屬北京天壇醫院
徐安定 暨南大學附屬第一醫院
徐 運 南京大學醫學院附屬鼓樓醫院
許予明 鄭州大學第一附屬醫院
楊 弋 吉林大學第一醫院
趙 鋼 空軍軍醫大學西京醫院
趙性泉 首都醫科大學附屬北京天壇醫院
周盛年 山東大學齊魯醫院

