HPLC法測定大鼠血漿華法林及紅參對華法林抗凝作用的影響
張 瑜1 鄭 宓1 張 寬1 陳 明1 鄢 琳1 葉 華1 李 雪 賴文婷
1.福建中醫藥大學附屬第二人民醫院藥學部,福建 福州 350003;2.福建中醫藥大學藥學院,福建 福州 350001
華法林(warfarin)是口服香豆素類抗凝藥,廣泛應用于機械瓣膜置換術、血栓栓塞性疾病、心房顫動[1]。但華法林在臨床使用過程中存在治療窗窄及藥物相互作用復雜的問題,使其臨床療效和不良反應個體差異大,劑量難以掌握,一定程度上限制了其臨床應用。目前,國內的現狀為阿司匹林應用較普及,而華法林的應用率較低,僅為2.5%~3%[2]。據報道[3],約40%的心血管疾病和腦卒中患者均合并使用中藥。由于中藥通常含有多種藥理活性成分,與成分單一的西藥相比,中藥與華法林產生藥物相互作用的可能性更高。近年來,中藥對華法林抗凝作用的影響也越來越受到臨床的重視。其中人參、西洋參與華法林的相互作用的研究較多[4]。紅參是人參的栽培品經蒸制后的干燥根和根莖。但國內外文獻均未見紅參與華法林相互作用實驗研究的相關報道。筆者旨在通過建立高效液相色譜法(High Performance Liquid Chromatography,HPLC)測定大鼠血漿華法林的血藥濃度并初步探討紅參與華法林是否存在藥物相互作用,為臨床合理用藥提供參考依據。
1 儀器與材料
1.1 儀器 高效液相色譜儀(賽默飛世爾科技(中國)有限公司);PDA-100 Photodiode Array;AcclaimTM120 C18(250×4.6 mm,5 μm)色譜柱;XY系列精密電子天平(常州市幸運電子設備有限公司);HC-2062高速離心機(安徽中科中佳科學儀器有限公司);CS-2000i全自動凝血分析儀 (希森美康醫用電子(上海)有限公司)。
1.2 藥品與試劑 紅參配方顆粒(批號:17003221,北京康仁藥業有限公司);華法林鈉片(規格:3 mg/片;批號:1680414;Orion Corporation Orion Pharma);華法林鈉標準品(批號:113062,LGC Labor GmbH.Bgm-Germany);乙腈 HPLC級別 (批號:20170314,國藥集團化學試劑有限公司);甲醇 HPLC級別(批號:021150601,上海星可高純溶劑有限公司);冰乙酸(批號:K1315019,Aladdin Industrial);肝素鈉注射液(批號:151712098A,常州千紅生化制藥股份有限公司);3.2%枸櫞酸鈉抗凝劑(批號:0328A18,上海銘博生物科技有限公司);全自動血液凝固分析裝置清洗液[批號:A7118,希森美康醫用電子(上海)有限公司];凝血酶試劑[批號:562801,希森美康醫用電子(上海)有限公司];凝血質控血漿水平(批號:548029A,Dade Ci-Trol);水為自制純化水。
1.3 實驗動物 實驗動物SD大鼠,雄性,體重(250±20)g(福建省福建醫科大學動物實驗中心提供,SPF級,許可證:SCXK(閩)2012-0001)。
2 方法
2.1 溶液的配制
2.1.1 華法林標準液 精密稱取華法林鈉標準品10.07 mg置于10 mL容量瓶內,加入甲醇超聲溶解后定容,即得1.007 mg/mL的華法林貯備液。精密吸取華法林貯備液1 mL置于100 mL容量瓶內,加甲醇定容,即得10.07 μg/mL的華法林標準溶液。均置于2~8 ℃冰箱中保存待用。
2.1.2 華法林溶液配制 華法林鈉3片(3 mg/片)置于研缽研磨成細粉,溶于300 mL水超聲溶解時即得濃度為0.030 mg/mL的華法林溶液。
2.1.3 紅參水溶液配制 稱取紅參顆粒5.4 g,加純化水300 mL,超聲溶解,配制成0.018 g/mL紅參水溶液(1 g紅參顆粒相當于5 g紅參飲片)。
2.2 動物實驗
2.2.1 動物分組及給藥方法 雄性SD大鼠35只,體重(220±20)g,適應性喂養3 d,隨機分為五組,每組7只大鼠,分別為:A組(空白組)、B組(紅參組)、C組(華法林組)、D組(紅參同服組)、E組(紅參預服組)。其中A組灌胃蒸餾水;B組灌胃紅參顆粒水溶液(0.18 g/kg);C組灌胃華法林溶液(0.3 mg/kg);D組先給予華法林溶液灌胃(0.3 mg/kg),給藥1 h后,再灌胃紅參顆粒水溶液(0.18 g/kg);E組先預服紅參7 d,后華法林和紅參給藥方法同D組。上述5組大鼠藥物連續灌胃給藥14 d。
2.2.2 血漿樣品的采集與處理 測定凝血酶原時間(Plasma prothrombin time,PT)血漿樣本:A組、B組、C組、D組和E組5組大鼠分別于華法林灌胃前(D0)和給藥后的D1、D4 、D7、D10、D14 采血點,經大鼠眼眶采血0.9 mL置于含有3.2%枸櫞酸鈉抗凝劑0.1 mL的抗凝管中,血液與抗凝劑的比例為9∶1(V∶V),充分混勻,立即離心力1500 g,離心15 min,分離血漿,室溫保存,24 h內待測。每次采血時間均為華法林給藥后3 h。
測定華法林血藥濃度血漿樣本:C、D、E組大鼠于華法林灌胃給藥后的D1、D4 、D7、D10、D14采血點,經大鼠眼眶采血1mL置于肝素鈉化EP管中,充分混勻,立即離心力1500 g,離心15 min,分離血漿,保存待測。每次采血時間均為華法林給藥后3 h。
2.3 指標測定
2.3.1 凝血酶原時間(PT)及國際標準化比值(INR)的測定 將經3.2%枸櫞酸鈉抗凝的血漿適量放入測試通道,采用凝血酶原時間測定試劑,通過全自動血凝分析儀自動檢測血漿標本PT及INR值,并記錄實驗結果。
2.3.2 華法林血藥濃度的測定 精密吸取肝素抗凝的血漿100 μL,加入乙腈300 μL,渦旋1 min,10000 rpm/min離心15 min,取上清液,進樣20 μL。記錄色譜圖,以外標法進行峰面積定量。
2.4 色譜條件的建立 色譜柱:AcclaimTM120C18(250 mm×4.6 mm,5 μm);柱溫:25℃;流動相:乙腈-乙酸水(1%)(70∶30)等度洗脫;流速:1 mL/min;檢測波長:308 nm;進樣量:20 μL。結果如圖1所示。
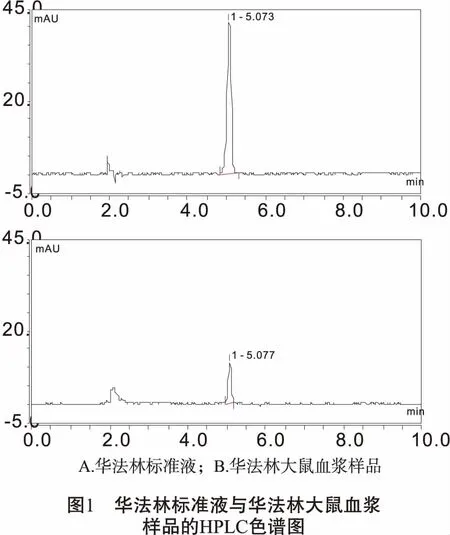
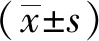
3 結果
3.1 HPLC方法的專屬性 取空白大鼠血漿180 μL,加入100.7 μg/mL華法林標準液20 μL配成的含華法林10.07 μg/mL血漿樣品200 μL作為陽性對照血漿。分別取空白大鼠血漿、陽性對照血漿、華法林大鼠血漿、紅參大鼠血漿、華法林+紅參大鼠血漿各100 μL,按2.3.2項下的預處理進行操作,得色譜圖(如圖2所示)。紅參與血漿內源性成分對華法林出峰無干擾,且華法林峰形良好。
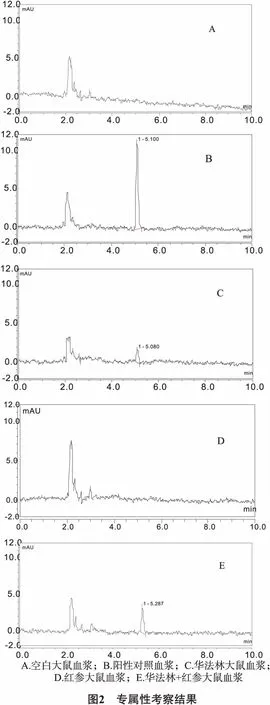
3.2 標準曲線的制備 取空白大鼠血漿5份,配制成200 μL華法林終濃度為50.35 μg/mL、10.07 μg/mL、7.552 μg/mL、5.035 μg/mL、2.518 μg/mL、1.007 μg/mL的標準血漿樣品,按2.3.2項下的預處理進行操作,每種濃度平行操作5次,記錄色譜圖華法林峰面積。以華法林色譜峰的峰面積均值為縱坐標y,標準血漿樣品的濃度為橫坐標x,進行線性回歸,繪制標準曲線。如圖3所示,得到回歸直線方程為y=0.1056x+0.0254,相關系數R=0.9996。結果說明:華法林血漿濃度在1.007~50.35 μg/mL范圍內與峰面積呈良好的線性關系。
3.3 最低檢測限 配制華法林終濃度為0.1007 μg/mL、0.504 μg/mL、1.007 μg/mL的血漿,按2.3.2項下的預處理進行操作,取上清,進樣20 μL。以信噪比為3確定出華法林的最低檢出濃度為0.504 μg/mL。
3.4 精密度和準確度考察 配制華法林終濃度為2.518 μg/mL、10.07 μg/mL、50.35 μg/mL的低、中、高濃度的血漿樣品分別于同1d內分5次以及連續5 d,每日1次,按2.3.2項下的預處理操作后,進樣20 μL,記錄色譜峰面積,計算日內精密度、日間精密度以及提取回收率、方法回收率,結果見表1、2。由表1可得該方法測得的血漿中華法林日內和日間精密度的RSD均小于10%,表明該法對含量的重現性和重復性均良好。從表2中得到低、中、高3種濃度的華法林血漿樣品提取回收率均值為91.75%、95.29%、85.17%,方法回收率均值分別為97.44%、109.3%、99.77%。參照生物樣品分析時的回收率一般要求在85%~115%(樣品藥濃度≥ 200 μg/L),RSD小于10%的標準,本實驗符合生物樣品加樣回收率的要求。
3.5 穩定性考察 配制成終濃度為低(2.518 μg/mL)、中(10.07 μg/mL)、高(50.35 μg/mL)3種華法林血漿樣品,每種濃度平行配制5份。在室溫下放置24 h、24 h反復凍融3次后、冷凍(-20℃)半個月,按2.3.2項下的預處理操作后,進樣20 μL,記錄色譜,結果見表3。從表3可看出,華法林血漿在未經預處理的狀態下,室溫24 h、24 h反復凍融3次以及冷凍(-20℃)半月后的RSD均在10%以內,可見華法林血漿樣品的室溫穩定性、凍融穩定性、長期穩定性的測定結果變化均在允許范圍內,保證了樣品測定結果的可靠性。
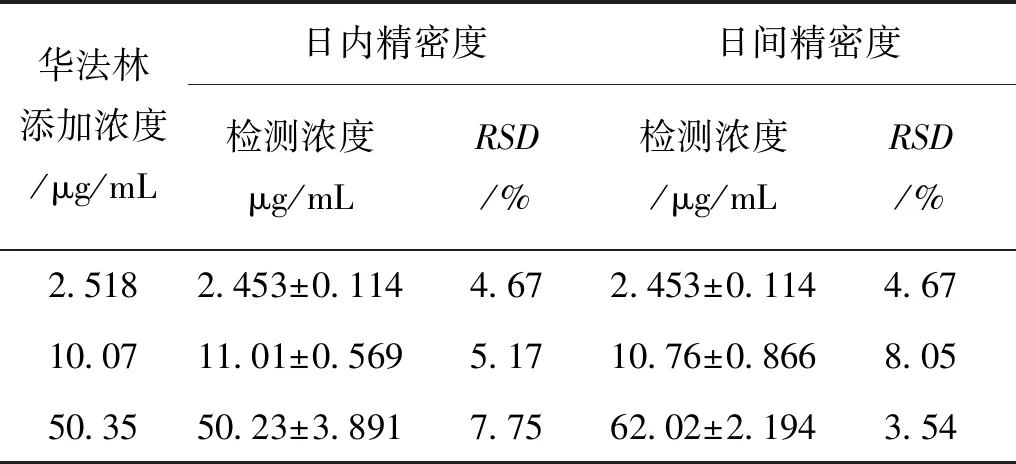
表1 華法林血漿濃度的精密度實驗
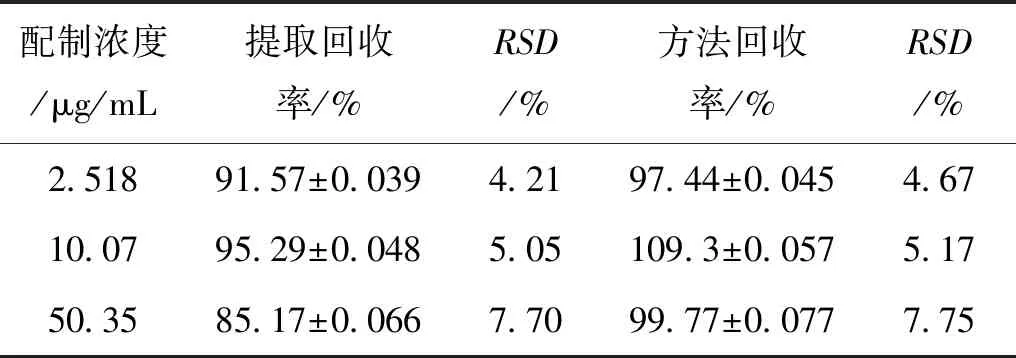
表2 低、中、高濃度華法林血漿的回收率 (n=5)

表3 低、中、高濃度華法林血漿的穩定性
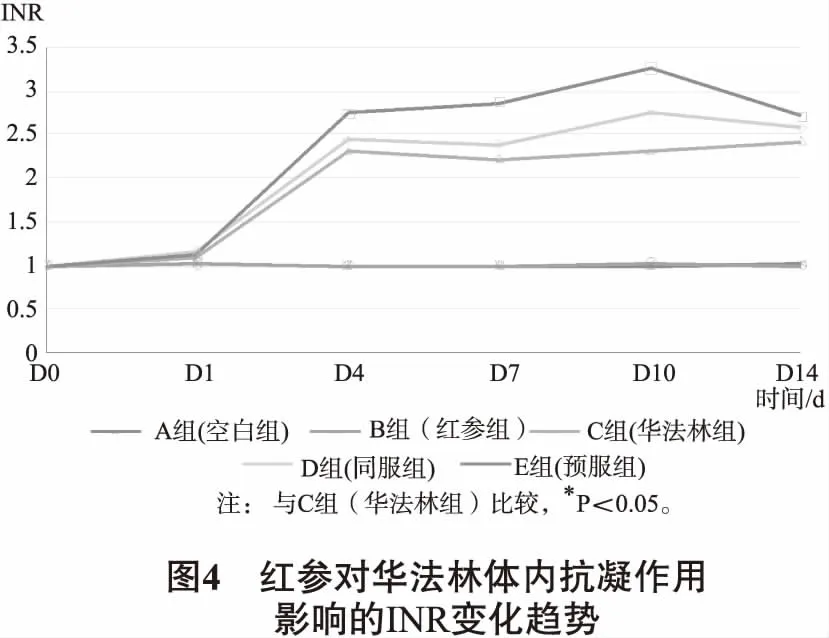
3.6 紅參對大鼠體內華法林抗凝作用的影響 運用全自動凝血分析儀分別測定A、B、C、D、E組大鼠在不同時間點的PT值變化,并根據PT值計算INR結果(見表4和圖4)。從表4可以看出,與A組相比,B組對PT沒有影響。與C組比較,D組和E組PT值均有不同程度的延長,其中E組在D7和D10時PT值延長具有顯著性差異。同樣,在INR的變化上,與C組比較,E組在D7和D10呈明顯的增高趨勢,差異具有統計學意義(P<0.05)。但C、D、E組在D14時,PT和INR未呈現明顯的差別。
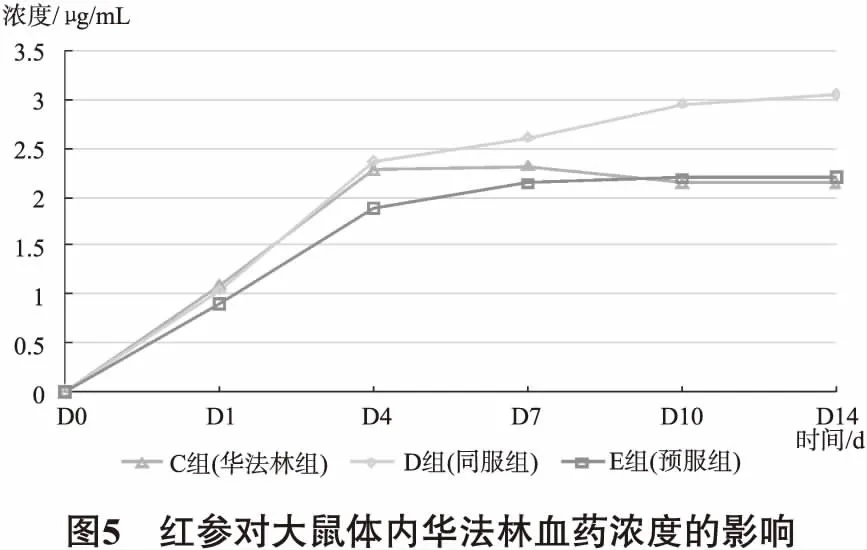
3.7 紅參對大鼠體內華法林血藥濃度的影響 紅參對華法林多次給藥大鼠穩態血藥濃度的影響。從圖5可以看出,在給藥后,E組華法林的血藥濃度較C組的差異均無統計學意義(P>0.05)。D組華法林的血藥濃度較C組有升高的趨勢,但亦未達到具有統計學意義的差異(P>0.05)。
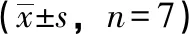
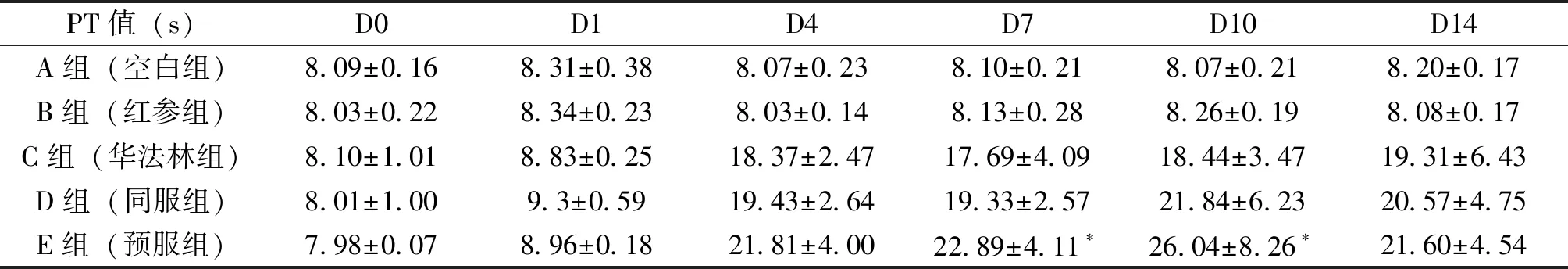
PT值(s)D0D1D4D7D10D14A組(空白組)8.09±0.168.31±0.388.07±0.238.10±0.218.07±0.218.20±0.17B組(紅參組)8.03±0.228.34±0.238.03±0.148.13±0.288.26±0.198.08±0.17C組(華法林組)8.10±1.018.83±0.2518.37±2.4717.69±4.0918.44±3.4719.31±6.43D組(同服組)8.01±1.009.3±0.5919.43±2.6419.33±2.5721.84±6.2320.57±4.75E組(預服組)7.98±0.078.96±0.1821.81±4.0022.89±4.11?26.04±8.26?21.60±4.54
注:與C組(華法林組)比較,*P<0.05。
4 討論
筆者首探討并建立了在聯用紅參和華法林的大鼠血漿中測定華法林含量的HPLC法,該法操作簡單,專屬性、精密度、重現性和重復性、回收率、穩定性均達到標準,可作為紅參與華法林藥物相互作用的研究中測定華法林血藥濃度的可靠方法。
從紅參對華法林藥效學影響結果看出:紅參單藥對PT值無明顯影響,表明紅參單藥對凝血無明顯影響。與華法林組比較,預服組大鼠PT和INR值在給藥的第7天和第10天顯著延長,而同服組PT和INR也有延長的趨勢,但未具有統計學差異。實驗第14天時,紅參同服組和紅參預服組與華法林組PT、INR值未再顯示明顯的差別。驗結果提示紅參與華法林聯合用藥后可產生藥效學的協同作用,增強華法林的抗凝作用。本研究結果與既往人參和西洋參抑制華法林的抗凝作用的結果不同[5-6],可能是由于紅參經過炮制加工后,其所含有效成分與人參或西洋參不同有關。
從血藥濃度結果看,紅參同服組和預服組華法林血藥濃度有升高的趨勢但未達到統計學差異。而其PT和INR值卻有顯著性差異。華法林為S型和R型兩種光學異構體組成的消旋體混合物[7]。S-華法林主要經CYP2C9代謝,R-華法林主要經CYP1A2和CYP3A4代謝,且S-華法林的藥理作用約為R-華法林作用的3-5倍。由于本研究未對華法林對映異構體濃度進行檢測,結合實驗結果初步推測,紅參可能對S-華法林的影響強于R-華法林,導致雖然華法林總體濃度變化不明顯,但仍然可以引起藥效學有意義的改變。
筆者觀察了紅參對華法林穩態血藥濃度及抗凝作用的影響,提示紅參可能增強華法林的抗凝作用。在臨床實踐中,應提醒臨床對于正在服用紅參的患者,在初始處方華法林時應注意劑量調整,適當減少華法林的劑量,并在用藥的前2周加強監測INR,以減少紅參與華法林兩藥聯合應用可能導致的出血風險。由于筆者未對華法林對映異構體濃度進行檢測,紅參是否是通過影響CYP2C9的活性而影響S-華法林濃度進而增強華法林抗凝作用值得進一步的探索。在今后的研究中,將可進一步觀察紅參對S-華法林血藥濃度以及對肝藥酶CYP2C9的影響,探討紅參與華法林相互作用的機制。

