Br?nsted-Lewis酸性離子液體催化合成乙酸正丁酯
武宇,王亞婷,高鵬翔,劉冉,趙地順,任培兵,張栓力,扈士海
(1.河北科技大學 化學與制藥工程學院,河北 石家莊 050018;2.石家莊焦化集團有限責任公司,河北 石家莊 050031;3.石家莊新宇三陽實業有限公司,河北 石家莊 051430)
乙酸正丁酯是重要的精細化工產品,被廣泛應用于涂料、醫藥、分析化學等領域[1-2]。制備乙酸正丁酯的傳統催化劑是濃硫酸[3],但濃硫酸存在著腐蝕設備、副反應多、污染環境等問題,開發綠色高效的催化劑倍受關注。
離子液體優良的性能[4-8],在催化反應中得到了廣泛的研究。酸性離子液體根據酸堿理論[9],可分為Br?nsted酸性離子液體[10-13]和Lewis酸性離子液體[14-15]。Br?nsted-Lewis酸性離子液體作為兼具雙重酸性,在脫硫[16]、烷基化[17]、酯交換[18]和酯化等反應[19]中更具有催化優勢。本文制備了4種Br?nsted-Lewis酸性離子液體,通過催化合成乙酸正丁酯,考察了離子液體的催化性能。
1 實驗部分
1.1 試劑與儀器
三乙胺、1,3-丙烷磺酸內酯、乙酸、正丁醇、環己烷、ZnCl2、FeCl3·6H2O、AlCl3·6H2O、CuCl2·2H2O均為分析純。
FTS-135型傅里葉變換紅外光譜儀;Bruker Avance 500MHz型核磁共振儀;DF-101S型集熱式恒溫加熱磁力攪拌器;RE-200B型旋轉蒸發器;GC-7900氣相色譜儀。
1.2 Br?nsted-Lewis酸性離子液體的制備
稱取0.2 mol三乙胺和0.2 mol 1,3-丙烷磺酸內酯置于盛有100 mL丙酮溶液的250 mL三口燒瓶中,反應溫度45 ℃,攪拌反應8 h。反應結束后減壓抽濾,乙酸乙酯洗滌濾餅3次,除去未反應的反應物。真空干燥,得到白色固體中間體(Ⅰ)。在250 mL 三口燒瓶中加入25 mL去離子水,并加入0.02 mol中間體(Ⅰ)攪拌溶解,待中間體全部溶解后滴加0.02 mol濃鹽酸,反應溫度70 ℃,攪拌反應4 h。反應結束后,旋蒸除去反應體系中的水,用乙酸乙酯洗滌產物3次,除去溶劑得淡黃色粘稠狀液體[HO3SC3-NEt3]Cl離子液體(Ⅱ)。最后在[HO3SC3NEt3]Cl離子液體(Ⅱ)中加入0.02 mol的金屬氯化物XCln(ZnCl2、FeCl3、AlCl3、CuCl2),反應溫度70 ℃攪拌反應,待金屬氯化物全部溶解,冷卻干燥,即得Br?nsted-Lewis酸性離子液體(Ⅲ)[HO3SC3-NEt3]FeCl4、[HO3SC3-NEt3]ZnCl3、[HO3SC3-NEt3]CuCl3、[HO3SC3-NEt3]AlCl4。合成路線見下式:
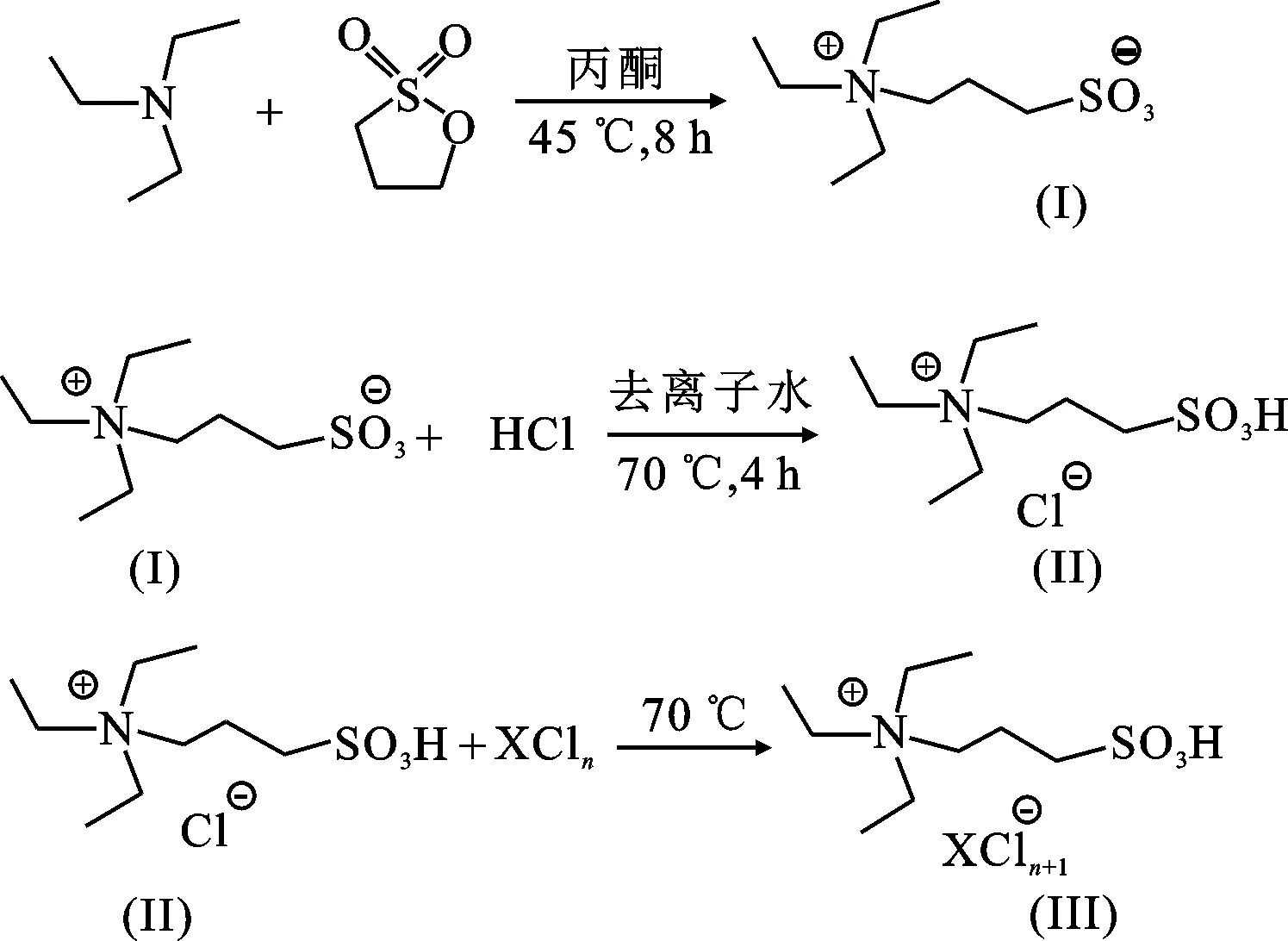
1.3 乙酸正丁酯的制備
在裝有分水器、溫度計、蛇形冷凝管的磁力攪拌三口燒瓶中加入37.06 g(0.5 mol)正丁醇、36.03 g(0.6 mol)乙酸、1.85 g離子液體和7.41 g環己烷,在分水器中加入環己烷至回流口處。反應溫度為95 ℃,反應時間為4 h,待反應結束后,靜置冷卻至室溫。反應體系分層,上層為酯層,下層為離子液體,減壓蒸餾回收離子液體以重復使用。
采用氣相色譜測定乙酸正丁酯收率,色譜柱HT-FFAP,30 m×0.32 mm×0.5 μm毛細管柱;進樣口溫度80 ℃;檢測器溫度180 ℃;柱溫條件:50 ℃保持2 min,35 ℃/min升溫至180 ℃;不分流進樣。以內標法定量分析乙酸正丁酯含量,乙醇作為內標物。
2 結果與討論
2.1 FTIR
[HO3SC3NEt3]Cl通過FTIR(KBr涂膜)表征,結果見圖1。
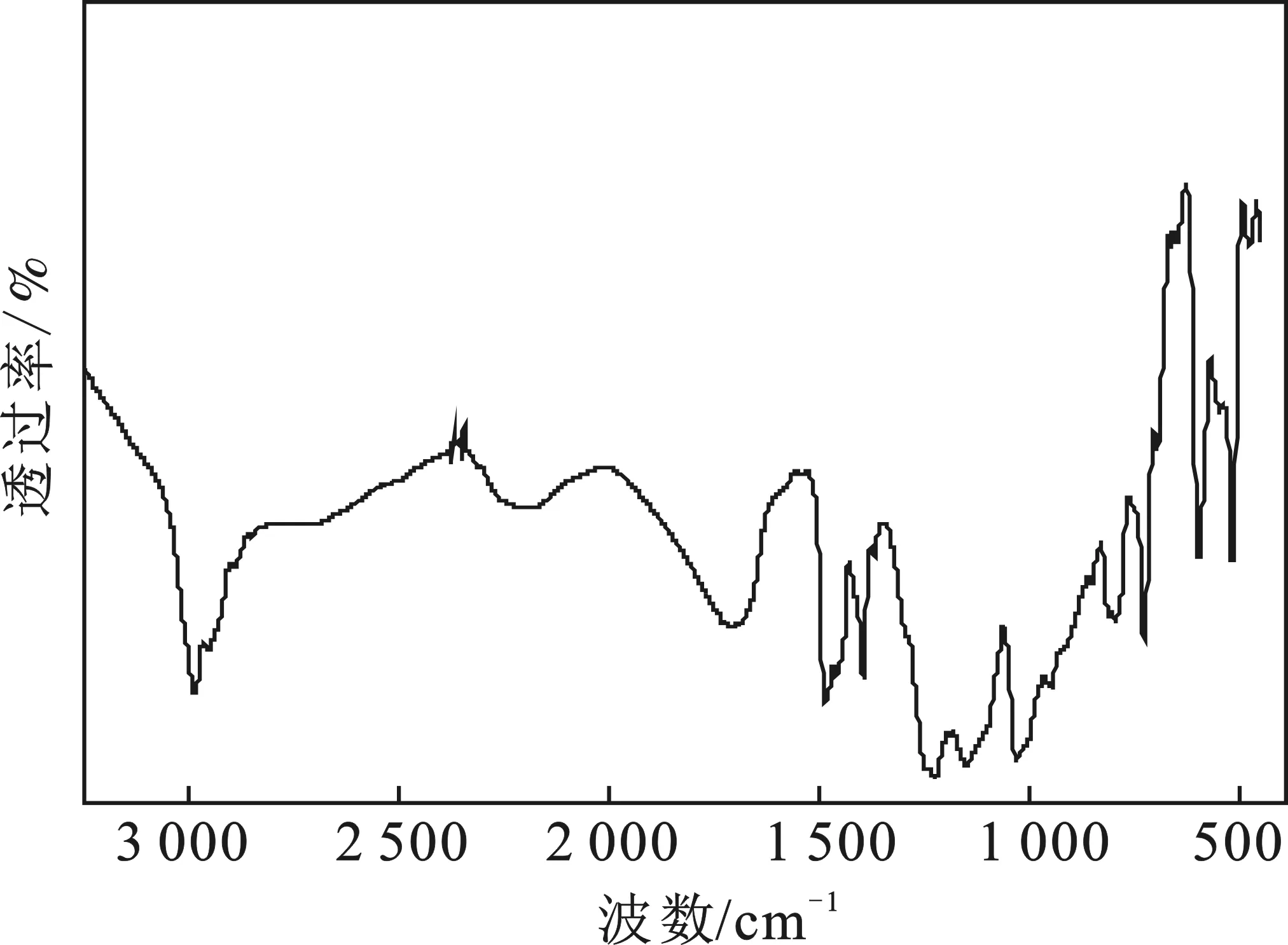
圖1 [HO3SC3NEt3]Cl紅外光譜Fig.1 FTIR spectra of [HO3SC3NEt3]Cl

2.2 1H NMR
以 D2O為溶劑對所合成的[HO3SC3-NEt3]Cl酸性離子液體進行了核磁表征,結果如下:
1H NMR(500 MHz,D2O)δ:3.41~3.24(m,8H),2.98(t,J=7.0 Hz,2 H),2.13(dt,J=14.9,7.1 Hz,2 H),1.28(t,J=7.2 Hz,9 H)。
結果表明,所合成制備的[HO3SC3-NEt3]Cl離子液體,為目標產物。
2.3 Br?nsted-Lewis酸性離子液體的腐蝕性
在酯化反應工業生產中,由于常使用濃硫酸作為催化劑,會造成生產設備的嚴重腐蝕,存在安全隱患,增大了設備費用的投入,不利于工業化生產。離子液體催化酯化性能優異、腐蝕性弱,在催化酯化反應中表現優異。在0.5 mol乙酸,0.6 mol正丁醇,1.85 g催化劑,反應溫度95 ℃,反應時間4 h的條件下,對316 L不銹鋼板(1 cm×1 cm×0.1 cm)腐蝕情況進行試驗研究,結果見表1。
由表1可知,不同金屬的Br?nsted-Lewis酸性離子液體對316 L不銹鋼板的腐蝕性不同,Fe3+、Cu2+的Br?nsted-Lewis酸性離子液體會對316 L不銹鋼板造成比較嚴重的腐蝕,可能是因為Fe3+、Cu2+會造成不銹鋼嚴重的電化學腐蝕,加速了316 L不銹鋼板的腐蝕,Al3+、Zn2+的Br?nsted-Lewis酸性離子液體對316 L不銹鋼的腐蝕較弱,只有濃硫酸腐蝕速率的1/4。對于工業生產而言,可以降低設備費用的投入,降低生產風險。
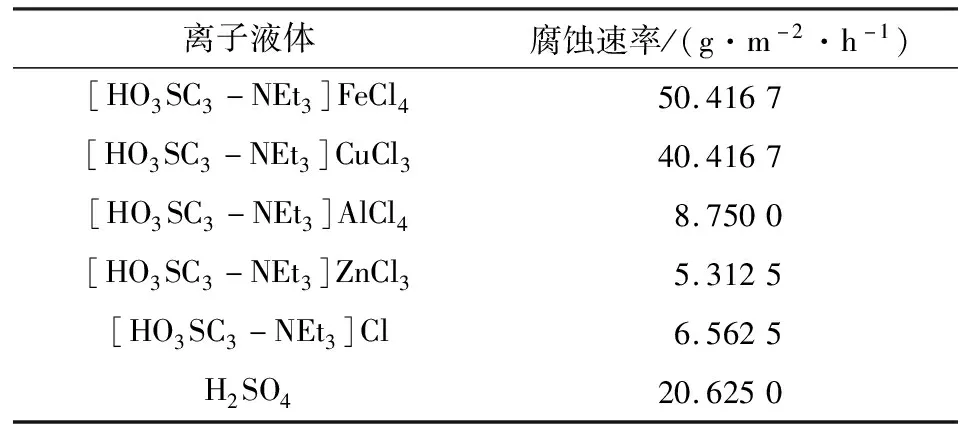
表1 離子液體的腐蝕性Table 1 Corrosion of ILs for austenitic stainless steel 316 L after immersion
2.4 Br?nsted-Lewis酸性離子液體催化合成乙酸正丁酯
2.4.1 Br?nsted-Lewis酸性離子液體催化活性 將所合成的Br?nsted-Lewis酸性離子液體用于催化合成乙酸正丁酯,考察各個離子液體的催化性能,并進行對比。酯化反應條件:醇酸摩爾比為1∶1.2,催化劑用量為5%(以正丁醇計量),反應溫度為95 ℃,反應時間為4 h,環己烷為帶水劑時,酯化結果見表2。

表2 離子液體催化性能Table 2 Catalytic activity of ionic liquids
由表2可知,酯化效果[HO3SC3-NEt3]ZnCl3>[HO3SC3-NEt3]FeCl4>[HO3SC3-NEt3]CuCl3>[HO3SC3-NEt3]AlCl4>[HO3SC3-NEt3]Cl。綜合離子液體腐蝕性實驗結果分析,[HO3SC3-NEt3]ZnCl3作為最優催化劑,表現出了高效的催化性能和較低的腐蝕性,故選用[HO3SC3-NEt3]ZnCl3為催化劑,并進一步優化酯化工藝條件。
2.4.2 酸醇摩爾比對酯化反應的影響 在反應溫度為95 ℃,催化劑為醇質量的5%,環己烷作為帶水劑,反應時間為4 h的條件下,研究不同醇酸摩爾比對酯化反應收率的影響,結果見圖2。
由圖2可知,酯化反應收率隨醇酸摩爾比的增大而增大,當醇酸摩爾比達到1∶1.2時收率達到96.94%,繼續增大醇酸摩爾比收率趨于平緩。可能造成的原因是,酯化反應為可逆反應增加任一反應物可使反應平衡向正方向移動,當醇酸摩爾比達到一定值時,繼續增大醇酸摩爾比只會增加生產成本,對酯化反應收率沒有明顯的提高。
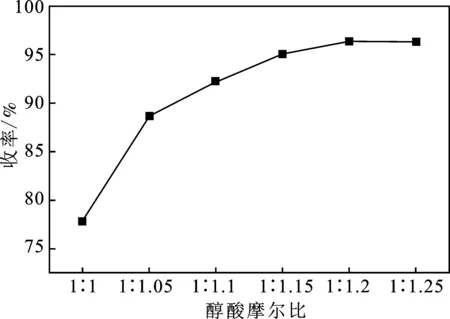
圖2 醇酸摩爾比對酯化反應的影響Fig.2 Effects of molar ratio on yield of esterification
2.4.3 催化劑使用量對酯化反應的影響 在反應溫度為95 ℃,醇酸摩爾比為1∶1.2,環己烷作為帶水劑,反應時間為4 h的條件下,研究離子液體用量對酯化反應收率的影響,結果見圖3。
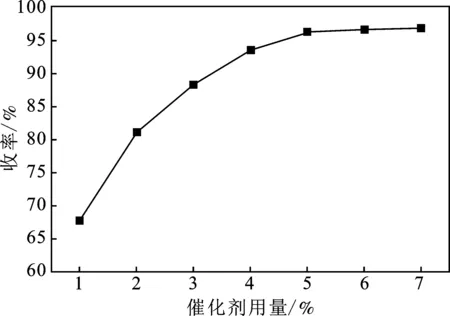
圖3 催化劑使用量對酯化反應的影響Fig.3 Effects of amount of catalyst on yield of esterification
由圖3可知,在其他反應工藝條件不變時,乙酸正丁酯收率隨離子液體用量的增加而增加,可能是由于催化活性中心的增多;當催化劑用量在達到醇質量的5%時,乙酸正丁酯收率達到96.94%,繼續增加催化劑的用量,收率不會有明顯的變化,且會造成催化劑的浪費。
2.4.4 反應溫度對酯化反應的影響 在醇酸摩爾比為1∶1.2,環己烷作為帶水劑,離子液體用量為5%,反應時間為4 h的條件下,研究不同反應溫度對酯化反應的影響,結果見圖4。
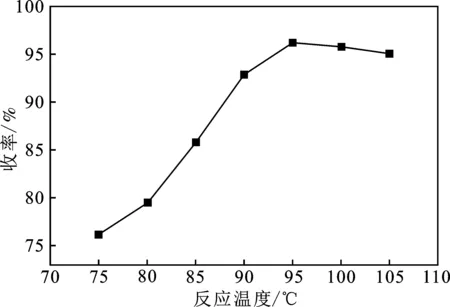
圖4 反應溫度對酯化反應的影響Fig.4 Effects of reaction temperature on yield of esterification
由圖4可知,在其他反應工藝條件不變時,乙酸正丁酯的收率隨著反應溫度的提高呈先增后降的趨勢,當反應溫度為95 ℃時,乙酸正丁酯收率達到96.94%,繼續提高反應溫度,乙酸乙酯的收率小幅度下降。這是因為該反應為放熱反應,過高的反應溫度會抑制反應的進行。
2.4.5 反應時間對酯化反應的影響 在反應溫度為95 ℃,醇酸摩爾比為1∶1.2,離子液體用量5%,環己烷用量20%的條件下,研究不同反應時間對酯化反應的影響,結果見圖5。
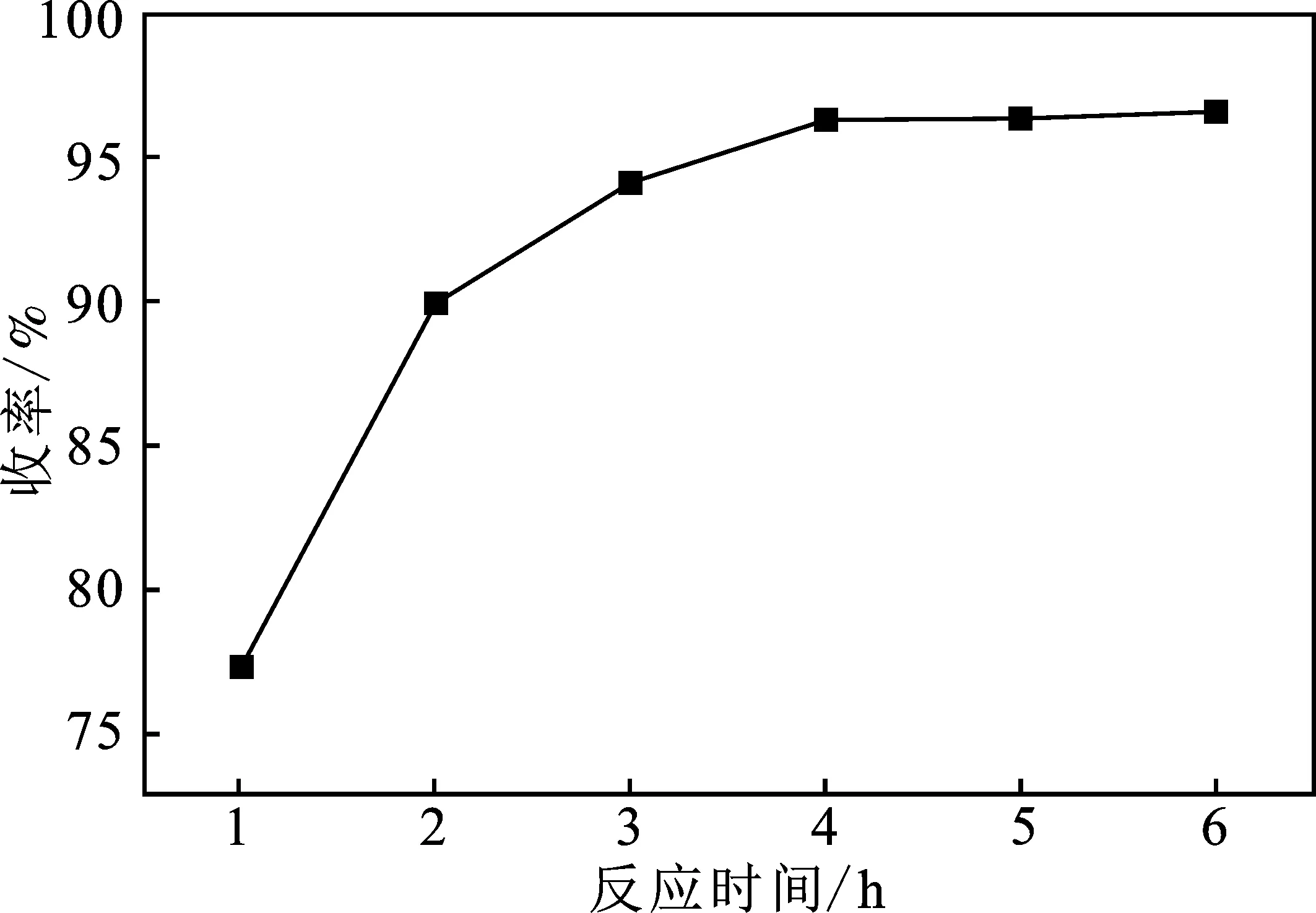
圖5 反應時間對酯化反應的影響Fig.5 Effects of reaction temperature on yield of esterification
由圖5可知,隨著反應時間的延長,乙酸正丁酯的收率呈增長趨勢,反應時間4 h時,酯化反應的收率達到96.94%,4 h后體系將近處于平衡狀態,繼續延長反應時間只會增加操作成本。
2.5 離子液體重復使用性能
離子液體除了有良好的催化性能之外,還應有優良的可重復使用性。在醇酸比為1∶1.2,催化劑用量為醇質量的5%,反應溫度為95 ℃,反應時間為4 h條件下,進行6次重復實驗,考察其可重復使用性,結果見圖6。
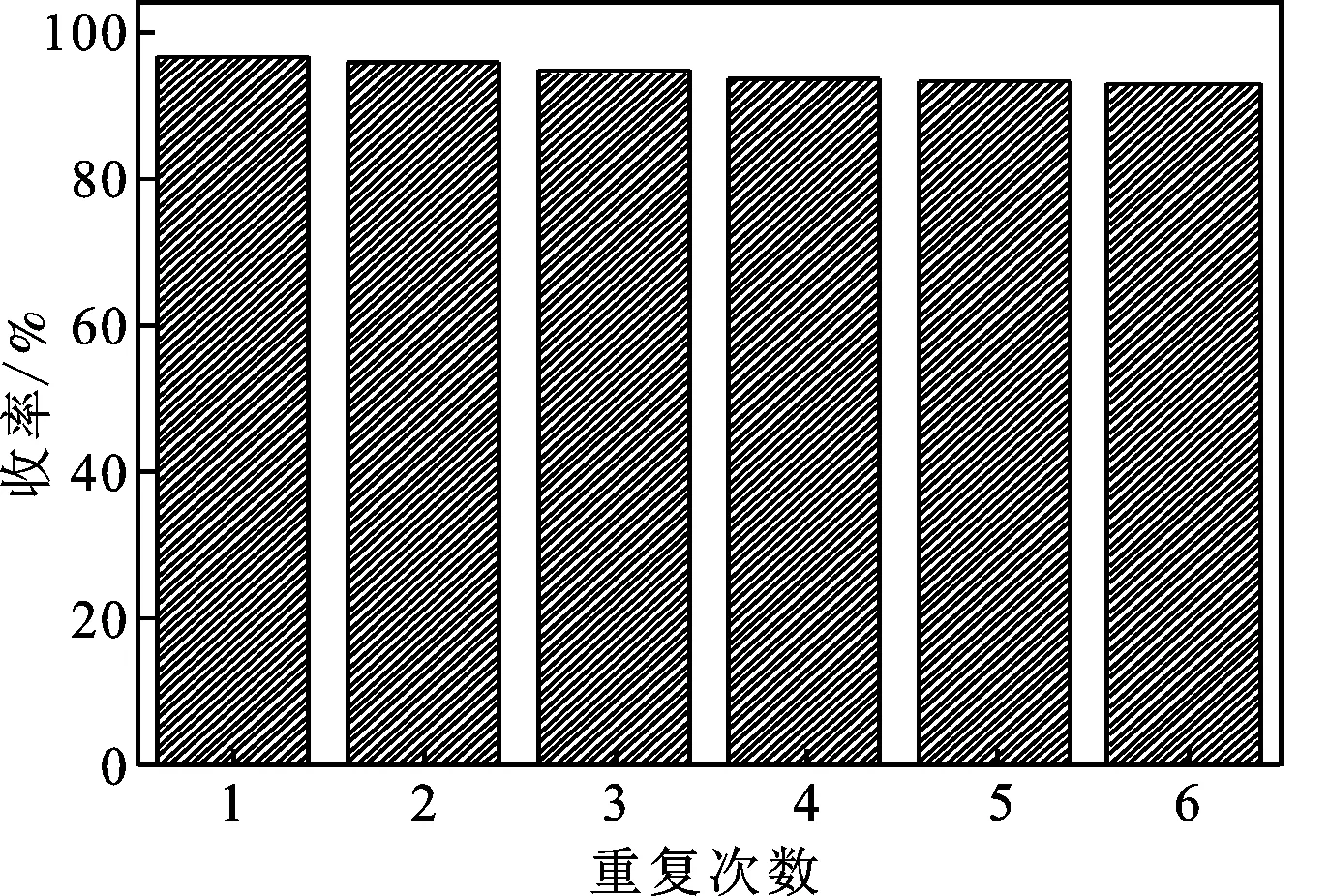
圖6 離子液體重復使用性能Fig.6 Recycling ability tests of ionic liquid
由圖6可知,離子液體可重復使用6次以上,其催化性能依然良好。離子液體催化性能略有下降,可能的原因是在重復使用過程中由于其溶于水而造成的質量損失,也可能是多次在較高溫度下反應使得部分催化劑活性降低,從而影響酯化反應收率。
3 結論
制備了4種Br?nsted-Lewis酸性離子液體,其中[HO3SC3-NEt3]ZnCl3在催化乙酸正丁酯反應中催化性能優異,腐蝕性低,易于產品分離,重復使用性能良好。相較于[HO3SC3-NEt3]Cl離子液體具有更高的催化活性,說明[HO3SC3-NEt3]ZnCl3的Br?nsted和Lewis雙酸位在催化合成乙酸正丁酯中起到了協同催化作用,提高了催化劑的催化活性。為酯化反應提供一種綠色高效的催化劑。

