體外沖擊波聯合高壓氧治療骨不連的隨機對照研究
趙子星,李宏宇△,尹東,梁斌,呂亞南,盤曉榮,黃青,黃思城,韋明照,王宏潤
骨不連是骨折術后常見并發癥,發生率約為1.9%~20%[1-2]。目前骨不連治療主要以手術為主,但有手術創傷大、并發癥嚴重,費用高等缺點。因此越來越多非手術方法被應用于臨床。體外沖擊波療法(ESWT)自20世紀90年代起就被成功地應用于骨科疾病。大量研究表明,ESWT治療骨不連安全、有效,但治療后容易發生局部皮膚水腫、瘀血。高壓氧治療能夠提高組織內氧分壓,促進軟組織修復。另有研究顯示,高壓氧治療還能促進骨折愈合[3]。筆者前期動物實驗證實,高壓氧對ESWT治療兔橈骨骨不連具有協同作用[4]。目前,有關ESWT聯合高壓氧治療骨不連的臨床隨機對照研究少見。本研究旨在探討ESWT聯合高壓氧治療四肢長骨骨不連的臨床療效,以期為臨床治療骨不連提供參考。
1 對象與方法
1.1研究對象 選取2017年1月—2018年4月在我院就診并符合入組標準的骨不連患者60例為研究對象。骨不連診斷標準:骨折9個月仍未愈合,并且已連續3個月沒有任何愈合跡象。按治療方法的不同分為3組。A組20例,予ESWT治療,其中1例失訪,骨折部位:股骨3例,脛骨10例,肱骨2例,橈骨3例,尺骨1例。B組20例,予ESWT聯合高壓氧治療,其中1例失訪,1例因個人原因退出,骨折部位:股骨2例,脛骨8例,肱骨2例,橈骨4例,尺骨2例。C組20例為對照組,予手術治療,骨折部位:股骨3例,脛骨12例,肱骨2例,橈骨2例,尺骨1例。各組患者基線資料比較差異無統計學意義,具有可比性,見表1。納入標準:(1)符合診斷標準的四肢骨折骨不連患者。(2)年齡在22~65周歲。(3)愿意接受ESWT或高壓氧治療,且簽署知情同意書。排除標準:(1)存在多處、多段骨折或病理性骨折者。(2)骨折處存在感染或骨外露者。(3)存在嚴重高血壓、糖尿病、心臟病、心肺肝腎功能異常、凝血功能異常等手術禁忌證。(4)預計依從性差且隨訪不足12個月的患者。(5)孕婦、哺乳期或絕經期婦女。(6)骨密度檢測提示中、重度骨質疏松者(T值低于-2.5)。(7)有酗酒、長期吸煙史。本研究經倫理委員會審批,并符合《赫爾辛基宣言》的道德準則。
1.2治療方法 A組:行ESWT治療。肌內注射杜冷丁后采用體外沖擊波治療儀對骨不連斷端進行治療。股骨和脛骨選3個基準點,肱骨和尺橈骨2個基準點,避開重要血管及神經。每周1次,每次30 min,連續3周。沖擊波參數設置為:股骨和脛骨沖擊量6 000次,焦點能量0.62 mJ/mm2;肱骨沖擊量4 000次,焦點能量0.56 mJ/mm2;尺橈骨和腓骨沖擊量3 000次,焦點能量0.56 mJ/mm2[5]。治療后常規口服非甾體類藥物。B組:行ESWT聯合高壓氧治療。第1次ESWT治療后即采用醫用加壓氧艙行高壓氧治療,每天1次,連續10 d,休息5 d后繼續治療10 d。高壓氧治療壓力為0.15 MPa,吸氧2次,30 min/次,中間間歇10 min吸艙內空氣[6]。治療后常規口服非甾體類藥物。C組:行傳統手術治療,切開復位加強內固定+自體髂骨取骨植骨術,術后于氟比洛芬酯注射液靜脈滴注3 d后改口服非甾體類藥物。
1.3觀察指標 (1)一般情況及并發癥:觀察并記錄所有患者治療及隨訪期間一般情況及并發癥發生情況。(2)治療有效率:所有患者在治療后6、9、12個月常規復查X線檢查,了解骨折愈合情況。如X線見達到骨折的骨性或臨床愈合標準,或者雖未達到上述標準但骨折斷端可見明顯骨痂形成、骨折線模糊,則為有效。反之,骨不連部位無明顯骨痂生長,或無愈合跡象,或骨髓腔封閉,則為無效。(3)堿性磷酸酶(alkaline phosphatase,ALP)及骨密度測定:所有患者在治療前及治療后第1、2、3、4和6周采集外周靜脈血,采用酶速率法(37℃)檢測ALP含量。因C組更換內固定材料而影響骨斷端骨密度測定,故本研究僅測量A、B組骨密度。在治療前和治療后第6、12和24周利用雙能X線骨密度儀測定A、B組骨斷端骨密度。
1.4統計學方法 采用SPSS 19.0軟件行統計學分析。符合正態分布的計量資料以均數±標準差(±s)表示,采用完全隨機或重復測量設計資料的方差分析,組間多重比較采用SNK-q檢驗;計數資料用例(%)表示,組間比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1一般情況及并發癥 所有患者未出現死亡及殘疾,A組1例患者失訪,治療過程中4例出現不同程度疼痛,6例出現局部皮膚腫脹及皮下瘀血。B組1例患者失訪,1例患者因個人原因退出,4例出現輕微疼痛,1例皮膚腫脹及皮下瘀血。2組患者予冰敷、抬高患肢、非甾體類藥物治療后好轉。C組出現傷口疼痛5例,傷口滲液、感染4例,予鎮痛、抗生素、傷口換藥后好轉,1例出現神經性麻痹,口服甲鈷胺片治療,隨訪5個月后完全恢復,并未造成功能障礙。所有患者隨訪12個月,所有均無遠期并發癥出現。
2.2治療有效率 治療6、9和12個月后,B組(66.67%,77.78%和77.78%)與C組(65.00%,80.00%和85.00%)治療有效率均優于A組(31.59%,42.11%和52.63%)(P<0.05),B組和C組間有效率差異無統計學意義,見表2。

Tab.1 Comparison of general data between the three groups of patients表1 3組患者一般資料比較
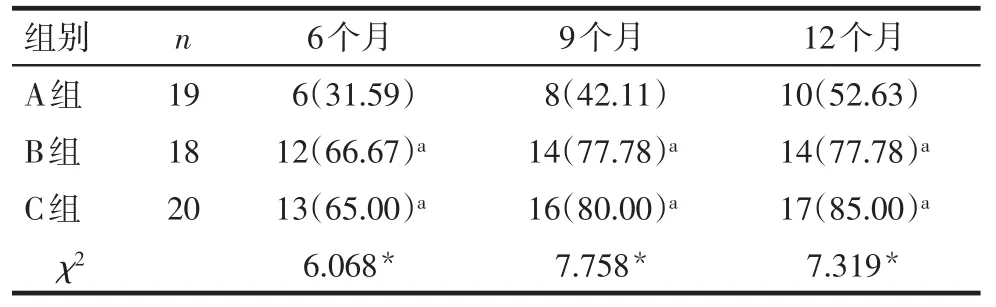
Tab.2 Comparison of the effective rates at different time points between the three groups of patients表2 各組患者在治療后各時間點有效率比較例(%)
2.3ALP含量差異 不同干預方式與時間效應間存在交互作用(P<0.05),組間比較:治療前各組間ALP差異無統計學意義,治療后各時點,B組和C組均較A組升高(P<0.05),但B組和C組間差異無統計學意義;組內各時點比較:各組內治療各時點ALP均較治療前升高,且隨時間延長,整體呈升高趨勢(P<0.05),見表3。
Tab.3 Comparison of the ALP expressions at different time points between the three groups of patients表3 各組患者在治療后各時間點ALP含量比較(U/L,±s)
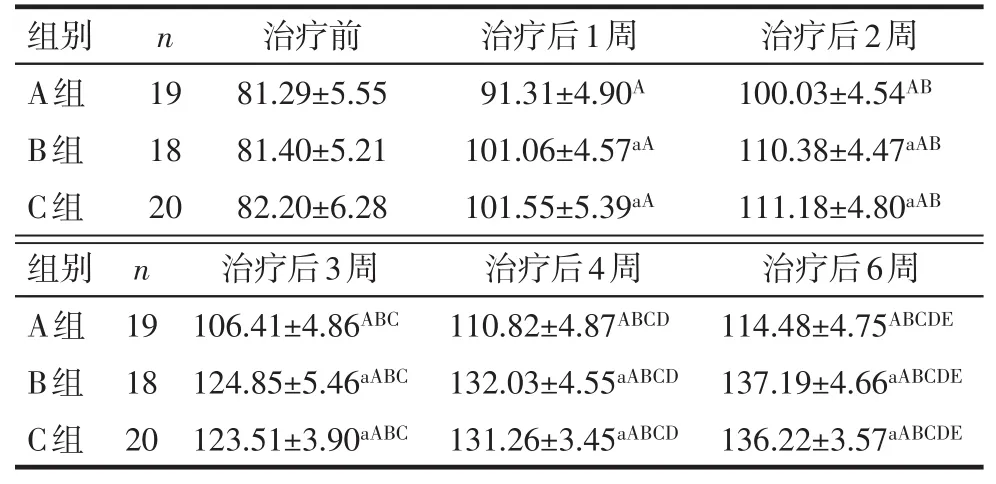
Tab.3 Comparison of the ALP expressions at different time points between the three groups of patients表3 各組患者在治療后各時間點ALP含量比較(U/L,±s)
F組間=5 358.098,F時間=229 066.553,F交互=5 207.182,均P<0.05;a與A組比較,b與B組比較,P<0.05;A~E分別為組內與治療前,治療后1、2、3、4周比較,P<0.05
組別A組B組C組19 18 20 81.29±5.55 81.40±5.21 82.20±6.28 91.31±4.90A 101.06±4.57aA 101.55±5.39aA 100.03±4.54AB 110.38±4.47aAB 111.18±4.80aAB組別A組B組C組n 19 18 20治療后3周106.41±4.86ABC 124.85±5.46aABC 123.51±3.90aABC治療后4周110.82±4.87ABCD 132.03±4.55aABCD 131.26±3.45aABCD治療后6周114.48±4.75ABCDE 137.19±4.66aABCDE 136.22±3.57aABCDE n治療前 治療后1周 治療后2周
2.4A組和B組骨密度變化 不同干預方式與時間效應間存在交互作用(P<0.05),組間比較:治療前2組間骨密度差異無統計學意義,治療后各時點,B組均較A組升高(P<0.05);組內各時點比較:各組內治療各時點骨密度均較治療前升高,且隨時間延長,整體呈升高趨勢(P<0.05),見表4。
Tab.4 Comparison of the bone densities at different time points between three groups of patients表4 A、B2組患者在治療后各時間點骨密度比較(g/cm2,±s)
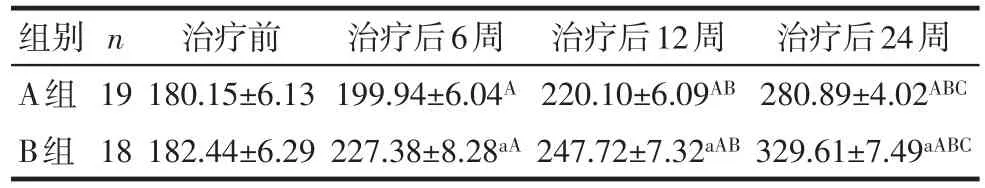
Tab.4 Comparison of the bone densities at different time points between three groups of patients表4 A、B2組患者在治療后各時間點骨密度比較(g/cm2,±s)
F組間=172.423,F時間=14 395.965,F交互=471.058,均P<0.05;a與A組比較,P<0.05;A~C分別為組內與治療前,治療后6、12周比較,P<0.05
組別A組B組n 19 18治療前180.15±6.13 182.44±6.29治療后6周199.94±6.04A 227.38±8.28aA治療后12周220.10±6.09AB 247.72±7.32aAB治療后24周280.89±4.02ABC 329.61±7.49aABC
3 討論
骨不連是骨折術后嚴重并發癥之一,手術仍是治療的主要方法,但常伴隨一些嚴重的并發癥[7],例如深部感染、持續傷口滲液、血腫形成、皮膚感覺喪失、持續疼痛和再次骨不連等,給患者帶來巨大的經濟及心理負擔。骨不連的非手術治療也有很多,但各有其優缺點,且療效不一,但非手術聯合治療骨不連仍是目前臨床研究的主要方向之一。
ESWT可以造成骨折端微骨折,刺激局部細胞因子增殖及骨痂形成,促進骨折愈合[8]。Fan等[9]認為,ESWT可以通過炎細胞刺激成骨細胞增殖,發揮成骨作用。Willems等[10]研究表明,ESWT治療骨不連有效率為50%~90%。本研究結果表明,A組治療方法可以提高血清ALP含量和骨密度,隨訪1年治療有效率達52.63%,但A組治療骨不連效果低于B、C組。骨折愈合是多種細胞因子相互作用的結果[11]。ALP是骨生長過程中持續釋放時間最長的細胞因子,也是反映骨形成和成骨細胞活性的敏感和特異指標。本研究證實,ESWT治療骨不連后ALP含量隨時間的推移而增高。Southwood等[12]在兔股骨缺損實驗中也證實,ALP在骨折愈合過程濃度會升高,而且會因為不同的治療方法和骨折類型而有不同水平升高,但促進ALP含量升高的分子機制還需進一步研究。而造成ESWT治療后骨密度升高的原因,Mackert等[13]認為是骨折斷端吸收沖擊波能量后,造成新鮮的微小粉碎性骨折,促進局部炎性反應,大量成骨細胞、原始成纖維細胞發生聚集和增殖,誘發了骨小梁形成,從而增加了骨密度。同時,ESWT還可以通過改變微循環,增加黏附白細胞并形成自由基,釋放血管內皮生長因子以及P物質等止痛物質,從而達到止痛效果[14]。既往研究報道了ESWT治療后出現皮膚軟組織及神經損傷的病例,本研究也證實ESWT可以造成皮膚局部水腫及淤血,但并無神經損傷病例,說明只要熟悉解剖,準確定位,就能避免類似并發癥發生。
高壓氧能夠改善骨折部位組織氧含量、氧分壓,迅速有效地改善缺氧狀態,改善微循環、組織代謝和供能,從而逆轉受損組織的缺氧、變性,逐漸修復、恢復功能[3]。本研究結果表明,B組治療后可以顯著提高血清ALP含量和骨密度,隨訪1年治療有效率達77.78%,明顯優于A組,但與C組無明顯差異,同時還能降低皮膚并發癥的發生率。最新研究結果證實,ESWT治療骨不連的最佳適應證為肥厚型骨不連且骨折間隙小于5 mm[15]。本研究B組治療骨不連骨折間隙平均為6.38 mm,說明聯合高壓氧治療還能擴大ESWT治療適應證。張玉松等[16]認為,跟骨骨折術后易并發切口感染、皮膚壞死等并發癥,術后采用序貫高壓氧治療可以明顯提高患者切口療效。另有研究認為,造成上述原因可能是高壓氧可刺激局部毛細血管新生及側支循環形成,消除微循環障礙,促使組織間水腫消退,從而減少ESWT或手術造成的皮膚并發癥[17]。近年來研究發現,骨折后骨斷端氧分壓很低,只有當骨髓腔完全重建后氧分壓才恢復正常[18]。Lu等[19]研究顯示,高壓氧對成骨細胞成骨分化具有明顯的促進作用,是高壓氧促進骨愈合的理論基礎,并認為這可能也是高壓氧協同ESWT可提高ALP含量和骨密度的原因。
綜上所述,ESWT聯合高壓氧治療可以顯著增加血清ALP含量和骨密度,減少皮膚并發癥的發生,提高骨不連治療有效率,具有效果顯著、無創、安全、經濟、治療無效時仍可選擇外科手術來彌補等優點,對于老年人、高風險病人及拒絕手術的病人是一個很好的選擇方案。

