某院抗腫瘤類原研與仿制藥品說明書調查分析
秦艷 沈赟 戴佩芳 陳喆 葉巖榮
摘 要 目的:為完善抗腫瘤類仿制藥的說明書與臨床合理用藥提供參考。方法:對14種抗腫瘤類的原研與仿制藥的說明書內容進行對比。結果:部分國產仿制藥相對原研藥缺少警示語,適應證不一致,用法用量描述不詳細,不良反應差異,注意事項不完善,禁忌內容不統一,特殊人群用藥描述不一致,藥物相互作用方面內容不完整以及貯藏條件標注不一致;14份國產仿制藥說明書中,只有1份說明書中有臨床試驗部分;2份注射劑說明書中缺乏靜脈用藥配制指導。結論:部分國產仿制藥說明書有待修訂和提高,相關企業應進一步完善說明書。
關鍵詞 抗腫瘤藥 原研藥 國產仿制藥 說明書
中圖分類號:R951 文獻標志碼:C 文章編號:1006-1533(2019)19-0061-04
Investigation and analysis of instructions of original and generic antitumor drugs in our hospital
QIN Yan*, SHEN Yun, DAI Peifang, CHEN Zhe, YE Yanrong**
(Department of Pharmacy, Zhongshan Hospital, Fudan University, Shanghai 200032, China)
ABSTRACT Objective: To provide reference for the improvement of drug instructions and clinical rational use. Methods: Fourteen kinds of generic and original drug instructions were compared and analyzed. Results: The contents, including warnings, indications, usage and dosage, adverse reactions, attention, taboo, special groups, drug interaction and storage, were different between original and generic drug instructions; among 14 generic drug instructions, only one contained the description of clinical trial, and 3 instructions lacked intravenous infusion preparation. Conclusion: Some of generic drug instructions need to be revised and improved. It is recommend that the manufactures should supplement the drug instructions.
KEy WORDS antitumor drugs; original drugs; generic drugs; instructions
我國惡性腫瘤的發病率逐年上升,腫瘤的治療藥物需深入研究,十二五規劃中提出我國部分仿制藥質量與國際領先水平存在較大差距,國產仿制藥在產品內在質量、說明書等方面與國外原研產品存在區別[1]。藥品說明書是具有法律效力的重要文件[2],為臨床醫護人員和藥師合理使用藥物提供依據,在臨床治療方面起著重要的作用。長期以來同品種、不同廠家藥品說明書的內容存在較大差異,尤其是國產藥品說明書的不良反應項和注意事項等關鍵信息與進口藥品說明書存在較多差異,使得藥品說明書不能有效地提供藥品的使用風險[3]。筆者在此總結我院常用的14種抗腫瘤治療藥物的仿制和原研藥品說明書的差異,為國產抗腫瘤藥品說明書提供合理的修改建議,同時為臨床的醫務工作者合理用藥提供參考。
1 資料與方法
1.1 資料
在我院常用的抗腫瘤治療藥物中,選取同時具備原研藥和仿制藥的14個品種,每種藥品各收集原研藥和仿制藥說明書各一份,對其進行差異性比較。14種抗腫瘤藥物可分為細胞毒類,分子靶向類,激素類和腫瘤輔助治療藥物(表1)。
1.2 方法
依據《化學藥品和生物制品說明書細則》[4](以下簡稱《細則》)和《藥品說明書和標簽管理規定》[5]結合相關文獻資料,對涉及用藥安全的相關信息項:警示語、用法用量、適應證、不良反應、注意事項、禁忌、兒童用藥、老年患者用藥、孕婦及哺乳期婦女、藥物相互作用及貯藏作為比對項目;進行說明書中藥品安全性信息比較。
2 結果
2.1 原研藥和國產仿制藥說明書項目對比結果
通過對14個抗腫瘤類藥品的原研和仿制藥品說明書進行對比,發現部分仿制藥說明書相對原研藥缺少警示語(占樣本總數的50.0%),適應證不一致(占14.2%),用法用量描述不詳細(占21.4%),不良反應差異(占21.4%),注意事項不完善(占28.5%),禁忌內容不統一(占21.4%),特殊人群用藥描述不一致(占7.1%),藥物相互作用方面內容不完整(占28.5%)以及貯藏條件標注不一致(占35.7%),并將存在問題的藥物總結如表2所示。此外發現部分國產仿制藥說明書中存在不止一個問題,共計8份藥品說明書中有2種或2種以上問題同時存在,占57.1%。
2.2 部分注射劑類抗腫瘤藥物缺少配制指導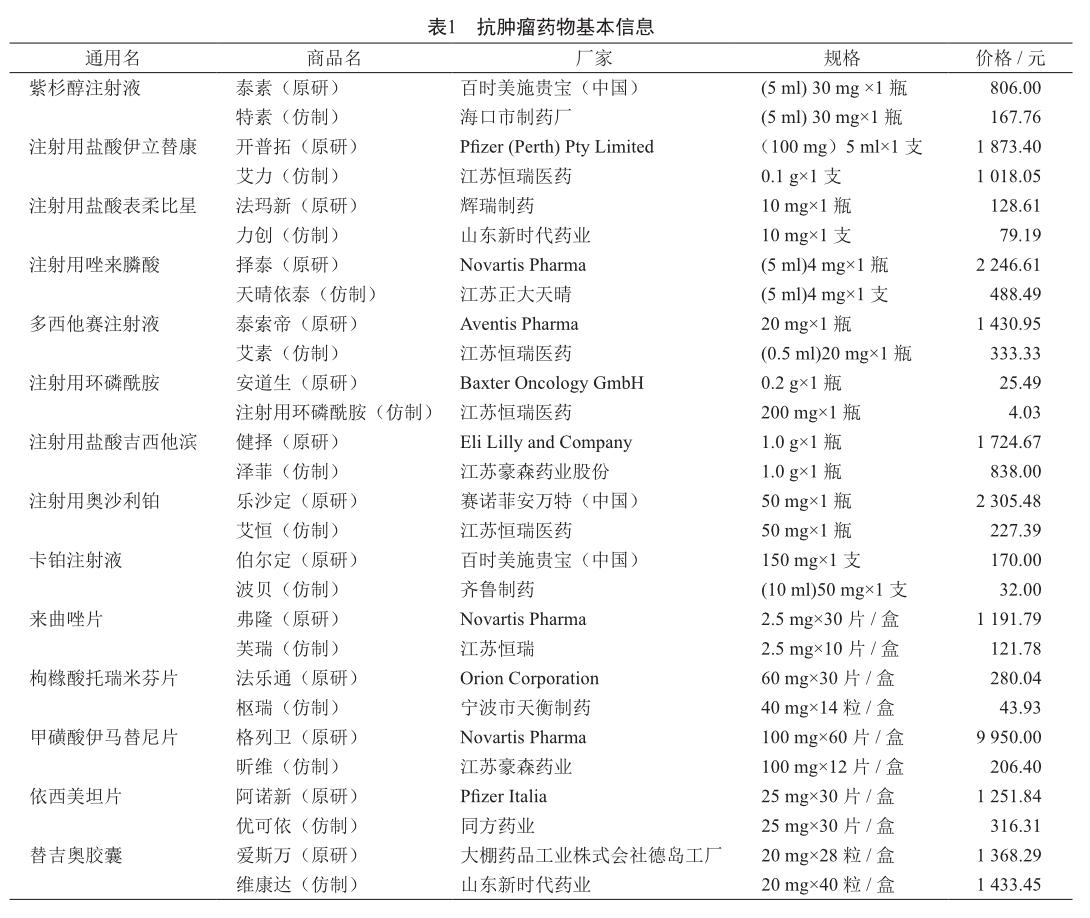
14種抗腫瘤產品中其中9種藥品為注射劑,說明書中缺乏用藥靜脈配置指導內容的2份(占22.2%)。該類藥物在配制過程中存在嚴重的安全隱患,藥師在配制的過程應當謹慎仔細,嚴格按照說明書的標注進行,然而在部分說明書中卻未見這一重要指導,其中國產仿制藥注射用鹽酸伊立替康,注射用鹽酸表柔比星,說明書中對該項目缺失,而相應的原研藥品中都具有相應的配制指導,在配制過程中可作為借鑒參考的重要內容。
2.3 臨床試驗項目缺失
臨床試驗項目是藥品說明書的重要組成部分,《細則》中明確提出該部分為臨床試驗概述,應當準確,客觀地進行描述,包括臨床試驗的給藥方法、研究對象、主要觀察指標、臨床試驗的結果包括不良反應等。也指出沒有進行臨床試驗的藥品可以不書寫該項內容。但筆者認為抗腫瘤藥物作為一種特殊的藥品,其潛在的危害較一般藥品高,應該在說明書中標注臨床試驗的項目,供醫藥專業人士在使用的過程中借鑒和參考。本文調查的14個國產仿制藥說明書中,僅1例(占7.12%)替吉奧膠囊藥品說明書中包含臨床試驗的內容。
3 討論
我國藥品的研發水平與歐美發達國家存在一定的差距,尤其是抗腫瘤相關的藥品以仿制藥為主,其優勢在于價格較原研藥低。但同時也要保證其安全有效,只有完善的藥品說明書才能夠為臨床的醫務工作者提供科學的理論依據,確保藥物治療的療效。通過分析國內外藥品說明書之間的差距,可以更好的指導國內仿制藥品說明書的制定,確保用藥安全合理。
3.1 特殊人群用藥
特殊人群由于其生理、心理方面與正常成年人有明顯差異,導致其體內的藥物代謝過程與成年人明顯不同,從而對藥物的有效性和安全性產生一定影響[6]。主要包括老人,兒童,孕婦和哺乳期婦女,這類人群在使用藥物的過程中應該謹慎,部分國產說明書對這類人群的用藥并未交代。例如國產鹽酸伊立替康注射液說明書中指出老年人應該謹慎選擇用藥劑量,卻未給出具體的方案,如對膽紅素超過正常值1.5倍患者禁用此藥品;而原研藥說明書中則指出超過65歲的患者應使用較低的初始劑量,并給出詳細的用藥指導,如對膽紅素大于正常值3倍的患者不推薦使用,并對大于正常值1.5~3倍的患者推薦可用劑量。
3.2 貯藏
溫度對藥品的質量影響較大,是確保藥品貯存質量的一項關鍵性指標[7],《細則》中規定藥品貯藏具體條件的表示方法按《中國藥典》要求書寫,并注明具體溫度。多數仿制藥品說明書中只是提及室溫保存,并沒有標注具體的溫度,或標注與原研藥品說明書不一致。例如注射用環磷酰胺原研藥中提出貯藏溫度不高于25 ℃,溶液制備后貯存于8 ℃以下,并在24 h內使用,而國產說明書只說保存在30 ℃以下。溫度影響可導致活性成分環磷酰胺的融化,因此需制定嚴格的溫度要求。
3.3 禁忌
所謂禁忌證,指藥品對患有某種疾病或者對某些藥物有過敏史的人禁止使用[8]。相同成分不同生產企業藥品說明書的差異,可能對醫療機構用藥行為構成風險[2]。《細則》中提出應當列出禁止應用該藥品的人群或者疾病情況。但實際國產仿制藥說明書標注并不完全或與原研藥存在差異,例如卡鉑注射液原研藥對出血的腫瘤患者禁用,枸櫞酸托瑞米芬片原研藥禁與延長QT間期的藥物聯用,而國產仿制藥說明書中均未提及。鹽酸伊立替康原研藥對膽紅素大于正常值3倍的患者禁用,而國產仿制藥對膽紅素大于正常值1.5倍的患者禁用。
3.4 不良反應
目前我國處方藥品說明書的不良反應部分,內容簡繁不一,表達形式各異,有時不能及時更新內容以傳達新近發現的不良反應信息,這無疑會給用藥安全帶來隱患[9]。例如注射用鹽酸伊立替康原研藥曾觀察到心肌缺血事件,主要發生在有潛在心臟疾病、具有其他心臟疾病危險因素或曾接受細胞毒藥物化療的患者中,而國產仿制藥說明書中未提及。
3.5 注意事項
藥品說明書的注意事項是臨床安全用藥的關鍵[10],許多藥品說明書在這一方面比較簡單。調查發現原研藥品說明書對特殊人群用藥的注意事項與國產仿制藥說明書中存在差異,例如注射用唑來膦酸原研藥說明書中指出治療過程中出現腎功能惡化的患者,當肌酐水平恢復到基線值10%以內才能繼續使用,國產仿制藥說明書中明確表示必須停藥直至腎功能恢復至基線水平。
3.6 說明書內容缺失可致的風險
國產仿制藥說明書在內容上的缺失和與原研藥的差異容易被醫務人員忽略,可能會造成不必要的醫療事故,給醫療機構帶來法律風險和治療風險[11-12]。在醫療糾紛案件處理中,藥品說明書作為重要的仲裁依據,具有法律作用。醫務人員若不了解仿制藥和原研藥說明書的差異,容易導致超說明書使用藥品。在門診日常工作中很常見的是,法律未限制超說明書使用藥品,但超說明書用藥缺乏相關法律的保障,一旦患者出現嚴重的不良反應,將造成醫療事故,給醫務工作者造成法律風險,給患者自身帶來治療風險。在臨床工作中,醫師遇到患者要求對同一成分的原研藥和國產仿制藥進行轉換時,要仔細閱讀兩者的說明書,為患者提供準確的治療方案,藥師提供合理的用藥指導,將風險降至最小程度。
4 結語
通過對比分析發現多數國產仿制藥在用法用量,不良反應,注意事項和藥物相互作用等方面描述不夠完整,臨床試驗項目缺失較多,特殊人群用藥方面不一致,這些問題的存在都會對臨床使用造成風險,并加劇醫患關系的惡化。因此相關企業應該自覺加強藥品說明書的修訂,及時補充臨床試驗數據,并確保信息真實。藥品監督管理機構應當提高我國仿制藥品說明書的審核標準,并監督藥品生產企業完善抗腫瘤藥品說明書,縮短與原研藥品說明書之間的差距,為醫務工作者合理使用抗腫瘤藥品提供科學依據,確保臨床用藥安全。
參考文獻
[1] 崔小康, 田月潔, 謝彥軍, 等. 阿德福韋酯國內外藥品說明書比較及其對藥品風險警示作用的思考[J]. 中國藥事, 2016, 30(5): 517-521.
[2] 王艷麗. 我院40組注射劑藥品說明書調查分析[J]. 中國藥物警戒, 2018, 15(3): 147-151.
[3] 傅書勇, 楊悅, 鄧劍雄, 等. 國產藥品說明書信息差異分析程序設計的探討[J]. 藥物評價研究, 2018, 41(2): 177-181.
[4] 國家食品藥品監督管理局. 關于印發《化學藥品和生物制品說明書規范細則》的通知[EB/OL]. (2006-05-10)[2019-01-03]. http: //www.nmpa.gov.cn/WS04/CL2196/323547. html.
[5] 國家食品藥品監督管理局. 藥品說明書和標簽管理規定[EB/OL]. (2006-03-15)[2019-01-03]. http: //www.nmpa.gov. cn/WS04/CL2174/300623.html.
[6] 張欣悅, 孫成春, 謝繼青, 等. 33份抗腫瘤類注射劑藥品說明書的調查分析[J]. 中國藥房, 2014, 25(1): 91-93.
[7] 桂凌. 從藥品說明書貯藏項內容淺談藥品貯藏環節的質量管理[J]. 安徽醫藥, 2011, 15(6): 786-788.
[8] 陳世才. 藥品說明書與用藥安全[J]. 中國現代醫藥雜志, 2009, 11(8): 122-123.
[9] 龔海虹, 林志強. 原研與國產仿制抗菌藥物藥品說明書的對比分析[J]. 中國藥房, 2015, 26(1): 141-144.
[10] 薛松, 吳高蕾, 孫顯峰, 等. 藥品說明書存在的問題及調查分析[J]. 中國醫藥導報, 2011, 8(18): 156-160.
[11] 劉敏豪, 鄔倩倩. 我院藥品說明書現狀調查及其相關風險分析[J]. 中國藥房, 2012, 23(17): 1619-1621.
[12] 孫華君, 黃瑾. 藥品說明書信息差異與臨用藥風險的倫理視角[J]. 藥學服務于研究, 2016, 16(4): 276-278.
*作者簡介:秦艷(1990—),女,初級藥師。從事醫院藥學和中藥藥效物質基礎研究。E-mail: LUCKY180808@163.com
**通信作者:葉巖榮(1974—),男,副主任藥師。從事醫院藥學研究。E-mail: yeyanrong1990@163.com

