ω-3多不飽和脂肪酸對重型顱腦損傷患者術后免疫功能影響的研究
湯崇輝 方戰艦 胡益嵐 單鈺棟 童云 陳夢丹 魏曉捷
[摘要] 目的 探討ω-3多不飽和脂肪酸對重型顱腦損傷患者術后營養狀況及免疫功能的影響。 方法 采用隨機數字法將2017年7月~2018年6月入住本院符合研究條件的82例重型顱腦損傷患者分為兩組:常規腸內營養組(對照組,40例)和ω-3多不飽和脂肪酸組(ω-3組,42例)。對照組給予常規腸內營養制劑瑞代,ω-3組給予富含ω-3多不飽和脂肪酸的腸內營養制劑瑞能。分別檢測患者第1天、第4天、第7天和第14天的血清白蛋白、前白蛋白、免疫球蛋白(IgG、IgA和IgM)水平,測定CRP的變化、GCS評分和感染的發生率。 結果 給予腸內營養支持后,兩組患者的血清白蛋白和前白蛋白均有升高,第14天與第1天比較,差異有統計學意義(P<0.05),組間比較差異無統計學意義(P>0.05);與對照組相比,ω-3組免疫球蛋白的增加差異有統計學意義(P<0.05);兩組患者CRP比較差異有統計學意義(P<0.05),ω-3組下降多于對照組,差異有統計學意義(P<0.05);兩組患者GCS評分均有改善,組間比較差異無統計學意義(P>0.05);ω-3組肺部感染的發生率低于對照組,差異有統計學意義(P<0.05)。 結論 ω-3多不飽和脂肪酸能夠改善重型顱腦損傷患者的營養狀況,促進免疫功能的恢復,減少患者術后肺部感染的發生率。
[關鍵詞] 顱腦損傷;腸內營養;免疫營養;ω-3多不飽和脂肪酸;免疫功能
[中圖分類號] R651.15 ? ? ? ? ?[文獻標識碼] A ? ? ? ? ?[文章編號] 1673-9701(2019)25-0018-05
Effect of omega-3 polyunsaturated fatty acids on postoperative immune function in patients with severe head injury
TANG Chonghui FANG Zhanjian HU Yilan SHAN Yudong TONG Yun CHEN Mengdan WEI Xiaojie
Department of Neurosurgery, Cixi Hospital Affiliated to Wenzhou Medical University, Cixi 315300, China
[Abstract] Objective To explore the effect of omega-3 polyunsaturated fatty acids on postoperative immune function in patients with severe head injury. Methods 82 patients with severe head injury treated in our hospital from July 2017 to June 2018 were randomly divided into two groups, the routine enteral nutrition group(control group, 40 cases) and the ω-3 polyunsaturated fatty acid group(ω-3 group, 42 cases). The control group was given a conventional enteral nutrition preparation, and the omega-3 group was given an enteral nutrition preparation rich in omega-3 polyunsaturated fatty acid. The serum albumin, prealbumin, and immunoglobulin (IgG, IgA, and IgM) levels were measured on day 1, day 4, day 7, and day 14, respectively, and CRP changes, GCS scores, and incidence of infection were measured. Results After administration of enteral nutrition, albumin and prealbumin were increased in both groups. On the 14th day compared with the first day, the difference was statistically significant(P<0.05). There was no significant difference between the two groups(P>0.05). The immunoglobulin in ω-3 group was more increased than that in the control group, with the difference statistically significant (P<0.05). The difference of CRP between the two groups was statistically significant(P<0.05). The ω-3 group decreased more than the control group, with statistical significance(P<0.05). The GCS scores of the two groups were improved. There was no significant difference between the two groups(P>0.05). The incidence of pulmonary infection in the omega-3 group was lower than that in the control group(P<0.05). Conclusion Omega-3 polyunsaturated fatty acids can improve the nutritional status of patients with severe craniocerebral injury, promote the recovery of immune function, and reduce the incidence of postoperative pulmonary infection.
[Key words] Craniocerebral injury; Enteral nutrition; Immune nutrition; Omega-3 polyunsaturated fatty acid; Immune function
近年來,盡管顱腦損傷患者的預后有所改善,但重型顱腦損傷患者的死亡率和致殘率仍居高不下[1]。重型顱腦損傷患者術后常存在意識及吞咽功能障礙、急性應激反應、激素分泌及內臟功能失衡等代謝紊亂,導致營養不良和免疫功能下降,繼而使患者感染、臟器功能障礙、死亡風險增加,影響臨床結局[2]。已有研究發現,免疫增強型腸內營養制劑能調節機體免疫系統,既能防止免疫功能低下,又能防止出現過度的炎性反應,維持機體免疫穩態,從而進一步改善蛋白代謝,維護腸黏膜屏障,以達到免疫營養的目的[3]。但免疫營養制劑對顱腦外傷術后患者的有效性尚未見系統性研究。本研究主要針對ω-3多不飽和脂肪酸(ω-3PUFAs)對重型顱腦損傷術后患者免疫功能、炎癥反應及肺部感染的發生率進行研究,現報道如下。
1 資料與方法
1.1一般資料
選取2017年7月~2018年6月我院神經外科收治的重型顱腦損傷患者。納入標準:①臨床明確診斷的急性重癥顱腦損傷開顱手術患者;②傷后48 h內入院;③術前GCS評分[4]4~8分;④年齡18~70歲;⑤患者家屬知情同意參與研究。排除標準:①雙瞳散大固定、無自主呼吸者;②嚴重復合傷,或主要損傷部位不在顱腦者;③術中急性腦膨出,血壓需大劑量升壓藥維持或多次開顱手術者;④基礎臟器疾病,如嚴重心臟病、肝腎功能異常者;⑤糖尿病及其他影響內分泌代謝疾病者;⑥消化道嚴重器質性疾病或腸內營養支持治療禁忌證者;⑦惡性腫瘤者;⑧妊娠期女性[5,6]。根據納入和排除標準,共入組患者82例,采用隨機數字表法分為常規腸內營養組(對照組)和ω-3多不飽和脂肪酸組(ω-3組)。對照組40例,其中男27例,女13例,年齡(42.6±10.1)歲;術前格拉斯哥昏迷(GCS)評分(5.5±1.0)分;腦挫裂傷12例,急性硬膜下血腫7例,腦內血腫7例,急性硬膜外血腫8例,急性硬膜下血腫合并腦挫裂傷6例;ω-3組42例,其中男26例,女16例,年齡(43.5±12.4)歲;術前GCS評分(5.6±0.9)分;腦挫裂傷11例,急性硬膜下血腫10例,腦內血腫7例,急性硬膜外血腫7例,急性硬膜下血腫合并腦挫裂傷7例。兩組間一般資料比較差異無統計學意義(P均>0.05),具有可比性。
1.2 方法
兩組患者均在入院第1天留置鼻胃管,使用營養泵經鼻胃管勻速泵入營養液。ω-3組首日給予400 mL的瑞能(華瑞制藥有限公司,國藥準字:H20040722)提供腸內營養(每100 mL瑞能中含ω-3多不飽和脂肪酸0.3 g),以后每天增加200 mL,至1 000 mL/d。對照組首日給予400 mL瑞代(華瑞制藥有限公司,國藥準字:J20140077)提供腸內營養能量,以后每天增加200 mL,至1 000 mL/d。所有患者供給目標為25 kcal/(kg·d)。控制血糖在(7.8~10.0)mmol/L。不足的熱量兩組患者均通過中心靜脈給予。所有患者均根據顱腦創傷指南予以靜脈營養、降顱壓、預防感染、神經營養、預防癲癇等同質化治療[7]。
1.3并發癥處理
患者出現腹脹或嘔吐,減慢營養液泵入速度,減少泵入總量,可加用胃腸道動力藥物。患者出現腹瀉(稀便>3 次),減慢泵入速度,減少泵入總量。患者出現上消化道出血,靜脈滴注奧美拉唑(辰欣藥業股份有限公司,國藥準字:H20083922)40 mg,2次/d。若血性胃內容物>100 mL,暫停腸內營養;若血性胃內容物<100 mL,減速泵入,每天查胃內容物潛血,直至2次潛血陰性。患者出現胃動力不全,若胃液殘留>200 mL,加用甲氧氯普胺(上海現代哈森藥業有限公司,國藥準字:H20044996)10 mg肌肉注射治療,若持續潴留,置入鼻空腸管給予腸內營養[8]。
1.4觀察指標
兩組患者分別于手術后第1天、第4天、第7天和第14天測定血清白蛋白、前白蛋白、IgG、IgA、IgM、C-反應蛋白的含量(日立全自動生化儀7600DDP,日本),評估GCS評分,統計住院期間肺部感染的發生率。
1.5 統計學分析
應用SPSS16.0統計學軟件進行統計分析,計量資料以均數±標準差(x±s)表示,采用t檢驗,組內各時間點比較采用單因素方差分析,并進一步用LSD檢驗作兩兩比較;計數資料以[n(%)]表示,采用χ2檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者血清白蛋白的變化比較
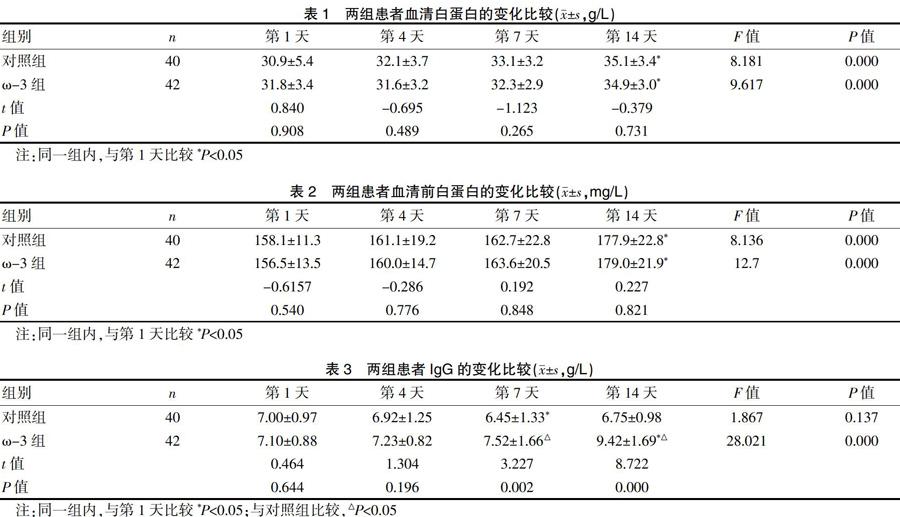
經腸內營養治療,兩組患者的白蛋白均逐步升高,對照組從第1天的(30.9±5.4)g/L升高到第14天的(35.1±3.4)g/L。ω-3組從第1天的(31.8±3.4)g/L升高到第14天的(34.9±3.0)g/L。兩組第14天與第1天比較,差異有統計學意義(P<0.05),ω-3組與對照組患者的血清白蛋白比較差異無統計學意義(P>0.05),見表1。
2.2 兩組患者血清前白蛋白的變化比較
經腸內營養治療,兩組患者的前白蛋白均逐步升高,對照組從第1天的(158.1±11.3)mg/L升高到第14天的(177.9±22.8)mg/L,ω-3組從第1天的(156.5±13.5)mg/L升高到第14天的(179.0±21.9)mg/L。兩組第14天與第1天比較,差異有統計學意義(P<0.05),ω-3組與對照組患者的血清前白蛋白含量比較差異無統計學意義(P>0.05),見表2。
2.3 兩組患者IgG的變化比較
在治療過程中,對照組IgG的含量有所下降,第7天與第1天比較差異有統計學意義(P<0.05),其余各時間點與第1天比較差異無統計學意義(P>0.05);ω-3組IgG的含量有所升高,第14天與第1天比較差異有統計學意義(P<0.05);在第7天和第14天,ω-3組與對照組IgG含量比較,差異有統計學意義(P<0.05),見表3。
2.4 兩組患者IgA的變化比較
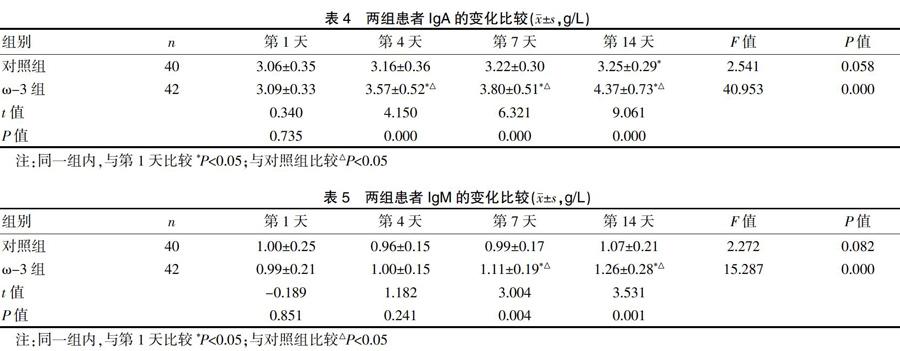
在治療過程中,對照組IgA的含量稍有增加,第14天與第1天比較差異有統計學意義(P<0.05),其余各時間點與第1天比較差異無統計學意義(P>0.05);ω-3組IgA的含量有升高,第4天、第7天和第14天與第1天比較差異有統計學意義(P<0.05);在第4天、第7天和第14天,ω-3組與對照組IgA含量比較,差異有統計學意義(P<0.05),見表4。
2.5 兩組患者IgM的變化比較
在治療過程中,對照組IgM含量的變化差異無統計學意義(P>0.05);ω-3組IgM的含量有升高,第7天和第14天與第1天比較差異有統計學意義(P<0.05);在第7天和第14天,ω-3組與對照組IgM含量比較,差異有統計學意義(P<0.05),見表5。
2.6 兩組患者CRP的變化比較
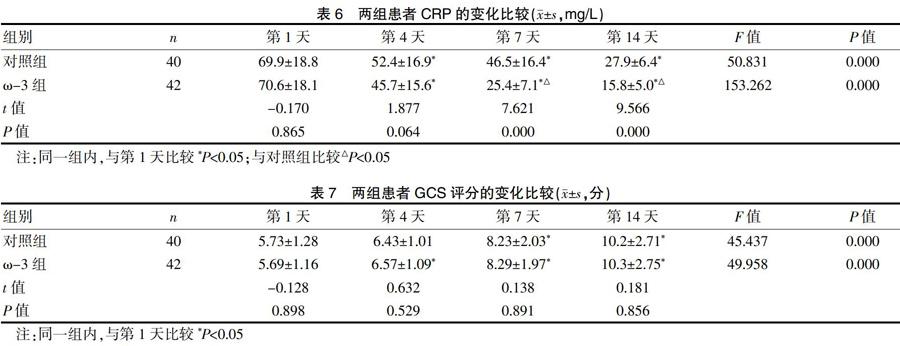
兩組患者的CRP均有下降,各時間點與第1天比較差異均有統計學意義(P<0.05);在第7天和第14天,ω-3組下降多于對照組,差異有統計學意義(P<0.05),見表6。
2.7 兩組患者GCS評分的變化比較
兩組患者GCS評分均有改善,對照組在第7天和第14天與第1天相比較,差異有統計學意義(P<0.05);ω-3組在第4天、第7天和第14天與第1天比較,差異有統計學意義(P<0.05);兩組間比較差異無統計學意義(P>0.05)。見表7。
2.8 兩組患者肺部感染的發生率
對照組發生肺部感染19例,發生率47.5%;ω-3組發生肺部感染11例,發生率26.2%,組間比較差異有統計學意義(χ2=4.010,P<0.05)。
3 討論
顱腦損傷(TBI)是一種常見的神經外科疾病,是全球人群致死和致殘的主要原因,并且顱腦外傷術后患者預后相對較差[9]。重型顱腦損傷術后患者常存在意識障礙,無法自主進食,導致營養不良和免疫功能下降[10],而患者的營養狀況與感染的發生密切相關,重型顱腦損傷術后患者的營養不良、低蛋白血癥是導致機體免疫功能低下、易感性增強的重要因素[11]。因此如何有效改善患者營養狀態,控制低蛋白血癥,維持正常的免疫功能,減少傷后感染率的發生是目前治療重度顱腦損傷重點。既往營養支持主要通過提供充足的能量和氮源,適應機體代謝需要,維持正常蛋白代謝,以達到促進患者康復的目的[12]。由于危重患者多存在頑固的高分解代謝,嚴重的酸堿失衡和水電解質紊亂,對營養底物的利用和耐受程度降低,使傳統營養支持對重癥患者療效不甚理想,最終造成機體營養不良和免疫力低下[13]。近年隨著臨床營養學的發展和對機體代謝規律的深入研究,提出了免疫營養(immunonutrition)這一概念[14]。其根據臟器組織不同的代謝特征進行代謝調理,并強調特殊營養素的營養效應,認為可通過提供一些特殊營養素,利用其藥理作用達到調節機體代謝和提高免疫功能的目的[15]。將特殊營養素添加到腸內營養中的制劑稱之為免疫增強型腸內營養制劑(immuneenhancing diets,IEDs),其實質就是通過調節機體免疫系統,既防止免疫功能低下,又防止出現過度的炎性反應,即維持機體免疫穩態[16]。從而進一步改善蛋白代謝,維護腸黏膜屏障,以達到免疫營養的目的[17]。目前,免疫營養制劑研究的熱門是ω-3多不飽和脂肪酸(ω-3 polyunsaturated fatty acids,ω-3PUFAs)。多不飽和脂肪酸包括ω-3PUFAs、ω-6PUFAs和亞油酸,是前列腺素、前列腺環素、血栓素和白三烯等花生四烯酸代謝產物的前體。ω-3PUFAs在深海魚油中含量豐富,代謝產物主要是二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)等[18];ω-6PUFAs主要來自大豆、菜籽等植物油,主要為亞油酸,均是細胞膜磷脂的主要成分;作為花生四烯酸代謝產物的前體,實驗證明ω-6PUFAs和亞油酸能促進促炎性反應因子如IL-1、TNF-α和IL-6的釋放,而ω-3PUFAs正好相反,可抑制亞油酸轉變成花生四烯酸,并且ω-3PUFAs可取代細胞膜磷脂中的ω-6PUFAs,減少前列腺素、白三烯的形成,從而降低促炎因子的產生,降低超敏反應,增強機體免疫能力,減少內毒素移位等,因此ω-3是免疫營養劑中的關鍵成分[19]。
在腫瘤患者圍手術期或術后給予ω-3PUFAs強化飲食,可降低IL-1和IL-6的可溶性受體,增加IL-2可溶性受體,延遲超敏反應,降低感染率的發生[20]。對嚴重腹部損傷的患者給予含有Gln、Arg和ω-3PUFA的免疫營養液,對照組給予常規營養液,發現使用免疫營養液組的患者敗血癥的發生率明顯降低,同時也減少了住院費用[21]。研究含Arg、魚油和核苷酸的營養劑對嚴重創傷患者的SIRS和MOF的影響,結果實驗組SIRS時間縮短和MOF的發生率顯著降低,膿毒血癥的發生率也明顯降低[22]。2016年ASPEN重癥患者營養支持治療指南認為含免疫調節成分配方可以在創傷性腦損傷患者中使用[23]。
血漿蛋白水平是反映機體蛋白質營養狀況的重要指標,不僅可提供客觀的營養評價結果,而且不易受主觀因素影響[24]。常用的指標包括血清白蛋白(albumin,Alb)和前白蛋白(prealbumin,PA),并且PA雖由肝細胞合成,但體積較小、半衰期較短,其濃度的變化能夠早期而敏感地反映肝臟蛋白質合成功能,故已作為檢測營養治療效果的指標而得到廣泛使用。本研究發現,給予腸內營養支持后,兩組患者的白蛋白和前白蛋白均有升高,第14天與第1天比較有明顯升高,但兩組間比較差異無統計學意義。故免疫腸內營養制劑與常規腸內營養制劑一樣能滿足重型顱腦損傷患者的營養要求。但早期腸內營養液存在一些并發癥,如嘔吐、胃潴留、腹瀉等,需注意預防和及時處理。
IgG、IgA、IgM是體液免疫的常用指標,在治療過程中,對照組IgG、IgA、IgM含量的變化均不明顯,ω-3組IgG、IgA、IgM的含量均有升高,與對照組比較,ω-3組在第7天和第14天IgG、IgA、IgM的含量有明顯升高。這說明ω-3PUFAs能夠提高免疫球蛋白水平。
CRP是炎癥標志物,以糖蛋白的形式存在于血液中,在健康人群血液中水平極低,當機體處于感染、創傷等應激狀態時,CRP顯著升高,且升高程度與損傷程度呈正比,可以用來評估感染的危重程度及預后[25]。研究證實細菌可經過組織學正常的腸道易位,細菌及其毒素易位腸外器官可造成毒性遞質或細胞因子釋放。在治療過程中,兩組患者的CRP均有明顯下降,并且ω-3組下降明顯多于對照組,說明ω-3PUFAs能夠減少炎癥反應。同時研究結果也顯示,盡管兩組患者的GCS評分無明顯差異,但ω-3組肺部感染的發生率明顯低于對照組。
綜上所述,重型顱腦損傷患者術后由于早期代謝明顯升高、熱量消耗增加,機體呈負氮平衡,免疫功能低下,易導致感染等并發癥的發生。給予重型顱腦損傷患者ω-3PUFAs能夠滿足營養需求,保持代謝平衡,糾正免疫異常,減少感染的發生率。
[參考文獻]
[1] Singh AK,Jena RK,Pal R,et al. Morbidity audit of 704 traumatic brain injury cases in a dedicated South Indian Trauma Center[J]. Asian J Neurosurg,2018,13(3):714-720.
[2] 中華醫學會神經外科分會. 中國神經外科重癥患者消化與營養管理專家共識(2016)[J].中華醫學雜志,2016, 96(21):1643-1647.
[3] Peker KD,Ozkanli SS,Akyuz C,et al. Preoperative immunonutrition regulates tumor infiltrative lymphocytes and increases tumor angiogenesis in gastric cancer patients[J]. Arch Med Sci,2017,13(6):1365-1372.
[4] 吳孟超. 外科學[M]. 北京:人民衛生出版社,2013:196-197.
[5] Chapple LA,Chapman M,Shalit N,et al. Barriers to nutrition intervention for patients with a traumatic brain injury:Views and attitudes of medical and nursing practitioners in the acute care setting[J]. JPEN J Parenter Enteral Nutr,2018,42(2):318-326.
[6] Duraski SA,Lovell L,Roth EJ. Nutritional intake,body mass index,and activity in postacute traumatic brain injury:A preliminary study[J]. Rehabil Nurs,2014,39(3):140-146.
[7] Palm NM,McKinzie B,Ferguson PL,et al. Pharmacologic stress gastropathy prophylaxis may not be necessary in at-risk surgical trauma ICU patients tolerating enteral nutrition[J]. J Intensive Care Med,2018,33(7):424-429.
[8] Justo Meirelles CM,de Aguilar-Nascimento JE. Enteral or parenteral nutrition in traumatic brain injury:A prospec-tive randomisedtrial[J]. Nutr Hosp,2011,26(5):1120-1124.
[9] 高亮. 顱腦創傷和腦科危重癥治療學[M]. 上海:上海科學技術出版社,2012:1.
[10] Mazaherpur S,Khatony A,Abdi A,et al. The effect of continuous enteral nutrition on nutrition indices,compared to the intermittent and combination enteral nutrition in traumatic brain injury patients[J]. J Clin Diagn Res,2016,10(10):JC01-JC05.
[11] Colleen N,Bodnar,Josh M,et al. Depression following a traumatic brain injury:Uncovering cytokine dysregulation as a pathogenic mechanism[J]. Neural Regen Res,2018, 13(10):1693-1704.
[12] Araki T,Yokota H,Morita A. Pediatric traumatic brain injury:Characteristic features,diagnosis,and management[J].Neurol Med Chir (Tokyo),2017,57(2):82-93.
[13] Diaz-Arrastia R,Kochanek PM,Bergold P,et al. Pharmacotherapy of traumatic brain injury:State of the science and the road forward:Report of the Department of Defense Neurotrauma Pharmacology Workgroup[J]. J Neurotrauma,2014,31(2):135-158.
[14] Lucas W,Thornblade,Thomas K,Varghese,et al. Preoperative immunonutrition and elective colorectal resection outcomes[J]. Dis Colon Rectum,2017,60(1):68-75.
[15] Xu J,Sun X,Xin Q,et al. Effect of immunonutrition on colorectal cancer patients undergoing surgery:A meta-analysis[J]. Int J Colorectal Dis,2018,33(3):273-283.
[16] Bharadwaj S,Trivax B,Tandon P,et al. Should perioperative immunonutrition for elective surgery be the current standard of care?[J]. Gastroenterol Rep (Oxf),2016,4(2):87-95.
[17] Klek S,Szybinski P,Szczepanek K. Perioperative immunonutrition in surgical cancer patients:A summary of a decade of research[J]. World J Surg,2014,38(4):803-812.
[18] McCowen KC,Bistrian BR. Immunonutrition:Problematic or problem solving?[J]. Am J Clin Nutr,2003,77(4):764-770.
[19] Alexander JW,Supp DM. Role of arginine and omega-3 fatty acids in wound healing and infection[J]. Adv Wound Care,2014,3(11):682-690.
[20] Song GM,Liu XL,Bian W,et al. Systematic review with network meta-analysis:Comparative efficacy of different enteral immunonutrition formulas in patients underwent gastrectomy[J]. Oncotarget,2017,8(14):23376-23388.
[21] Kudsk KA,Minard G,Croce MA,et al. A randomized trial of isonitrogenous enteral diets after severe trauma. An immune-enhancing diet reduces septic complications[J]. Ann Surg,1996,224(4):531-543.
[22] Binkowska AM,Michalak G,Sotwiński R. Current views on the mechanisms of immune responses to trauma and infection[J]. Cent Eur J Immunol,2015,40(2):206-216.
[23] McClave SA,Taylor BE,Martindale RG,et al.Guidelines for the provision and assessment of nutrition support therapy in the adult critically Ⅲ patient:Society of critical care medicine(SCCM)and American Society for parenteral and enteral nutrition(ASPEN)[J]. J Parenter Enteral Nutr, 2016,40(2):159-211.
[24] Xu J,Sun X,Xin Q,et al. Effect of immunonutrition on colorectal cancer patients undergoing surgery:A meta-analysis[J]. Int J Colorectal Dis,2018,33(3):273-283.
[25] Dietrich WD,Bramlett HM. Therapeutic hypothermia and targeted temperature management for traumatic brain injury:Experimental and clinical experience[J]. Brain Circ,2017,3(4):186-198.
(收稿日期:2019-01-10)

