酯交換法合成碳酸甲乙酯研究進展
石 磊, 于 悅, 王吉宇, 張志剛, 許光文
(1. 沈陽化工大學 資源化工與材料教育部重點實驗室, 遼寧 沈陽 110142;2. 沈陽化工大學 能源與化工產業技術研究院, 遼寧 沈陽 110142;3. 沈陽化工大學 應用化學學院, 遼寧 沈陽 110142)
碳酸甲乙酯(EMC)是一種具有不對稱結構的線型碳酸酯類化合物,它同時兼有碳酸二甲酯(DMC)與碳酸二乙酯(DEC)的特性,可作為羰基化或烷基化試劑用于有機合成[1]反應。EMC是一種有前途的汽油添加劑[2],可提升汽油辛烷值[3],降低汽車尾氣中固體顆粒物以及氮氧化合物的排放。EMC更為重要和廣泛的應用是作為一種優良的鋰離子電池電解液溶劑[4],在結構上具有空間位阻小和不對稱性,能夠輔助增加鋰離子的溶解度,提高電池的電容量密度和電量[5];EMC作為溶劑有利于拓寬電解液工作溫度范圍[6],同時具有優良的導熱性、低電阻性和電化學環境結構穩定性[7],有效提升鋰電池的安全性[5]并延長電池使用壽命[7,8]。
EMC的合成方法主要有光氣法、氧化羰基化法以及酯交換法等[9]。光氣法生產效率高,但原料光氣劇毒[10,11],產生強酸性HCl嚴重腐蝕設備,該方法已經逐步被淘汰。氧化羰化法[12]以MeOH、EtOH、CO和O2為主要原料,但是EMC收率太低,且反應有O2參與,存在安全隱患。改進的氧化羰化法中,CO2可以代替CO和O2一步合成碳酸酯[13,14],但碳酸酯收率一般低于20%。酯交換法制備EMC包括DMC與EtOH[15-24]的酯醇交換和DMC與DEC[25-32]的酯酯交換。它們的反應過程如方程式(1)和(2)所示。酯交換法反應條件溫和、催化效率高、工藝相對簡單、且幾乎沒有副產物生成,比起其他合成路線更加綠色環保,所以工業上多使用酯醇交換法制備EMC。但該反應體系存在三種共沸產物,分別為MeOH-DMC(63.7 ℃,86.6 mol% MeOH)、EtOH-DMC(74.9 ℃,69 mol% EtOH)和EtOH-EMC(78.9 ℃,95 mol% EtOH)[15],這些共沸物給后續分離帶來困難。如果碳酸酯產品中混有少量醇,會造成鋰電池效率降低,甚至形成安全隱患。工業上采用催化精餾的方式實現產物分離,主要以強堿性甲醇鈉(CH3ONa)為催化劑,催化活性較高,但CH3ONa遇水敏感,容易失活,參與反應生成的鈉鹽在碳酸酯中溶解度較低,容易析出,導致催化劑不能循環使用,并且難以分離,少量殘留就導致生產的EMC純度降低,產生強堿性固廢污染環境。強堿性催化劑也可以催化DMC與DEC的酯酯交換合成EMC,該反應體系不存在共沸分離問題,但是催化劑在碳酸酯中的溶解度較低,工業上暫時無法提供萬噸級的DEC。
CH3OCOOCH3+C2H5OH→ CH3OCOOC2H5+CH3OH
(1)
CH3OCOOCH3+C2H5OCOOC2H5→
2CH3OCOOC2H5
(2)
DMC與EtOH的酯交換反應體系中,還包括EMC與EtOH酯交換生成DEC和MeOH、EMC歧化反應生成DMC和DEC、DMC與EtOH酯交換生成DEC和MeOH等三個反應,如方程式(3)、(4)和(5)所示。反應(1)、(3)與反應(5)為相關反應,反應(2)是反應(4)的逆反應。
CH3OCOOC2H5+C2H5OH→
C2H5OCOOC2H5+CH3OH
(3)
2CH3OCOOC2H5→
CH3OCOOCH3+C2H5OCOOC2H5
(4)
CH3OCOOCH3+2C2H5OH→
C2H5OCOOC2H5+2CH3OH
(5)
最新碳酸酯相關綜述為2016年張旭[33]發表,主要討論了DMC酯交換反應合成EMC的路線,對比DMC分別與EtOH和DEC進行反應的特點以及部分催化劑研究進展。本研究在此基礎上總結了近五年來該領域的研究新進展,系統整理和綜述了酯交換法制備EMC的反應熱力學、動力學、催化劑進展、反應機理及反應工藝。并分類闡述了均相催化劑(可溶堿、離子液體和可溶鹽類)以及非均相催化劑(離子交換樹脂、金屬氧化物、堿性分子篩和MOFs材料類)的最新研究,最后指出合成鋰電池級EMC所面臨的問題以及未來的研究方向。
1 反應熱力學


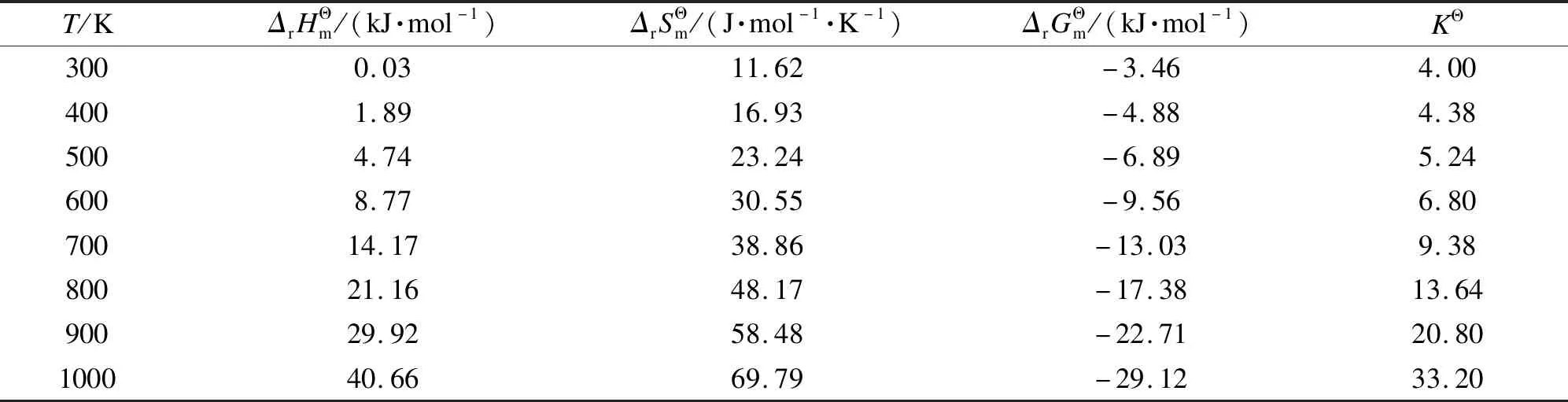
表 1 DMC與DEC酯交換反應的熱力學參數[34]
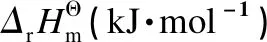
表 2 DMC與EtOH的酯交換反應體系的和

表 3 DMC與EtOH酯交換反應體系的和KΘ[37]
值得注意的是,文獻[37]中提到的EMC歧化反應是DMC與DEC酯交換反應[34]的逆反應,兩者對各自的討論對象都得出是吸熱反應以及熵增的結論,因此是互相矛盾的,但是對反應自發性的判斷是一致的。說明在分析過程中,選擇數據處理模型以及引用熱力學參數都會對理論分析結果產生影響。針對DMC和DEC酯交換制備EMC的反應,作者完成了20 kg級別固體催化劑中試,催化劑為圓柱形,長度8-12 mm,直徑1.5 mm,混合原料中DMC和DEC物質的量比1∶1,混料質量空速5 h-1,原料經預熱器加熱到105 ℃以后通過單管催化劑床層,反應器已做外保溫處理,并在距反應器入口1/3及出口1/3處設有測溫熱電偶。隨著反應進行,反應溫度逐漸降低,反應器出口溫度在80-85 ℃,產物組成(質量分數)約為19.8% DMC、51.7% EMC以及28.5% DEC,沒有其他副產物生成。根據各測溫點物料的溫度變化情況,得出DMC和DEC酯交換制備EMC是一個吸熱反應的事實。

2 反應動力學
通過碳酸酯交換體系中反應動力學研究可以計算出反應速率隨溫度、反應物濃度隨時間變化的規律,借此對EMC的生產工藝進行校驗,從而有助于提高生產效率和產品質量。Luo等[15]以K2CO3和相轉移試劑為催化劑,基于各物質摩爾濃度計算出反應(1)和(3)在45-100 ℃反應速率常數k(1)和k(3)分別隨溫度T變化的關系式,即
k(1)=2.148×104exp
(6)
k(3)=3.076×103exp
(7)
由上式可知,反應(3)的活化能比(1)的活化能略小,但是其Arrhenius方程的指前因子比后者低近一個數量級,因此反應(1)反應速率快于(3)。
Zielinska-Nadolska等[16]考察了分子篩、離子交換樹脂、水滑石、金屬氧化物、改性K2CO3等物質催化DMC與EtOH酯交換反應的動力學特征。反應溫度313-348 K,計算出改性K2CO3、凝膠型強酸離子交換樹脂(Lewatit K1221)和超強酸離子交換樹脂(Nafion SAC-13)催化上述反應的動力學數據如表4所示。由于活性中心的酸堿性差異,反應(1)和(3)體現出不同的動力學特征。改性K2CO3作催化劑時,反應(1)的活化能大于反應(3)的活化能,但是其Arrhenius方程的指前因子數值大約是后者的四倍,因此反應(1)快于(3),此特點與其他文獻[15]給出的結果類似;樹脂酸催化時,反應(1)的活化能小于反應(3)的活化能,其Arrhenius方程的指前因子明顯小于后者。因此,無論是堿性還是酸性催化劑,反應(3)總是這一“連串反應”的控速步驟[16]。

表 4 反應(1)和(3)的Arrhenius方程的指前因子與活化能[16]
Keller等[20]以C2H5ONa為催化劑,基于反應物活度討論了DMC與EtOH酯交換動力學特性。反應溫度323-363 K,反應(1)和(3)的Arrhenius方程為:
(8)
(9)
此結果表明反應(3)的活化能明顯大于反應(1)的活化能,兩者的Arrhenius方程的指前因子分別為k0,(1)=1.34×1011mol/(m3·s)和k0,(3)=1.80×1013mol/(m3·s),反應速率(1)仍高于(3)。
王紅星等[38]考察了303-333 K 時CH3ONa催化DMC與EtOH酯交換體系,建立了基于摩爾濃度的連串反應(1)和(3)的反應動力學方程:

(10)
(11)
式中,cDMC、cEtOH、cEMC、cMeOH、cDEC分別是DMC、EtOH、EMC、MeOH和DEC的摩爾濃度(mol/L)。反應(3)的活化能明顯大于反應(1)的活化能,其Arrhenius方程的指前因子大約是后者的4.2倍,反應(1)和(3)的活化能與指前因子的大小關系與文獻[20]一致。
張運茂等[39]考察了堿性咪唑離子液體催化DMC與DEC的酯交換特性,該反應是EMC歧化反應的逆反應,測得的均相可逆反應動力學參數見表5。正向反應(2)的活化能大于歧化反應(4)的活化能,但是(2)的指前因子是(4)的74.5倍,因此,反應(2)平衡常數更易受溫度影響,提高溫度促進反應向正向進行,當反應溫度由353.15 K升高到368.15 K時,反應平衡常數由3.04提高至3.45。

表 5 反應(2)和(4)的Arrhenius方程的指前因子與活化能[39]
對于DMC與EtOH酯交換反應體系的動力學研究還存在少許疑問:當催化劑為強堿或酸時,第一步酯交換反應(1)的活化能和指前因子都比第二步酯交換反應(3)的小。但是,以K2CO3為催化劑時,反應(1)的活化能和指前因子皆大于(3),這說明不同堿強度的催化劑催化反應機理可能有所差別。
3 催化劑進展
酯交換法合成EMC的催化劑分均相和非均相兩大類,其中,均相催化劑主要包括:可溶有機強堿,如甲醇鈉(CH3ONa)、乙醇鈉(C2H5ONa)或叔丁醇鈉(C4H9ONa)等;可溶無機強堿包括KOH、NaOH等;中等強度堿或弱堿,如K2CO3、Na2CO3或KF等;離子液體,目前研究主要集中在具有不同陰、陽離子結構的烷基咪唑鹽,如[Mmim]Cl、[Emim]Br或[Bmim]I等;可溶鹽類催化劑,如Mg(NO3)2、La(NO3)3、 Ti(OBu)4或Bu2SnO等。非均相催化劑主要包括:離子交換樹脂;金屬氧化物,如MgO、CaO、MgO-Al2O3、Mg-Al-O-t-Bu或AlPO等;堿性分子篩,如Al-Zn-MCM-41;MOFs材料,如ZIF-8或ZIF-67等。
3.1 均相催化劑
3.1.1 可溶堿類催化劑
可溶堿類催化劑對酯交換法制備EMC催化效率較高,表6按照催化劑堿強度比較了有機強堿催化劑C4H9ONa、C2H5ONa以及CH3ONa;無機強堿催化劑KOH和NaOH;無機中等強度堿和弱堿催化劑K2CO3、Na2CO3、NaHCO3、KF和NaF對酯交換反應的影響。為保證反應數據的系統性和反應結果的可對照性,本論文進行了部分補充,在參考文獻處用“*”來表示。補充數據統一反應條件為:nDMC∶nEtOH=1∶1,催化劑含量0.15%-1.5%(占反應物總摩爾百分數),反應溫度30-78 ℃,常壓反應0.5 h。
從表6可以看出,有機強堿C4H9ONa、C2H5ONa和CH3ONa作催化劑時,DMC轉化率和EMC收率依次下降,表明隨著催化劑親核性減弱,酯交換效率降低。當CH3ONa含量為1.5%,在接近室溫(30 ℃)反應0.5 h,取得了良好的催化效果。繼續升溫至50或者78 ℃,基本保持不變,表明該結果是等物質的量比的DMC和EtOH混合原料在一定溫度范圍內(0-80 ℃)的平衡轉化率。中國科學院成都有機所[40]報道了CH3ONa和CH3OK催化劑在78 ℃反應4 h時的結果,按EtOH計算EMC收率達到54.7%。Keller等[20,21]采用C2H5ONa催化劑用于DMC與EtOH反應精餾過程。有機強堿催化劑如CH3ONa在萬噸級/年EMC工業生產過程中會造成精餾塔結垢,產生白膜,同時催化劑在第一精餾塔塔釜析出。姚潔等[40,41]認為,該現象是CH3ONa在反應混合產物中溶解度不好所致,在塔釜中尤為明顯。因此,向CH3ONa中添加了醇胺類[41]化合物作溶劑和助催化劑,復合物在反應液中溶解性良好,有利于酯交換反應在均相狀下進行,達到了良好的催化效果。
作者發現有機強堿催化劑CH3ONa和無機強堿催化劑NaOH在催化DMC與EtOH的酯交換過程中因參與反應而逐步失活,其反應路徑和機理如圖1所示:CH3ONa首先與原料中極少量的水(H2O)發生反應,生成NaOH和CH3OH;第二步:OH-會親核進攻DMC中的羰基碳,使C=O鍵斷裂形成中間體a;第三步:由于a不穩定,與C相連的四個C-O至少需要斷裂一條,這是典型的親核加成-消去反應。1位C-O鍵在堿催化體系下無法斷裂,除非C+和O-能夠分別以自由基的形式穩定存在,這顯然無法實現。如果3位C-O鍵斷裂則又生成DMC和OH-,2位或者4位鍵斷裂則生成CH3O-和中間體b甲氧基甲酸;第四步:在堿性環境下b無法穩定存在,與NaOH發生中和反應,生成甲氧基甲酸鈉和H2O;第五步:OH-還可以親核進攻甲氧基甲酸鈉中的羰基碳,使C=O鍵斷裂形成中間體c;第六步:中間體c中2位C-O鍵斷裂形成CH3O-和NaHCO3;第七步:NaHCO3可以繼續與NaOH反應生成Na2CO3和H2O。在第四和七步中生成的H2O會持續參與循環,同CH3ONa反應,直至全部生成催化活性較低的Na2CO3或NaHCO3,導致催化劑失活。失活產物甲氧基甲酸鈉、NaHCO3或Na2CO3定性和定量分析會在今后工作中給出詳細的表征和證明。萬噸級/年EMC合成裝置的精餾塔內壁產生白膜是因為CH3ONa失活生成了Na2CO3,Na2CO3無論在碳酸酯還是在MeOH或EtOH溶劑中溶解度均極低,析出并附著在精餾塔內壁。大量累積的Na2CO3導致精餾過程中EMC純度達不到要求,因此,精餾塔需要每隔一段時間水洗溶解Na2CO3。

表 6 可溶堿類催化劑對酯交換反應的影響
*: this research

圖 1 CH3ONa/NaOH催化酯交換反應失活機理示意圖
KOH和NaOH是最常用的兩種無機強堿催化劑,NaOH堿強度略低,在50 ℃反應時,其催化效率約為KOH的2/3。由于兩種堿的堿強度較高,高溫下酯交換效率基本一致,均在短時間內達到反應平衡[40]。隨著堿強度進一步降低,Na2CO3、NaHCO3和NaF三種堿在50 ℃下對酯交換反應幾乎沒有活性。李琳等[1]以K2CO3為催化劑,nDMC∶nEtOH=1∶1,100 ℃反應7 h,以EtOH計算的EMC收率為55.7%。加入聚乙二醇(PEG)對K2CO3進行改性[16],nDMC∶nEtOH=1∶2,75 ℃時實現EMC收率51.8%。文獻中并沒有明確給出PEG增效原因,K2CO3或Na2CO3在碳酸酯、MeOH和EtOH中溶解度極低是客觀事實,猜測PEG改性能夠提升催化劑與原料的接觸效率,增加K2CO3的分散度[42],進而提升催化效率。
可溶堿類催化劑(包括有機堿和無機堿)對DMC和EtOH的酯醇以及DMC和DEC的酯酯交換反應遵循親核加成-消去反應機理,一般堿強度越高,其親核性越強,催化效率越高。作者試圖以pKb值[43](堿度系數)為標準建立堿強度與催化效率之間的關系。以C4H9ONa、CH3ONa、KOH、NaOH、Na2CO3及NaF為例,其pKb值分別為-5.00、-1.54、-1.10、-0.56、3.60、10.86,pKb值越低其堿強度越強,催化效率越高。使用同種催化劑時,在一定范圍內,催化劑加入量越多,催化活性越高;升高反應溫度及延長反應時間,均有利于促進反應向正方向進行,提升產物EMC收率,直至反應達到熱力學平衡值。
3.1.2 離子液體類催化劑
離子液體具有蒸氣壓低、溶解性強、熱穩定性好、可重復利用等特點[44-46],因此,受到廣泛關注,目前,EMC合成的研究主要集中在烷基咪唑鹽類離子液體[47-53]。表7考察了具有不同陰、陽離子結構的咪唑鹽類離子液體:1,3-二甲基咪唑氯鹽([Mmim]Cl)、1-乙基-3-甲基咪唑氯鹽([Emim]Cl)、1-丁基-3-甲基咪唑氯鹽([Bmim]Cl);1-乙基-3-甲基咪唑溴鹽([Emim]Br)、1-丁基-3-甲基咪唑溴鹽([Bmim]Br)、1-丁基-2-乙基-3-甲基咪唑溴鹽[Bemim]Br、1-丁基-2-丙基-3-甲基咪唑溴鹽([Bpmim]Br);1,3-二甲基咪唑碘鹽([Mmim]I)、1-乙基-3-甲基咪唑碘鹽([Emim]I)、1-丁基-3-甲基咪唑碘鹽([Bmim]I);1-丁基-3-甲基咪唑丁酸鹽([Bmim]CH3(CH2)2COO)和(1-(4-羥基)丁基-3-甲基咪唑苯甲酸鹽([OHBmim]PhCOO)對碳酸酯酯交換反應的影響。

表 7 離子液體類催化劑對酯交換反應的影響
結合本實驗室[47]工作分析發現,當陽離子相同時([Bmim]+),陰離子活性變化順序:I-> Br-> Cl-;陽離子為[Emim]+和[Mmim]+時,陰離子也符合如上規律。原因是鹵素陰離子中I-半徑最大,較容易擺脫咪唑陽離子的束縛,有利于活化EtOH,增加體系中EtO-的含量,從而提高DMC轉化率和EMC選擇性。亓虎等[48]合成了[Bmim]Br離子液體,反應溫度由90 ℃升至140 ℃,DMC轉化率提高9.4%,EMC收率提高13%[49]。說明在一定范圍內升高溫度有利于提高反應物分子之間的有效碰撞,促進反應正向進行,從而提高反應物轉化率及產物收率。李永昕課題組[50,51]合成了[Bemim]Br和[Bpmim]Br兩種離子液體分別催化DMC與DEC以及DEC與MeOH的酯交換反應,在相對較高溫度長時間反應才得到60%EMC收率。[Bmim][CH3(CH2)2COO][52]催化雙酯交換反應,增加DMC含量,DEC轉化率升高,催化劑重復使用五次后仍保持較高的轉化率,合成的[OHBmim]PhCOO[53]離子液體重復使用六次活性沒有變化。
咪唑類離子液體在催化EMC合成過程中受烷基取代基、鹵素和反應溫度等因素影響較為明顯。當陽離子相同時,陰離子活性變化順序為:I-> Br-> Cl-;陰離子相同時,陽離子活性變化順序為:[Mmim]+> [Emim]+> [Bmim]+;酯交換反應制備EMC是一個可逆反應,在一定范圍內,增加一種反應物濃度、升高反應溫度,均有利于反應向產物方向進行,提升EMC收率。
3.1.3 可溶鹽類催化劑
Mei等[18,54]研究了不同種硝酸鹽催化劑用于DMC與EtOH的酯交換反應效果,催化活性順序為:La(NO3)3> Mg(NO3)2> KNO3> Al(NO3)3,DMC轉化率最高可以達到86.5%。文獻[54]認為La3+具有較強的Lewis酸性,能夠活化反應底物,降低反應活化能。以La(NO3)3·6H2O為催化劑時,同La(NO3)3催化反應結果相差不大,說明以La3+(Lewis酸)為活性中心催化酯交換反應時,受水的影響不大。文章[54]還研究了LaCl3以及La(CF3SO3)3催化效果,DMC轉化率分別為48.0%和83.2%,其中,LaCl3催化活性小于La(NO3)3和La(CF3SO3)3,認為這與陰離子同配位中心與La3+間配位作用力大小有關,由于Cl-與La3+之間的配位能力較強,抑制了體系中EtOH、DMC等供電子物質占據配位點,難以活化反應底物,所以催化劑活性相對較差。綜上,對于可溶性Lewis酸催化劑,其接受孤對電子能力越強即其酸性越強,其催化酯交換能力越好,反應體系中的水對催化活性影響不大。
卓廣瀾等[55]以鈦酸鹽Ti(OBu)4或Ti(OPh)4為催化劑,催化DMC和DEC的酯交換反應,當nDMC∶nDEC=1∶1,催化劑含量為反應原料總量的2.5%,103 ℃反應3 h時DEC轉化率分別為43.1%和41.7%。通過GC-MS分析,檢測到-OPh或-OBu官能團與-OCH3或-OC2H5發生交換的副產物,導致EMC選擇性未能達到100%。通過本實驗室經驗分析這可能是鈦酸鹽類均相催化劑的共同缺點,雖然催化效率較高,但鈦酸鹽與原料進行酯交換或鈦酸鹽水解會生成副產物。對于碳酸酯的酯交換反應,今后可嘗試以Ti(OCH3)4或Ti(OC2H5)4為催化劑,既保證催化劑在碳酸酯中較好的溶解性,良好的催化活性,又沒有副產物生成。文獻[55]同時考察了有機錫類化合物Bu2SnO和BuSnCl3的催化性能,DEC轉化率分別為45.6%和43.3%,產物EMC選擇性可以達到100.0%。從實驗數據分析,在催化DMC與DEC的酯交換反應中,有機錫類化合物比鈦酸鹽類催化性能略高。Lewis酸催化酯交換反應在于配位化合物中的金屬存在不飽和空軌道,能夠接納羰基O的孤對電子,從而活化C-O-,發生-OCH3和-OC2H5酯交換反應。
3.2 非均相催化劑
3.2.1 離子交換樹脂類催化劑
Zielinska-Nadolska等[16]研究了離子交換樹脂類催化劑對DMC和EtOH酯交換的影響,反應條件:nDMC∶nEtOH=1∶2,75 ℃反應26.7 h,催化劑占反應原料總質量的6.75%。發現強酸性磺酸樹脂中Lewatit K1221催化活性最高,DMC轉化率54%,EMC收率53%。文獻認為該樹脂聚合結構中二乙烯基苯含量最低,導致樹脂交聯度比較低,在樹脂溶脹過程中有更多孔道形成,促進反應原料及產物擴散,提升催化效率。作者更傾向認為制備工藝和廠家不同,導致樹脂酸含量、酸強度以及孔道結構不同,影響酯交換反應活性。大孔弱酸性樹脂Dowex MAC-3,其酸性官能團為聚丙烯酸和羧酸,該樹脂無催化活性;超強酸性樹脂Nafion SAC-13為四氟乙烯和全氟-3,6-二氧雜-4-甲基-7-辛烯磺酰氟的共聚物,由于-CF2CF2SO3H的強吸電子能力導致磺酸基團具有超強酸性,其催化活性較高,與Lewatit K1221接近。一般酸性樹脂的活性中心為苯磺酸,苯磺酸還可以直接嫁接到其他材料上。薛冰等[56]采用氧化石墨烯和對氯苯磺酸為原料,以共價鍵的方式將磺酸基嫁接到氧化石墨烯表面,獲得一種強酸性固體催化劑。nDMC∶nEtOH=1∶1,90 ℃反應6 h,催化劑占DMC質量的3.0%,EMC收率為86.7%,催化劑重復使用三次,EMC收率僅下降3.6%。
3.2.2 金屬氧化物類催化劑
楊延釗等[57]以AlCl3·6H2O和氨水為主要原料,采用沉淀法合成了γ-Al2O3催化劑,在600 ℃焙燒4 h后用于DMC和DEC的酯交換反應。nDMC∶nDEC= 3∶1,100 ℃反應3 h,催化劑加入7.0%,EMC收率約63.0%。這類催化劑的優勢是機械強度高,催化活性好。柳娜等[58]采用真空浸漬法制備了Al2O3/SiO2催化劑,當Al2O3負載量12%,催化劑加入量7%,nDMC∶nDEC=1∶1,120 ℃反應8 h時,EMC的收率可以達到63.6%。通過表征手段觀測到隨著Al2O3負載量的增加,催化劑表面活性位數量隨之增加,因此,收率也不斷提高;但當Al2O3負載量超過一定量(12%)時,可能會堵塞催化劑部分孔道,傳質作用減弱,導致產物收率下降。負載量為12%的Al2O3/SiO2催化劑重復使用三次,EMC收率僅降低1.3%,未發現明顯失活,穩定性較好。
Murugan等[19]合成了不同KF負載量的KF/Al2O3催化劑,用于催化DMC和EtOH的酯交換反應。反應條件:nDMC∶nEtOH=1∶4,80 ℃反應4 h,使用無水KF為催化劑時,EMC收率為49.6%,采用10% KF /Al2O3催化劑時,EMC收率為51.4%,但是以20% KX/Al2O3(X為Cl、Br、I中的一種)作催化劑時,均無催化活性。文獻認為可能是KF和Al2O3在反應過程中形成表面活性物質Al-[OH…F]-和K+,Al-[OH…F]-物種作為活性中心有利于活化EtOH產生EtO-,EtO-親核進攻DMC生成EMC,提高了反應效率。此外,分別在300、600以及900 ℃下焙燒20% KF/Al2O3催化劑,發現均形成了氟鋁酸鉀(K3AlF6),焙燒溫度越高,活性組分K+和F-損失越多,催化劑堿強度下降,導致活性降低。
Shen等[25]在氣相和液相體系中研究了自制固體堿催化DMC和DEC的酯交換反應,發現催化活性順序一致:MgO>ZnO>La2O3>CeO2,具有較多強堿性中心的La2O3和較多弱堿性中心的CeO2催化活性均較差,而ZnO和MgO中等堿性位點較多,活性較好,文獻認為中等強度的堿性中心更有利于催化DMC和DEC的酯交換反應。同時MgO的BET比表面積大于ZnO,吸附反應物多,反應相對容易進行,催化活性較高。陳英等[59]將市售MgO、CaO于500 ℃焙燒4 h后用于催化酯交換反應,nDMC∶nDEC=1∶1,90 ℃反應時EMC收率均在1%-5%,升溫至100 ℃時,EMC收率約為35%和5%,繼續升高溫度至103 ℃,EMC收率在44%和41%左右,催化效果差別不大。由此可見,反應溫度對MgO和CaO兩種催化劑活性影響很大。
Zhao等[28]選用不同炭材料作載體,包括杏殼炭(AC)、煤質炭(CC)及介孔CMK-3和NC-2,采用浸漬法制備了負載型MgO催化劑,活性組分MgO負載量為4.0%。反應條件:nDMC∶nDEC=1∶1,103 ℃反應0.5 h,催化劑加入4.8%,MgO/NC-2為催化劑時,EMC收率49.3%,其他三種催化劑的收率均在10%以下,活性順序為:MgO/NC-2>MgO/CC>MgO/AC>MgO/CMK-3。MgO/NC-2催化劑使用后在氬氣氣氛中800 ℃焙燒可以再生,重復使用五次其催化活性基本不變。結合表征分析,NC-2材料表面存在著豐富的羧酸、內酯、酸酐等含氧基團,該含氧基團與Mg物種之間相互作用,促使MgO高度分散,進而提高催化活性和穩定性。Lv等[60]以HZSM-5為載體制備了負載型催化劑,采用催化精餾裝置進行評價,nDMC∶nEtOH=2.56∶1,90 ℃反應7 h,回流比20∶1,當以HZSM-5、2.3%CaO/HZSM-5和2.3%MgO/HZSM-5為催化劑時(2.3%為MgO相對于HZSM-5的質量百分比),EMC收率分別為46.9%、86.1%和97.5%。結合表征發現,三種催化劑均具有介孔結構,其中,2.3%MgO/HZSM-5催化劑堿量最高,文章認為堿性越強,越有利于活化EtOH形成EtO-,促進酯交換反應的進行。
陳英等[59]采用共沉淀法合成了MgO-Al2O3復合金屬氧化物,沉淀劑為NaOH和Na2CO3,發現該催化劑催化活性優于市售的MgO以及CaO。nDMC∶nDEC=1∶1,103 ℃反應4 h,EMC收率可達45.8%。XRD譜圖發現MgO-Al2O3復合氧化物中存在MgAl2O4物種,猜測該物種與A12O3晶面協同催化,從而提高催化活性。CO2-TPD分析表明,MgO和CaO催化劑均具有較強的堿中心,而MgO-Al2O3堿性較弱,文章認為較弱的堿性位更有利于催化DMC和DEC的酯交換反應。Wang等[61]以異丙醇鋁和硝酸鎂為主要原料,通過蒸發誘導自組裝法合成介孔鎂鋁尖晶石MgAl2O4(MAO)催化劑,采用MAO-x表示(x為Mg/Al物質的量比)。nDMC∶nDEC=1∶1,103 ℃反應0.5 h,催化劑加入5%,以MAO-1、MAO-1.5和MAO-2為催化劑時,EMC收率均接近49.0%(達到平衡轉化率);以MAO-0.5和MAO-3為催化劑時,EMC收率分別為23.0%和18.0%。結合表征分析,MAO催化劑具有酸堿雙功能特性,所有樣品表面均存在弱酸性位,酸強度幾乎相同,但堿強度存在明顯差異。MAO-0.5堿強度最弱,隨著Mg含量增加,催化劑堿強度增強,MAO-2具有中等強度堿性位,而MAO-3僅展現出弱堿性位,催化活性也呈現先上升后下降的趨勢,因此,得出結論:MAO系列催化劑隨著堿強度增強,其催化活性逐步提升。分離MAO-2催化劑,80 ℃干燥5 h后循環利用五次,EMC收率僅降低1.2%,說明催化劑具有良好的重復使用性能。Shi等[29]以硝酸鋁為鋁源,采用檸檬酸輔助溶膠-凝膠法制備無定型的介孔磷酸鋁材料(AlPO),以異丙醇鋁和三乙胺為原料通過常規的溶膠-凝膠法合成微孔磷酸鋁材料(AlPO-5)。nDMC∶nDEC=1∶1,反應溫度93 ℃,5.0%催化劑,活性順序為:AlPO>MgO>Al2O3>AlPO-5>P2O5,AlPO僅反應0.5 h即實現47.7% DEC轉化率(平衡轉化率)。AlPO重復使用三次后,其催化活性下降2%左右。表征發現AlPO材料表面存在較豐富的弱酸和弱堿中心,有利于活化DMC和DEC;而且介孔材料的孔徑較大,促進了反應原料及產物間的傳質,提升了反應速率。Chen等[62]合成了一種酸堿雙功能介孔材料MgO-Al2O3-SBA-15(SBA-15為介孔二氧化硅),簡寫為MA-SBA-15(n),n表示MgO-Al2O3的質量百分比。nDMC∶nDEC=1∶1,104 ℃反應4 h,催化劑加入4%,MA-SBA-15(10)為催化劑時,EMC收率低于30%;隨著鎂鋁物種含量增加,EMC收率不斷提高,其中,MA-SBA-15(30)活性最佳,EMC收率達到46.1%,比SBA-15高20余倍;繼續增加鎂鋁物種含量至40%,此時復合材料的介孔結構被破壞,催化效率有所下降(約44% EMC收率)。通過表征發現未經改性的SBA-15僅有較少量的酸堿活性位,而所有的MA-SBA-15都存在較多量的酸堿活性位。隨著鎂鋁物種含量增加,催化劑酸堿活性位數量也逐漸增多,催化活性加強,但達到一定值(40%)時,會破壞催化劑介孔結構,影響物質間的傳質作用,導致催化活性減弱。適量的酸堿活性位及優良的介孔結構共同作用,有利于提升催化效率。
Wang等[32]通過共沉淀法制備磁性Mg-Fe二元復合氧化物催化劑,采用xMgFe-t表示(x為Mg/Fe物質的量比,t為焙燒溫度)。nDMC∶nDEC=1∶1,100 ℃反應1.5 h,催化劑加入量1%,MgFe-400催化劑能夠實現51%EMC產物收率。XRD和Mossbauer光譜表明,催化劑中Mg與Fe氧化物之間存在協同效應,有助于提高催化劑性能。催化劑在400 ℃焙燒時活性最高,文章認為隨著焙燒溫度升高,催化劑中MgO含量降低,總堿量減少,導致EMC的收率顯著下降。MgFe-400催化劑循環使用10次,催化性能保持不變。
Miao等[63]采用“一鍋法”合成雙金屬Co/Zn-ZIF前驅體(ZIF為沸石咪唑酯骨架),然后在N2氣氛下熱解得到ZnCo/NC(NC是ZIF的分解產物)催化劑。nDMC∶nDEC=1∶1,100 ℃反應7 h,催化劑加入量1.0%。采用ZnO/NC-600(600為催化劑煅燒溫度)作催化劑時,EMC收率為29.5%;以ZnCo/NC-600為催化劑時,EMC收率為51.5%,催化效率接近前者的兩倍,結合CO2-TPD表征結果,文獻認為Zn、Co兩種元素間的相互作用促進了強堿性活性位的產生,更有效地促進了酯交換反應。該催化劑重復使用五次,EMC收率下降11.3%。同時發現600 ℃煅燒的催化劑比550、650、700 ℃煅燒的催化劑擁有更高的活性。根據XRD譜圖分析,當煅燒溫度為600 ℃時,前驅體中的Zn元素變為ZnO晶體,高于或低于600 ℃煅燒均未形成該結構,說明ZnO對于Zn-Co材料的催化活性是必不可少的,煅燒溫度影響催化劑的微觀結構和化學狀態,進而影響催化性能。作者更傾向于認為雙酯交換的催化活性中心為ZnO和表面官能團豐富的炭材料,當焙燒溫度較低時,Co/Zn-ZIF沒有完全分解,并未形成ZnO活性中心,起到催化作用的是炭材料表面官能團;當焙燒溫度適中時,形成了ZnO活性中心,但ZnO在高溫條件下升華,因此,繼續升高溫度時,ZnO升華導致催化劑中ZnO含量較低,催化效果較差。
Mei等[17]以NaOH為沉淀劑,硝酸鹽為前驅體,采用共沉淀法制備了Mg-Al-NO3HT催化劑;然后將Mg-Al-NO3HT在叔丁醇鉀的四氫呋喃溶液中攪拌24 h制備Mg-Al-O-t-BuHT催化劑;通過尿素水解法制備了Mg-Al-CO3HT催化劑;將Mg-Al-CO3HT在500 ℃焙燒5 h后得到Mg-Al HT催化劑。nDMC∶nEtOH=1∶5,80 ℃反應7 h,催化劑加入1%,以Mg-Al-O-t-Bu HT為催化劑時,DMC轉化率可達86.4%,EMC選擇性25.9%,循環使用五次催化效果基本不變,其他催化劑活性順序為:Mg-Al-NO3HT>Mg-Al-CO3HT>Mg-Al HT。Mg-Al-O-t-Bu HT催化DMC與EtOH反應生成的主產物是DEC,其他催化劑主產物為EMC,說明Mg-Al-O-t-Bu HT催化酯交換效率更高。Srivastava等[64]以亞鐵氰化鉀、氯化鋅和叔丁醇以及三嵌段共聚物EO20PO70EO20為原料合成Fe-Zn雙金屬氰化物配合物,nDMC∶nEtOH=1∶10,反應釜中170 ℃反應8 h,催化劑加入5%,DMC轉化率接近98%,EMC選擇性接近38%。相比較而言,Fe-Zn雙金屬氰化物配合物催化酯交換效率不高。綜上,雙金屬復合氧化物催化酯交換反應活性明顯優于單一金屬氧化物,歸功于酸堿協同作用,并隨著堿性的增強,其催化劑效率逐漸提升。
3.2.3 堿性分子篩類催化劑
Palani等[26]以偏硅酸鈉為硅源、硫酸鋁和硫酸鋅為主要原料,通過水熱法合成了一系列MCM-41分子篩催化劑(Si/Al=50,Si/(Al+Zn)=100)。固定床評價,nDMC∶nDEC=1∶1,原料流量1.5 mL/h,混合原料質量空速約為3.0 h-1,反應溫度175 ℃,發現Al-Zn-MCM-41(50)活性最佳,EMC收率85%,反應活性與吡啶紅外測定的催化劑B酸含量一致:Al-Zn-MCM-41(50)> Al-Zn-MCM-41(100)> Al-MCM-41(50)> Al-MCM-41(100)。隨著反應溫度從125升至175 ℃,EMC收率逐漸增加,但溫度達到200 ℃時,EMC收率下降,歸因于碳酸酯在高溫下分解。
3.2.4 MOFs材料類催化劑
Zhou等[27]將六水合硝酸鋅和對苯二甲酸溶解于N,N-二甲基甲酰胺中,再加入有機堿三乙胺形成沉淀,洗滌干燥后制得金屬有機骨架MOF-5催化劑(Zn4(O)(BDC)3,BCD為苯-1,4-二羧酸酯)。nDMC∶nDEC=1∶1,100 ℃反應3 h,催化劑加入2%:合成原料六水合硝酸鋅基本無催化效果,MOF-5催化劑展現出50.1%EMC收率。通過表征發現,MOF-5催化劑在90或300 ℃下干燥相同時間,催化劑結構及表面官能團保持不變,說明MOF-5熱穩定性較好。重復使用三次后,EMC收率僅降低1.7%。Zhou等[30]以2-甲基咪唑、氨水和Zn(OH)2為主要原料合成沸石咪唑骨架ZIF-8([Zn(MeIm)2],MeIm為2-甲基咪唑)。nDMC∶nDEC=1∶1,100 ℃反應3 h,催化劑加入1%:以制備原料Zn(OH)2、2-甲基咪唑或兩者的混合物為催化劑時,幾乎沒有催化活性;MgO催化劑活性一般,EMC收率為30.5%;ZIF-8展現出最優的催化效果,EMC收率為50.7%;同為金屬有機骨架結構的MOF-5催化劑活性偏低,EMC收率為42.0%,而且MOF-5在潮濕的空氣中易分解,不能穩定存在[65]。BET、CO2-TPD和NH3-TPD表征證明,ZIF-8具有高比表面積及酸堿雙功能特性。Yang等[66]采用2-甲基咪唑、甲醇和[Zn(NO3)2]·6H2O為原料制備ZIF-8催化劑,并添加了MS 4A分子篩作為助催化劑。nDMC∶nDEC=1∶1,100 ℃反應12 h,僅以ZIF-8或MS 4A為催化劑時,EMC收率分別為50.32%、34.89%,向ZIF-8中加入助催化劑時,催化活性明顯提高,EMC收率達到84.72%。Yang等[31]以2-甲基咪唑和六水合硝酸鈷為主要原料合成沸石咪唑骨架ZIF-67(Co(MeIm)2)。nDMC∶nDEC=1∶1,100 ℃反應24 h,催化劑加入2%:采用ZIF-8催化劑時,EMC收率為50.32%;ZIF-67催化活性較高,EMC收率高達83.39%。將ZIF-67重復利用三次后,EMC收率減少2%左右,穩定性較好。結合表征發現ZIF-67酸堿性適中,同時ZIF-67的比表面積大于ZIF-8,文獻認為中等強度酸堿性和高比表面積更有利于催化雙酯交換反應。Desidery等[24]以均苯三甲酸和ZrOCl2·8H2O為原料制備MOF-808(Zr6O4(OH)4(BTC)2(HCOO)6)酸堿雙功能催化劑。nDMC∶nEtOH=1∶3,90 ℃反應24 h,催化劑加入1%,比較了多種MOF材料催化雙酯交換的結果,發現Cr-MIL 101和Fe-MIL 100完全沒有活性,其他MOF材料活性順序為:MOF-808>UiO66-NH2>>UiO66-SO3H>ZIF-67>ZIF-8>UiO66,由于MOF-808比表面積、孔體積和孔徑較大,能夠有效促進產物擴散;大量酸堿性位點的協同催化作用提升了酯交換效率。MOF-808在75 ℃反應24 h也能夠達到49.6% EMC收率,循環使用三次后,產物收率僅下降0.8%。
4 反應機理
據作者所知,目前文獻報道的DMC與EtOH[19,24]或DMC和DEC[25-27,29,31,32,55]酯交換反應機理是根據有機化學基礎理論推導得來,而不是由光譜等表征手段真實觀測證明,推斷的酯交換反應機理如圖2-5所示。圖2為親核試劑烷氧基負離子(CH3O-或C2H5O-)與碳酸酯(DEC或DMC)交換后生成EMC的過程。烷氧基負離子首先進攻DMC或DEC中的羰基,使C=O鍵斷裂形成中間體a或b,a和b結構相近,穩定性均較差,與C相連的四個C-O至少需要斷裂一條,這是典型的親核加成-消去反應過程。頂端C-O-鍵斷裂困難,除非C+和O-能夠分別以自由基的形式穩定存在,這顯然是無法實現的。其他位置C-O鍵斷裂可生成EMC和CH3O-或C2H5O-。
可見,烷氧基負離子地生成在碳酸酯交換過程中十分重要。幾種典型催化劑:醇鈉或醇鉀有機堿、能夠電離出OH-的可溶堿、離子液體和金屬氧化物活化甲醇、乙醇、或碳酸酯過程如圖3-5所示。醇鈉或鉀(以CH3ONa或CH3OK為例)在有機溶劑中很容易電離出CH3O-,CH3O-可以進攻并奪取C2H5OH中的H生成CH3OH和C2H5O-;同樣C2H5O-可以奪取CH3OH中的H生成C2H5OH和CH3O-。該反應是一個可逆反應,但理論上由于甲基的供電子效應使得C2H5O-電負性比CH3O-強,C2H5O-進攻CH3OH更容易進行。OH-通過氫鍵與CH3OH分子中的羥基H相互作用,可以活化CH3OH分子,生成CH3O-,另一種產物為H2O,該反應也為可逆反應,逆向進行平衡常數更大,也就是說CH3O-更容易與H2O反應,生成OH-和CH3OH。如果希望提高反應體系中CH3O-的濃度,可以將H2O分離出反應體系,推動反應正向進行。OH-也可以進攻DMC或DEC中的羰基,發生親核反應,生成帶負電的中間體,該中間體解離出CH3O-并生成甲氧基甲酸,甲氧基甲酸在堿催化體系下不能穩定存在,會迅速與OH-作用生成甲氧基甲酸鹽與H2O。

圖 2 烷氧基負離子活化碳酸酯機理

圖 3 無機可溶強堿活化碳酸酯機理

圖 4 咪唑類離子液體活化甲醇生成烷氧基負離子過程
以1,3-二甲基咪唑碘鹽為代表描述咪唑類離子液體活化醇類化合物(以MeOH為例),生成烷氧基負離子過程如圖4所示,鹵素負離子I-與CH3OH分子接觸并通過誘導作用形成氫鍵,I-奪走H使羥基中的氫氧鍵斷裂并形成CH3O-。理論上I-也可能直接親核進攻DMC中的羰基,使C=O鍵斷裂,解離出CH3O-并生成碳酸碘甲酯,但GC-MS聯用并未檢測到該產物地生成。
根據文獻[25,27,29],金屬氧化物中的O通過共價鍵與不同金屬相連,同時存在未配對的孤對電子,其活化醇類化合物(以MeOH為例),生成烷氧基負離子過程見圖5。O孤對電子顯電負性,會吸電子誘導CH3OH中的H,形成類CH3O-結構。O孤對電子也可以親核進攻DMC中的羰基,使C=O鍵斷裂,形成DMC在金屬氧化物表面吸附的物種以及解離出類CH3O-結構。金屬氧化物催化碳酸酯交換機理還需要原位表征手段證明。

圖 5 金屬氧化物活化甲醇生成烷氧基負離子過程
5 反應工藝
以DMC和EtOH為反應原料通過酯醇交換法合成EMC的反應體系中主要包含五種物質:MeOH、EtOH、DMC、EMC和DEC,存在MeOH-DMC(63.7 ℃,86.6% MeOH)、EtOH-DMC(74.9 ℃,69% EtOH)以及EtOH-EMC(78.9 ℃,95% EtOH)[15]三組共沸物。由于酯醇或酯酯間交換均為可逆反應,為了使反應正向進行得更徹底,生成更多的EMC,需打破反應平衡,盡快將產物MeOH移除反應體系。催化精餾技術借助精餾分離與酯交換反應的耦合來強化反應正向進行,從而實現EMC的連續化生產。
閆志軍等[67]將混有C2H5ONa催化劑的EtOH原料從反應精餾塔中部泵入,DMC從塔釜進料,VDMC∶VEtOH= 2∶1,反應溫度90-110 ℃,塔頂收集MeOH、EtOH和DMC進入輕組分精餾塔,塔釜DMC、EMC和DEC進入重組份精餾塔。輕組分精餾塔操作條件:回流比2-4,塔釜76-78 ℃,塔頂63.7-64.7 ℃,塔頂收集到MeOH和DMC(≥98%)共沸物,再進一步分離DMC,塔釜EtOH(≥95%)重新回到反應精餾塔;重組分精餾分離按三步進行:首先控制塔頂溫度低于91 ℃蒸出DMC,然后升至91-106 ℃,收集含有少量DMC的EMC混合物,重新回到重組分精餾塔釜再次循環精餾,最后升至106-110 ℃,從塔頂蒸出EMC產品,塔釜收集DEC,最終EMC總收率為35%。梁志廣等[68]設計并優化了生產EMC的工藝流程,如圖6 所示。同樣以均相C2H5ONa為催化劑,反應物DMC、EtOH分別由C1反應精餾塔中部或下部進料,塔釜混合液經過固液分離后得到粗產品,再由精餾塔C2分離,頂部收集的DMC循環利用,塔釜為EMC和DEC的混合液,再經過下一個精餾塔C3分離收集純產品EMC和DEC;C1塔頂為MeOH-DMC共沸物,經C4萃取精餾塔(鄰二甲苯作萃取劑)脫除MeOH,再經精餾塔C5實現DMC和萃取劑的分離。文中利用化工模擬軟件Aspen Plus優化了精餾塔操作參數,總進料流量105 kmol/h,EtOH進料流量40 kmol/h,回流比約1.4,萃取劑85 ℃循環利用,實現聯產EMC和DEC,且兩種產品純度均達到99.8%。

圖 6 EMC生產工藝流程圖[68]
Keller等[21]采用中試規模(高度5.4 m,直徑50 mm)的精餾塔對DMC與EtOH的酯交換反應進行研究,反應精餾柱示意圖及精餾柱裝填如圖7和圖8所示。以C2H5ONa為催化劑,原料分別于填料高度2.0 m處進料,進料溫度60 ℃,通過分子篩吸水減少原料中的含水量,以免C2H5ONa催化劑遇水失活。改變操作參數:EtOH與DMC物質的量比由0.9變為2.6,催化劑由0.1%增至0.2%,回流比從1.2改為2.0,餾出物與進料量質量比由0.27升至0.48,實現由EMC為主產物(79.2%選擇性)轉變成DEC為主產物(80.2%選擇性),證明了反應精餾塔可以作為多功能的反應器完成多種產物選擇性調控。Werth等[22]研究了微波輔助對反應精餾的影響,模擬精餾塔總填料高度為5.4 m,其中,2 m作為反應部分,以C2H5ONa為催化劑,nDMC∶nEtOH=1∶1,回流比1.2,餾分與進料比0.35。常規實驗在加熱套或油浴中進行,微波實驗以微波合成儀作為加熱源/再沸器,發現微波輔助對反應結果影響較小,沒有觀察到分離效率明顯提高。
Luo等[15]為了使反應原料在精餾塔中停留更長時間,將DMC和EtOH原料由塔釜加入,催化劑K2CO3和助催化劑從塔頂加入,nDMC∶nEtOH=1∶6,回流比6,DMC的進料速率為5.5 mol/h,再沸器溫度132.3 ℃,維持精餾塔內部溫度80 ℃左右,塔頂溫度75.5 ℃,能夠實現DMC幾乎完全轉化,DEC選擇性大于99.5%。王紅衛等[69]采用間歇精餾裝置考察精餾塔操作條件(回流比、塔板數等)對混合物分離效果的影響。原料(0.2% MeOH、0.5% EtOH、9.3% DMC、56% EMC、34% DEC)加入塔釜,然后采取全回流操作,當塔頂、塔釜溫度穩定后,再按回流比采出,當理論塔板數50,回流比17.5,投料量與上升蒸氣量之比為5 kg/(kg·h-1)時,EMC產品純度最高能夠達到99.5 %。

圖 7 Keller使用的中試規模反應精餾柱[21] Figure 7 Scheme of the pilot-scale RD column used by Keller[21]
孫蘭義等[70]發明了共沸反應精餾法生產EMC,將DMC、EtOH及CH3ONa催化劑分別加入共沸反應精餾塔,再加入共沸劑正己烷,得到第一混合物(DMC、EMC及DEC)和第二混合物(MeOH和正己烷),第一混合物依次經隔壁塔,分離得到三種碳酸酯產品。第二混合物進入分液罐中,向其中加入水分離出正己烷,并得到第三混合物(MeOH+H2O),再經過提純塔分離得到純物質。共沸劑能夠抑制MeOH-DMC形成,方便分離,簡化工藝流程,降低反應能耗。賈風雷等[71]改進了反應塔的內部結構,采用多級絲網填料體和多級塔盤式填料體,且兩者間隔安裝排列,實現連續進料產出產品,避免堵塞,解決了絲網填料堵塞降低反應效率的問題,提高裝置處理量。對于MeOH-DMC共沸物,目前工業上主要采用萃取精餾法和變壓精餾分離法。萃取精餾法是加入一種揮發性小、不與原組分形成新共沸物的萃取劑,以此提高原組分間的相對揮發度,實現共沸物分離[72]。該體系中使用最多的萃取劑有鄰二甲苯[73]、乙二醇、糠醛、水、氯苯及N,N-二甲基甲酰胺[74]等。畢利君等[75]和姚林祥等[76]分別采用常壓(0.1 MPa)-加壓(1.3 MPa)-常壓(0.1 MPa)精餾塔和常壓(0.1 MPa)-加壓(1 MPa)精餾塔分離共沸物,通過模擬軟件優化了塔板數、進料位置和回流比,均實現DMC和MeOH質量分數達到99.9%以上。

圖 8 流體分離實驗室中試精餾柱(a); 填充Sulzer BXTM填料的玻璃段柱(b); PT-100熱電偶液體分布器(c); 第一隔離層和加熱絲(d); 分子篩(e) [21]Figure 8 Pilot-scale RD column at the laboratory of fluid separations(a); glass segments filled with Sulzer BXTM packing elements(b); liquid distributor with PT-100 thermocouple(c); first isolation layer and heating wire(d); molecular sieves(e)[21]
石磊等[77]發明一種均相耦合非均相催化EMC的生產工藝,圖9為流程示意圖。原料DMC和EtOH經計量泵P-1泵入K-1預反應釜,加入均相催化劑CH3ONa反應5-10 min即達到熱力學平衡值,其中,DMC轉化率接近70%,EtOH轉化率接近60%,產物中EMC選擇性約為80%,DEC選擇性為20%。第一混合物進入T-1第一反應精餾塔,回流比2∶1,塔頂溫度63.6 ℃采出共沸物(DMC和MeOH),質量比接近3∶7,然后通過高、低壓或萃取-精餾分離得到DMC和MeOH。塔釜反應混合物(0.02%MeOH、0.2%EtOH、12%DMC、64%EMC及24%DEC)閃蒸蒸去MeOH及EtOH得到第二混合物,經E-1冷凝器冷凝,F-1過濾器除去不溶的催化劑,然后通入酸性CO2氣體,再次過濾后得到的第三混合物(DMC、EMC和DEC)進入T-2第二精餾塔,緩慢升溫,當塔頂溫度94 ℃時,采出DMC組分,125 ℃時采出EMC組分,其中,純度合格的作為產品。不合格的EMC、塔頂采出的DMC以及塔釜DEC作為原料,同時額外加入DMC配成物質的量比為1∶1的混合原料。混合原料經過預熱器加熱到一定溫度后進入裝有自制固體堿催化劑的B-1固定床反應器,反應溫度75-120 ℃,原料質量空速0.2-20 h-1,反應后的產物組成大致為20%DMC,55%EMC以及25%DEC,重新循環至第二精餾塔塔釜分離。

圖 9 均相耦合非均相催化高純EMC合成工藝流程示意圖[79]
6 結 論
本研究介紹了酯交換法合成EMC的反應熱力學、動力學、均相和非均相催化劑、反應機理及反應工藝方面的研究進展。DMC和DEC酯交換是熱力學上可自發進行的吸熱反應。DMC和EtOH酯交換反應的熱效應和自發性都較弱,符合二級動力學方程,反應速率與反應物濃度的平方成正比,可溶強堿催化時,生成EMC的活化能和指前因子較生成DEC的小;而可溶弱堿催化時,活化能和指前因子與強堿催化時相反。均相催化劑整體活性高,反應速率快,但易失活、可回收性差。文中以pKb值為標準,總結出可溶堿類催化劑的pKb值越低其堿強度越強,催化效率越高,針對工業采用的CH3ONa催化劑,描述了失活現象并提出失活機理。非均相催化劑重復使用性好,不存在后續分離問題,但是活性偏低、反應速率慢,金屬氧化物類是現在研究最多的催化劑,其活性主要受催化劑酸堿性強弱及表面活性位數量的影響。堿催化酯交換是典型的親核加成-消去反應,關鍵是烷氧基負離子的生成。催化精餾工藝中以CH3ONa/C2H5ONa為催化劑,塔頂采出DMC和MeOH共沸物,塔底三種酯類混合物經精餾分離得到目標產品,但均相催化劑易溶于產物,有少量殘留就會造成EMC純度下降;而非均相催化劑效率低、反應溫度高,目前,相關工藝的研究報道極少。
盡管全球的固態鋰電池研發和投資熱鬧非凡,但整體來看,固態鋰電池尚處于研發階段,固態鋰電池存在界面阻抗大、快充難度大、成本高等一系列問題。在未來很長一段時間內(10-15年)使用液態電解液的鋰電池仍處于市場主導地位。EMC具有鋰離子溶解度高、穩定性好、凝固點低等一系列優點,作為鋰電池電解液溶劑的主體地位不可替代。在未來鋰電池級EMC的研究中,不僅要從提升產品純度和降低生產成本的角度出發,而且要考慮減少能耗及綠色環保等問題,高效固體堿催化劑和涉及氣、液、固三相的催化精餾技術是今后開發的重點和發展方向。

