阿帕替尼聯合S-TACE 治療中晚期原發性肝癌的療效及安全性評價△
翁志成,彭建揚,吳偉達,張春生,林群,潘喜鵬
福建莆田學院附屬醫院介入科,福建 莆田 351100
近年來,原發性肝癌的發病率及病死率均呈逐年上升趨勢,原發性肝癌的病死率較高,已高居腫瘤死因的第二位。作為肝病高發國家,中國每年的肝癌新發病例數和死亡病例數均占全球50%以上,并且呈年輕化趨勢[1]。中晚期原發性肝癌患者多已失去手術切除的機會,局部療法是目前臨床治療中晚期原發性肝癌的主要手段,其中以超選擇性肝動脈化療栓塞術(super-selection transcatheter arterial chemoembolization,S-TACE)最為多見[2]。S-TACE不僅安全性高,而且創傷小,但S-TACE術后會形成缺氧環境,促使腫瘤細胞因子、腫瘤刺激因子、血管內皮生長因子表達異常增加,導致內皮細胞增殖、血管新生,可使代償性側支循環出現,導致病灶組織轉移風險、復發概率增加,不利于患者術后病情轉歸,因此如果在栓塞治療的同時加用抗血管生成藥物治療,可以為患者帶來良好的治療效果[3]。阿帕替尼為小分子類型的抗血管生成靶向藥物,具有抗癌范圍廣的特征。因此,本研究分析了阿帕替尼聯合S-TACE治療中晚期原發性肝癌患者的療效、安全性及對血清基質金屬蛋白酶(matrix metalloproteinase,MMP)表達水平的影響,現報道如下。
1 對象與方法
1.1 研究對象
選取2015年12月至2017年2月福建莆田學院附屬醫院收治的70例中晚期原發性肝癌患者。納入標準:①處于疾病中晚期,經檢查后確診;②預計生存期>3個月;③入組前未曾接受過介入治療、放射治療或化學治療等抗腫瘤治療;④意識及精神狀態均正常。排除標準:①存在化療禁忌或S-TACE禁忌;②合并凝血功能障礙;③存在活動性出血問題;④合并其他類型腫瘤;⑤過敏體質。根據隨機數字表法將患者隨機分為觀察組和對照組,每組35例。對照組中,男25例,女10例;年齡36~75歲,平均(52.26±3.19)歲;腫瘤直徑4.0~7.9 cm,平均(5.63±0.50)cm;巴塞羅那分期:B期23例,C期12例。觀察組中,男26例,女9例;年齡35~74歲,平均(51.77±2.90)歲;腫瘤直徑4.0~8.1 cm,平均(5.70±0.49)cm;巴塞羅那分期:B期24例,C期11例。兩組患者的性別、年齡、腫瘤直徑、巴塞羅那分期比較,差異均無統計學意義(P>0.05),具有可比性。本研究經醫院醫學倫理委員會審核批準,患者及其家屬均對本研究知情并簽署知情同意書。
1.2 治療方法
對照組給予S-TACE治療,具體方法:①建立靜脈通路,患者取仰臥位,定位右股動脈后,以改良Seldinger法予以穿刺。②將動脈鞘、導管妥善置入,予以肝動脈造影、側支供血動脈造影,通過造影觀察病灶組織位置、數量、血管特征以及病灶組織大小等信息。③于微導絲的引導下,將2.3 F型微導管超選擇性置入患者病灶動脈中,將適量碘化油乳劑緩慢注入,碘化油乳劑包含碘化油、奧沙利鉑、5-氟尿嘧啶及吡柔比星,再結合造影結果選擇適合患者的栓塞劑。④以明膠海綿顆粒進行栓塞,對門靜脈的小分支進行觀察,達到局部顯影狀態時,表明栓塞已結束,于結束前給予再次造影,重點觀察腫瘤組織中是否存在血供,確定無血供后,可結束栓塞。⑤給予穿刺點常規包扎,以防持續出血。
觀察組患者在對照組S-TACE治療的基礎上聯合阿帕替尼治療,阿帕替尼治療方法:①于術后1天起服用500 mg阿帕替尼,每天1次,餐后30 min用藥,觀察周期為1個周期,28天為1個周期。②用藥期間,若患者出現手足綜合征、白細胞計數降低、蛋白尿、粒細胞降低、高血壓或血小板降低等不良反應,需暫停用藥,待患者不適癥狀消失、緩解后,再以原劑量繼續用藥,暫停用藥時間通常在14天內,如果停藥14天后不適癥狀仍然存在,需將阿帕替尼口服劑量調整至250 mg,每天1次,若不適癥狀始終未能消失,酌情停藥。
1.3 觀察指標及評價標準
采用修正的實體瘤療效評價標準(modified response evaluation criteria in solid tumor,mRECIST)[4]對兩組患者治療1個周期后的臨床療效進行評價:完全緩解(CR),經影像學專業檢查,結果顯示動脈期未出現靶病灶強化征;部分緩解(PR),經影像學專業檢查,結果顯示動脈期的靶病灶組織無強化,病灶直徑之和已縮小30%及以上;疾病穩定(SD),經影像學專業檢查,結果顯示病灶直徑之和的縮小程度不足30%;疾病進展(PD),經影像學專業檢查,結果顯示出現新病灶組織。臨床獲益率=(CR+PR+SD)例數/總例數×100%。
不良反應:治療后,記錄兩組患者皮疹、高血壓、手足綜合征、瘙癢、蛋白尿、發熱、乏力、腹痛、腹瀉及惡心嘔吐的發生情況。
血清學指標:抽取兩組患者治療前及療程結束后次日的空腹靜脈血4 ml,常規離心后提取上清液;采用酶聯免疫吸附法對MMP-2、MMP-9、MMP-11、血管內皮細胞生長因子受體2(vascular endothelial growth factor receptor 2,VEGFR2)的表達水平進行檢測。
1.4 統計學分析
采用SPSS 18.0軟件對數據進行分析;計數資料以例數和率(%)表示,組間比較采用χ2檢驗;符合正態分布的計量資料以均數±標準差(±s)表示,組間比較采用t檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 臨床療效的比較
觀察組患者治療后的臨床獲益率為65.71%(23/35),明顯高于對照組的34.29%(12/35),差異有統計學意義(χ2=6.914,P<0.01)。(表1)
2.2 不良反應發生率的比較
治療后,觀察組患者皮疹、高血壓、手足綜合征、蛋白尿的發生率均高于對照組,差異均有統計學意義(P<0.05);兩組患者瘙癢、發熱、乏力、腹痛、腹瀉、惡心嘔吐的發生率比較,差異均無統計學意義(P>0.05);兩組患者的上述不良反應均在給予對癥處理后得到緩解。(表2)
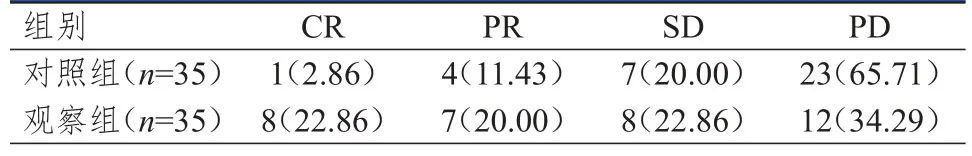
表1 兩組患者的臨床療效[n(%)]*
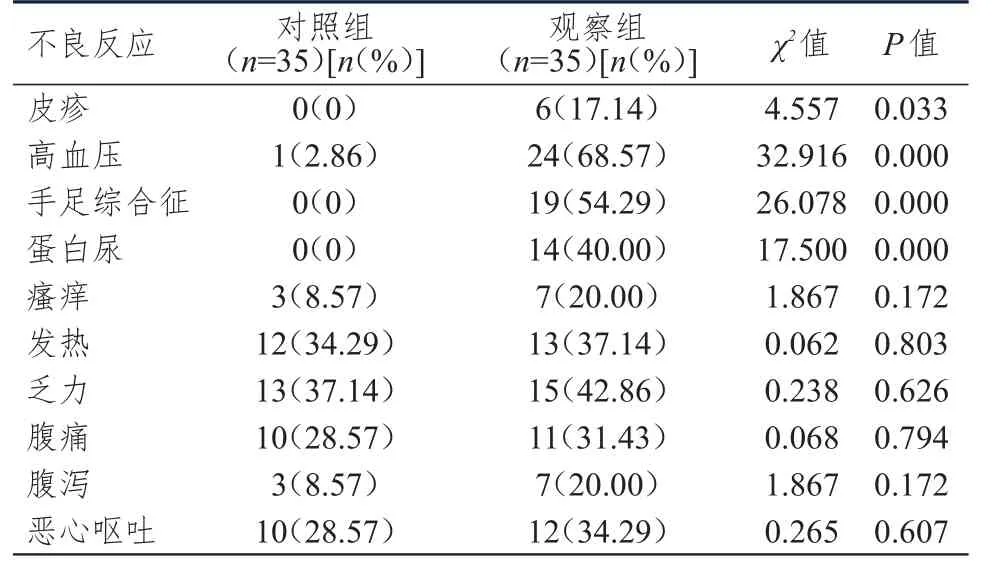
表2 兩組患者不良反應發生情況的比較
2.3 血清學指標的比較
治療前,兩組患者的血清MMP-2、MMP-9、MMP-11、VEGFR2表達水平比較,差異均無統計學意義(P>0.05);治療后,兩組患者的血清MMP-2、MMP-9、MMP-11、VEGFR2表達水平均較本組治療前降低,且觀察組患者的血清MMP-2、MMP-9、MMP-11、VEGFR2表達水平均低于對照組,差異均有統計學意義(P<0.05)。(表3)
表3 兩組患者治療前后血清MMP、VEGFR2表達水平的比較(±s)
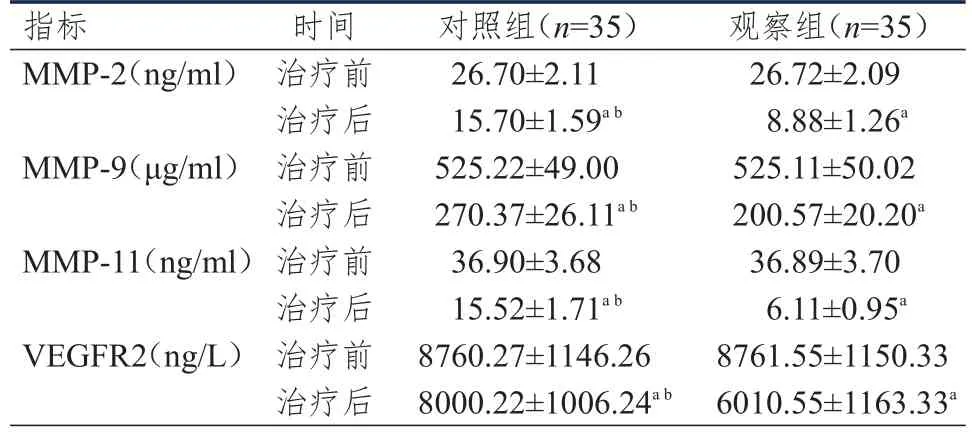
表3 兩組患者治療前后血清MMP、VEGFR2表達水平的比較(±s)
注:a與本組治療前比較,P<0.05;b與觀察組治療后比較,P<0.05
指標MMP-2(ng/ml)MMP-9(μg/ml)MMP-11(ng/ml)VEGFR2(ng/L)時間治療前治療后治療前治療后治療前治療后治療前治療后對照組(n=35)26.70±2.11 15.70±1.59a b 525.22±49.00 270.37±26.11a b 36.90±3.68 15.52±1.71a b 8760.27±1146.26 8000.22±1006.24a b觀察組(n=35)26.72±2.09 8.88±1.26a 525.11±50.02 200.57±20.20a 36.89±3.70 6.11±0.95a 8761.55±1150.33 6010.55±1163.33a
3 討論
原發性肝癌具有治療難度大、轉歸難度大等特征,其發病機制、發病原因等均未能確定,且疾病確診時,多已處于中晚期階段,加大了治療難度[5]。S-TACE屬于微創治療療法,術后患者病灶組織微環境會長時間處于缺氧、缺血狀態,受MMP因子、血管內皮生長因子影響,腫瘤組織新生血管出現風險升高,致使病灶組織出現進展問題和復發現象[6-7]。阿帕替尼屬于酪氨酸激酶抑制劑,已在多種惡性腫瘤專業治療中得到應用。
薄雪萍等[8]以S-TACE聯合熱療的形式治療原發性肝癌,結果發現患者的卡氏功能狀態評分升高,不良反應減少。宋錦添等[9]采用阿帕替尼治療晚期原發性肝癌患者,結果發現患者的客觀緩解率為18.86%,疾病控制率為56.6%,盡管有不良反應出現,但患者多能耐受。本研究結果顯示,觀察組患者的臨床獲益率為65.71%,高于對照組患者的34.29%(P<0.05),提示與單純S-TACE治療相比,聯合阿帕替尼可進一步提升患者臨床獲益率。針對阿帕替尼的安全性,本研究結果顯示,觀察組患者皮疹、高血壓、手足綜合征、蛋白尿的發生率均高于對照組(P<0.05),但對癥處理后所有不良反應均緩解,提示阿帕替尼聯合S-TACE治療中晚期原發性肝癌可能會出現不良反應,但是患者的耐受性強。本研究結果還發現,治療后,觀察組患者血清MMP-2、MMP-9、MMP-11、VEGFR2的表達水平均低于對照組,提示阿帕替尼聯合STACE治療可降低患者血清MMP、VEGFR2的表達水平。
阿帕替尼為當前中晚期胃癌患者接受標準化療且失敗后進行治療的靶向藥物,為口服制劑類藥物;相關研究表明,阿帕替尼對于中晚期胃癌患者生存質量起著改善作用,還能延長患者的生存時間,通過對VEGFR2的活性產生高度抑制作用,防止與血管內皮細胞生長因子受體大量結合,以控制新生血管出現[10-11]。S-TACE法通過對栓塞劑以及化療藥物進行混合形成乳劑形式,以S-TACE為途徑注入中晚期原發性肝癌患者病灶組織供血動脈中,使病灶組織供血受阻,形成缺氧、缺血狀態,從而有效殺滅病灶組織,防止其持續生長。張雄杰和丁佑銘[12]研究發現,MMP參與了原發性肝癌患者腫瘤細胞的侵襲、轉移過程,且血清MMP表達與患者病灶組織的惡性程度呈正相關。而阿帕替尼聯合S-TACE治療中晚期原發性肝癌時,通過發揮協同作用對術后缺氧、缺血環境產生改善作用,在防止血管新生的基礎上,促使患者療效提升,從而提高其臨床獲益率[13-14]。不僅如此,盡管阿帕替尼會對患者腎小球的通透性、血管的舒張能力產生影響,致使皮疹、高血壓、手足綜合征以及蛋白尿等不良反應出現,但上述癥狀較輕,且對其進行對癥處理后,相關癥狀消失,表明阿帕替尼聯合S-TACE治療的安全性有保障[15]。同時,阿帕替尼聯合S-TACE治療可對病灶組織產生抑制作用,通過對胃癌細胞中血管內皮生長因子自分泌進行充分抑制,防止肺癌移植瘤持續生長,從而降低血清MMP表達。此外,阿帕替尼聯合S-TACE治療可對VEGFR2的ATP結合位點產生高度競爭性的抑制作用,并對c-SRC、c-KIT及Ret信號轉導產生阻斷作用,在防止腫瘤血管持續生成的基礎上,降低VEGFR2水平。
綜上所述,阿帕替尼聯合S-TACE治療中晚期原發性肝癌有助于提高臨床獲益率,降低血清MMP及VEGFR2的表達水平,且安全性有保障。但本研究缺乏大樣本數據,且隨訪時間短,因此尚需進一步擴大樣本量并延長隨訪時間,以探討阿帕替尼聯合S-TACE治療中晚期原發性肝癌的臨床價值。

