法匹拉韋治療新型冠狀病毒肺炎的可行性分析*
張競文,胡 欣,金鵬飛△
(1. 北京大學藥學院藥事管理與臨床藥學系,北京 100191; 2. 北京醫院藥學部·國家老年醫學中心·中國醫學科學院老年醫學研究所·藥物臨床風險與個體化應用評價北京市重點實驗室,北京 100730)
2019 年12 月,由新型冠狀病毒(SARS-CoV-2)感染導致的新型冠狀病毒肺炎(COVID-19)在我國武漢暴發,隨著疫情的蔓延,目前已傳播至全球超過70 個國家,且仍在不斷增長。我國乃至世界各地的研究團隊都在致力于研究針對COVID-19 的有效治療方案。2020 年2 月15 日,以成人流感為主要適應證的法匹拉韋(favipiravir)正式獲得國家藥品監督管理局的有條件批準上市[1]。作為首個在這次疫情期間批準上市的抗病毒藥物,法匹拉韋引起了各界的高度關注,關于其治療COVID-19 的臨床試驗也迅速在全國多家中心啟動[1]。本研究中對法匹拉韋的作用機制及臨床應用進行系統評價,并對其治療COVID-19 的可行性進行分析,為臨床的藥物治療提供參考。
1 法匹拉韋研發進程及作用機制
1.1 研發進程
法匹拉韋是核苷類廣譜抗病毒藥物,最早由日本富山化工制藥公司開發,2009 年被日本富士膠卷控股公司收購,2014 年3 月在日本批準上市,用于治療新型和復發型流感[2]。研究表明,除流感病毒外,法匹拉韋對其他多種RNA 病毒如埃博拉病毒、布尼亞病毒等均有抑制作用[3]。2014 年,在抗擊埃博拉病毒疫情中,發現法匹拉韋在降低埃博拉病毒早期感染者死亡率方面有積極作用[4]。2020 年2 月15 日,法匹拉韋片在我國上市,獲批適應證為治療成人新型或再次流行流感,僅限于其他抗流感病毒藥物治療無效或效果不佳時使用。法匹拉韋還獲得《藥物臨床試驗批件》,開展以COVID-19 為適應證的臨床試驗,并允許臨床在現階段小范圍內給藥治療COVID-19[1]。
1.2 抗病毒作用機理
法匹拉韋的化學式為C5H4FN3O2,相對分子質量為157.10,化學名為6-氟-3-羥基吡嗪-2-甲酰胺[5]。科學家首先發現的是與法匹拉韋結構類似的2 種吡嗪甲酰胺類似物—— T1105 和T1106,它們都具有抗病毒活性,但其極性較大,不易溶于水,成藥性差[6],經過結構改造,制備成了成藥性更好的法匹拉韋。法匹拉韋及其衍生物的化學結構[7]見圖1。研究顯示,在病毒復制的各個階段,用法匹拉韋治療流感病毒感染的細胞均可明顯降低病毒滴度,但在病毒顆粒釋放階段卻無法發揮藥物作用[8-9]。可見,法匹拉韋是在病毒感染細胞的增殖階段通過阻斷病毒的復制中間體而發揮作用。進一步研究發現,法匹拉韋在病毒復制中“扮演”了嘌呤堿基的角色[10],并分離鑒定出了具有生物活性的法匹拉韋核苷三磷酸化物—— 法匹拉韋RTP(favipiravir- ribofuranosyl-5′-triphosphate,favipiravir-RTP)。檢測病毒滴度后,可以確定除法匹拉韋RTP 外,其他形式的法匹拉韋均不能抑制流感病毒RNA 聚合酶的活性[11]。故確定法匹拉韋是一種前藥,本身沒有抗病毒活性,在體內可被宿主細胞酶磷酸核糖基化生成具有生物活性的法匹拉韋RTP(見圖2),被當作嘌呤摻入早期病毒RNA 中,或競爭性抑制病毒RNA 依賴的RNA 聚合酶[12],阻斷RNA 的復制和轉錄,從而對病毒產生抑制作用。
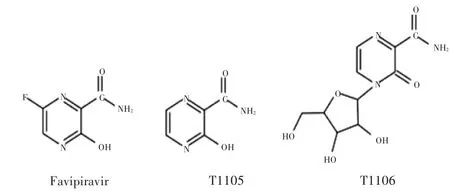
圖1 法匹拉韋及其衍生物的化學結構
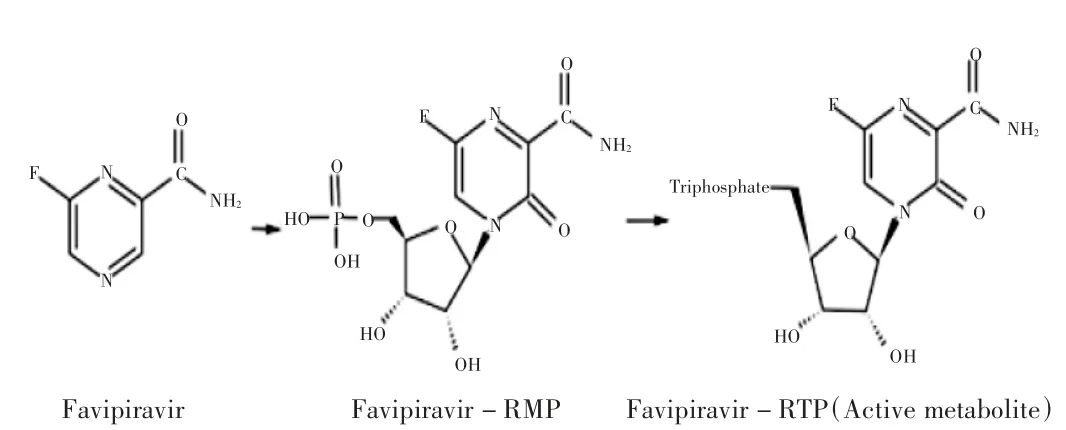
圖2 法匹拉韋的活化過程
另有研究表明,法匹拉韋RTP 還可滲入病毒基因,通過誘發致命性的突變而發揮抗病毒作用[13]。在對許多種核蛋白克隆進行序列分析后發現,發生突變的基因數量都明顯增長,核蛋白基因編碼信息也明顯改變,但不能分離出任何抗法匹拉韋的突變克隆。目前有研究者認為,法匹拉韋的作用機制幾乎可以發生在任何不同種屬病毒感染的細胞中,從而發揮廣譜抗病毒功能[14]。
2 法匹拉韋臨床研究
2.1 抗甲型、乙型流感病毒
抗流感病毒經典藥物如M2 離子通道抑制劑、神經氨酸酶抑制劑等,均非直接作用于病毒復制,療效有限[15]。而法匹拉韋直接抑制病毒RNA 復制,目前已在我國與日本上市用于流感的治療[1]。在法匹拉韋抗流感病毒的體內、體外試驗中,TAKAHASHI 等[16]將法匹拉韋與奧司他韋的療效進行對比,結果表明,法匹拉韋對甲型H1N1 流感病毒的抑制作用明顯優于奧司他韋。在國際多中心Ⅲ期臨床試驗中,以甲型、乙型成人流感患者作為研究對象,以奧司他韋作為對照,法匹拉韋組和奧司他韋組表現出相似的抗病毒療效[2]。在病毒滴度極大或病毒增殖速度過快時,法匹拉韋抗病毒的作用會降低。SMEE 等[17]在研究中建議,治療嚴重流感病毒感染時,法匹拉韋與神經氨酸酶抑制劑聯用可保證治療效果。
2.2 抗其他致病性RNA 病毒
在抗埃博拉病毒的多個體外試驗、動物試驗中,法匹拉韋都體現了良好的抗病毒作用。2015 年2 月公布的一項關于法匹拉韋治療埃博拉病毒感染者的多中心非隨機臨床試驗中,法匹拉韋對聚合酶鏈反應(PCR)檢測為高度或中度病毒載量的患者療效較好[18]。沙粒病毒可導致無菌性腦炎、病毒性出血熱等嚴重疾病[19]。在沙粒病毒的體外試驗中發現,與安慰劑組或利巴韋林組比較,法匹拉韋可更有效地抑制病毒滴度[20]。發熱伴血小板減少綜合征病毒(severe fever with thrombocytopenia syndrome virus,SFTSV)是常見的布尼亞病毒[15],病死率較高,目前無特異性抗病毒藥物及預防性疫苗。HIDEKI 等[21]在體外試驗中發現,法匹拉韋的抗病毒作用明顯,且不影響細胞活性。此外,法匹拉韋對黃病毒、狂犬病毒也呈現了良好的抑制作用,但這些研究尚停留在體外試驗和動物試驗階段。加強臨床研究,對于RNA 病毒的攻克有重大意義。
3 SARS -CoV -2 致病機制及臨床治療
3.1 致病機制
SARS -CoV -2 屬β 屬冠狀病毒,與蝙蝠體內檢測到的β 冠狀病毒相似,是感染人類的冠狀病毒家族第7 個成員[22]。研究者將SARS -CoV -2 基因序列與已知感染人類的冠狀病毒進行比較,發現其與嚴重急性呼吸綜合征(SARS)冠狀病毒(SARS-CoV)的同源性很高,相似性約為70%,與中東呼吸綜合征(MERS)冠狀病毒(MERS -CoV)的相似性約為40%[23]。基因序列差異主要在開放閱讀框1a / b(open reading frame,ORF1a / b)和編碼S -蛋白的spike 基因上,這是冠狀病毒與宿主細胞作用的關鍵蛋白[23]。
冠狀病毒顆粒包含4 種主要的結構蛋白,分別為纖突蛋白(spike,S)、囊膜蛋白(membrance,M)、小包膜蛋白(envelope,E)、核蛋白(nucleocapsid,N)[24]。病毒體與宿主細胞的初始附著是通過S 蛋白與其受體間的相互作用而開始的。與SARS -CoV 類似,SARS -CoV -2 通過S 蛋白與呼吸道上皮細胞表面的ACE2 受體結合,隨后病毒包膜蛋白與細胞膜融合而入侵人體,病毒將遺傳物質釋放入細胞內,進而復制倍增,引起一系列病理改變。
3.2 臨床治療方案
因SARS-CoV-2 與SARS-CoV 同源性較高,當前部分治療方案借鑒了SARS 期間的方案。目前對于COVID-19 尚無特異性抗病毒藥物,治療方案多以緩解癥狀、預防繼發感染、減少并發癥及器官功能支持為主。為了在短時間內滿足臨床防治COVID-19 的迫切需求,國家衛生健康委員會《新型冠狀病毒肺炎診療方案(試行第七版)》[25]、北京協和醫院《北京協和醫院關于“新型冠狀病毒感染的肺炎”診療建議方案(V2.0)》[26]以及華中科技大學同濟醫學院附屬同濟醫院《新型冠狀病毒肺炎診療快速指南》[27]等,均針對COVID-19 的藥物治療給出了意見,推薦的抗病毒藥物主要有α-干擾素、洛匹那韋/利托那韋、利巴韋林、硫酸氯喹、阿比多爾等,但均未提及法匹拉韋。2020 年2 月26 日,軍隊前方專家組《軍隊支援湖北醫療隊新型冠狀病毒感染疾病診療方案(試行第一版)》[28]首次推薦了法匹拉韋,其可行性值得探討。
4 法匹拉韋治療COVID-19 的可行性
4.1 臨床抗病毒應用史
法匹拉韋雖在我國剛上市,但在日本已有數年抗流感病毒治療的歷史,療效確切,安全性好。至今,研究者們仍在不斷挖掘其對抗其他多種RNA 病毒的治療潛力,如埃博拉病毒、布尼亞病毒等。本次COVID -19疫情中,法匹拉韋亦被臨床專家用于小范圍同情給藥,在已開展的小規模初步臨床研究中呈現出了較好的結果[29]。
4.2 作用機制
冠狀病毒的復制周期包括侵入、復制、組裝與分泌等階段[30]。SARS-CoV-2 進入宿主細胞后,病毒包膜與溶酶體膜融合后釋放RNA 至胞漿[31],病毒將遺傳物質以內吞方式釋放至宿主細胞質中,病毒RNA 聚合酶(RdRp)被合成[32],該聚合酶識別冠狀病毒基因組正鏈RNA,并以其為模板合成負鏈RNA,生成的負鏈RNA進一步復制,形成亞基因組小片段正鏈RNA 和正鏈基因組RNA。在胞漿內,核糖體以亞基因組小片段正鏈RNA 為模板,翻譯生成前體蛋白。此后,核衣殼蛋白(N)與新合成的基因組RNA 結合而形成螺旋核衣殼,與其他結構蛋白結合而形成病毒顆粒。子代病毒由高爾基體轉移至細胞膜,并釋放至細胞外。理論上,對SARSCoV-2 生命周期任何環節予以干預都可阻斷病毒的感染過程,如抑制病毒復制過程(抑制RNA 聚合酶)或干預病毒蛋白成熟過程(蛋白酶抑制劑)等。法匹拉韋的作用靶點正是病毒RNA 依賴的RNA 聚合酶[12],其在體內活化后生成具有生物活性的法匹拉韋RTP,競爭性地抑制RNA 聚合酶,從根本上阻礙病毒RNA 鏈的復制和轉錄,從而發揮抗病毒作用。

表1 國內法匹拉韋抗新型冠狀肺炎的臨床試驗
另外,因細胞中修復DNA 復制錯誤的機制并不會修復病毒RNA,而冠狀病毒的基因組較長(3 萬個堿基),RNA 復制過程中易發生錯誤,故易導致SARSCoV-2 出現變異性[33]。傳統抗病毒藥物對新發病毒往往不能起到及時、有效的治療效果,而廣譜抗病毒藥物可作用于多種病毒或同一種病毒的多種基因型[34]。法匹拉韋作為一種廣譜抗病毒藥物,很可能對SARSCoV-2 起到抑制作用。
4.3 臨床療效及安全性
中國科學院武漢病毒所和軍事醫學科學院毒物藥物研究所檢測了法匹拉韋體外抗SARS-CoV-2 的活性,其半數有效濃度為61.88 μmol/L,高于其體外抗流感病毒半數有效濃度(EC50:3 ~20 μmol/L)[35]。由于該藥之前對埃博拉病毒的抑制效果較好,仍值得進一步研究,目前正在進行治療SARS-CoV-2 的臨床試驗。截至2020 年2 月25 日,中國臨床試驗注冊中心注冊的針對COVID-19 的臨床試驗共有247 個,其中涉及法匹拉韋的研究已開展5 項(見表1)。深圳市第三人民醫院開展的法匹拉韋臨床研究中,試驗組和對照組共入組80 例,法匹拉韋治療組的不良反應明顯低于洛匹那韋/利托那韋(克力芝)組,且尚未發現嚴重不良反應,抗病毒療效也優于克力芝組。但對于法匹拉韋治療COVID-19 療效的確認,仍需更大樣本量、更大規模的臨床試驗進行驗證。
從安全性方面看,日本開展的Ⅲ期臨床試驗中,共有501 例進行了安全性評價,觀察到臨床檢驗閾值異常的不良反應100 例(19.96%),主要不良反應有血尿酸增加(24 例,4.79%)和腹瀉(24 例,4.79%)等[5]。一旦發生上述不良反應,應及時采取對癥治療措施。法匹拉韋應用于COVID -19 的治療屬“老藥新用”,“老藥”相比于全新結構藥物,其合成工藝成熟、安全性和藥代動力學數據已知,可在很大程度上避免新藥研究的高失敗率[34]。
5 結語
面對COVID-19 的肆虐,特效新藥的研制無法一蹴而就,利用好現有藥物,有利于縮短研發時間、降低研發成本。法匹拉韋是首個在此次疫情期間批準上市的抗新型冠狀病毒藥物,其適應證為成人新型病毒或再次流行的流感。作為核苷類的廣譜抗病毒藥物,已有多個研究表明,法匹拉韋對多種RNA 病毒療效顯著,而且從理論上對SARS-CoV-2 也有作用。在已開展的針對COVID-19 的小規模臨床試驗中,法匹拉韋顯示出了較好的療效和較低的不良反應。法匹拉韋治療COVID-19 的作用有待更大規模的臨床試驗驗證,但值得期待。

