特發性肺纖維化患者中睡眠呼吸紊亂的研究
張麗萍,畢小瑞,侯洪艷
(北京市海淀醫院/北京大學第三醫院海淀院區 呼吸內科,北京 100080)
0 引言
近年來,特發性肺纖維化(IPF)的患病率、發病率呈上升趨勢,死亡率也較前增加。阻塞性睡眠呼吸暫停低通氣綜合征(OSAHS)在呼吸內科較為常見,主要以“夜間睡眠打鼾伴呼吸暫停、白天嗜睡”為特征的睡眠呼吸疾病,嚴重影響患者的身體健康及生活質量。既往國外研究發現,IPF患者中存在睡眠呼吸結構紊亂,且發病率較高[1]。而國內有關IPF 合并睡眠呼吸紊亂的研究較少。本研究通過對IPF 患者進行多導睡眠圖監測,試圖探討IPF 患者中睡眠呼吸紊亂的特征和OSAHS 的發病情況。
1 對象與方法
1.1 對象。樣本來源:北京市海淀醫院呼吸科門診就診或住院患者;樣本時間:2015 年1 月至2019 年1 月;樣本對象:44 例IPF 患者,診斷依據為中華結核和呼吸雜志2011 年發布的特發性肺纖維化診治循證指南(摘譯本)[2]。排除繼發性肺纖維化、排除合并其它慢性呼吸系統疾病,如慢性阻塞性肺病、肺結核等;排除合并慢性心、肝、腎功能不全的患者。其中男性31 例,女性13 例,年齡45-80 歲,平均(64.2±9.4)歲。患者一般資料見表1。
1.2 方法。①采用意大利科時脈公司肺功能儀測量:患者的肺通氣功能及彌散功能。指標包括:肺總量占預計值百分比(TLC%pred)、用力肺活量占預計值百分比(FVC%pred)、第1 s 用力呼氣容積占預計值百分比(FEV1%pred)、FEV1/FVC、一氧化碳彌散量占預計值百分比(DLCO%pred)。②以Epworth 嗜睡量表進行評價患者睡眠質量,總分24 分,得分越高說明嗜睡現象越嚴重,評分大于等于9 分認為有白天嗜睡現象。③采用美國Embla 多導睡眠監測儀進行夜間多導睡眠圖(PSG)監測,時長≥8 h,內容包括胸腹呼吸運動及外周血氧飽和度(SpO2)、腦電圖、心電圖、肌電圖、眼電圖、口鼻氣流等。監測結果判定為以下兩種情況:a.呼吸暫停。指口鼻氣流較基線水平下降≥90%且時間持續≥10 s;b.低通氣。與基線水平相比,口鼻氣流速度下降≥30%,并伴SpO2下降≥4%,且持續時間不低于10 s,或口鼻氣流速度下降不低于50%,伴SpO2下降≥3%,持續時間≥10 s。睡眠呼吸暫停低通氣指數(AHI)主要是指患者平均1 h 內上述兩種癥狀出現的次數;微覺醒指數是指睡眠期間平均1 h內發生的微覺醒次數;氧減指數(ODI)指睡眠期間平均1 h內發生血氧下降的次數。依據AHI 進行OSAHS 疾病嚴重程度判定,5 次/h ≤AHI<15 次/h、15 次/h ≤AHI<30 次/h、AHI ≥30 次/h 分別對應輕度、中度、重度。
1.3 統計學處理。44 例IPF 患者調查數據采用SPSS 17.0 統計包分析。多導睡眠圖監測結果及睡眠評分用()表示。P<0.05 為差異顯著。
2 結果
2.1 肺功能測定。IPF 患者的肺功能顯示限制性通氣功能障礙及彌散功能減退(結果見表1)。
2.2 多導睡眠圖監測結果分析。44 例IPF 患者均存在夜間外周血氧飽和度的下降,睡眠結構紊亂,睡眠效率降低,微覺醒指數、睡眠分期I 期和II 期比例增加,III 期、快速動眼睡眠期(REM 期)比例減少。參與本次研究的44 例IPF 患者中,有68%(30 例)的患者合并OSAHS,其中14%(6 例)為輕度,54%(24 例)為中重度;而其余的14 例患者AHI 小于5 次/h,未達到OSAHS 的診斷標準,診斷為鼾癥(結果見表2、表3)。
表1 IPF 患者一般資料
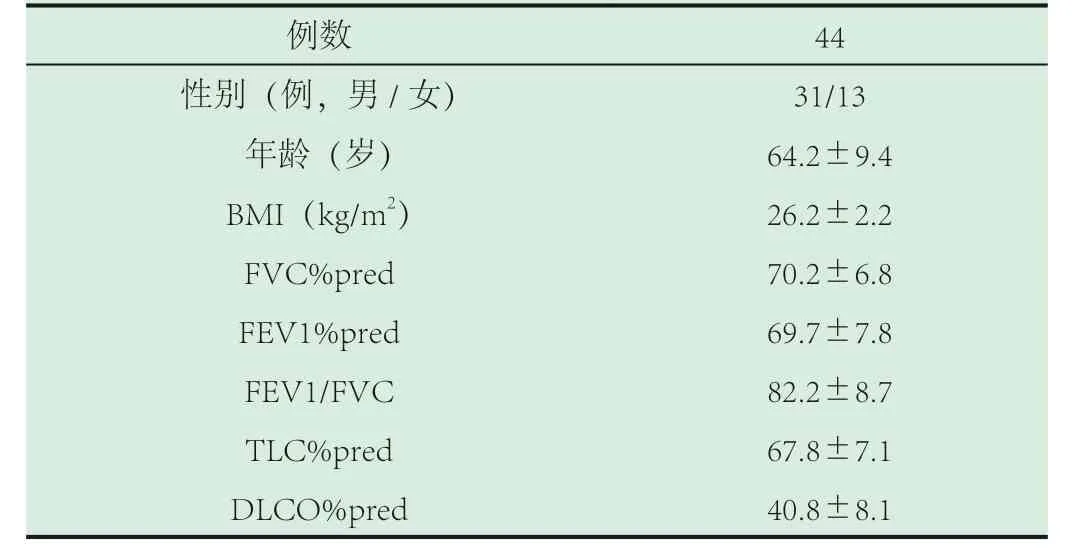
表1 IPF 患者一般資料
例數 44性別(例,男/女) 31/13年齡(歲) 64.2±9.4 BMI(kg/m2) 26.2±2.2 FVC%pred 70.2±6.8 FEV1%pred 69.7±7.8 FEV1/FVC 82.2±8.7 TLC%pred 67.8±7.1 DLCO%pred 40.8±8.1
表2 44 例IPF 患者多導睡眠圖監測結果及睡眠評分
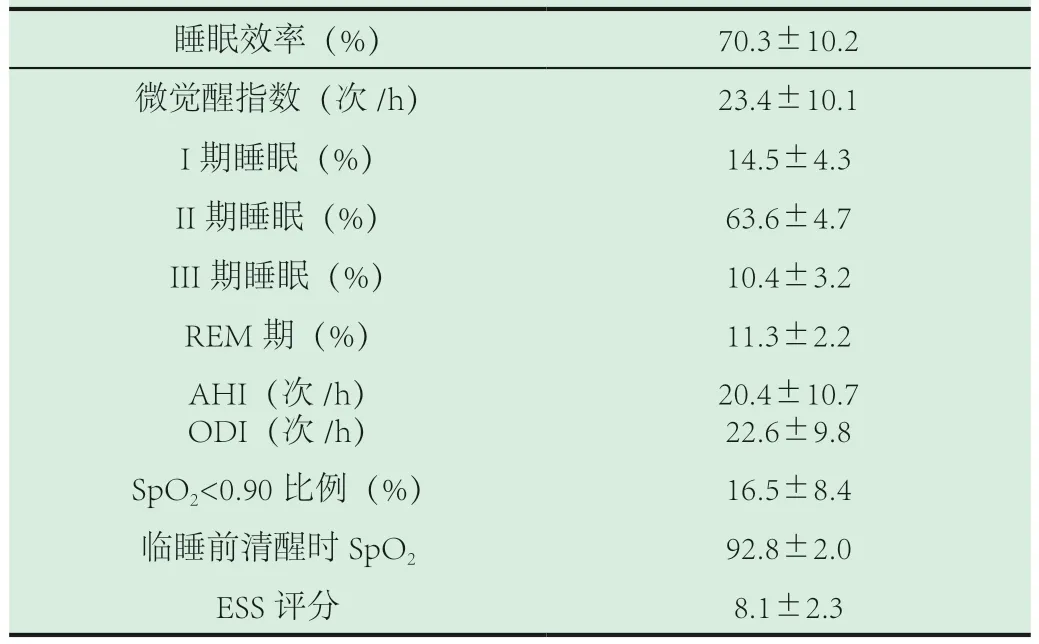
表2 44 例IPF 患者多導睡眠圖監測結果及睡眠評分
睡眠效率(%) 70.3±10.2微覺醒指數(次/h) 23.4±10.1 I 期睡眠(%) 14.5±4.3 II 期睡眠(%) 63.6±4.7 III 期睡眠(%) 10.4±3.2 REM 期(%) 11.3±2.2 AHI(次/h)20.4±10.7 ODI(次/h)22.6±9.8 SpO2<0.90 比例(%) 16.5±8.4臨睡前清醒時SpO2 92.8±2.0 ESS 評分 8.1±2.3
表3 AHI ≥5 次/h 的IPF 患者多導睡眠監測結果及睡眠評分
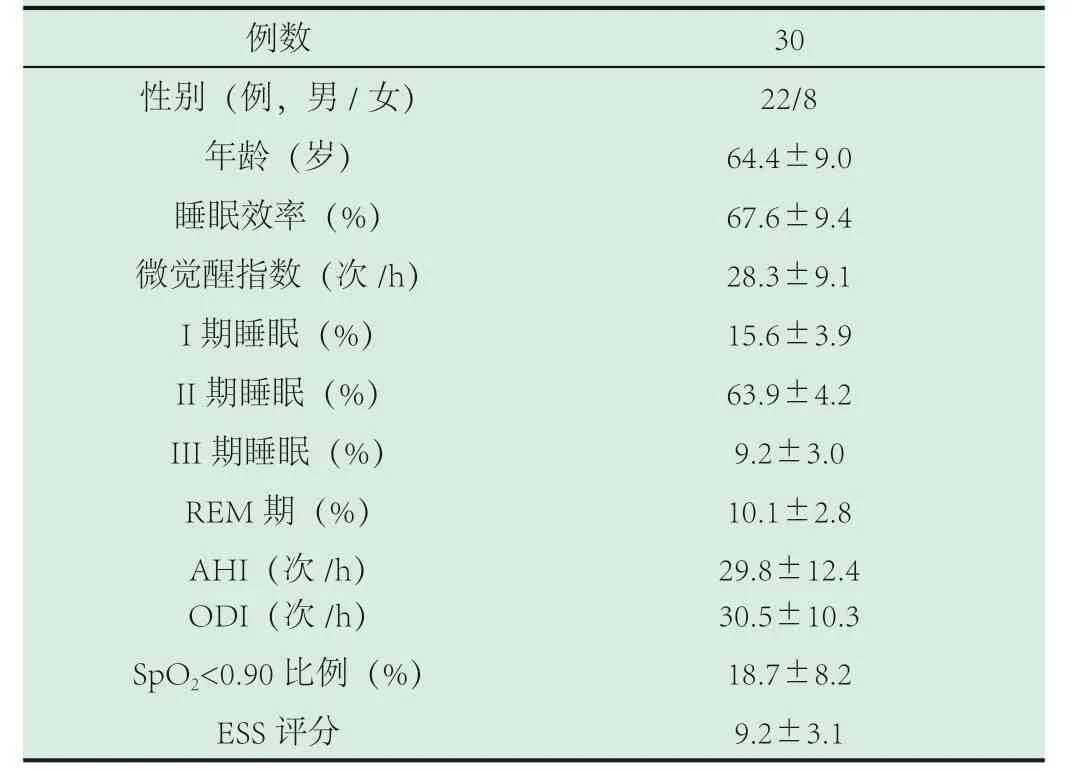
表3 AHI ≥5 次/h 的IPF 患者多導睡眠監測結果及睡眠評分
例數 30性別(例,男/女) 22/8年齡(歲) 64.4±9.0睡眠效率(%) 67.6±9.4微覺醒指數(次/h) 28.3±9.1 I 期睡眠(%) 15.6±3.9 II 期睡眠(%) 63.9±4.2 III 期睡眠(%) 9.2±3.0 REM 期(%) 10.1±2.8 AHI(次/h)29.8±12.4 ODI(次/h)30.5±10.3 SpO2<0.90 比例(%) 18.7±8.2 ESS 評分 9.2±3.1
3 討論
特發性肺纖維化(IPF)是特發性間質性肺炎中最常見的一種,臨床表現為干咳、漸進性呼吸困難或活動后氣喘等。阻塞性睡眠呼吸暫停低通氣綜合征(OSAHS)是常見的睡眠呼吸疾病。既往對OSAHS 的研究多集中在慢性阻塞性肺病患者,而最新的美國胸科學會(ATS)指南已經將OSAHS作為IPF 的合并癥之一[3]。Perez-Padilla 等[4]研究顯示,間質性肺疾病患者睡眠質量惡化、睡眠結構改變,存在睡眠片段化及夜間低氧現象。Mermigkis 等[5]研究發現IPF 患者睡眠效率及慢波睡眠比例降低,睡眠分期I 期比例及微覺醒指數增加,患者的日常功能受到影響。本研究所示IPF 患者存在睡眠結構紊亂,睡眠效率降低,微覺醒指數、睡眠分期I 期和II 期比例增加,III 期、快速動眼睡眠期(REM 期)比例減少,與既往研究一致。Mermigkis 等[6]另一項研究顯示18 例IPF 患者合并OSAHS 的比例為61%(11 例)。Lancaster 等[1]研究顯示,IPF 患者合并OSAHS 的概率大大增加,50 例IPF 患者中OSAHS 的發病率為88%(44 例)。參與本次研究的44 例患者中,有30 例(68%)患者合并OSAHS,其中6 例為輕度,24 例為中重度;進一步證實了IPF 患者中OSAHS 的高發病率。
當前,學界關于IPF 并OSAHS 的發生機制尚未完全闡明,臨床多認為與IPF 導致上氣道阻力、容量發生異常改變所致。特發性肺纖維化存在明顯換氣功能障礙,隨著疾病進展,機體呈現缺氧狀態,影響大腦中樞神經對低氧的敏感性,由于上述兩種因素相互作用,增加了患者夜間呼吸事件發生風險。雖然最新指南不主張使用激素,但既往臨床中常常用激素來治療IPF,長期使用激素可引起肥胖、頸部脂肪堆積,從而使IPF 中OSAHS 的發病率增加。
目前IPF 缺乏有效的治療藥物,優化睡眠及生活質量是治療IPF 合并OSAHS 的首要目標[7]。持續氣道正壓通氣(CPAP)治療合并OSAHS 的IPF 患者,通過面罩使氣道維持正壓,增加上氣道穩定性,防止上氣道塌陷,能在很大程度上緩解患者的嗜睡癥狀,提高注意力。Mermigkis 研究表明,合并OSAHS 的IPF 患者經過CPAP 治療后,其睡眠質量、生活質量均有所提高[8]。
綜上所述,OSAHS 在IPF 患者中發病率高,影響患者的日常功能和生活質量,故建議對IPF 患者均進行PSG 監測,及早發現IPF 患者中睡眠呼吸紊亂問題。盡早通過CPAP 治療,可能會達到改善癥狀、提高生活質量的目的。

