地佐辛聯合羅哌卡因超前鎮痛對乳腺癌改良根治術患者麻醉效果及術后躁動的影響
趙晨璐,孫 婷,李 林,張國慶
(駐馬店市中心醫院麻醉科,駐馬店 463000)
乳腺癌(breast cancer)是全球最常見的女性惡性腫瘤,統計顯示2012年全球乳腺癌發病人數和死亡人數分別約170萬和52萬,我國占比分別為11.2%和9.2%[1-2]。手術治療在乳腺癌治療中占有重要地位,其中根治術為現行標準術式,可明顯提高患者生存率和生存期,但術后疼痛、應激、并發癥等問題也會對患者術后康復和生活質量造成不利影響。因此,圍術期麻醉和疼痛管理已逐漸受到學術界重視[3]。目前常用圍術期鎮痛藥物包括阿片類藥物或非甾體類抗炎藥(NSAIDs),其中地佐辛、帕瑞昔布等鎮痛效果已獲得證實且藥物毒副作用相對較少,因而在臨床應用較為廣泛[4]。代坤吾等[5]研究表明,地佐辛對乳腺癌術后的鎮痛效果優于舒芬太尼且耐受性良好,但容易延遲麻醉蘇醒時間。因此,對于如何提升手術患者麻醉效果并減少不良反應仍有較大空間。本研究主要探討地佐辛聯合羅哌卡因超前鎮痛對乳腺癌改良根治術患者麻醉效果及術后躁動的影響,為提高乳腺癌患者圍術期麻醉和疼痛管理水平提供參考依據。
1 資料與方法
1.1 一般資料
選取2017年6月~2018年6月我院擬擇期行根治術治療的76例乳腺癌患者,經醫院倫理委員會批準,采用隨機數字表法均分為兩組,各38例。觀察組年齡37~64歲,平均(52.34±8.71)歲;國際抗癌聯盟(UICC)臨床分期[6]為Ⅱ期者21例、Ⅲ期17例。對照組年齡39~62歲,平均(51.96±8.47)歲;UICC臨床分期為Ⅱ期者18例、Ⅲ期20例。兩組基本資料無統計學差異(P>0.05)。
納入標準:① 臨床確診為乳腺癌患者。② 年齡18~65歲。③ 臨床分期為Ⅱ~Ⅲ期。④ 美國麻醉師協會(ASA)分級為Ⅰ~Ⅱ級。⑤ 患者及家屬知曉本研究并簽署知情同意書。
排除標準:① 乳腺癌治療后復發患者。② 伴嚴重系統性疾病或凝血功能障礙者。③ 伴酒精或鎮痛藥物依賴者。
1.2 研究方法
兩組患者術前完善相關檢查并向患者交代手術和麻醉相關流程及可能出現的并發癥等,待患者了解后簽署知情同意書。術前常規禁食8 h,禁飲4 h。兩組患者均采用靜吸全麻,進入手術室后仔細進行三方安全核查,建立外周靜脈通路,監測生命體征,以6 L/min吸氧3~5 min后開始誘導麻醉。方案為依次緩慢靜脈注射咪達唑侖2 mg、舒芬太尼0.35 μg/kg、順式阿曲庫銨0.15 mg/kg、依托咪酯0.2~0.3 mg/kg,患者意識消失后行面罩加壓給氧3~5 min 后行氣管插管并連接呼吸機。麻醉維持方案為微量泵持續泵注丙泊酚及瑞芬太尼,藥物濃度分別為4~5 mg/(kg·h)和0.15~0.3 μg/(kg·min),術中行腦電雙頻譜指數(BIS)監測,使患者術中BIS維持在45~55。七氟烷吸入1.5%~2%,并于術前30 min降至1%,手術結束后停止吸入七氟烷和停止泵注丙泊酚及瑞芬太尼,并采用4 L/min新鮮氧氣沖洗麻醉劑。術前30 min靜脈注射舒芬太尼 5 μg、托烷司瓊5 mg,術畢由手術醫生給予0.375%羅哌卡因20 ml對手術及引流切口行局部浸潤麻醉,送入麻醉后恢復室(PACU)進行復蘇。觀察組在上述常規麻醉誘導前5 min靜脈注射地佐辛0.1 ml/kg。
1.3 觀察指標
生命體征:記錄兩組拔管(氣管插管)即刻及拔管后10 min、30 min、60 min時兩組患者的心率(HR)、呼吸頻率(RR)、收縮壓(SBP)及舒張壓(DBP)水平。② 疼痛評分:采用視覺模擬法(VAS)評估兩組患者術后1 h、6 h、12 h及24 h時的疼痛程度,總分0~10分:0分:無疼痛;1~3分:輕微疼痛;4~6分:疼痛可忍受但影響睡眠;7~10分:疼痛劇烈,難以忍受。③ Ramsay鎮靜評分[7]:拔管后即刻進行評估,總分1~6分:1分:煩躁不安;2分:睜眼、安靜,可合作;3分:嗜睡,對命令及聲音等刺激產生反應;4分:睡眠狀態,大聲刺激可喚醒;5分:對大聲刺激反應遲鈍;6分:深度睡眠,無法喚醒。其中,2~4分為鎮靜滿意,5~6分為鎮靜過度。④ 躁動評估:采用RSS躁動分級評估兩組患者在PACU中躁動程度,其中0級為安靜合作;1級為輕度躁動,受吸痰等刺激發生肢體躁動或間斷呻吟;2級為無刺激時肢體躁動伴持續呻吟;3級為劇烈掙扎、喊叫或試圖拔出各種引流管,需用外力按壓四肢[8]。⑤ 不良反應:觀察兩組患者術后呼吸抑制、嗆咳、頭暈、惡心嘔吐等不良反應發生情況。
1.4 統計學方法

2 結果
2.1 麻醉后生命體征
拔管后兩組HR、SBP及DBP先升高后降低,且觀察組各時間點HR、SBP及DBP均低于對照組,有統計學差異(P<0.05);RR無統計學差異(P>0.05)。詳見表1和圖1。

表1 兩組麻醉后生命體征比較
與手術結束時相比,a:P<0.05;與拔管即刻相比,b:P<0.05;與拔管后10 min相比,c:P<0.05;與拔管后30 min相比,d:P<0.05;與對照組相比,e:P<0.05

圖1 兩組麻醉后生命體征比較
2.2 術后疼痛情況
兩組術后疼痛VAS評分逐漸降低,組內各時間點有統計學差異(P<0.05),且相同時間點觀察組VAS評分高于對照組,有統計學差異(P<0.05)。見表2和圖2。

表2 兩組術后疼痛情況比較分
與術后1 h相比,a:P<0.05;與術后6 h相比,b:P<0.05;與術后12 h相比,c:P<0.05

圖2 兩組術后24 h內VAS評分比較
2.3 麻醉后Ramsay鎮靜評分及躁動情況
觀察組Ramsay鎮靜評分高于對照組,躁動發生率及嚴重程度低于對照組,有統計學差異(P<0.05)。見表3和圖3。
2.4 不良反應發生情況
兩組麻醉蘇醒后不良反應發生情況無統計學差異(P>0.05)。見圖4和表4。

表3 兩組麻醉后Ramsay鎮靜評分及躁動情況比較 n=38,n(%)
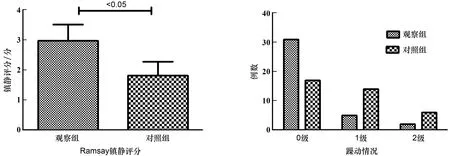
圖3 兩組麻醉后Ramsay鎮靜評分及躁動情況比較

圖4 兩組麻醉蘇醒后不良反應發生情況

表4 兩組不良反應發生情況比較n=38,n(%)
3 討論
疼痛是中樞神經系統(CNS)受傷害性刺激后興奮而產生的主觀感覺或不良情感。乳腺癌改良根治術對患者創傷較大且常涉及腋窩淋巴結清掃,造成術后嚴重疼痛,增加患者應激反應水平,導致各器官系統功能異常和并發癥發生;還可引起患者焦慮、恐懼等不良情緒,影響患者術后康復速度和生活質量[9]。加速康復外科(enhanced recovery after surgery,ERAS)理念近年來發展迅速,已成為現階段外科手術發展趨勢,其主要內容為在圍術期采用有效鎮痛方法減輕患者疼痛,減少應激和并發癥發生,促進患者術后身心健康并降低醫療成本,是非常有效的圍術期疼痛管理方法[10]。
超前鎮痛(preemptive analgesia)概念最初由Crle在21世紀初提出,是一種利用外周神經阻滯減少全麻鎮痛不全時手術創傷造成的傷害性刺激傳入中樞,防止脊髓或大腦皮層疼痛中樞持續敏化,抑制CNS興奮產生疼痛[11]。本研究中,術前靜脈注射地佐辛即為根據超前鎮痛原理在患者受到傷害刺激前阻斷沖動傳入,從而減輕術后疼痛和應激反應水平。付葵等[12]的研究表明,地佐辛聯合帕瑞昔布鈉用于乳腺癌改良根治術超前鎮痛效果良好且不增加患者心血管不良反應發生風險。本研究中,觀察組患者拔管即刻及拔管后10 min、30 min、60 min時HR、SBP及DBP均低于對照組,術后1 h、6 h、12 h及 24 h 時疼痛程度VAS評分均低于對照組,表明地佐辛聯合羅哌卡因超前鎮痛可有效減輕乳腺癌改良根治術患者術后疼痛,有利于減輕機體應激反應,維持血流動力學穩定和減少心肺并發癥發生。兩組麻醉后各時間RR均無明顯差異,其原因可能為地佐辛容易引起呼吸抑制和鎮靜過深,其作用正好與應激反應所致RR加快相反,兩者共同作用導致患者RR未發生明顯變化。地佐辛為阿片類受體混合激動-拮抗劑,可完全激活κ受體及部分μ受體,且對δ受體作用很弱,因而其鎮痛效果明顯且引起呼吸抑制作用較輕;同時可降低胃腸道不適、藥物依賴及煩躁焦慮感發生率,減少患者麻醉蘇醒期躁動發生[13-14]。
術后躁動發生機制目前尚未完全清楚,推測可能是由于術后麻醉藥物對中樞抑制作用減弱,但其殘余效果仍可對上行網狀激活系統和大腦皮層造成影響,導致CNS功能未全部恢復,對外界刺激發生異常反應[15]。研究表明,術后躁動常發生于拔管后15 min左右,主要表現為興奮、躁動不安、定向障礙和血流動力學異常,可增加心腦血管意外發生風險,并使氣道壓力升高,肺通氣量降低,造成機體代謝障礙,從而延緩患者術后康復速度[16]。臨床上常采用鎮痛或鎮靜藥抑制患者麻醉蘇醒期間躁動發生,地佐辛鎮痛效果已獲得臨床普遍認可。高燕鳳等[17]研究證實,地佐辛術前給藥可降低腹腔鏡結腸癌根治術患者躁動發生率和應激反應水平,且臨床效果優于芬太尼。本研究中觀察組患者蘇醒期Ramsay鎮靜評分高于對照組,且躁動發生率及嚴重程度均低于對照組。其機制可能為地佐辛可抑制患者麻醉恢復期痛覺過敏,其鎮痛效果顯著,可減輕機體應激反應水平和血流動力學波動;同時地佐辛對呼吸及消化系統不利影響水平較低,可減少傷害性刺激對CNS刺激,從而減少躁動發生;此外,還有學者推測與地佐辛鎮靜作用可減輕中樞對有害刺激不適感有關[18]。但本研究中觀察組鎮靜效果滿意,未見過度鎮靜情況發生。以上均表明采用地佐辛聯合羅哌卡因超前鎮痛可有效抑制乳腺癌改良根治術患者術后躁動發生。本研究比較兩組患者麻醉后不良反應可見觀察組呼吸抑制、嗆咳和頭暈發生率高于對照組,惡心嘔吐發生率低于對照組,但均無統計學差異。表明地佐辛聯合羅哌卡因超前鎮痛用于乳腺癌改良根治術患者圍術期處理,安全性良好。
綜上,地佐辛聯合羅哌卡因用于乳腺癌改良根治術患者超前鎮痛可有效提升鎮痛效果,降低麻醉蘇醒期間躁動發生率及嚴重程度,維持血流動力學穩定,且未增加不良反應發生,對患者術后康復具有重要意義。

