單一還原劑氨基羥基脲凈化PUREX流程鈾純化循環中的釕
肖松濤,葉國安,叢海峰,歐陽應根,劉協春,蘭 天,王玲鈺
中國原子能科學研究院 放射化學研究所,北京 102413
對核電產生的乏燃料采取閉式燃料循環戰略,不僅可以實現鈾、钚、镎等資源的充分利用,滿足核材料再利用的要求,而且可以有效處理和回收核廢物,滿足核安全和環境安全需求[1]。PUREX流程是國內外后處理廠普遍采用的水法后處理流程,包括了鈾钚共去污分離循環、鈾純化循環和钚純化循環三個萃取過程[2]。其中,鈾純化循環的目的是為了進一步去除初級鈾產品液中的微量釕、镎、钚以及鋯等放射性核素[3],通常采用一個或者兩個萃取循環來達到鈾純化的目的。鈾純化循環可采用濃流程和稀流程兩種方式。濃流程是將獲得的初級鈾產品液進行蒸發濃縮后,利用萃取過程中的高鈾飽和度對裂片元素釕等進行凈化。稀流程是對獲得的初步鈾產品進行預處理,利用預處理過程中的高溫、低酸和還原氛圍的條件,使釕化合物改變化學形態,再進行萃取,達到對釕的凈化目的[4]。
釕(Ru)是乏燃料的裂變產物之一,屬于高產額裂變產物。隨著核動力堆燃耗不斷加深,乏燃料中裂片元素釕的含量隨著燃料燃耗的增加呈指數關系。對于豐度為3.25%235U的UO2核燃料元件,燃耗為33 GWd/t時,冷卻3年后Ru的含量約為2 200 g/t[2]。同時,由于Ru在硝酸溶液中的化學形態和行為十分復雜,故在PUREX流程中Ru貫穿了整個流程,其在PUREX流程中的行為和走向一直是一個重要的問題。
國內外核科學工作者對釕的化學形態及其在PUREX流程中的行為進行了廣泛的研究。Bottomley等[5]認為在核燃料的后處理流程中,溶液中釕存在的狀態大致可分為四類:(1) 亞硝酰釕硝酸基配合物;(2) 亞硝酸釕亞硝酸基配合物;(3) 非配位的陽離子狀態的釕,如[RuNO(OH)]2+;(4) Ru4+和以氧橋形式存在的釕,如[RuORu]4+。Joon等[6]通過磷酸三丁酯(TBP)萃取色層法對亞硝酰釕進行了研究,認為易萃取組分與m(NO2)+n(NO3)有關,當m+n=3時為易萃取組分,并驗證了RuNO(NO2)(NO3)2(H2O)2和RuNO(NO2)2(NO3)(H2O)2是易萃取組分。黃浩新等[7]對Joon的易萃取組分理論進行了驗證,認為在硝酸介質中亞硝酰釕主要存在5種形態,分別為:RuNO(NO2)2(NO3)(H2O)2、RuNO-(NO2)(NO3)2(H2O)2、[RuNO(NO2)2(H2O)3]+、[RuNO(NO2)(NO3)(H2O)3]+和[RuNO(NO2)-(H2O)4]2+,并進行了萃取分配研究,認為裂變產物釕形成RuNO的硝酸根和亞硝酸根絡合物,其中易被TBP萃取的組分是三硝酸根絡合物和四硝酸根絡合物。Siczek等[8]對硝酸-TBP-煤油體系中亞硝酰釕化合物的形態和化學行為做了綜述,認為其形態主要和硝酸濃度有關,并且隨著溶液中硝酸濃度的增加,易萃取組分明顯減少。
由于RuNO(NO2)m(NO3)n(H2O)x配合物的化學行為比較復雜,在研究中發現放射性釕的凈化系數隨著TBP使用循環次數的增加而迅速下降。為了改善鈾純化循環中釕的凈化,通常認為必須采取有效手段改變來自共去污循環的初級鈾產品液中釕的化學形態。目前已研究過的鈾純化循環預處理還原試劑有肼[9]、單甲基肼[10]、羥胺[11]、U(Ⅳ)[12]、乙異羥肟酸[13]等,通過改變釕的價態,使其轉化為不易萃取的化學形態。也有人研究了絡合劑在鈾純化循環中的凈化效果,如巴比妥酸、硫脲、低碳異羥肟酸等[14-16],使釕化合物與絡合劑形成絡合物,通過降低TBP對釕的萃取能力而達到提高凈化效果的目的。其中肼在后處理廠中被廣泛應用,但其被氧化后會形成易爆的疊氮酸,給應用帶來了不穩定因素。而采用加入絡合劑的方法雖然能夠有效阻止TBP對Ru的萃取,但會向體系引入難以被去除的物質,會對后續工藝過程產生嚴重影響。
氨基羥基脲(HSC)是中國原子能科學研究院自行開發的無鹽有機還原劑,其既有有機還原劑的共性,又具有自己獨有優點,其在PUREX流程的鈾钚分離和钚凈化濃縮循環中均取得了良好的效果[17],如果在PUREX流程的鈾純化循環預處理工藝中也采用同一試劑,會對降低PUREX流程的運行成本和廢物的處理處置成本有重要意義。本工作擬使用氨基羥基脲代替肼作為鈾純化循環的預處理還原劑,研究預處理時間、預處理還原劑濃度、預處理酸度、預處理溫度對釕分配比的影響,并通過臺架試驗對鈾純化循環中Ru的凈化進行實驗驗證。
1 實驗部分
1.1 試劑與儀器
氨基羥基脲、N,N-二甲基羥胺,純度大于99%,自制;單甲基肼,純度大于99%,中國飛航技術研究院;羥胺、水合肼、硝酸和硝酸鈉,分析純,北京化學試劑公司。
SL6000LL液閃儀,美國Bechman;DC-1020型低溫恒溫水浴槽,寧波新芝生物科技公司;PHS-3C型酸度計,上海雷磁儀器廠;混合澄清槽,加工定制;Elan9000/DRCII/DRC-e電感耦合等離子體質譜儀(ICP-MS),珀金埃爾默儀器(上海)有限公司;L 邊密度計,自制;Alpha Ensemble型鈍化離子注入平面硅(PIPS)α能譜儀測量系統,美國ORTEC公司。
1.2 實驗方法
單級反萃取實驗:單級反萃取實驗在離心萃取管中進行,將配制好的有機相料液和還原反萃液在恒溫水浴槽中恒溫0.5 h后,按設計的相比加入萃取管中,在設定溫度下,振蕩至預定時間,快速離心分相,澄清后分別取有機相、水相樣品并測定各組分含量。
多級逆流反萃取實驗流程圖示于圖1,模擬PUREX流程2D槽钚還原反萃工藝。具體工藝參數見2.2節。
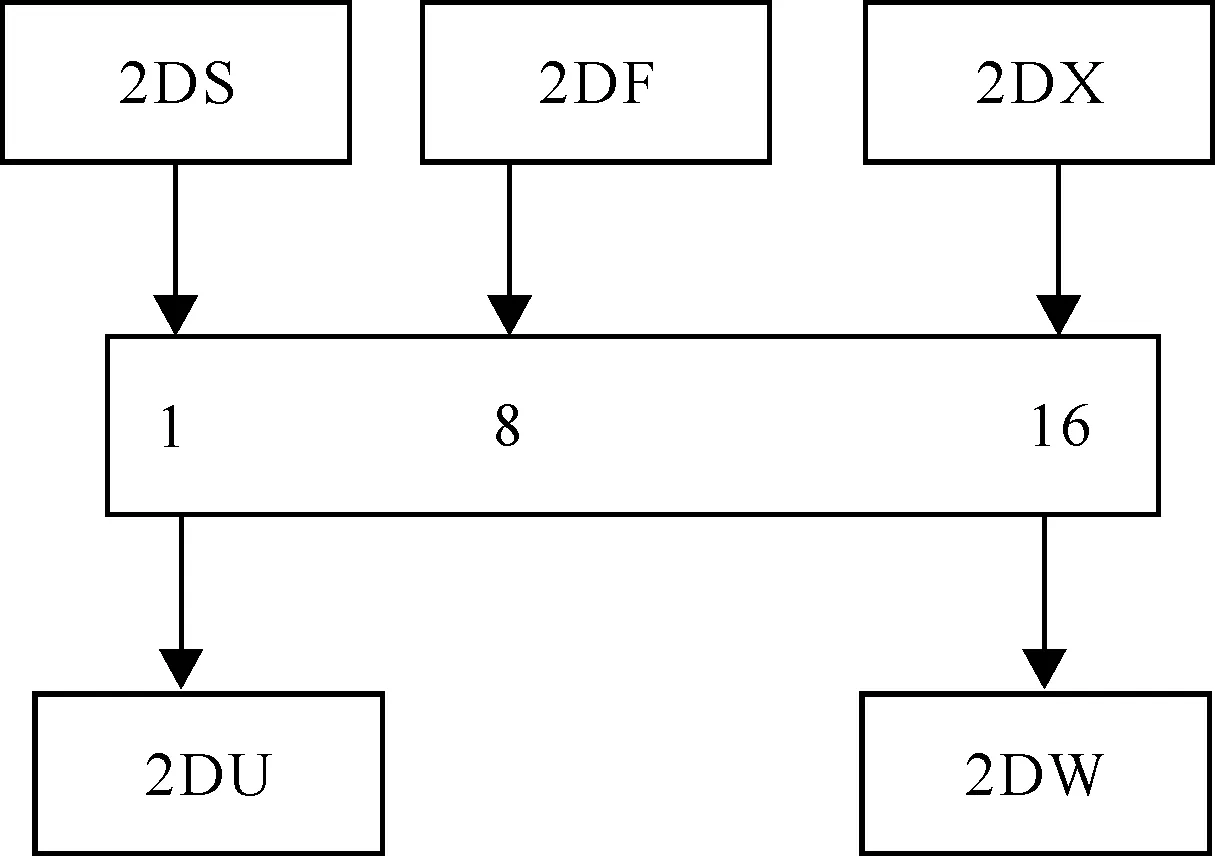
圖1 PUREX流程2D工藝示意圖
1.3 分析方法
鈾濃度的分析:部分鈾樣品采用L邊密度計分析,部分樣品采用ICP-MS分析。
Ru濃度的測定:采用ICP-MS分析。
HNO3濃度的分析:水相樣品中HNO3濃度采用飽和草酸銨絡合鈾钚,用標準NaOH進行pH滴定;有機相樣品中HNO3先用去離子水反萃入水相,再以與水相相同方法測定。
2 結果與討論
2.1 預處理對Ru萃取率的影響
進行了Ru的預處理后單級萃取性能研究,考察預處理時間、酸度、HSC濃度、溫度等對釕萃取率的影響。
2.1.1預處理時間對Ru萃取率的影響 在預處理溫度(θ)為80 ℃、ρ0(Ru)=1.0 mg/L、c0(HNO3)=0.20 mol/L、c0(HSC)=0.20 mol/L條件下,預處理時間(t)分別為20、40、60、90、120、180、240、300 min,然后取1 mL預處理后的料液,冰浴,室溫下加入0.9 mL 4.0 mol/L的HNO3,加入1.9 mL 30%(體積分數,下同)TBP/煤油,萃取20 min后,測定Ru的萃取率,結果示于圖2。由圖2可知:以30%TBP/煤油萃取預處理后的含Ru的硝酸溶液時,由于購買的釕化合物形態原因,使Ru的分配比較低,但隨著還原預處理時間的增加其萃取率進一步降低。結果表明:與未經過預處理的Ru硝酸溶液相比,實驗所采用的預處理方法能明顯改變釕的化學形態;隨著預處理時間的增加,Ru轉化為不易被萃取形態,該條件下半轉化時間約為40 min。
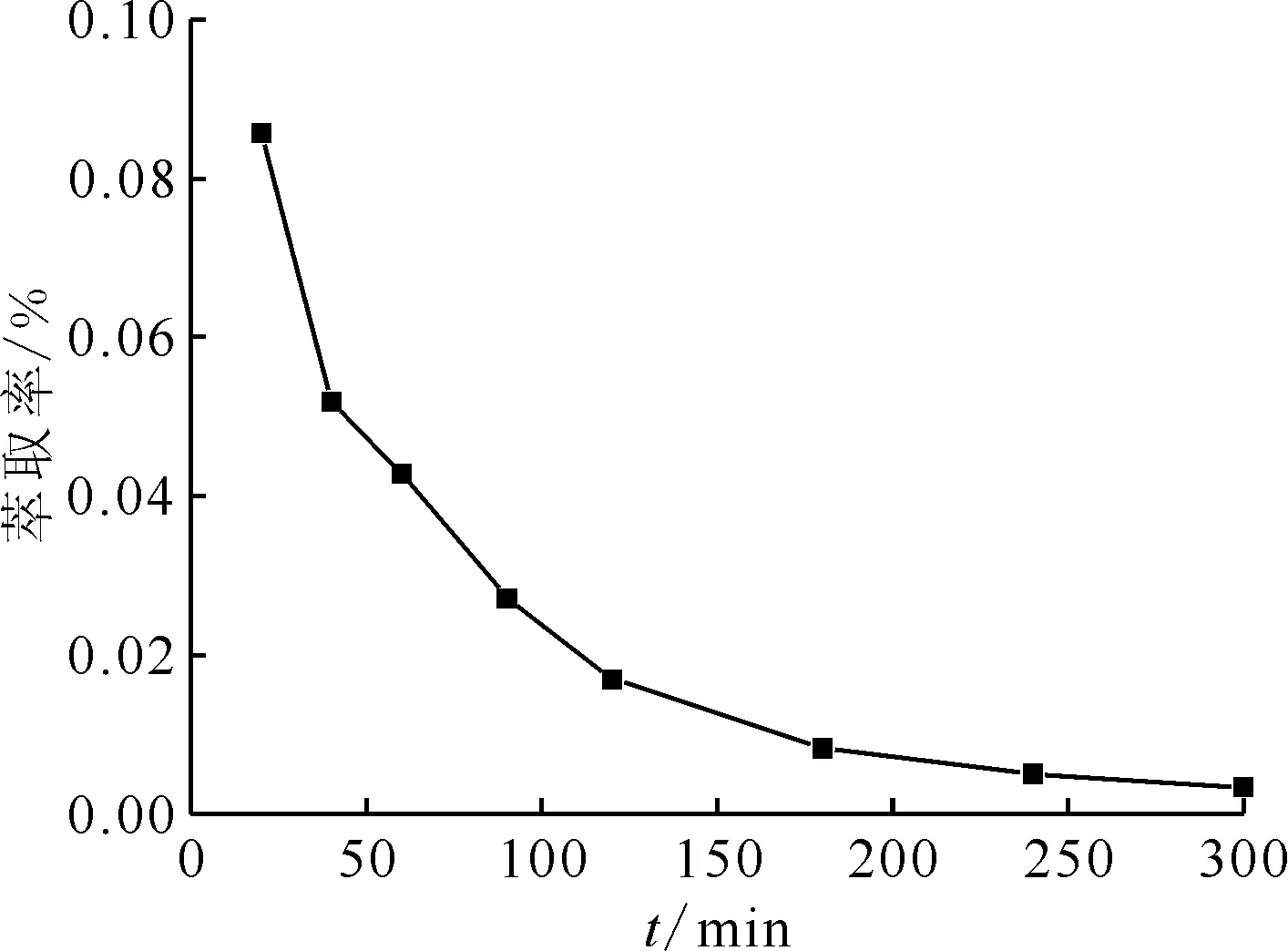
θ=80 ℃,ρ0(Ru)=1.0 mg/L,c0(HNO3)=0.2 mol/L,c0(HSC)=0.2 mol/L,萃取20 min,萃取溫度25 ℃
2.1.2預處理溶液中HSC濃度對Ru萃取率的影響 在預處理溫度為80 ℃、ρ0(Ru)=1.0 mg/L、c0(HNO3)=0.20 mol/L、c0(HSC)分別為0.05、0.10、0.15、0.20、0.30 mol/L下,預處理時間為300 min,然后取1 mL預處理后的料液,冰浴,室溫條件下加入0.9 mL 4.0 mol/L的HNO3,加入1.9 mL 30% TBP/煤油,在25 ℃時萃取20 min后,測定Ru的萃取率,結果示于圖3。由圖3可知:以30%TBP/煤油萃取預處理后的含Ru的硝酸溶液時,Ru的萃取率基本恒定,可認為隨著預處理過程中還原劑濃度的增加,Ru形態轉化率基本沒有提升,這是因為釕濃度是微量,還原劑與釕摩爾濃度比為5 000倍以上。
2.1.3預處理溶液中酸度對Ru萃取率的影響

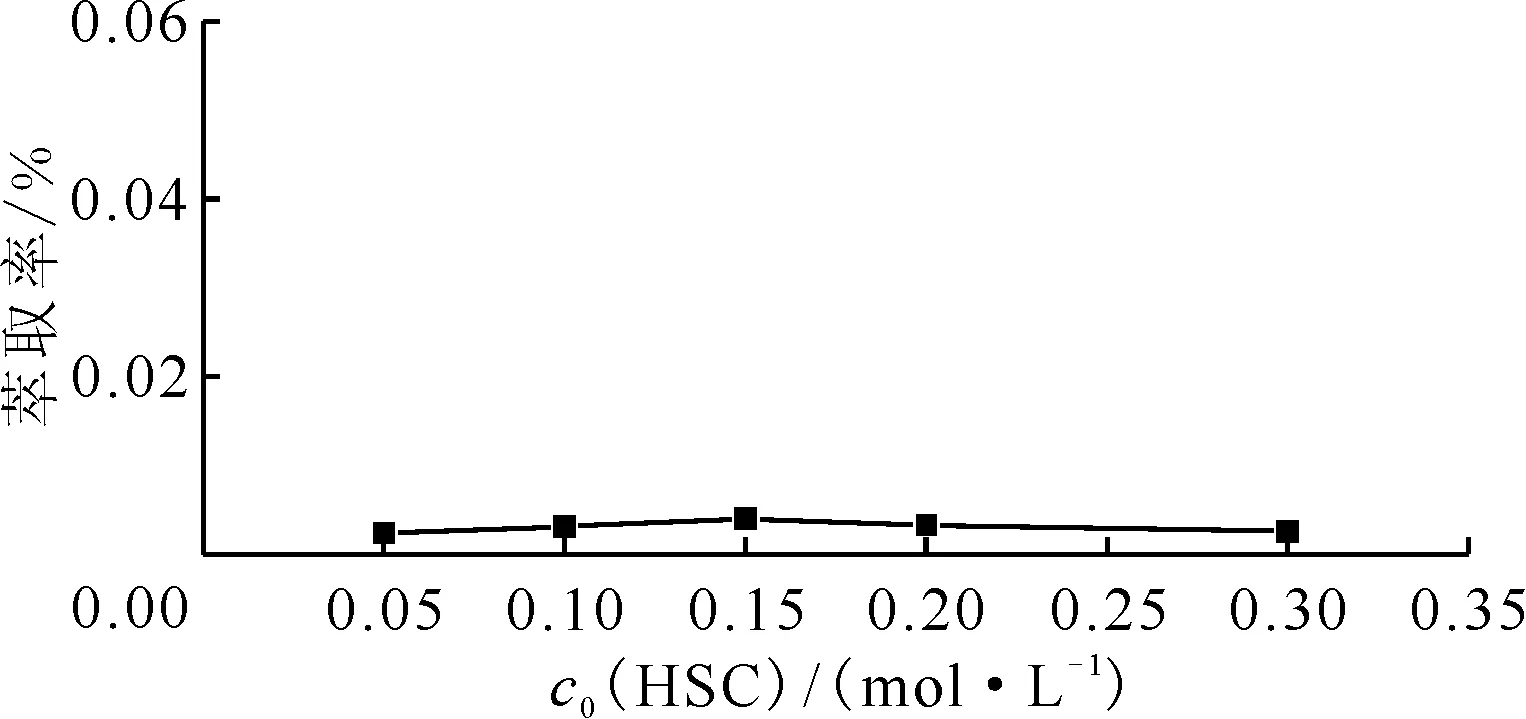
θ=80 ℃,預處理時間300 min,ρ0(Ru)=1.0 mg/L,c0(HNO3)=0.20 mol/L,萃取20 min,萃取溫度25 ℃
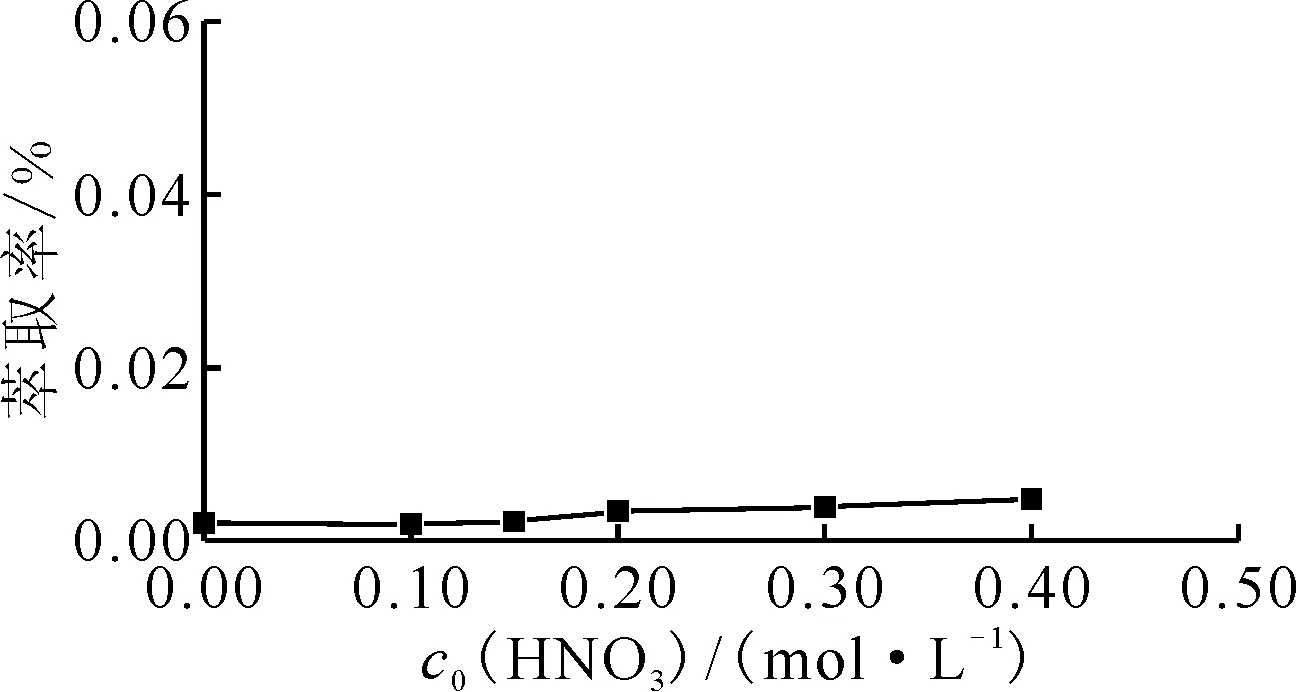
θ=80 ℃,預處理時間300 min,ρ0(Ru)=1.0 mg/L,c0(HSC)=0.20 mol/L,萃取20 min,萃取溫度25 ℃
2.1.4預處理溫度對Ru萃取率的影響ρ0(Ru)=1.0 mg/L、c0(HSC)=0.20 mol/L、c0(HNO3)=0.20 mol/L,在預處理溫度(θ)分別為20、45、60、70、80、90 ℃下,預處理時間為300 min,然后取1 mL預處理后的料液,室溫條件下加入0.9 mL 4.00 mol/L的HNO3,加入1.9 mL 30%TBP/煤油,在25 ℃時萃取20 min后,測定Ru的萃取率,結果示于圖5。由圖5可知:以30%TBP/煤油萃取預處理后的含Ru的硝酸溶液時,隨著溫度的增加Ru萃取率有較大下降;溫度小于60 ℃時,隨著溫度的升高,釕萃取率降低幅度較大,達到60 ℃以上時,釕易萃取形態化合物含量降低幅度趨緩,這表明預處理過程中,溫度對釕化合物形態轉換具有較大影響。
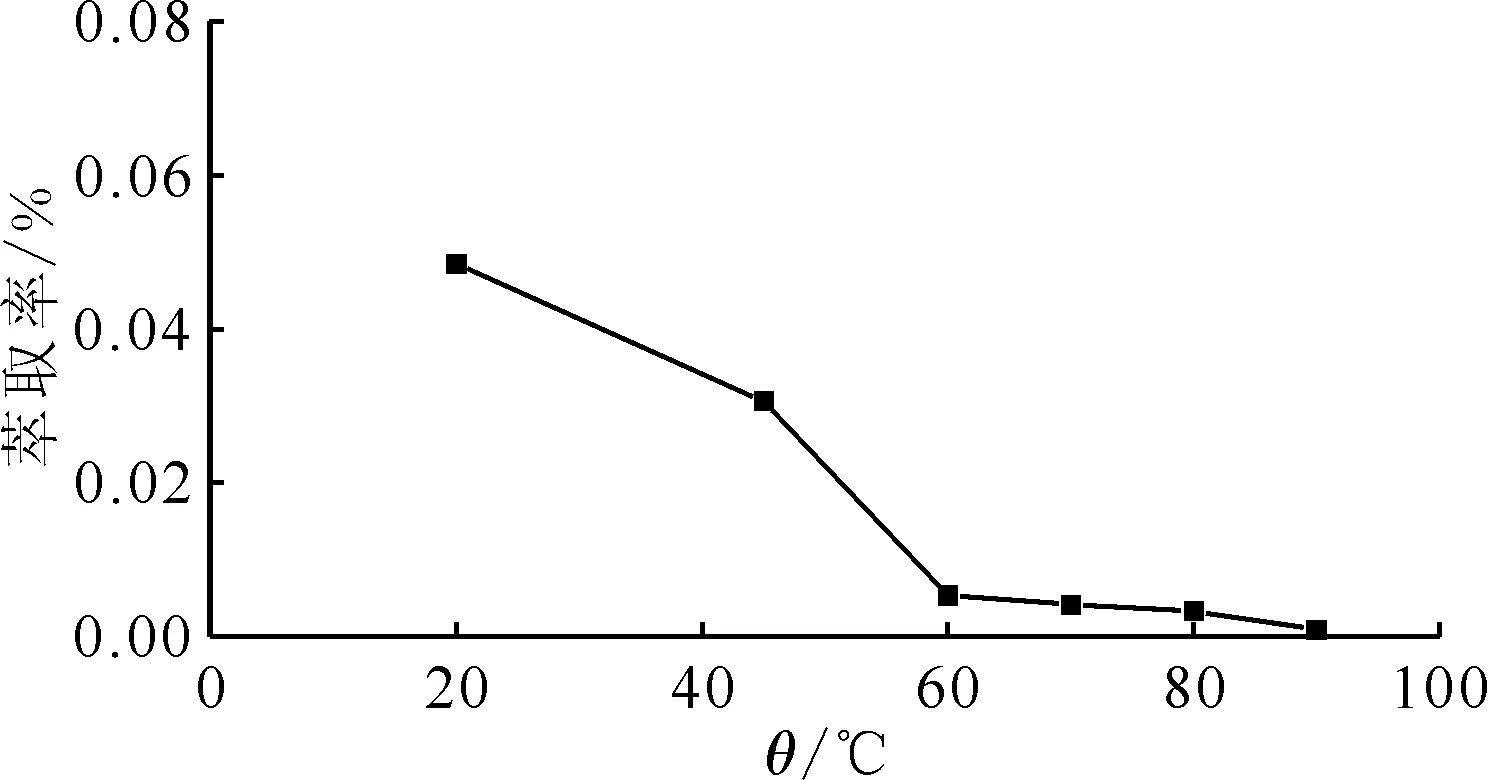
預處理時間300 min,ρ0(Ru)=1.0 mg/L,c0(HSC)=0.20 mol/L,c0(HNO3)=0.20 mol/L,萃取20 min,萃取溫度25 ℃
2.2 臺架溫試驗
為了解鈾純化循環中HSC對Ru凈化的影響,進行了含鈾的釕凈化多級逆流萃取試驗。在經過U/Pu分離工藝后,鈾純化循環中Ru濃度較低。預處理料液ρ0(U)=67.2 g/L、ρ0(Ru)=1.23 mg/L、c0(HSC)=0.20 mol/L、c0(HNO3)=0.20 mol/L, 80 ℃下,預處理時間為180 min,然后冷卻至室溫,調酸至2.0 mol/L作為鈾純化循環料液。萃取臺架試驗溫度為室溫,約25 ℃,設備采用混合室體積5 mL、澄清室體積為12.5 mL的混合澄清槽,料液在混合室停留時間為1 min,8級萃取,8級洗滌,混合澄清槽內有機相(o)與水相(a)相比約為1.5∶1,2DF為ρ0(U)=55 g/L、c0(HNO3)=2.0 mol/L、ρ0(Ru)=1.0 mg/L的水溶液,2DX為30%TBP/煤油,2DS為c0(HNO3)=1.0 mol/L的水溶液,流比2DF∶2DX∶2DS=1∶0.7∶0.16。試驗時,先以不含鈾料液進行充槽2 h,然后加入含鈾料液,運行3.0 h后,每0.5 h取一個瞬時樣品(樣品編號為1—6),運行6.0 h后,停槽,采用負壓設備抽取各級樣,分析。2DW和2DU瞬時樣品中鈾和酸的濃度分析表明,運行4.0 h后,鈾酸分布已達到平衡。平衡后各級鈾、酸濃度分布示于圖6。在實驗中鈾的回收率大于99.9%,對鈾的物料衡算為99.9%,對酸的物料衡算為97.5%。根據圖6以及鈾回收率和鈾酸物料衡算,表明實驗過程運行良好,實驗結果可靠。
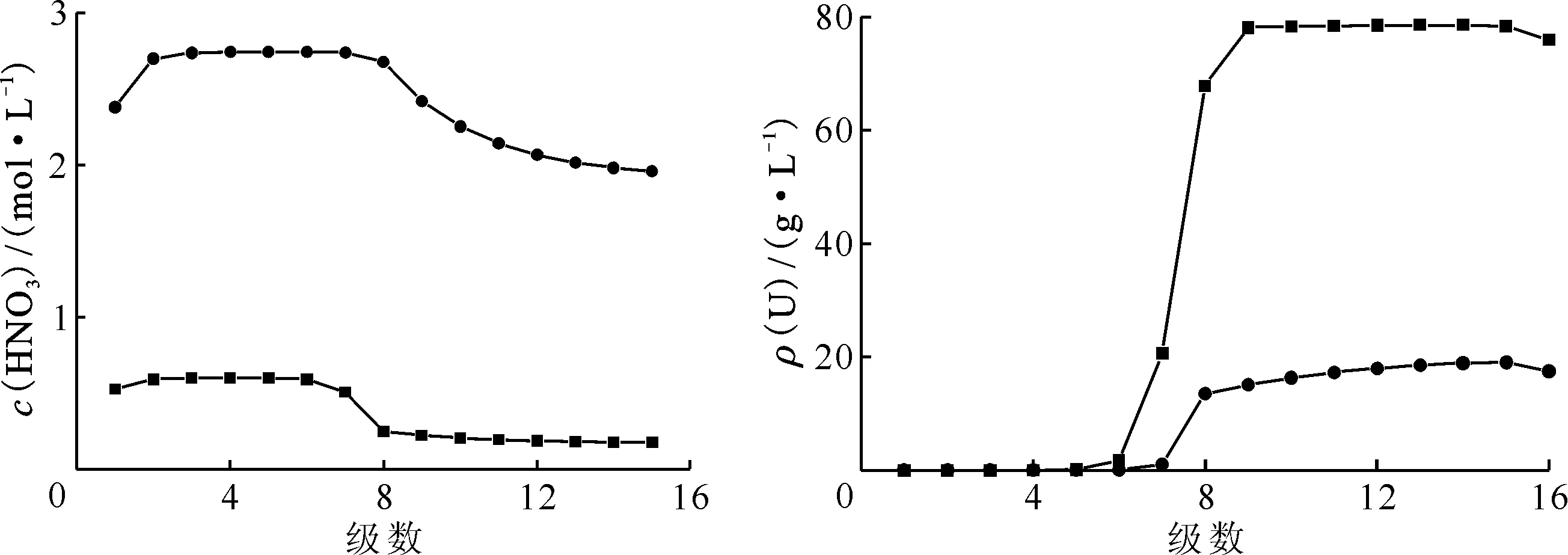
■——有機相,●——水相
2DW和2DU瞬時樣品中Ru濃度分布列入表1,其各級濃度分布示于圖7。Ru的物料衡算為103.3%。
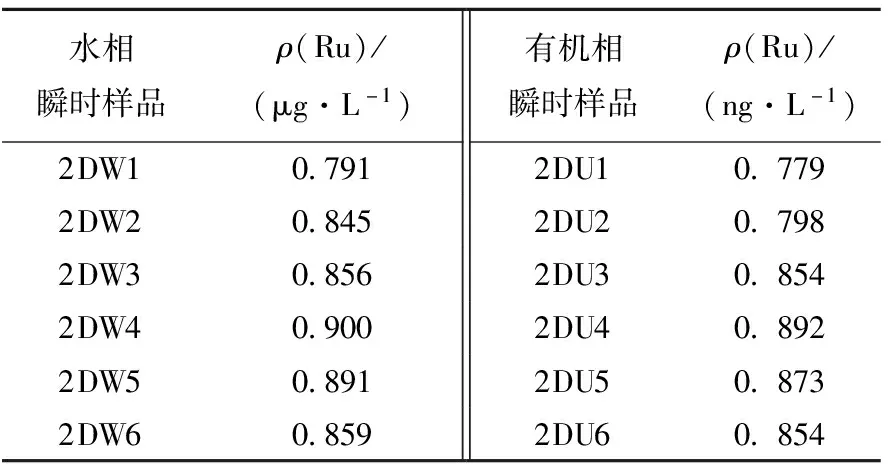
表1 平衡后2DW 和 2DU Ru瞬時樣品濃度分布
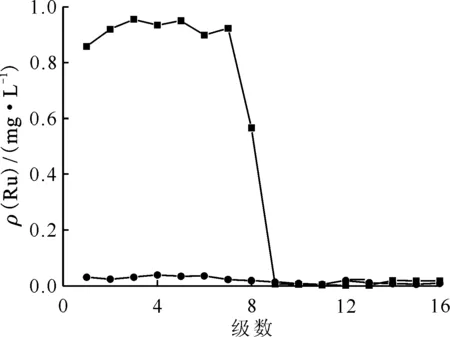
■——水相,●——有機相
根據實驗數據可計算出:Ru的凈化系數DF(Ru)=1 455。后處理廠鈾純化循環釕凈化系數要求在100以上,具體要求與乏燃料燃耗及處理工藝有關。本實驗結果表明:經過預處理,鈾純化循環中Ru的凈化系數可以達到一個較理想的數值。需要強調的是:在強輻照的核燃料溶液中,Ru的實際狀態可能會更加復雜,與模擬可能會有一定差別,需要做進一步的研究。
3 結 論
(1) 氨基羥基脲可以改變鈾純化循環預處理工藝中的釕形態,從而降低30%TBP/煤油對其的萃取性能,提高鈾純化循環中釕的凈化系數,滿足工藝要求。
(2) 氨基羥基脲可提高鈾純化循環中釕的凈化系數。由于氨基羥基脲在鈾钚分離工藝和钚凈化濃縮循環反萃工藝中具有良好的應用前景,其在鈾純化循環預處理工藝中的應用可以使整個PUREX流程所用還原性試劑統一,會對降低整個流程的運行成本及廢物的處理處置成本具有重要意義。

