睪丸混合性生殖細胞腫瘤1例報道并文獻復習
尤祥云 易成 喻俊峰

[摘要]睪丸混合性生殖細胞腫瘤(TMGCT)是一種十分罕見且惡性程度較高的腫瘤,多是年輕人發病,癥狀隱匿,在臨床中容易誤診及漏診。現報道1例TMGCT,并結合文獻對該腫瘤的臨床特征、診斷、治療進行分析,以期提高對TMGCT的全面認識,從而選擇更合理的治療方法,提高患者的生存率。
[關鍵詞]生殖細胞腫瘤;睪丸腫瘤;病理學;病例;文獻分析
[中圖分類號] R737.21? ? ? ? ? [文獻標識碼] A? ? ? ? ? [文章編號] 1674-4721(2020)4(a)-0200-04
[Abstract] Testicular mixed germ cell tumor (TMGCT) is very rare and highly malignant tumor, which mostly occurs in young people, with concealed symptoms, and is easily misdiagnosed and underdiagnosed in clinical practice. One case of TMGCT is reported, and the clinical features, diagnosis and treatment are analyzed in correlation with literature in order to improve the overall understanding of TMGCT, so as to choose a more reasonable treatment method and to enhance the survival rate of patients.
[Key words] Germ cell tumor; Testicular tumor; Pathology; Case; Literature analysis
睪丸腫瘤發病率低,據統計歐美國家的發病率為2.5/10萬~9.2/10萬,我國發病率及死亡率均為1/10萬[1]。其中約95%的睪丸腫瘤是睪丸生殖細胞腫瘤(testicular germ cell tumor,TGCT),是最常見的睪丸實體腫瘤[2]。TGCT有兩個主要的亞型:精原細胞瘤和非精原細胞瘤兩類,前者表現出原始生殖細胞的組織學特征,后者則不同程度地表現出向胚胎和胚胎外結構分化的特征[3]。精原細胞瘤沿著非精原細胞腫瘤的方向局限性分化,導致了睪丸混合性生殖細胞腫瘤(testicular mixed germ cell tumor,TMGCT)的發生:形成原始胚胎細胞,向胚體和胚外結構分化為胚胎性癌;向胚外中胚層、內胚層分化為卵黃囊瘤;向胚內三胚層分化為畸胎瘤;形成原始胚囊的滋養層細胞成分為絨毛膜癌[4]。在TGCT中僅有32%~54%的是TMGCT,臨床中十分罕見,其惡性程度較高,多發生于20~40歲的男性,占男性所有腫瘤的1.0%~1.5%,發病率和死亡率在不同的地理區域有很大的區別,發病率最高的是歐洲、北美洲,然而亞洲和非洲發病率卻很低[5-6]。現將收治的1例TMGCT報道如下,以加強對該病的認識,引發對其診療的探討。
1病例資料
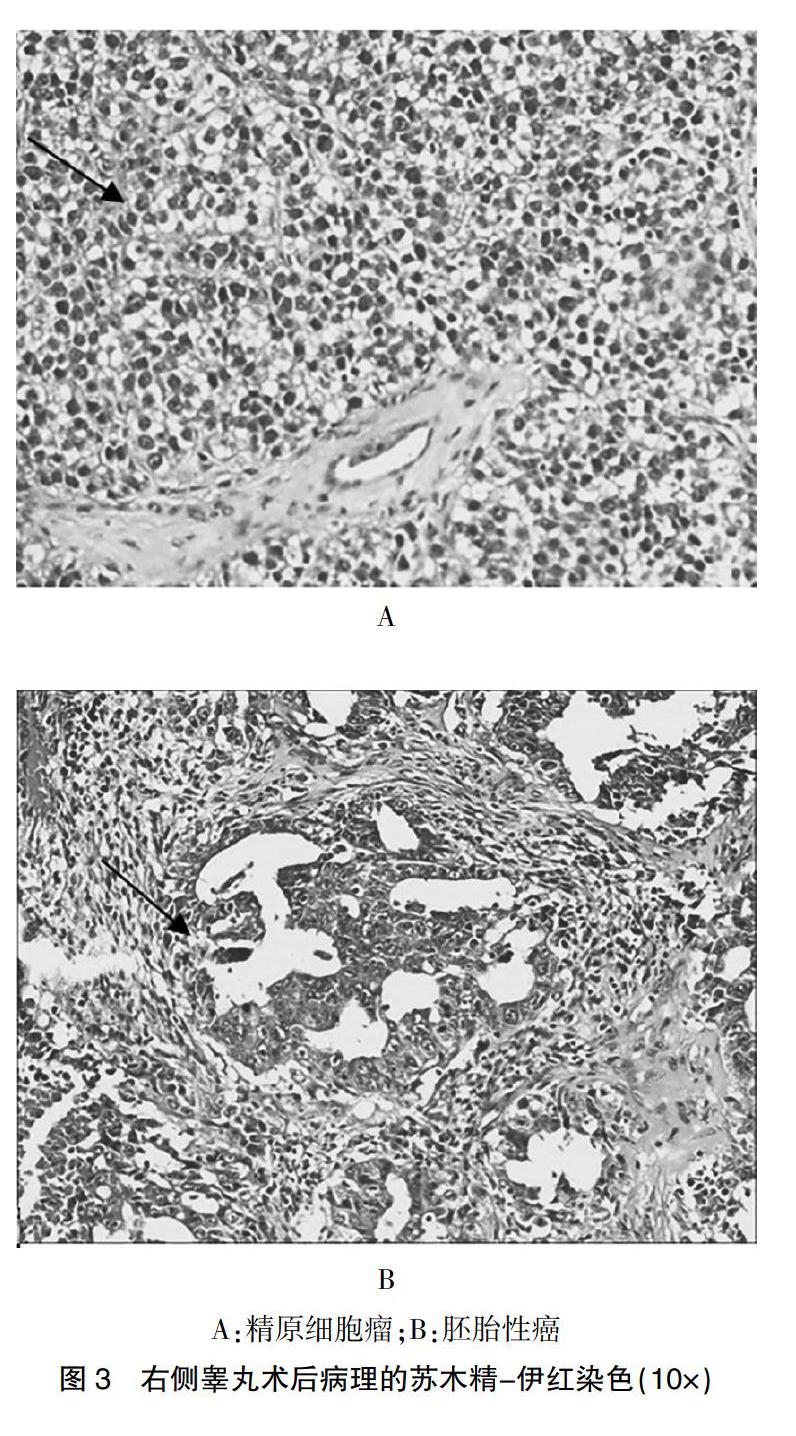
患者,男,32歲,身高170 cm,體重60 kg,因“右側陰囊疼痛2個月,發現右側睪丸包塊半個月”于2017年6月16日到湖北省宜昌市第一人民醫院就診。患者陰囊疼痛起初為間歇性墜脹、隱痛感,無放射痛,不影響日常生活,未行診治,入院前半個月因疼痛加重、呈持續性疼痛于門診就診,發現右側睪丸包塊。查體:體溫(T)36℃,脈搏(P)78次/min,呼吸(R)20次/min,血壓(BP)120/87 mmHg。神清、精神可,心、肺、腹等查體正常。專科檢查:右側睪丸大小約5×4 cm,觸診質地偏硬,表面尚光滑,觸痛明顯,透光(-),附睪結構欠清晰,雙側腹股溝可捫及淋巴結。陰囊彩超示右側睪丸體積增大(4.6×2.8 cm),其內可見4.0×3.2×1.9 cm3混合性回聲包塊,以稍高回聲為主,邊界清晰,形態欠規則,呈多結節狀,包塊內血流豐富。甲胎蛋白(alpha fetoprotein,AFP)22.90 ng/ml,血清β人絨毛膜促性腺激素(β-human chorionic gonadotrophin,β-HCG)2.11 mIU/ml。磁共振成像(magnetic resonance imaging,MRI)如圖1所示,右側睪丸增大,其內見類圓形等長T1等T2信號影,邊界清,大小約4.4×3.4×2.7 cm3,其內信號不均;磁共振彌散加權成像(diffusion weighted imaging,DWI)呈稍高信號,兩側腹股溝區可見多發小結節狀長T1長T2信號影。胸部及腹部CT檢查未見明顯異常,腹膜后彩超探查未見明顯異常。患者于入院后第6天行右側根治性睪丸切除術,標本見圖2。術后病檢:睪丸、附睪及部分精索切除標本,睪丸大小4.0×3.0×2.0 cm3,切面灰白色,實質性,質中,附睪大小2.0×2.0×1.5 cm3,切面灰白灰黃色,可見壞死,精索10×2.5×1.5 cm3,切面灰紅色灰黃色,質軟。免疫組化(immunohistochemistry,IHC):在精原細胞瘤中胎盤堿性磷酸酶(placental alkaline phosphatase,PLAP)、血清癌胚抗原(carcinoembryonic antigen,CEA)、AFP均為陽性;胚胎性癌中角蛋白(keratia)陽性。術后病理診斷如圖3所示:右側TMGCT,伴局灶性出血及壞死,為經典型精原細胞瘤(40%)和胚胎性癌(60%)混合。精索切緣未見腫瘤細胞。患者因拒絕腹膜后淋巴結清掃術及放療,自術后第2周開始依托泊苷(齊魯制藥有限公司,批號 H37023182)+順鉑(齊魯制藥有限公司,批號 H20023461)方案(EP方案)規律化療化療,共完成4個周期。化療中患者未出現乏力、惡心等癥狀,無肝功能受損、骨髓抑制,每月監測AFP、β-HCG、CEA無異常,術后2年余隨訪未發現明確轉移病灶,目前尚無婚育報告。
2討論
TMGCT起始于胎兒發育階段,來自于不能分類的曲細精管內生殖細胞腫瘤(intratubular germ cell neoplasia of the unclassified type,IGCNU),又稱睪丸生殖細胞腫瘤前體。TMGCT前體的遺傳學改變主要是12號染色體短臂出現等臂染色體[isochromosome of 12p,i(12p)][7]以及其他一些遺傳學改變,如12號染色體缺失后引起抑癌基因的丟失等,Miyai等[8]認為位于12號染色體上的6p和10q等位基因的丟失與TMGCT的發生相關。目前TMGCT已知的危險因素包括:隱睪、生殖器畸形等多種先天性發育障礙、睪丸內的小鈣化灶、睪丸生殖細胞腫瘤家族史、本人其他的生殖細胞腫瘤史等[9]。
TMGCT早期可無典型臨床癥狀,大多數患者起病隱匿,常因睪丸增大伴墜脹不適、睪丸內出現結節就診,約20%的患者表現為陰囊疼痛,此外約10%的患者表現為咳血、腰背痛、胃腸道出血、食欲減退等轉移癥狀,極少數患者因乳腺、性腺發育等內分泌癥狀就診[10-13]。本例患者陰囊疼痛起初為間歇性墜脹、隱痛感,其臨床表現缺乏特異性,符合上述一般TMGCT臨床表現的特征。當睪丸在超聲下顯示回聲不均勻,彩色多普勒顯示腫塊內血流豐富,多考慮為睪丸惡性腫瘤[14]。此患者入院后彩超檢查示:“陰囊彩超示右側睪丸體積增大,其內可見4.0×3.2×1.9 cm3混合性回聲包塊,呈多結節狀,包塊內血流豐富。”幫助了對于該病的篩查和診斷。TMGCT在MRI上表現為T1WI腫塊與正常睪丸信號相等,T2WI腫塊與正常睪丸比呈相對低信號,其內信號大多較均勻,當腫瘤伴有出血、壞死、液化時,則表現為信號強度不均[15-16]。此外黃夢娜等[17]認為常規MRI影像結合DWI及表觀彌散系數(ADC)有助于鑒別精原細胞瘤與非精原細胞瘤,可以初步鑒定腫瘤的性質,明確腫瘤的浸潤范圍和發現盆腔及遠處轉移有明顯的優勢,幫助臨床醫生進行腫瘤的分期,是選擇治療方案及手術方式選擇的重要依據。本例患者通過盆腔MRI、胸部CT及查體確定該患者腫瘤TNM分期為PT2N0M0IB期。
TMGCT臨床起病隱匿和臨床表現缺乏特異性,但由于其組織結構典型,病理診斷較易。當各成分出現典型病理形態時即可診斷,腫瘤組織常完全替代正常睪丸組織,外觀呈多樣性,以囊性、實性及出血、壞死為常見。其病理組合形式以畸胎瘤和胚胎性癌多見(25%),其次為胚胎性癌和精原細胞瘤(15%)、畸胎瘤及胚胎性癌和精原細胞瘤(15%),精原細胞瘤和卵黃囊瘤少見,約有40%的TMGCT可見灶狀卵黃囊瘤[18]。因此可通過病理來確診該病,各組織成分之間可以通過IHC檢查加以鑒別,精原細胞瘤:AFP、CEA、PLAP、角蛋白均為陽性;胚胎性癌:角蛋白、PLAP為陽性,CEA為陰性,AFP可陽性可陰性;絨毛膜癌:β-HCG、角蛋白為陽性;卵黃囊瘤:AFP、角蛋白和PLAP多為陽性[19]。本例患者也常規做了病理IHC,大體符合一般特征,更進一步明確了對該患者的診斷。
TMGCT的治療主要取決于腫瘤病理類型及臨床分期,依據《中國泌尿外科疾病診斷治療指南》[20],腫瘤分期為Ⅰ期時,行根治性睪丸切除術,并行腹膜后淋巴結清掃,術后化療加放療。分期為Ⅱ期時,行根治性睪丸切除術,如術前評估腹膜后淋巴結能夠切除,則行腹膜后淋巴結清掃,術后化療加放療;考慮切除困難,則先行化療,待復查淋巴結縮小而評估能切除時,再行腹膜后淋巴結清掃,術后追加化療。Ⅲ期時以化療為主,有孤立性轉移灶,化療后穩定的,也應手術切除[19-21]。在腫瘤根治性切除后,適當選擇后腹膜淋巴結清除術、放療和化療,化療目前多采用以順鉑(Cisplatin,DDP)為中心的聯合化療方案,化療過程中如有乏力、惡心、肝功能異常、粒細胞減少等不良反應,則予以對癥處理[20]。本例患者因拒絕腹膜后淋巴結清掃術及放療,采用了右側根治性睪丸切除術+術后EP方案規律化療,術后恢復效果較好。
TMGCT患者應該長期嚴密隨訪,隨訪內容包括體格檢查、睪丸超聲和腫瘤標志物檢查,其中AFP、β-HCG和血清乳酸脫氫酶(lactate dehydrogenase,LDH)等指標若持續升高或再次增高,往往提示腫瘤有轉移或復發,預后不良[10,22]。本例患者自術后開始定期(每半年到一年)隨訪復查,未發現明確轉移病灶且血清學檢查正常范圍,尚無婚育報告,其遠期效果仍在隨訪中。
綜上所述,TMGCT發病率相對較低但惡性程度較高,臨床上早期篩查診斷,通過根治性手術結合放化療可得到較好療效。
[參考文獻]
[1]陳力博,劉志洪,王豪,等.睪丸混合性生殖細胞腫瘤的診斷和治療(附27例報告)[J].中華男科學雜志,2018,24(11):987-991.
[2]王宇,胡俊,王亮良,等.超聲、腫瘤標志物結合術中快速病理對睪丸腫瘤手術方式選擇的指導價值[J].現代泌尿生殖腫瘤雜志,2016,8(3):159-161.
[3]李哲銘,劉冬冬,陳攀,等.睪丸支持細胞瘤1例[J].疑難病雜志,2019,18(9):955,973.
[4]Tavella VJ,Walters JN,Crofton LM,et al.Mixed germ cell tumor composed of a tridermic testicular teratoma and seminoma in a rooster[J].J Vet Diagn Invest,2019,31(3):395-398.
[5]楊華,王東文,高揚杰,等.睪丸精原細胞瘤35例臨床分析[J].中國藥物與臨床,2019,19(16):2790-2792.
[6]Liu P,Li W,Song HC,et al.Characteristics,treatment decisions and outcomes of prepubertal testicular germ cell tumor:A descriptive analysis from a large Chinese center[J].J Pediatr Urol,2018,14(5):443.e1-443.e7.
[7]沈勤,饒秋,余波,等.免疫組化染色及FISH檢測12號染色體短臂捕獲對Ⅱ型睪丸生殖細胞腫瘤的診斷意義 [J].中華男科學雜志,2016,22(8):692-697.
[8]Miyai K,Ito K,Nakanishi K,et al.Seminoma component of mixed testicular germ cell tumor shows a higher incidence of loss of heterozygosity than pure-type seminoma[J].Hum Pathol,2019,84:71-80.
[9]朱冬冬,朱軍,虞巍,等.雙側睪丸腫瘤12例報道及文獻回顧[J].北京大學學報(醫學版),2018,50(4):755-758.
[10]胡佳林,呂家駒,談月清,等.睪丸腫瘤86例臨床分析[J].山東大學學報(醫學版),2019,57(4):77-83.
[11]Batool A,Karimi N,Wu XN,et al.Testicular germ cell tumor:a comprehensive review[J].Cell Mol Life Sci,2019,76(9):1713-1727.
[12]王華禮,王永超,郭靜,等.睪丸腫瘤42例臨床分析[J].中國男科學雜志,2017,31(6):42-44,56.
[13]Shogbesan O,Abdulkareem A,Jehangir A,et al.Gastrointestinal involvement of testicular germ cell tumor:a case report and literature review[J].Case Rep Gastrointest Med,2017,2017:4 789 259.
[14]敬文莉,王紅,楊裕佳,等.睪丸混合性生殖細胞瘤的超聲表現[J].中國醫學影像技術,2018,34(S1):38-41.
[15]顧文華,宋黎濤,黃松.MRI在睪丸腫瘤中的診斷價值[J].系統醫學,2017,2(10):96-98.
[16]Liu R,Lei Z,Li A,et al.Differentiation of testicular seminoma and nonseminomatous germ cell tumor on magnetic resonance imaging[J].Medicine(Baltimore),2019,98(45):e17937.
[17]黃夢娜,高雪梅,程敬亮,等.DWI結合ADC值鑒別診斷睪丸生殖細胞瘤[J].中國醫學影像技術,2017,33(1):89-92.
[18]陳志剛,尚東浩,陳永騫.睪丸混合性生殖細胞腫瘤1例[J].臨床泌尿外科雜志,2012,27(2):159-160.
[19]賀慧穎,饒秋,趙明,等.泌尿及男性生殖系統腫瘤病理診斷免疫組化標志物選擇專家共識[J].臨床與實驗病理學雜志,2018,34(3):237-243.
[20]那彥群,葉章群,孫穎浩,等.中國泌尿外科疾病診斷治療指南[M].北京:人民衛生出版社,2014:95-102.
[21]張忠云,孫忠全,汪東亞,等.睪丸混合性生殖細胞腫瘤臨床分析[J].中國男科學雜志,2019,33(3):57-59,69.
[22]Hassan O,Epstein JI.The clinical significance of a small component of choriocarcinoma in testicular mixed germ cell tumor(MGCT)[J].Am J Surg Pathol,2018,42(8):1113-1120.
(收稿日期:2019-10-24? 本文編輯:任秀蘭)

