術前中性粒細胞和淋巴細胞比值對腎上腺皮質癌的預后評估研究
宣強,沈洲,陶陶,林垚,胡學春,穆祥宇,夏開國
[中國科學技術大學附屬第一醫院(安徽省立醫院)泌尿外科,合肥 230001]
腎上腺皮質癌(ACC)是發生于腎上腺皮質的惡性腫瘤,其發病率極低,為(0.7~2)/1 000 000,近年來有升高趨勢[1-2],惡性程度高,五年生存率較低(16%~40%)[3]。腎上腺皮質癌診斷目前依據影像學檢查及術后病理檢查確診,其治療首先選擇手術切除,對于部分伴有遠處轉移者,若患者身體狀況好,也可考慮做減瘤手術,延長患者生存周期[4]。由于腎上腺皮質癌預后較差,尋找有效的預后評估因子十分必要。相關文獻報道腫瘤細胞的增殖、侵襲受到炎癥的影響,臨床常用的炎性指標為中性粒細胞與淋巴細胞比值(NLR)[5],目前已在胰腺癌、前列腺癌等多種惡性腫瘤中有過應用報道[6-9]。本文通過回顧性分析了我院22 例腎上腺皮質癌患者的臨床資料,探討術前NLR 對ACC 預后評估的價值。
1 資料與方法
1.1 臨床資料 回顧性分析2009 年5 月—2019 年10 月在我院就診的腎上腺皮質癌患者的臨床資料。
1.2 納入與排除標準 納入標準:①行腎上腺皮質癌切除術者;②術后病理診斷為腎上腺皮質癌。排除標準:①合并心力衰竭、肝功能不全等嚴重疾病者;②術前行化療、放療者;③具有自身免疫疾病、血液病史者。收集患者的年齡、體質指數(BMI)、腫瘤最大直徑、中性粒細胞值、淋巴細胞值、白蛋白、血紅蛋白相關數據,通過電話隨訪,咨詢并記錄每一位患者生存時間、轉移及預后情況。
1.3 實驗室數據收集及計算 通過中國科學技術大學附屬第一醫院檢驗科信息系統,統計患者術前中性粒細胞計數、淋巴細胞計數、血紅蛋白值以及白蛋白值、血糖值等。其中,血常規通過全自動血液分析儀測定。血生化通過全自動生化分析儀測定。NLR 為中性粒細胞數與淋巴細胞數的比值,利用術前血常規數據,計算出NLR 值。
1.4 評價標準及定義 患者總生存時間(OS)定義為患者確診為腎上腺皮質癌至死亡時間或最后隨訪時間;患者復發或轉移的診斷標準是:患者復診過程中有明確的影像學檢查證明患者原位有新發腫瘤或有淋巴結腫大,或其他遠處轉移。患者無進展生存期(PFS)指的是行根治性切除術后,從確診為腎上腺皮質癌至患者相關影像學檢查確定患者有轉移灶的時間。
1.5 統計學處理 采用SPSS 20.0 軟件進行統計學分析。文中OS 和PFS 采用中位數和四分位數表示,其余計量資料采用表示;根據受試者工作曲線(ROC)分析確定患者年齡、腫瘤最大徑、BMI、血清白蛋白、血紅蛋白、NLR 的最佳臨界值,以約登指數(Youden index)最大值(敏感度+特異度-1)所對應的為最佳臨界值,即cut off 值,利用χ2檢驗和Fisher 精確計算法單因素分析每種影響因素與患者預后影響,對于P <0.05 者,采用Cox 回歸模型進行多因素分析,P <0.05 為差異有統計學意義,并采用Kaplan-Meier 法進行生存分析,繪制生存曲線,組間生存率采用Log-rank 檢驗。
2 結果
2.1 患者的基線資料 22 例患者中男性7 例,女性15 例;腫瘤位于左側者16 例,右側者6 例;患者年齡(56.41 ±12.83)歲;BMI 值為(21.93 ±3.57)kg/m2;腫瘤直徑大小為(10.70 ±3.59)cm;OS 為26(11.25,50.75)月;PFS 為18(3.75,39.00)月。
2.2 NLR 最佳臨界點 以患者是否發生轉移為分類變量,ROC 曲線提示最佳臨界值為2.479,最大約登指數為0.547,特異性為77.8%,敏感性為76.9%,曲線下面積為0.795,如圖1 所示。本文以NLR 為2.479 為臨界值將患者分為兩組,其中NLR>2.479 為高NLR 組,共12 例;NLR≤2.479 為低NLR 組,共10 例,比較兩組患者年齡、BMI、腫瘤最大直徑、白蛋白、血紅蛋白、血糖等臨床數據,本組發現高NLR 組的平均年齡、血糖水平高于低NLR 組,而白蛋白水平低于低NLR 組,差異有統計學意義(P <0.05),如表1 所示;比較兩組患者的平均總生存時間和無進展生存時間,本組發現高NLR 組顯著低于低NLR 組,差異有統計學意義(P <0.05)。高NLR 組的PFS 為6(2.25,18.00)個月,OS 為18.5(7.50,29.75) 個月,而低NLR 組PFS 為31.5(19.25,74.25)個月,OS 為42(25.75,74.25)個月。
2.3 影響ACC 的PFS 及OS 的單因素及多因素分析 如表2 所示,經單因素分析發現NLR 高低與患者的PFS 及OS 相關,而腫瘤最大徑與患者的OS 相關,BMI 水平與患者的PFS 相關。再應用Cox 比例風險回歸模型進行多因素回歸分析,結果顯示NLR為影響患者PFS 和OS 的獨立危險因素。NLR 偏高者發生轉移的概率高(HR=7.402,95%CI:1.662~32.963,P=0.009),且死亡風險大(HR=13.713,95%CI:1.287~146.093,P=0.030)。再用Kaplan-Meier 法繪制生存曲線,發現NLR 越高,ACC 患者越容易發生轉移,PFS 及OS 越短。見圖2。
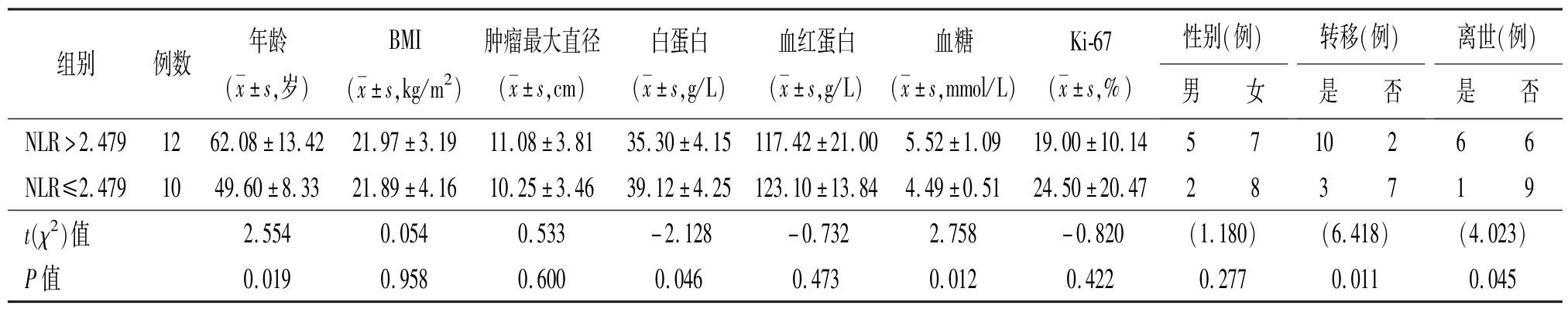
表1 22 例腎上腺皮質癌患者臨床資料與NLR 的相關性

表2 影響腎上腺皮質癌患者總生存時間/無進展生存時間的單因素分析
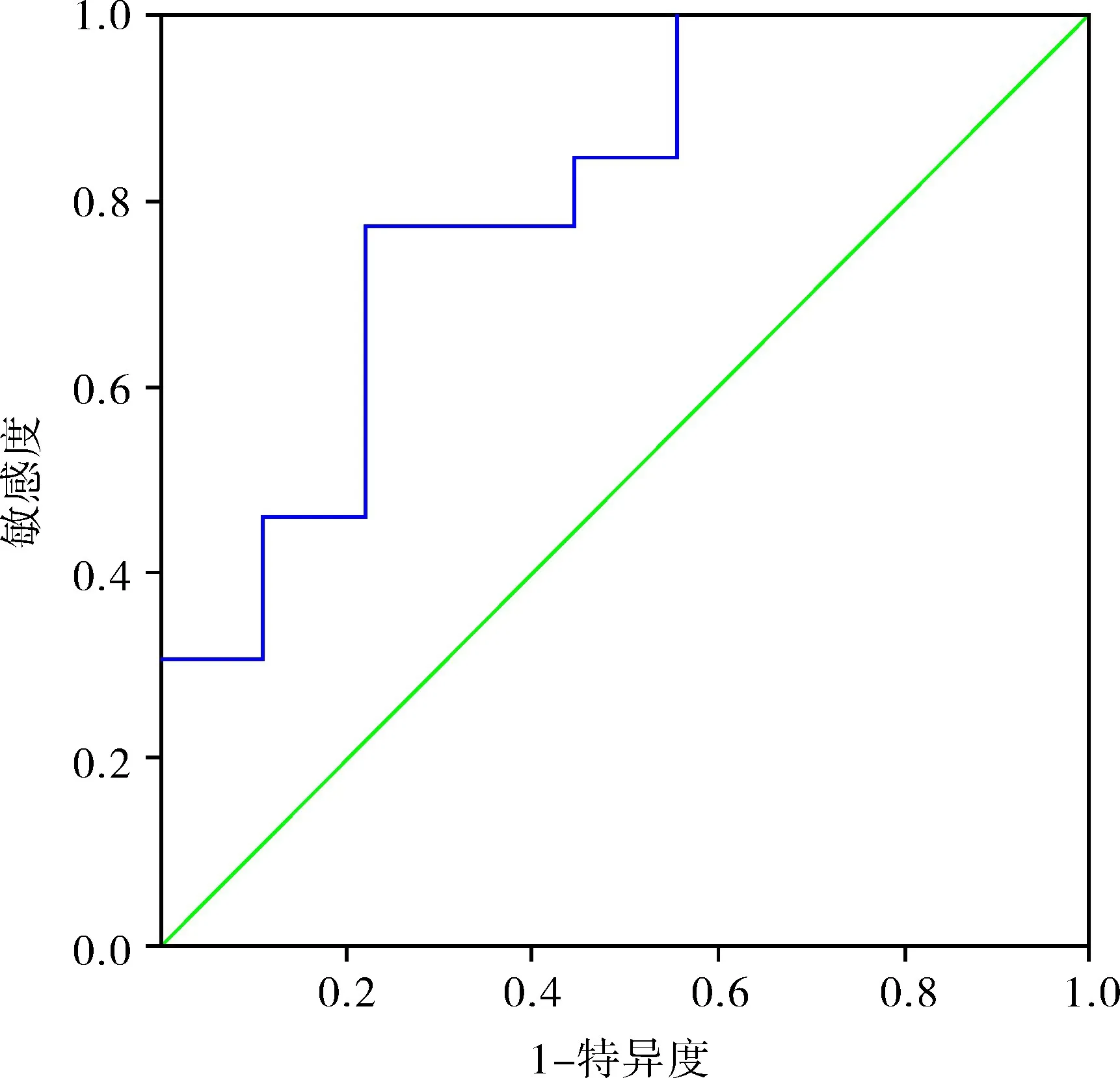
圖1 NLR 以腎上腺皮質癌是否轉移為分類變量形成的ROC 曲線
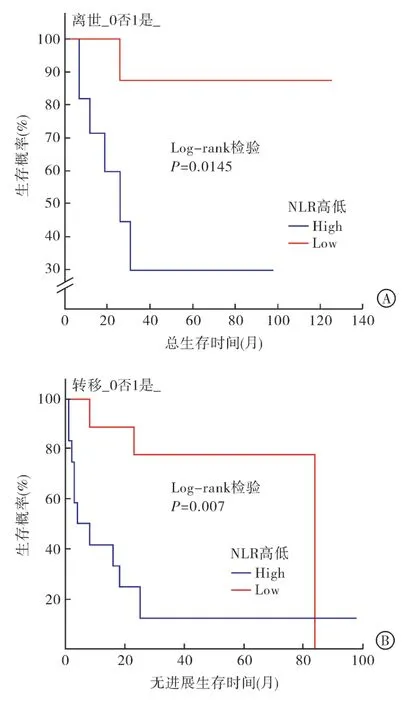
圖2 NLR 高低對患者總生存時間(圖A)和無進展生存時間(圖B)的影響
3 討論
腎上腺皮質癌早期并無典型癥狀,大部分患者發現時已是中晚期,約25%伴有遠處轉移[10],部分患者表現為Cushing 綜合征,出現滿月臉,水牛背,向心型肥胖,血液檢查發現血中皮質醇濃度異常增高[11];部分患者出現腰痛不適,多為腫瘤破裂出血引起。晚期腎上腺皮質癌患者通常侵犯周圍組織,并通過血管、淋巴管等途徑進行遠處轉移,常伴有肺部轉移,肝臟轉移等[12]。晚期腎上腺皮質癌患者乏力、納差,體質消瘦,常伴有貧血、惡病質[13]。
腎上腺皮質癌的治療目前仍以手術切除為主,優先選擇腹腔鏡切除,但對于一些腫瘤較大,與周圍組織黏連嚴重者,仍以開放切除為主[14]。對于一些伴有遠處轉移灶,周圍組織粘連較輕者,也可選擇行減瘤手術,術后再行化療,可進一步提高患者的生存時間[15]。關于腎上腺皮質癌的預后,由于其發病率較低,目前相關文獻報道較少。李少華等[16]認為影響腎上腺皮質癌預后的獨立危險因素為皮質醇高分泌和低鉀血癥,其文章中報道患者平均生存時間為49.2 個月,1 年生存率為70.0%,中位無瘤生存時間為36 個月,1 年無瘤生存率為55.6%。而張明峰等[17]報道影響腎上腺皮質癌的預后的獨立危險因素為術前低蛋白血癥、女性患者、年齡>45 歲及腫瘤分期晚,其文章中報道ACC 患者平均生存時間為29 個月,1 年、3 年及5 年生存率分別為71%、47%及42.7%。通過對本院22 例腎上腺皮質癌患者影響預后因素的研究,發現NLR 對于腎上腺皮質癌患者預后有一定的評估作用。
血中性粒細胞可以分泌腫瘤壞死因子、白細胞介素等細胞因子,促進腫瘤侵襲、轉移,而淋巴細胞分泌的淋巴因子具有抗腫瘤作用,故血液中中性粒細胞計數越多,腫瘤進展越快,預后越差;而淋巴細胞計數越多,腫瘤進展變慢,生存時間延長。NLR為中性粒細胞計數與淋巴細胞計數的比值,其比值的大小,在一定程度上預示了患者的生存時間。高翔等[18]認為NLR≥2.6 對非肌層浸潤性膀胱癌預后不利;桑尊孟[19]認為NLR≥2.731 不利于前列腺癌患者的預后;而周冠文[20]認為NLR≥2.19 對于腎癌患者的預后不利。
本文根據ROC 曲線分析,確定NLR 臨界值為2.479,NLR >2.479 有12 例,≤2.479 有10 例,兩組患者的性別、平均腫瘤最大徑、BMI 值、Hb、ki-67表達量差異無統計學意義(P >0.05),而高NLR 組的平均年齡、血糖水平高于低NLR 組,白蛋白水平低于低NLR 組,差異有統計學意義(P <0.05),這在一定程度上說明高齡、高葡萄糖、低蛋白可能與人體炎癥的發生和發展相關。本組發現高NLR 組患者的總生存時間為18.5(7.50,29.75)個月,無進展生存時間為6(2.25,18.00)個月,低NLR 組患者的總生存時間為42(25.75,74.25)個月,無進展生存時間為31.5(19.25,74.25)個月,兩組患者差異有統計學意義(P <0.05)。本研究發現NLR >2.479為腎上腺皮質癌患者預后的獨立危險因素。
綜上所述,NLR 作為相關腫瘤的預后影響因素已經被報道,但是NLR 與腎上腺皮質癌的相關報道極少,本文對我院22 例腎上腺皮質癌患者的臨床資料進行分析,得出NLR >2.479 者總生存時間和PFS 均明顯減少。本研究顯示高NLR 與腎上腺皮質癌預后不良相關,NLR 可能成為腎上腺皮質癌患者預后的評估指標,也可能為該疾病的免疫治療提供新思路。

