中藥人源性毒性評判的科學基礎、策略與技術關鍵點
馬紅紅 魏桂林 潘秋莎 楊凌
摘要 中藥毒性研究中因倫理原則不可能在人體進行還原論模式的臨床研究,體內外結合、動物與人體臨床研究的結合成為研究模式的必然選擇。有毒中藥藥材面臨著藥材組成成分的定性與定量水平差異、各不同產地藥材組成成分巨大變異、毒理機制的萬變、體內外模型差異、種屬差異、器官組織細胞組成差異、代謝與功能非均一性、評價指標與檢測方法多重性等差異的眾多挑戰與難題。現代毒理學高度重視與強調對人源性毒理學(而非動物毒性或細胞毒性)特征及其本質的研究,但人源性毒性在體內外體系、種屬差異、臟器組織特征差異、形態結構學與分子組成差異等眾多影響因素的干擾下,常常迷失本質性、機制性或原理性研究方向,理清研究邏輯,選擇正確的策略與技術切入點才能避免中藥毒性評價與研究誤入歧途。
關鍵詞 有毒中藥;人源性;系統毒理學;標志物
Scientific Basis,Strategy,Key Technical Point and of Human-derived Toxicity Evaluation of Traditional Chinese Medicines
MA Honghong,WEI Guilin,PAN Qiusha,YANG Ling
(Institute of Interdisciplinary Integrative Medicine Research,Shanghai University of Traditional Chinese Medicine,Shanghai 201203,China)
Abstract Owning to the ethics concerns,it is impossible to carry out clinical research of reductionism model in human body for the toxicity research of the traditional Chinese medicine,the combination of in vivo and in vitro,animal and human clinical research has become the inevitable choice of research mode.Toxic traditional Chinese medicine(TCM)are faced with many challenges and difficult problems,such as qualitative and quantitative differences in composition,huge variation in composition of medicinal materials from different origin,variation of toxicological mechanism,differences in models in vivo and in vitro,species differences,differences in organ tissue and cell composition,heterogeneity of metabolism and function,multiplicity of evaluation indexes and detection methods.Modern toxicology attaches great importance to and emphasizes the research of the characteristics and nature of the human-derived toxicity rather than animal toxicity or cytotoxicity.However,due to the interference of many influential factors,such as in vivo and in vitro systems,species differences,organ tissue characteristics differences,morphological structure and molecular composition differences,the evaluation of human-derived toxicity often loses its essential,mechanism or theoretical research direction.Only by clarifying the research logic and choosing the right strategy and technical breakthrough point can we avoid the wrong way of toxicity evaluation and research of traditional Chinese medicine.
Keywords Toxic traditional Chinese medicine; Human-derived; System toxicology; Biomarker
中圖分類號:R285文獻標識碼:Adoi:10.3969/j.issn.1673-7202.2020.23.006
中藥的有效性和安全性是中醫藥傳承和發展的基石,中醫藥千百年的臨床實踐也使得中醫藥的用藥經驗及方式具有多樣性與多變性,同時也有“人源性”“辨證論治”和“整體觀”等優勢,但在物質基礎發現和機制研究方面仍然存在天然缺陷,中藥毒性的人源性與其中藥的多成分、多靶點作用使得中藥的毒性評價具有極高難度,因此建立“有毒”中藥材的效應物質、毒性效應和致毒機制數據庫、毒效標志物與檢測方法學的數據庫,構建符合中醫特色且國際認可的中藥毒效評價模式,形成針對“有毒”中藥材的科學認知、客觀評價和安全使用、有效防控的系統方法尤為重要,也可進一步為中藥臨床合理用藥,建立有效的質量控制標準提供科學依據。
1 有毒中藥材組成成分的復雜性
中藥材成分極其復雜,所含成分還因品種、產地、炮制工藝等發生變化;同時藥材還有可能受重金屬,霉菌等成分的污染。根據所含有效成分或有效成分的不同,中藥可分為道地藥材普通藥材。我國土地遼闊,地形錯綜復雜,氣候條件多種多樣。不同地區的地形、土壤、氣候等條件,形成了不同的道地藥材。獨特的環境下,物種形成了自己的品質與生長、繁衍習性,所含成分也因此而發生變化。因此,中藥因來源于天然或種植,其組成穩定性是一極大挑戰[1]。
中藥經炮制后,由于加熱、加輔料等處理,可以使某些中藥中的化學成分發生變化,有的成分被溶解出來,有的成分被分解或轉化成新的成分,有的成分有量的增減,只有在搞清楚中藥在炮制過程中多成分之間的轉變及機制,才能完成中藥質量的穩定及控制[2]。更好地了解中藥炮制的目的,進而為探討中藥炮制原理,據現代藥學研究表明,炮制對中藥材成分有著很顯著的影響。例如,生物堿是一類含氮有機物,通常有似堿的性質,味苦。炮制此類中藥材常用的輔料有醋、酒2種。醋,呈弱酸性。可使生物堿成鹽而易被水煮出(溶水性),增強療效。酒,弱極性。可使生物堿游離其內,便于煎出有效成份。許多中藥經炒制后,可殺酶保苷,如芥子,牛蒡子等;煅制常用于處理礦物藥,動物甲殼及化石類藥物,能使質脆易碎,而且作用也會發生變化。如白礬煅后燥濕、收斂作用增強。血余煅炭后能止血。川烏、草烏加熱煮制后,其毒性顯著降低,保證了臨床用藥安全有效。中藥經輔料制后,在性味、功效、作用趨向歸經和不良反應方面都會發生某些變化,從而最大限度地發揮療效。除以上可造成中藥成分復雜性增加之外,由于儲存不當,中藥還會受到霉菌污染,使成分發生改變,產生毒性或其他不良反應[3]。中醫藥理論認為,毒性是中藥最基本的性能之一。如中藥藥源性肝損傷,是指由于中藥自身或其代謝產物導致的肝臟損傷。在2016版的《中草藥相關肝損傷臨床診療指南》中也提到了常見的中藥肝損傷就按損傷靶細胞類型分為肝細胞損傷型,混合型,膽汁淤積型和肝血管損傷型[4]。不僅是肝毒性,許多中藥活性成分都具有潛在的毒性,如《中華人民共和國藥典》中列出的10大有毒中藥,川烏,馬錢子等[5]。多數具有生物堿,例如早已耳熟能詳的草烏,因含有雙酯型二萜生物堿,其可對神經系統產生不良反應,那是否會有更多中藥的各類生物堿具有毒性有待進一步研究。由此可見,中藥毒性機制的復雜多樣同時也是中藥材復雜的重要原因之一。
2 人源性毒性的特點
中藥的毒性/藥效是中藥多成分與機體相互作用的結果,其效應評價不僅取決于中藥本身成分還取決于被作用的評價模型,模型不同其作用效果也不同。在實際研究中,也需依據中藥材所作用的靶器官或者中藥材中某一活性成分作用的靶細胞及亞細胞器選定評價模型,若此中藥材或成分現并未有文獻對其毒性/藥效進行報道,應先從其活性成分組成及分子結構特征推斷其可能毒性/藥效,并進一步推進整體動物實驗,從而觀察其真實毒性/藥效靶器官、靶細胞及靶細胞器,最后再在體外模型上對其機制進行研究。雖然哺乳動物與人體絕大多數組織/器官的形態和解剖結構相似,但其成分組成(如蛋白種類和水平等)及主要代謝通路/網絡存在較大差異,因此,中藥成分在不同種屬中的代謝過程及關鍵影響因素往往存在較大差異,這直接導致動物實驗結果與臨床數據間的不匹配[6]。因模型選擇的不匹配性,重復性研究往往變成為不斷創新的探索性研究。
3 體外模型的缺陷
在對中藥材人源性毒性的研究中,因模型存在著各種局限及困難,例如,體外研究常常因使用細胞而將組織或器官特征簡單化,是不同來源器官或組織特征同質化,例如只有線粒體代謝,其他特征性代謝的信息缺失,如果再缺乏針對性的評價指標及技術方法,其提供的毒性信息十分有限。體外研究模式的不確定性或者說在學術界并未形成學術共識,這導致大量的新穎的體外模型不斷引入,但研究的系統性、目標性與規范性極差。其中體外模型及其缺陷還存在大量的技術障礙。
體外模型指的是在體外對人體的生理環境進行模擬,進而揭示疾病本身的發生發展,或者借以體外模型對相關治療藥物的藥理學或毒理學機制進行研究。在科學研究中,體外模型建模依據的多樣性也決定了其具體模型的多樣性及復雜性,同時隨著科學研究與日俱增的嚴謹性及準確性,體外模型也能更加精確的對體內真實情況進行模擬,且體外模型簡便易行,實驗條件容易控制,在藥物的機制研究上能極大程度的減少類似于體內反應所帶來的的連帶作用,如在研究藥物在腸道的吸收及轉運機制時,就常采用Caco2細胞模型對藥物的腸道吸收進行模擬,且Caco2模型也是最為常用的腸道轉運模型及上皮轉運模型[7]。
4 動物模型的缺陷
體內研究因使用動物,又常常忽視種屬差異、過程信息缺失、低通量高耗費、致毒機制不清、致毒過程不明、無法前瞻預測等缺點,且個體及臟器之間也存在巨大的差異,這就造成了中藥材人源性毒性的甄別產生巨大阻礙及困難。對于應用中藥動物模型,由于同樣缺乏系統評價,其中引發的問題更加嚴重[8]。
在一項對221起引起人類毒性反應的150種藥物的調查中發現,嚙齒動物和非嚙齒類動物與人類毒性反應陽性一致率為71%,其中非嚙齒類動物僅可預測63%的人類毒性反應,僅嚙齒類動物僅可預測43%的人類毒性反應[9]。
動物模型是指依靠實驗動物對疾病或者治療藥物對相關疾病治療情況進行模擬,以進一步闡釋其藥物在動物體內的作用。實驗動物和人的各器官系統不僅在形態上相似,而且生理解剖功能都與人體有一定的相似性,可極好的對人體各功能進行模擬,如皮膚、心血管系統、內分泌系統、胃腸道和泌尿系統,因此采用動物進行實驗為科學研究中必不可少的環節。動物胰腺的生理功能與人體類似,在糖的吸收、轉運和利用研究中可以用動物模型進行前期模擬[10-11],如豬的胰島素與人類的胰島素只差一個氨基酸,因此,用豬制作糖尿病模型對糖尿病的研究極其重要[12]。動物中有著與人類相似的細胞色素氧化酶P450系統,所以,在藥物的代謝研究中常用動物模型進行前期的探究[13]。
動物與人體之間種屬差異大,如多種CYP酶在物種間的表達和活性均存在差異[14]。生物體由多個系統組成,而各個系統又構成一個復雜的有機體,而人體是更為復雜且有感情的有機體,所以機體內所發生的都不是單一反應,均是復雜的級聯反應,這就使得了解簡單具體體內某一反應或某一通路變化變得困難,進而使得藥效預測能力較差,難以實現真實模擬人類反應的目的,因此,動物實驗只能作為藥物的臨床前研究模型,藥物的安全性及療效必須依靠臨床試驗得出最終結論。動物實驗費用高,且飼養條件要求也較高。
5 本研究團隊的策略與研究優勢
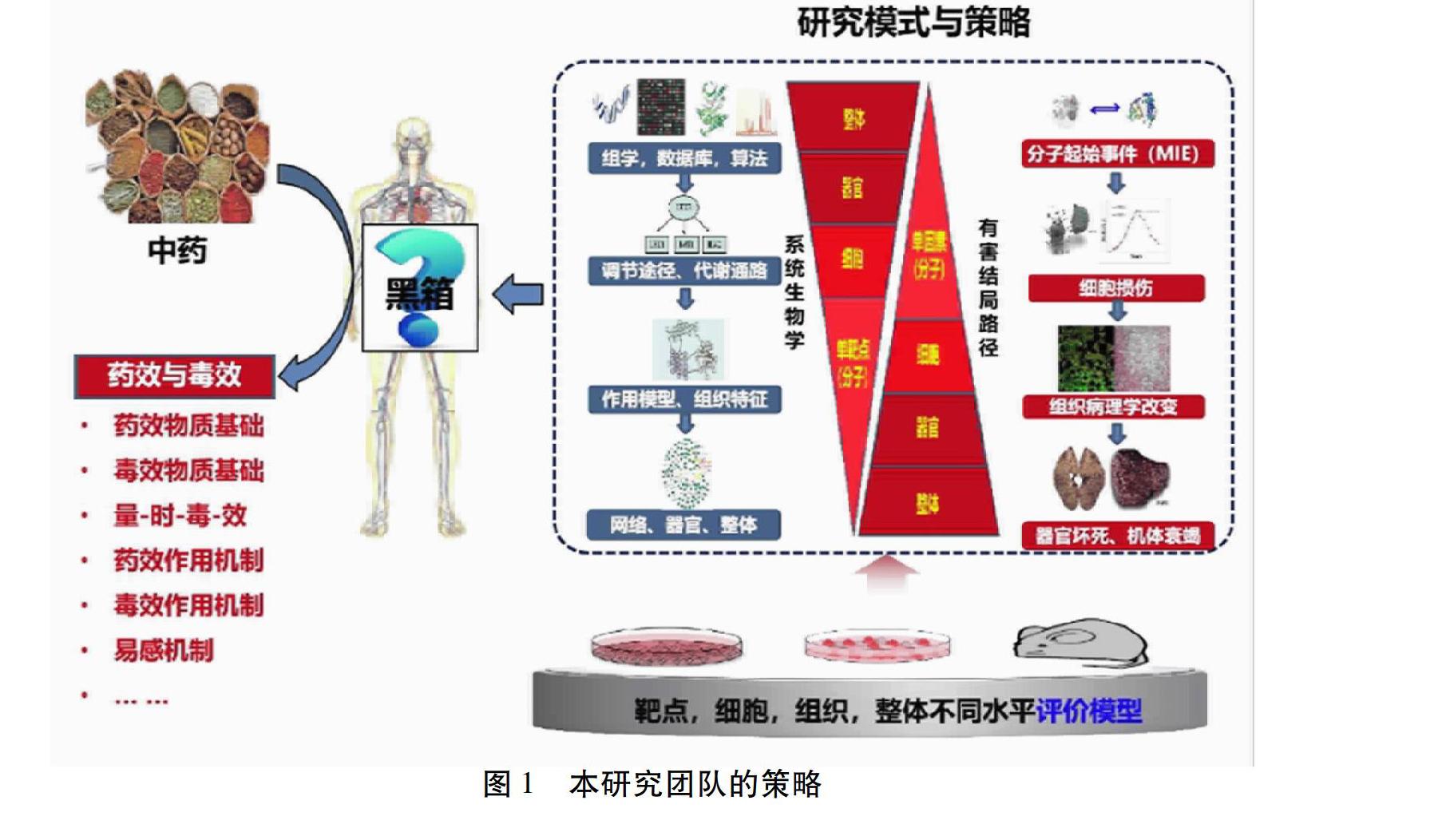
中藥材成分的復雜性直接決定了其作用于人體后藥效與毒效研究的難度和局限,同時機體的復雜內部環境也使得中藥的體內研究成為一個難以透視化及標準化的“黑箱”。本研究團隊一方面借以系統生物學從整體動物到單靶點(分子)對中藥的藥效及毒效進行研究。見圖1。采用組學、數據庫及各種算法篩選中藥復方或成分對機體的調節途徑及代謝通路,并進一步根據其作用模型及作用組織的特征對其在器官水平及整體水平上做出互作關系網絡圖,另一方面,有害結局路徑邏輯框架對中藥的作用進行預判,即從早期起始分子事件-亞細胞損傷-細胞生死-組織病理結構改變-終點效應間存在嚴格的邏輯與因果關系,也即組織病理結構改變這一有害結局出現前,微觀水平的代謝異常和細胞異常死亡等往往早已出現,因此,如果以毒性發生的“起始事件”、代謝紊亂、細胞生死異常凋亡/死亡為早期評判標準,則可能完成早期“有害結局”預判。本研究團隊擬通過以上策略及研究優勢闡明藥物各成分“黑箱操作”,進而推動中藥發展。
5.1 生物標志物 標志物首先是源于機體器官、組織、細胞、亞細胞器中的標志性或/和功能性分子。我們從標志物的相似性評價角度首先來規范與評價體內外模型的差異、人源性與動物種屬間差異性、臟
器組織細胞及亞細胞間的差異性。因此,標志物的選取是最核心的技術切入點,也是科學問題的落腳點。盡管病理學改變是目前毒性評價的金標準,但由于病理學改變往往發生在毒性的中后期、具有不
可逆性,因此,找到早期毒性的定量檢測指標,是藥物毒性研究首先需要解決的問題。通過分析代謝水平、細胞水平和組織整體水平毒性數據指標,篩選出可準確定量檢測的毒性特征性指標和生物標志物,能夠在毒性發生的早、中、晚期對毒性進行定量監測。再結合離體器官、細胞水平等體外技術及毒代動力學結果,揭示“有毒”中藥材的毒性劑量、靶器官、毒性物質基礎、制毒機制,多成分的相互作用規律。利用標志物,將機體(分子、細胞、組織與器官種類)的組成、結構與功能緊密結合,實現系統生物學水平的中藥毒物學與毒理學突破。
5.2 體外技術 依照人源性器官、組織、細胞的組成與結構要求,構建時空多維度一體化整合的微流控器官芯片[15-16],將檢測與反應體系整合進入芯片體系,實現生化、細胞與組織三水平工程上的生長、反應、控制與檢測的協調與統一。例如,通過將人源實質細胞與基質細胞共培養的方式,模擬器官的生理結構,構建系列“高仿生”動物/人源的肝、腎、腸、心、神經系統等微流控器官芯片以及多器官集成芯片;與組學等檢測技術相結合,構成能夠動態連續性多維度定性/定量評價中藥安全性與有效性微流控器官集成芯片。以模塊化的方式構建組織的器官微流控芯片系統,模擬藥物在體內的吸收(A)、分布(D)、代謝(M)和排泄(E)過程,測出藥時曲線,得到藥物的達峰時間、半衰期、消除速率常數等藥代動力學參數,并與動物實驗結果比較,取得可比性和關聯性,實現吸收、分布、代謝和消除等過程的參數測定。在整體毒性評判水平,逐漸形成一個具有普適性、接近或不低于實驗動物毒性評價能力與標準的體外模擬與研究平臺,應用于有毒中藥材的“量-時-毒-效”關系的評估。
5.3 體內技術 基于微流控器官芯片技術銜接人體與動物源、體外與體內研究體系,揭示并解決有毒中藥安全性和有效性[17]。利用公認的造模方法,在嚴格的質控標準指導下,建立與人源性毒性相匹配或相似度極高的動物毒性評判模型,具體目標是建立肝、腎、腸、神經、心臟毒性的動物模型;作為研究的陽性對照,檢測活體動物的各項指標,其中包括內源性物質與能量變化與外源性毒物及其代謝變化隨時間的同步監測體系,具體利用各種組學技術,對可能收集到的體液與組織樣本如尿液和血液中的內外源性相關代謝物進行定性定量分析,在對動物進行最終處理時,結合解剖與病理學結構形態學檢查,在時間上,將組成、功能與結構的變化同步。通過多變量數據分析,篩選出分子水平、細胞水平、組織水平等多水平的差異性指標,結合同步的功能性變化,解析毒性發生、發展的機制。在理念上,高度正視傳統采用動物試驗方法進行毒性研究的缺陷。特別是注意試驗結果的簡單種屬間外推或經驗性外推[18]。
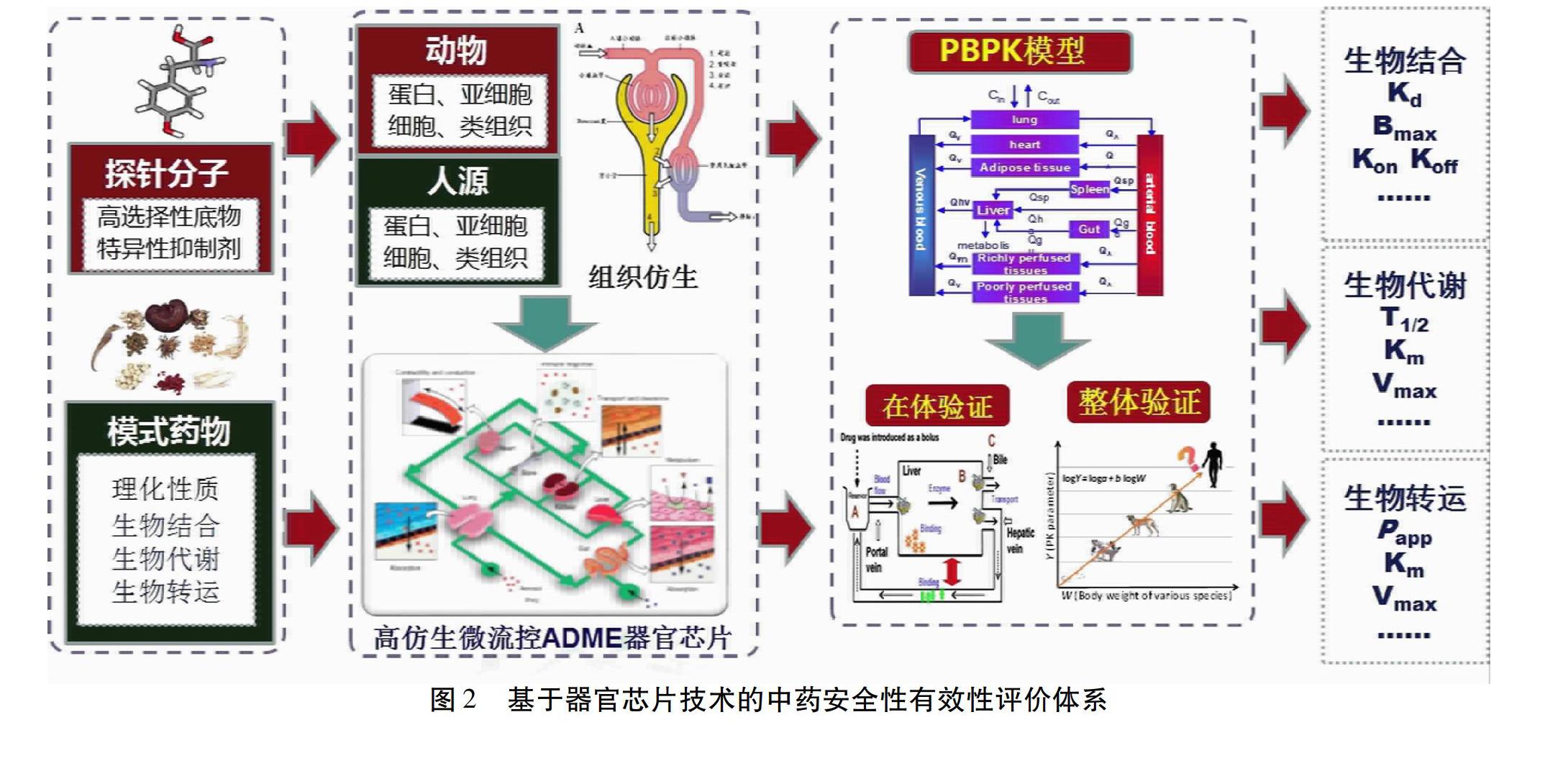
5.4 多系統毒性的“量-時-效-毒”信息與數據的整合 利用體外和整體動物的數據構建模式動物的整體PBPK-PD/TK模型,預測單味藥材單成分、多成分在血漿及肝腎等重要毒靶器官的暴露量的經時變化關系和多成分互作關系;在此基礎上,整合用藥劑量、毒效和暴露量數據,構建單味藥材的整體量-時-效關系,對多系統毒性的量-時-效-毒關系進行人體內動力學行為的定量預測,為臨床合理用藥提供可靠準確的資料。見圖2。
評價細胞活性及毒性效應是中藥人源性毒性的評價手段之一。通過分子、細胞、組織水平上毒效標志物的確立和驗證,例如,早期毒性標志物的建立,通過對體外人源細胞/類組織與組學分析技術的結合,以代謝異常及亞細胞特征性標志物的異常泄露,結合各組學數據和組織病理學、生化指標,從而可準確定量檢測的毒性生物標志物,能夠在毒性發生的各個時期對毒性進行定量監測。通過構建動物模型,對有毒中藥進行量時毒效關系評價以及相關整體實驗與驗證。再在體外代謝中研究建立不同毒性靶器官的有害結局評價方法,分別采用血液生化與組織學指標進行比較研究。構建模式動物的整體PBPK-PD/TK模型,進行人體內源性物質代謝譜與外源性物質代謝譜間的動力學行為整合,形成定量預測模型。通過系統藥理學和網絡藥理學技術,對特定的分子水平、細胞水平、組織水平等多水平的毒物靶點進行整合,整合各種體內外模型構建技術,以及針對相應毒效指標及標志物開發建立的組學、酶活檢測、組織病理檢查等定性定量檢測技術,進而預測和評價中藥成分-機體、成分相互、量-毒關系,闡明有毒中藥成分在體內的效應物質基礎和多成分互作關系,預測這些成分在人體的“量-時-毒-效”關系,可以確定中藥的安全用藥范圍及可能的易感物質和易感機制。
基于生物信息學和網絡藥理學技術的毒性成分預測和分析是對實驗的必要補充。1)利用前期開發計算ADME技術和藥物體內半衰期數學模型,確定候選有毒成分。借助系統藥理學和網絡藥理學技術,預測多成分之間的互作關系及其所產生的不良反應,借此剖析中藥單味藥以及復方內有毒成分群;2)采用人工智能、機器學習以及現代統計理論構建人體主要臟器藥物毒性數學模型、構建人體多臟器生物富集模型。開展和完善前期所開發的化學成分在多個臟器內(主要包括腸、肝腎、大腦等)分布、富集預測數學模型。借助前期開發的藥物靶點預測方法,開展有毒中藥多成分毒性互作蛋白的預測和驗證研究,以鎖定毒物靶點,揭示有毒中藥的易感分子機制;3)開展基于靶點和通路作用的有毒成分毒性分級評價。借助基元動力學技術結合網絡藥理學分析工具,構建定量預測和評價多成分互作量-毒關系。
5.5 有毒中藥的毒性將怎樣進行研究? 目前,有毒中藥材其毒性分為3級:“有大毒”“有毒”“有小毒”,這一種模糊定量概念。中藥產生毒性的機制復雜多樣,何種藥材中的何種成分會導致毒性,這是需要首先定性的問題。我們從以下幾方面來展開:1)物質基礎的分析與確定;2)主要靶細胞模型與生物標志物的選擇;3)代謝或轉運干擾機制以及引發的多成分或藥藥相互作用模型;4)整體內動力學變化過程與毒性產生動力學間的關系。
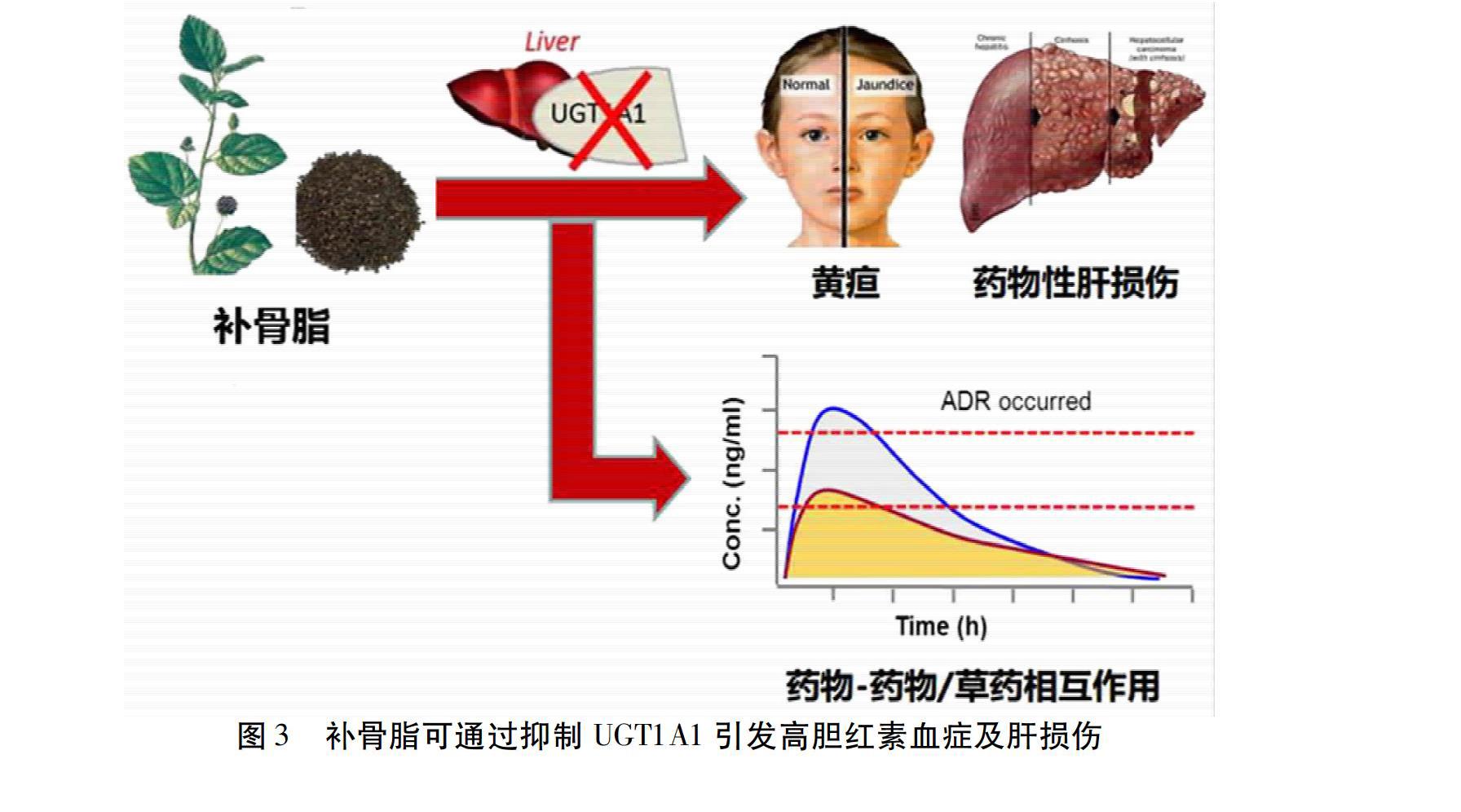
尿苷二磷酸葡萄糖醛酸轉移酶(Uridine 5′-diphospho-glucuronosyltransferase,UGTs)是一種緊密相連細胞膜內表面且存在于細胞內質網腔內的膜蛋白,主要分布在肝臟和腸道中,介導多種葡萄糖醛酸結合反應[19]。眾多UGTs亞型中,只有尿苷二磷酸葡萄糖醛酸轉移酶(UGT1A1)酶能代謝肝臟中膽紅素,通過促進葡萄糖醛酸與間接膽紅素接合,并將其轉化為直接膽紅素[20]。UGTIA1在維系機體內源性物質的代謝平衡中發揮的作用是至關重要的,它介導了大量藥物、毒物或致癌物質的代謝清除。但是,當UGT1A1活性受到抑制時,將會導致內源性物質膽紅素代謝紊亂,還能夠引起臨床上不良的藥物/草藥-藥物相互作用,從而引發多種與人體密切相關的疾病,如黃疸、高膽紅素血癥、肝毒性、神經毒性等[14]。例如,中藥及其活性成分會通過抑制UGT1A1的活性導致高膽紅素血癥及引發其他不良反應,諸如補骨脂、首烏、穿心蓮等提取物均可以強效抑制UGT1A1[21-22]。見圖3。
總之,針對“有毒”中藥材的藥效物質、毒性成分、安全用藥劑量尚未明確等問題,結合人源性毒性發生特點、選擇明確的標志物、建立高仿生微流控整合體外技術,完成體外的初步篩選;明確目標毒性,建立一套質控系統,選擇與人體體系相似的模型動物,通過系統生物如組學技術,開展目標物質的“量-時-毒-效”關系研究,確定安全用藥范圍、易感因素與和機制;最終建立毒-效關系的中藥質量控制標準,建立符合中醫藥特點的中藥安全性評價模式和技術體系。見圖4。為臨床合理用藥和建立有效的質量控制標準提供科學依據。
參考文獻
[1]Luo X,Chen X,Shen X,et al.Rapid identification and analysis of the active components of traditional Chinese medicine Xiaoxuming decoction for ischemic stroke treatment by integrating UPLC-Q-TOF/MS and RRLC-QTRAP MSn method[J].J Chromatogr B Analyt Technol Biomed Life Sci,2019,1124:313-322.
[2]閆曉哲.中藥炮制方法對中藥飲片臨床療效的影響[J].深圳中西醫結合雜志,2020,30(18):52-53.
[3]張宏,谷偉玲.中藥炮制對其化學成分及臨床應用的作用探討[J].當代化工研究,2020,10(19):167-168.
[4]肖小河,李秀惠,朱云,等.中草藥相關肝損傷臨床診療指南[J].中國中藥雜志,2016,41(7):1165-1172.
[5]金若敏.中藥肝毒性的評價與思考[A].中國毒理學會、臺灣毒物學學會.2019年海峽兩岸暨港澳青年科學家毒理學學術交流會論文集[C].中國毒理學會、臺灣毒物學學會:中國毒理學會,2019:2.
[6]Wang YQ,Shang XF,Wang L,et al.Interspecies variation of clopidogrel hydrolysis in liver microsomes from various mammals[J].Chem Biol Interact,2020,315:108871.
[7]Hulbert ML,Shenoy S.Hematopoietic stem cell transplantation for sickle cell disease:Progress and challenges[J].Pediatr Blood Cancer,2018,65(9):e27263.
[8]唐素勤,于國俊.中藥腎毒性原由及應對策略探析[J].中藥與臨床,2020,11(4):30-33,46.
[9]Harry Olson,Graham Betton,Denise Robinson,et al.Concordance of the Toxicity of Pharmaceuticals in Humans and in Animals[J].Regul Toxicol Pharmacol,2000,32(1):56-67.
[10]Iansante V,Mitry RR,Filippi C,et al.Human hepatocyte transplantation for liver disease:current status and future perspectives[J].Pediatr Res,2018,83(1-2):232-240.
[11]atej M,Zupani Slavec Z.Development of homologous skin,bone and other soft tissues transplantation in Slovenia[J].Acta Med Hist Adriat,2017,15(1):151-158.
[12]古展輝,郭姣.實驗小型豬2型糖尿病模型的研究進展[J].廣東藥科大學學報,2019,35(2):301-306.
[13]Bodzin AS,Baker TB.Liver Transplantation Today:Where We Are Now and Where We Are Going[J].Liver Transpl,2018,24(10):1470-1475.
[14]Llull R,Murase N,Ye Q,et al.Chimerism,graft-vs-host disease,rejection,and their association with reciprocal donor-host immune reactions after cell,organ,and composite tissue transplantation[J].Transplant Proc,1997,29(1-2):1203-1204.
[15]Noor N,Shapira A,Edri R,et al.3D Printing of Personalized Thick and Perfusable Cardiac Patches and Hearts[J].Adv Sci(Weinh),2019,6(11):1900344.
[16]Maares M,Haase H.A Guide to Human Zinc Absorption:General Overview and Recent Advances of In Vitro Intestinal Models[J].Nutrients,2020,12(3):762.
[17]曲玥陽,鄧九,王帥,羅勇.基于腎、肝和心臟芯片的藥物毒性鑒定新方法[A].中國毒理學會中藥與天然藥物毒理專業委員會.中國毒理學會中藥與天然藥物毒理專業委員會第二次(2017年)學術交流大會論文集[C].蘇州:中國毒理學會中藥與天然藥物毒理專業委員會:中國毒理學會,2017:1.
[18]蔡樂.基于肝器官芯片的中草藥成分肝毒性評價[D].大連:大連理工大學,2019.
[19]Tukey RH,Strassburg CP.Human UDP-glucuronosyltransferases:metabolism,expression,and disease[J].Annu Rev Pharmacol Toxicol,2000,40:581-616.
[20]Lv X,Xia Y,Finel M,et al.Recent progress and challenges in screening and characterization of UGT1A1 inhibitors[J].Acta Pharm Sin B,2019,9(2):258-278.
[21]劉新豫,呂俠,吳敬敬,等.膽紅素代謝酶UGT1A1介導的中藥不良反應研究進展[J].藥物評價研究,2018,41(5):716-726.
[22]Wang XX,Lv X,Li SY,et al.Identification and characterization of naturally occurring inhibitors against UDP-glucuronosyltransferase 1A1 in Fructus Psoraleae(Bu-gu-zhi)[J].Toxicol Appl Pharmacol,2015,289(1):70-78.
(2020-11-19收稿 責任編輯:王明)

