口服細胞穿膜肽Penetratin對小鼠肝臟、腎臟和腸道的急性毒性反應研究
魏振宇 李林 尉秀清
【摘要】目的 研究口服細胞穿膜肽Penetratin對小鼠肝臟、腎臟以及腸道的急性毒性反應,評估其安全性。方法 將24只Balb/c雄性小鼠隨機分為正常對照組、低劑量組和高劑量組3組,每組各8只小鼠。各組小鼠均予正常飲食,其中正常對照組予200 μl生理鹽水灌胃,低劑量組、高劑量組分別予200 μl由生理鹽水配制的濃度為5、100 μmol/L的Penetratin灌胃。各組小鼠予不同處理24 h后收集標本,采集標本為小鼠的血液、肝臟、腎臟以及腸道組織,用生化法檢測各組小鼠血清中ALT、AST、尿素氮、肌酐水平,用ELISA檢測血清中二胺氧化酶(DAO)及脂多糖的含量,用實時熒光定量PCR方法檢測肝臟、腎臟及腸道炎癥因子TNF-α、IL-1β、IL-6以及IL-10的mRNA表達水平,用HE染色評估肝臟、腎臟以及腸道病理損傷情況,TUNEL法檢測肝臟、腎臟以及腸道細胞凋亡情況。結果 各組小鼠的ALT、AST、尿素氮、肌酐水平、DAO及脂多糖含量、炎癥因子TNF-α、IL-1β、IL-6以及IL-10的mRNA表達水平比較差異均無統計學意義(P均> 0.05);與正常對照組對比,低劑量組和高劑量組各臟器均未見明顯損傷及炎性細胞浸潤,細胞凋亡無明顯增多。結論 口服細胞穿膜肽Penetratin對小鼠的肝臟、腎臟以及腸道均無明顯急性毒性反應,作為腸道促吸收劑安全性較好。
【關鍵詞】細胞穿膜肽,Penetratin;組織損傷;炎癥;細胞凋亡
【Abstract】Objective To observe the acute toxic reaction and evaluate the safety of oral cell-penetrating peptide Penetratin in mouse liver, kidney and intestine. Methods Twenty-four male Balb/c mice were randomly and evenly divided into the normal control, low-dose and high-dose groups. All mice in each group were given a normal diet. In the control group, the animals were gavaged with 200 μl of physiological saline. In the low-dose group, the mice were gavaged with 200 μl of Penetratin at a concentration of 5 μmol/L,?and 200 μl of 100 μmol/L Penetratin was given in the high-dose group. The blood, liver, kidney and intestinal samples were collected 24 h later. The expression levels of ALT, AST, BUN, and Cr in the mouse serum in each group were measured by biochemical methods. The levels of diamine oxidase (DAO) and lipopolysaccharide (LPS) were detected by ELISA. The expression levels of inflammatory cytokines including TNF-α, IL-1β, IL-6 and IL-10 mRNA in each organ were detected by RT-PCR. The pathological injury of liver, kidney and intestinal tissues was evaluated by HE staining. The cellular apoptosis of each organ was detected by TUNEL staining. Results The expression levels of ALT, AST, BUN, Cr, the contents of DAO and LPS, and the expression levels of TNF-α, IL-1β, IL-6 and IL-10 ?mRNA did not significantly differ among three groups (all P > 0.05). Compared with the normal control group, no significant pathological injury or inflammatory cellular infiltration was observed and the cellular apoptosis was not significantly aggravated in the low-dose and high-dose groups. Conclusion Oral cell-penetrating peptide Penetratin yields no evident acute toxicity in mouse liver, kidney and intestine, and it can serve as a safe intestinal absorption enhancer.
【Key words】Cell-penetrating peptides,Penetratin;Tissue damage;Inflammation;Cellular apoptosis
細胞穿膜肽(CPP)是一類長度一般為5 ~ 30個氨基酸殘基,能夠攜帶大分子物質穿過細胞膜或組織屏障的短肽[1]。Penetratin是一種含有16個氨基酸(RQIKIWFQNRRMKWKK)的CPP,能夠以不依賴能量的形式攜帶生物大分子有效地穿過細胞膜[2-3]。CPP可通過內吞或直接穿透等機制運載小分子、核酸、蛋白質、顯影劑、藥物等進入細胞內發揮其效應功能,具有生物相容性好、完成入胞轉運后可降解、可定向設計和改造等優點,目前已經成為靶向治療藥物遞送載體的研究熱點[4]。國內外已有不少研究表明,將CPP與生物活性蛋白直接混合或利用基因工程技術進行重組融合表達,具有促進不吸收或低吸收藥物的腸道吸收、皮膚滲透的作用[5-6]。
盡管CPP在生物醫藥領域展現出了廣闊的應用前景,但是其安全性問題仍然不容忽視,目前尚缺乏口服Penetratin安全性的有力證據,本文擬通過研究口服Penetratin對小鼠肝臟、腎臟以及腸道的急性毒性反應,評估其安全性,為后續運用Penetratin作為腸道促吸收劑提供一定的實驗支撐。
材料與方法
一、實驗動物
無特定病原體(SPF) Balb/c小鼠24只,雄性,6 ~ 8周齡,體質量20 ~ 30 g,動物來源為江蘇集萃藥康生物科技有限公司,許可證號:SCXK(蘇)2018-0008,動物合格證號:1107271911000884,飼養于暨南大學實驗動物中心,實驗單位使用許可證編號:SYXK(粵)2017-0174,動物實驗倫理編號:IACUC-20191122-11。實驗期間嚴格遵循實驗動物中心的管理指南和行為規范,所有操作均符合實驗動物倫理。
二、實驗試劑和儀器
1.主要試劑
Penetratin(Glpbio,美國)、小鼠二胺氧化酶(DAO)ELISA試劑盒(MEIMIAN,上海)、小鼠脂多糖 ELISA試劑盒(MEIMIAN,上海)、Trizol 試劑盒(Thermo Fisher,美國)、逆轉錄試劑盒(Invitrogen,美國)、SYBR? Green Realtime PCR?Master Mix 酶(TOYOBO,日本)、HE染料 (Leagene,北京),TUNEL試劑盒(Servicebio,武漢)。
2.主要儀器
多功能酶標儀(美谷分子儀器,上海),紫外分光光度計(Thermo Scientific,美國),Light Cycler 480Ⅱ實時熒光定量PCR儀(Roche,美國),低溫高速冷凍離心機(Eppendorf,德國),熒光倒置顯微鏡(Leica,德國)。
三、實驗方法
1.實驗動物的分組與干預
將24只經過暨南大學實驗動物管理中心隔離檢疫及適應性喂養10 d的Balb/c雄性小鼠隨機分為正常對照組、低劑量組和高劑量組3組,每組各8只小鼠。各組小鼠均予正常飲食,正常對照組予200 μl生理鹽水,低劑量組予200 μl由生理鹽水配制的濃度為5 μmol/L的Penetratin,高劑量組予200 μl由生理鹽水配制的濃度為100 μmol/L的Penetratin。給藥方式均為灌胃,各組小鼠均給藥1次,24 h后收集標本進行相應檢測。
2. 標本的采集與處理
各組小鼠予相應干預24 h后,用1%戊巴比妥鈉溶液對小鼠進行腹腔注射,充分麻醉后采用眼眶取血法將血液收集至提前備好的真空收集管中并做好標記,每個標本分裝2管,室溫靜置1 h后離心收集血清,保存于-80℃冰箱備用;取血后對小鼠進行解剖,迅速分離取下肝臟、腎臟以及腸道組織,用液氮速凍,保存于-80℃冰箱中備用,待提取RNA用作后續檢測,另取部分組織放入組織固定液中固定,用于制作石蠟標本。
3. 血液標本的檢測
將此前保存于-80℃冰箱中的血清標本取出,1管送至廣州剪刀手基因科技有限公司用生化法檢測ALT、AST、尿素氮和肌酐水平,1管分別用小鼠DAO ELISA試劑盒、小鼠脂多糖 ELISA試劑盒檢測DAO及脂多糖水平;每個樣本做2個復孔。
4.組織細胞的RNA提取、cDNA逆轉錄及實時熒光定量PCR擴增
取出液氮中保存的組織,先按照Trizol試劑說明書的步驟對組織細胞中RNA的進行提取,并用紫外分光光度計測定提取的RNA 濃度及純度,然后按照逆轉錄試劑盒說明書將RNA 逆轉錄合成cDNA,選取β-actin為內參基因,通過Primerbank網站查找各目的基因以及內參基因的PCR引物序列,交由北京六合華大基因科技有限公司合成,應用 SYBR Green 法對TNF-α、IL-1β、IL-6以及IL-10進行RT-PCR擴增。每組隨機選取3只小鼠,每個樣本做3個復孔,用2-△△CT法對數據進行相應處理,對正常對照組進行均一化處理后設定為相對數“1”,以此為參照分析相應炎癥因子的相對mRNA表達水平。
5. HE染色
將石蠟切片,經過脫蠟和階梯水化后,用蘇木素染細胞核1 ~ 3 min,然后在流動的蒸餾水中洗去多余的染液,1%的鹽酸乙醇分化數秒,自來水沖洗,磷酸鹽吐溫緩沖液返藍,流水沖洗,伊紅復染30 ~ 60 s后進行漂洗,最后用中性樹膠進行封片,在顯微鏡下采集圖像。
6. TUNEL 檢測及凋亡指數
參照操作說明書對各組織的切片進行染色,顯色后陽性細胞在熒光顯微鏡下呈綠色。每張切片隨機選取10 個高倍視野(×400),計算陽性細胞數和組織細胞總數,凋亡指數 = 陽性細胞數/組織細胞總數 ×100%。
四、統計學處理
應用SPSS 24.0進行統計學分析。計量資料以表示,多組間比較應用單因素方差分析,P < 0.05為差異有統計學意義。
結果
一、各組小鼠血液中ALT、AST、尿素氮、肌酐、DAO及脂多糖水平比較
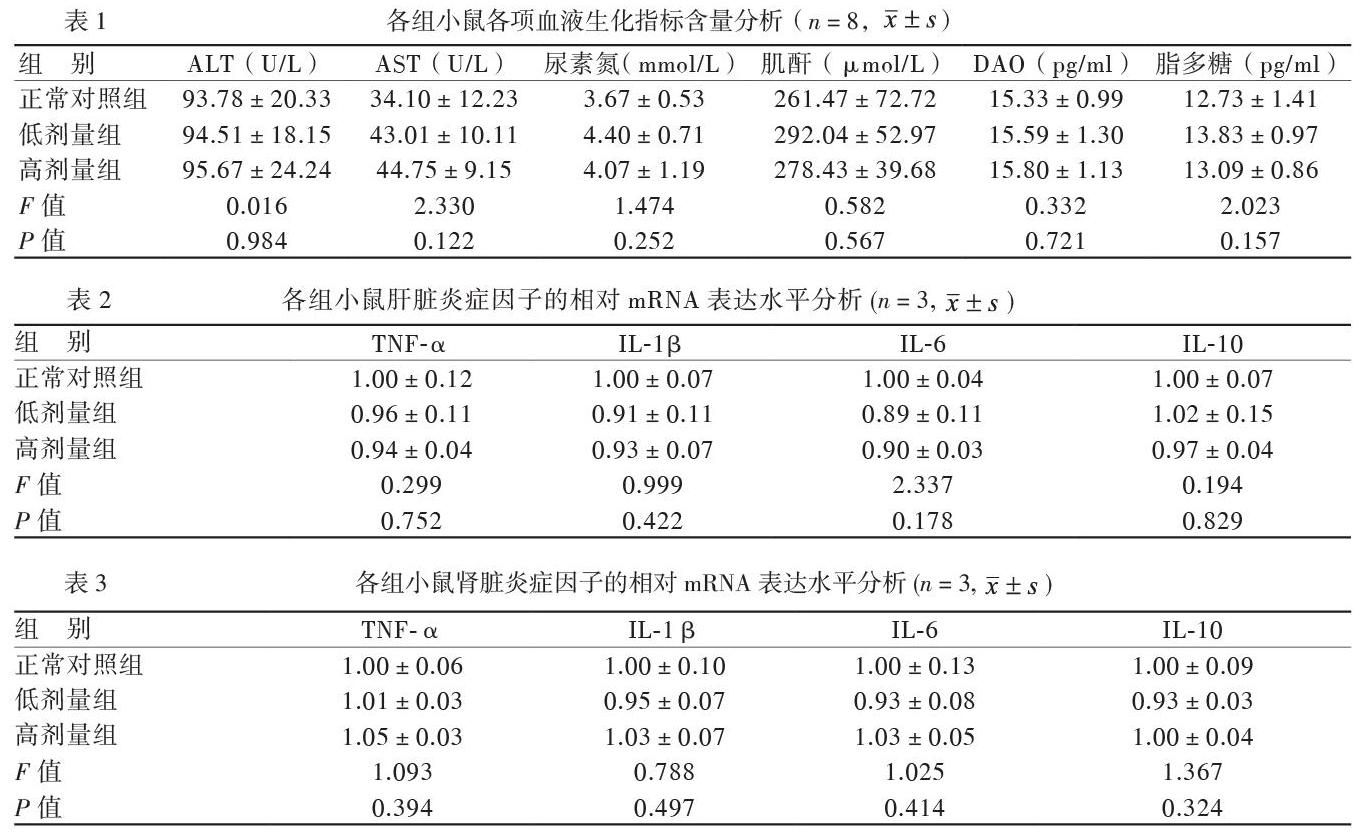
對各組小鼠的各項血液生化指標進行統計歸納,通過單因素方差分析可知,正常對照組、低劑量組與高劑量組3組小鼠血清中ALT、AST、尿素氮、肌酐、DAO及脂多糖水平比較差異均無統計學意義(P均> 0.05),見表1。
二、各組小鼠肝臟、腎臟、腸道組織中炎癥因子的相對mRNA表達水平
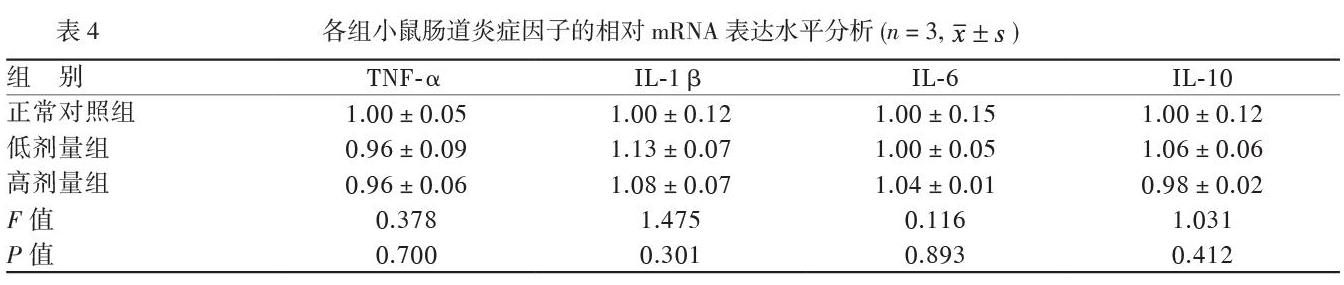
從每組小鼠中隨機選取3只小鼠對其相應臟器的RNA進行炎癥因子TNF-α、IL-1β、IL-6及IL-10的RT-PCR擴增,對所得數據進行統計分析,各組小鼠相應臟器中炎癥因子TNF-α、IL-1β、IL-6和IL-10的相對mRNA表達水平比較差異均無統計學意義(P均> 0.05),見表2、3、4。
三、各組小鼠肝臟、腎臟、腸道組織的病理損傷評估
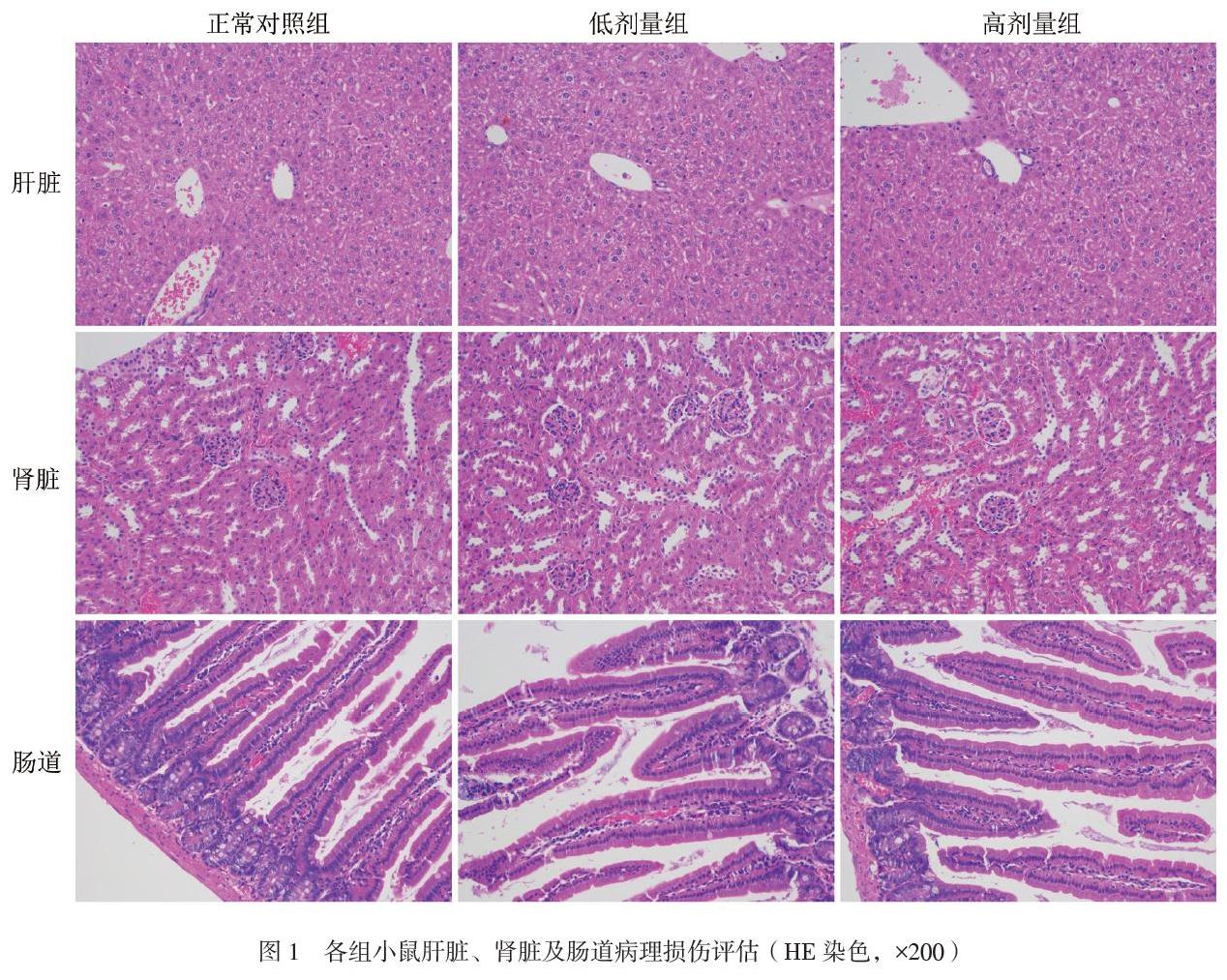
各組小鼠的肝臟HE染色情況:與正常對照組相比,低劑量組和高劑量組肝細胞無水腫、壞死,肝小葉結構完整,肝竇間隙正常,未見明顯肝內淤血及炎性細胞浸潤。腎臟HE染色情況:與正常對照組相比,低劑量組和高劑量組腎小球形態正常,無明顯體積增大或細胞數增多,腎小管上皮細胞無水腫、壞死,系膜細胞無明顯增多,未見明顯淤血腫脹和炎癥細胞浸潤。腸道HE染色情況:與正常對照組相比,低劑量組和高劑量組小腸層次分明,絨毛形態正常,腺體結構清晰,無明顯腫脹充血和上皮細胞脫落,固有層未見明顯淋巴細胞、漿細胞浸潤,見圖1。
四、各組小鼠肝臟、腎臟及腸道的細胞凋亡情況
各組小鼠的肝臟TUNEL染色結果顯示,正常對照組、低劑量組和高劑量組均未見TUNEL明顯凋亡的陽性信號,未能計算凋亡指數,各組小鼠肝臟、腎臟及腸道的細胞凋亡并無顯著性差異,見圖2。
討論
CPP的安全性問題是可能限制其臨床應用的一大重要因素,主要包括免疫原性以及質膜擾動可能引起的細胞毒性問題等[7]。Penetratin作為CPP中的一種,其安全性也受到了廣泛的關注。一些學者認為Penetratin作為腸道促吸收劑在轉運目的蛋白或藥物的同時,也可能促進腸道內的內毒素等有害物質的吸收,從而引起肝臟等臟器的損傷[8]。Nielsen等[9]通過動物實驗對Penetratin可否引起小鼠的肝臟損傷進行了研究,結果表明Penetratin攝入對小鼠肝臟無明顯毒性,但其并未對Penetratin的腎臟和腸道毒性以及Penetratin的劑量與其毒性反應是否相關作進一步研究。
在本次研究中,我們關注的焦點不僅僅是Penetratin的肝臟毒性,還包括其腎臟毒性和腸道毒性,腎臟和肝臟一樣都是研究藥物急性毒性反應和機體代謝的重要器官,而腸道作為直接與口服藥物接觸的第一道屏障,是本次研究必需關注的一個重要方面。除此之外,我們還關注Penetratin的劑量與其毒性反應是否相關,并通過設置了不同濃度的Penetratin處理組嘗試加以探討。
為研究Penetratin是否具有急性肝毒性,我們首先利用生化法檢測了提示急性肝損傷的敏感指標ALT和AST,相應地,為研究其對腎臟和腸道是否具有急性毒性反應,反映急性腎臟損傷的敏感指標尿素氮和肌酐以及反映急性腸道損傷的敏感指標 DAO和脂多糖也被納入了我們的檢測之中。這些檢測的結果顯示,正常對照組與低劑量組和高劑量組之間的差異均無統計學意義,表明口服Penetratin并未對小鼠的肝臟、腎臟和腸道造成急性損傷。
我們又對肝臟、腎臟、腸道組織中炎癥因子TNF-α、IL-1β、IL-6及IL-10進行RT-PCR擴增,并對其相對mRNA表達水平進行統計分析,得到了Penetratin未引起相應組織炎癥的結果,也進一步證實了我們的結論。最后,為了能夠更直觀的觀察正常對照組和不同處理組之間的相應臟器是否存在組織形態異常或細胞凋亡的差異,我們還對肝臟、腎臟和腸道組織進行了HE和TUNEL染色,通過觀察比較我們發現,與正常對照組相比,低劑量組和高劑量組相應臟器均未見明顯的病理改變,也未見明顯的細胞凋亡增多,提示Penentratin未引起急性的組織損傷或凋亡。
綜上所述,本研究通過對Penetratin高低劑量的設置,采用反映不同臟器急性毒性損傷和炎癥反應的敏感指標,并結合直觀的組織改變和細胞凋亡情況,比較系統地證實了口服Penetratin對小鼠的肝臟、腎臟以及腸道均無明顯急性毒性反應,其作為腸道促吸收劑的安全性良好,這無疑為后續研究的開展奠定了堅實的基礎。但必須指出的是,僅僅研究口服Penetratin對小鼠肝臟、腎臟以及腸道的急性毒性反應還存在著一定的局限性,下一步我們將繼續利用動物實驗對口服Penetratin的慢性毒性進行研究,以期對其作為腸道促吸收劑的安全性作出更為全面和整體的評估。
參 考 文 獻
[1] Wang F, Wang Y, Zhang X, Zhang WJ, Guo S, Jin F. Recent progress of cell-penetrating peptides as new carriers for intracellular cargo delivery. J Control Release, 2014, 174:126-136.
[2] Joliot A, Pernelle C, Deagostini-Bazin A. Prochiantz A. Antennapedia homeobox peptide regulates neural morphogenesis. Proc Natl Acad Sci U S A, 1991, 88(5):1864-1868.
[3] Pescina S, Ostacolo C, Gomez-Monterrey IM, Sala M, Bertamino A, Sonvico F, Padula C, Santi P, Bianchera A, Nicoli S. Cell penetrating peptides in ocular drug delivery: state of the art. J Control Release, 2018, 284:84-102.
[4] Pooga M, Langel ?. Classes of cell-penetrating peptides. Methods Mol Biol, 2015, 1324:3-28.
[5] Rádis-Baptista G, Campelo IS, Morlighem JRL, MeloLM, Freitas VJF. Cell-penetrating peptides (CPPs): from delivery of nucleic acids and antigens to transduction of engineered nucleases for application in transgenesis. J Biotechnol, 2017, 252:15-26.
[6] Kristensen M, Birch D, M?rck Nielsen H. Applications and challenges for use of cell-penetrating peptides as delivery vectors for peptide and protein cargos. Int J Mol Sci, 2016, 17(2).pii: E185.
[7] 謝洋洋,王邵娟,袁權,夏寧邵. 細胞穿膜肽研究應用的新進展. 生物工程雜志, 2019, 35(7): 1162-1173.
[8] Tünnemann G, Ter-Avetisyan G, Martin RM, St?ckl M, Herrmann A, Cardoso MC. Live-cell analysis of cell penetration ability and toxicity of oligo-arginines. J Pept Sci, 2008, 14(4): 469-476.
[9] Nielsen EB, Kamei N, Takeda-Morishita M. Safety of the cell-penetrating peptide penetratin as an oral absorption. Biol Pharm ?Bul, 2015, 38(1):144-146.
(收稿日期:2019-12-18)
(本文編輯:楊江瑜)

