基于網絡藥理學探討交泰丸治療失眠的作用機制
洪曹棟,尹 嘉,張 萌,門九章,馮 明
失眠(insomnia)是全球普遍存在的睡眠障礙,給人們身心健康帶來重大風險[1]。根據世界衛生組織(WHO)統計,全球睡眠障礙率達27%,在我國,成年人失眠發生率高達38.2%,超過3億人有睡眠障礙,且這個數據仍在逐年攀升[2]。失眠已成為影響人們生活質量的重要因素之一,甚至可能誘發交通事故等意外而危及個人及公共安全,對個體和社會都構成嚴重的負擔[3]。研究表明,失眠可以增加心血管代謝疾病的風險,包括血壓的變化、心率變異性受損等,增加死亡率[4]。因此,通過有效防治失眠,對于預防心血管代謝疾病發生、發展至關重要。現代臨床醫學以藥物治療為主,雖然短期內有效,但存在依賴性和耐受性, 停藥后療效無法持續的弊端;而中醫學治療失眠方法多樣,使用的方劑眾多,但其現代藥理作用機制尚不完全明確。因此,通過現代藥理學的思路研究中藥方劑的作用機制具有重要的意義[5]。中醫學認為失眠的病機變化與心、肝、脾、腎關系密切,病機的表現形式主要有肝火擾心、痰熱擾心、心脾兩虛、心腎不交型。腎是人體之根本,心腎相交是人體正常的氣機升降,若心腎不交即可表現出夜不能寐的病理癥狀。交泰丸是中醫內科中治療心腎不交型失眠的經典方劑。通過前期的研究發現,交泰丸的現代藥物成分復雜、靶點眾多,其作用機制尚不明確。因此,本研究利用網絡藥理學方法,建立交泰丸-成分-靶點-失眠癥交互作用網絡,詮釋交泰丸治療失眠的可能作用機制,為失眠的防治提供新的治療方法。
1 資料與方法
1.1 數據來源 本研究采用中藥系統藥理學分析平臺TCMSP數據庫(http://tcmspw.com/tcmsp.php),Batman數據庫(http://bionet.ncpsb.org/batman-tcm/),Swiss Target Prediction數據庫(http://www.swisstargetprediction.ch/),Gene Cards數據庫 (https://www.genecards.org/),STRING數據庫(https://string-db.org/),Venny 2.1在線軟件作圖工具平臺(https://bioinfogp.cnb.csic.es/tools/venny/),Uniprot數據庫(https://www.uniprot.org/),Cytoscape 3.7.1軟件,R 3.6.0軟件等。
1.2 研究方法
1.2.1 交泰丸活性成分與潛在靶點篩選 使用TCMSP、Batman數據庫檢索交泰丸中的黃連、肉桂2味中藥,并結合文獻收集藥物的化學成分及靶點信息,使用Uniprot數據庫,將靶點名稱進行矯正統一,并使用Swiss Target Prediction數據庫對靶點信息進行補充。
1.2.2 失眠疾病作用靶點篩選 使用Gene Cards數據庫以“失眠”為關鍵詞進行檢索,獲得疾病作用靶點,得到失眠的相關基因和靶點蛋白。與交泰丸潛在作用靶點相映射,得到交泰丸治療失眠的潛在靶點。 Gene Cards數據庫又稱為“人類基因數據庫”,是一個可搜索的集成數據庫,可提供有關所有帶注釋和預測的人類基因的全面、用戶友好的信息,包括基因組、轉錄組學、蛋白質組學、遺傳、臨床和功能信息[6]。
1.2.3 藥物-疾病共同靶點的篩選 在Venny 2.1在線軟件作圖工具平臺上分別錄入黃連、肉桂與失眠癥的靶點,繪制韋恩圖,得到藥物與疾病的共同靶點。
1.2.4 網絡模型的構建及分析 使用Cytoscape 3.7.1軟件,構建“藥物-成分-疾病-靶點”相互作用網絡圖,使用Network Analyzer功能對中藥復方的主要活性成分進行分析。
1.2.5 構建蛋白相關作用關系(PPI)網絡圖 將交泰丸-失眠疾病共同靶點輸入到STRING數據庫中進行檢索,選取置信度分數(minimum required interaction score)>0.4作為篩選條件,構建蛋白相互作用的PPI網絡,并根據蛋白之間的關聯度進行排序。
1.2.6 通路富集分析 在R軟件安裝Bioconductor軟件包“org.Hs.eg.db”并運行,將藥物-疾病共同靶點轉換成entrezID。然后在R軟件安裝“clusterProfiler”包,根據已轉換的entrezID,以P<0.05,Q<0.05進行關鍵靶基因的基因本體論(GO)與京都基因和基因組百科全書(KEGG)功能富集分析,并將結果以條形圖和氣泡圖形式輸出。
2 結 果
2.1 交泰丸的潛在活性成分 通過在TCMSP、Batman數據庫中檢索交泰丸中黃連、肉桂2味中藥的全部化學成分,根據在TCMSP數據庫中設定生物利用度(OB)≥30%、藥物相似性(DL)≥0.18,在Batman數據庫中設定Score cutoff≥20%,對黃連、肉桂的有效成分進行篩選,結合文獻[7]補充納入藥根堿,共得到有效活性成分34個,根據OB值排列前20位的活性成分信息見表1。其中黃連有15個有效活性成分,肉桂有19個有效活性成分,將活性成分對應的靶點輸入UniProt數據庫,并使用Swiss Target Prediction數據庫對靶點信息進行補充,刪除去重,共篩選出498個藥物靶點。
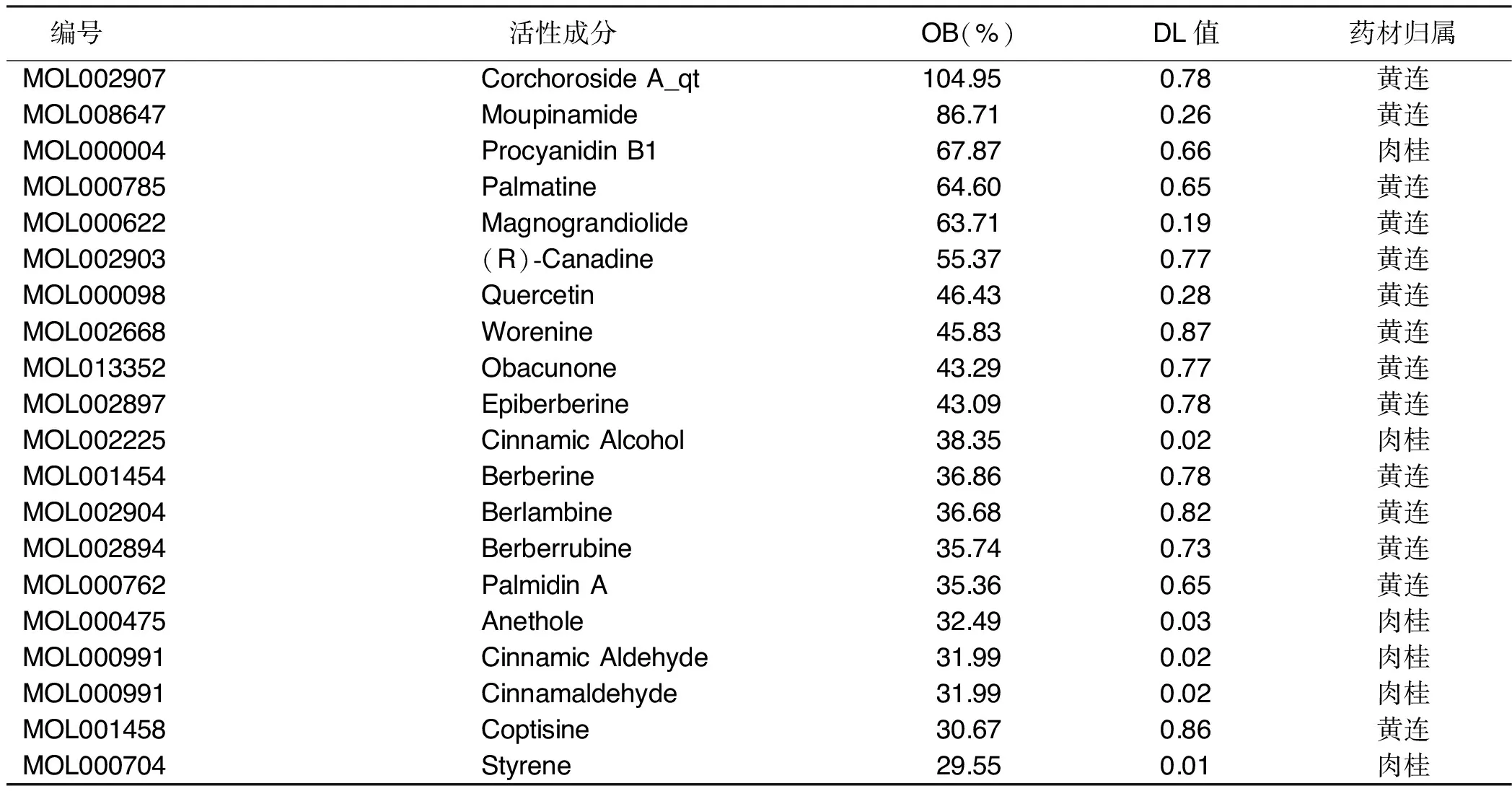
表1 復方中OB值前20位的活性成分基本信息
2.2 失眠疾病作用靶點篩選 以“失眠”為關鍵詞在Gene Cards數據庫進行檢索,去重后共獲得疾病靶點2 279個。
2.3 藥物-疾病共同靶點的篩選 在Venny 2.1在線軟件作圖工具平臺上輸入498個藥物靶點、2 279個疾病靶點,繪制韋恩圖,取交集后獲得藥物-疾病共同靶點160個(見圖1),其中黃連73個,肉桂108個,黃連-肉桂與失眠癥共同靶點基因21個(見圖2)。結果提示,交泰丸2味藥可能通過共同靶點的協調作用發揮治療失眠癥的效果。
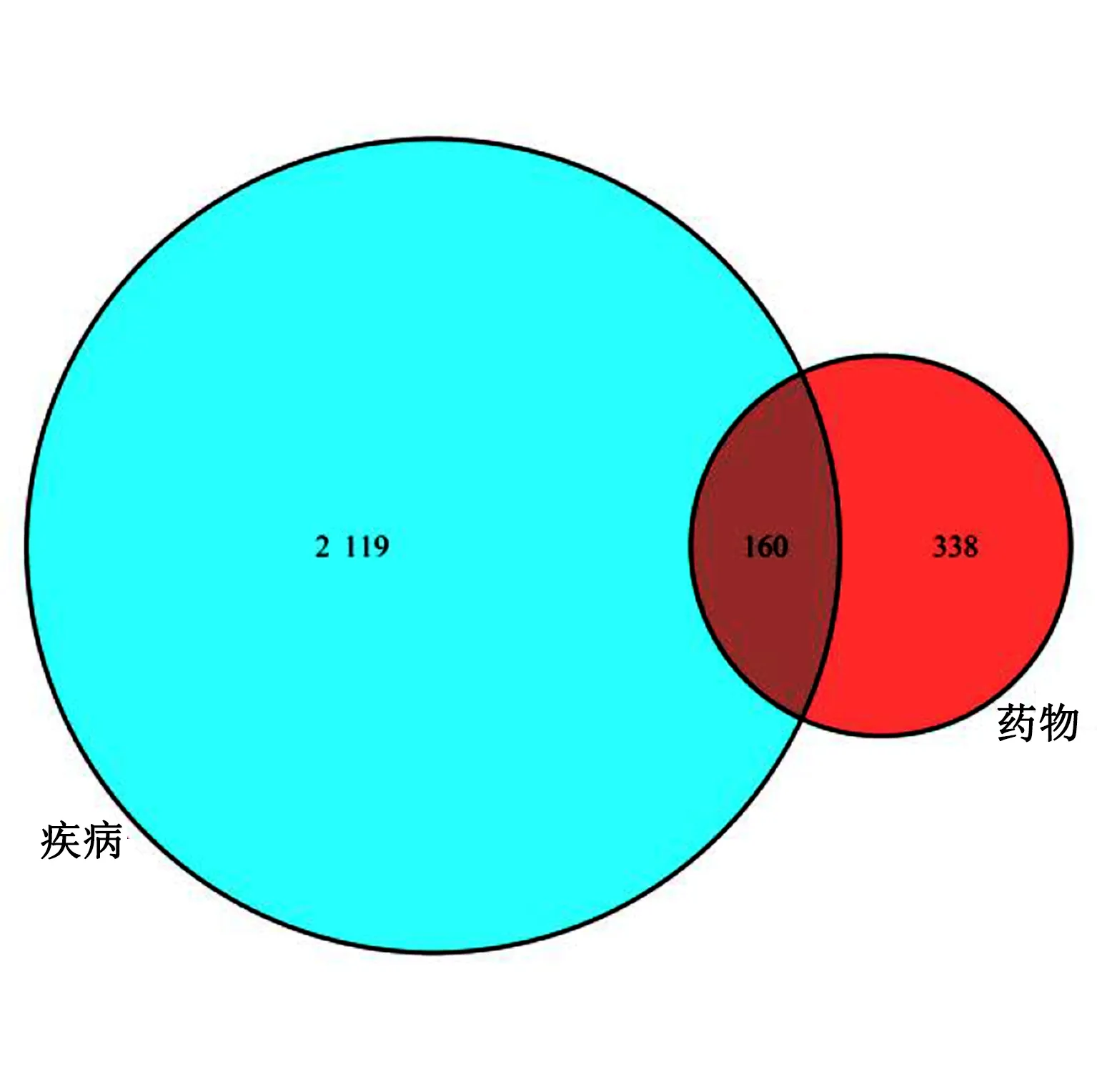
圖1 交泰丸-失眠共同基因靶點數
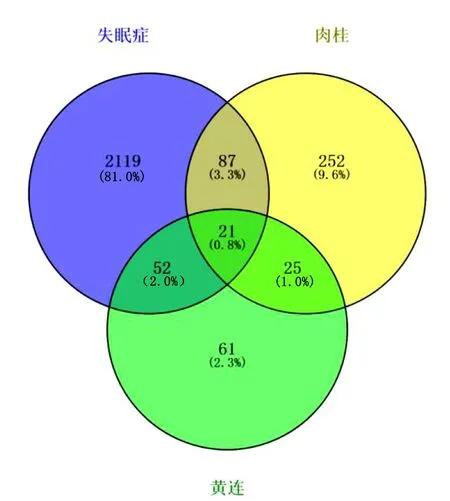
圖2 黃連-肉桂與失眠癥靶點韋恩圖
2.4 藥物-成分-靶點-疾病相互作用網絡模型的構建及分析 將中藥復方中34個潛在活性成分與160個藥物-疾病共同靶點輸入Cytoscape軟件中,繪制出“藥物-成分-靶點-疾病”相互作用的網絡圖(見圖3)。圖中紫色代表藥物,藍色代表交泰丸中的25種活性成分(9個活性成分靶點與疾病靶點無交集,予刪除),綠色代表160個共同靶點,紅色代表疾病。Degree值表示預測出該成分與作用靶點的關聯個數,Degree值越大說明該成分越重要,使用Network Analyzer對網絡圖進行分析顯示:其中作用靶點數量Degree值>10的化合物有10個,分別為槲皮素(quercetin)61個、苯乙烯(Styrene)60個、苯甲酸肉桂酯(Cinnamyl Benzoate)21個、乙酸肉桂酯(Cinnamyl Acetate)21個、(R)-氫化小檗堿[(R)-Canadine]14個、茴香腦(Anethole)13個、反肉桂酸(Trans-Cinnamic Acid)12個、肉桂酸乙酯(Ethylcinnamate)12個、肉桂酸(Cinnamic Acid)12個、肉桂醛(Cinnamic Aldehyde)10個,這些化合物能與10個以上靶點鏈接,可能是交泰丸中治療失眠的主要活性成分。此外,靶點人β2腎上腺素能受體(ADRB2)13個、前列環素G/H合酶和環氧合酶(PTGS1)12個、雄激素受體(AR)10個,與成分鏈接次數>10次,這說明ADRB2、PTGS1、AR可能是交泰丸治療失眠的重要靶點;而雌激素受體1(ESR1)、腎上腺素受體1B(ADRA1B)、白介素-1β(IL-1β)、腎上腺素受體2C(ADRA2C)、腎上腺素受體1A(ADRA1A)、γ-氨基丁酸A型受體alpha-1(GABRA1)的鏈接次數>5次,表明這些靶點在失眠的治療中可能也發揮一定的作用。說明交泰丸治療失眠的機制是非常復雜的。
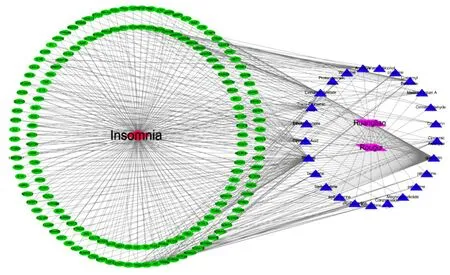
圖3 藥物-成分-靶點-疾病相互作用的網絡圖
2.5 PPI關系網絡分析 在STRING數據庫中錄入上述160個藥物-疾病共同靶點,分析得到蛋白相互作用的PPI網絡(見圖4),每條邊代表蛋白與蛋白之間的相互作用關系,線條越多代表關聯度越大,得到PPI圖中的靶點排序(排名前30位),見圖5。表明這些蛋白在PPI網絡中具有重要的地位,對于交泰丸治療失眠具有重要的臨床意義。通過PPI網絡中關鍵靶點相互映射,可推測交泰丸的有效成分可能通過胰島素(INS)、白介素-6(IL-6)、IL-1β、腫瘤壞死因子(TNF)、血管內皮生長因子A(VEGFA)等靶點發揮治療作用。
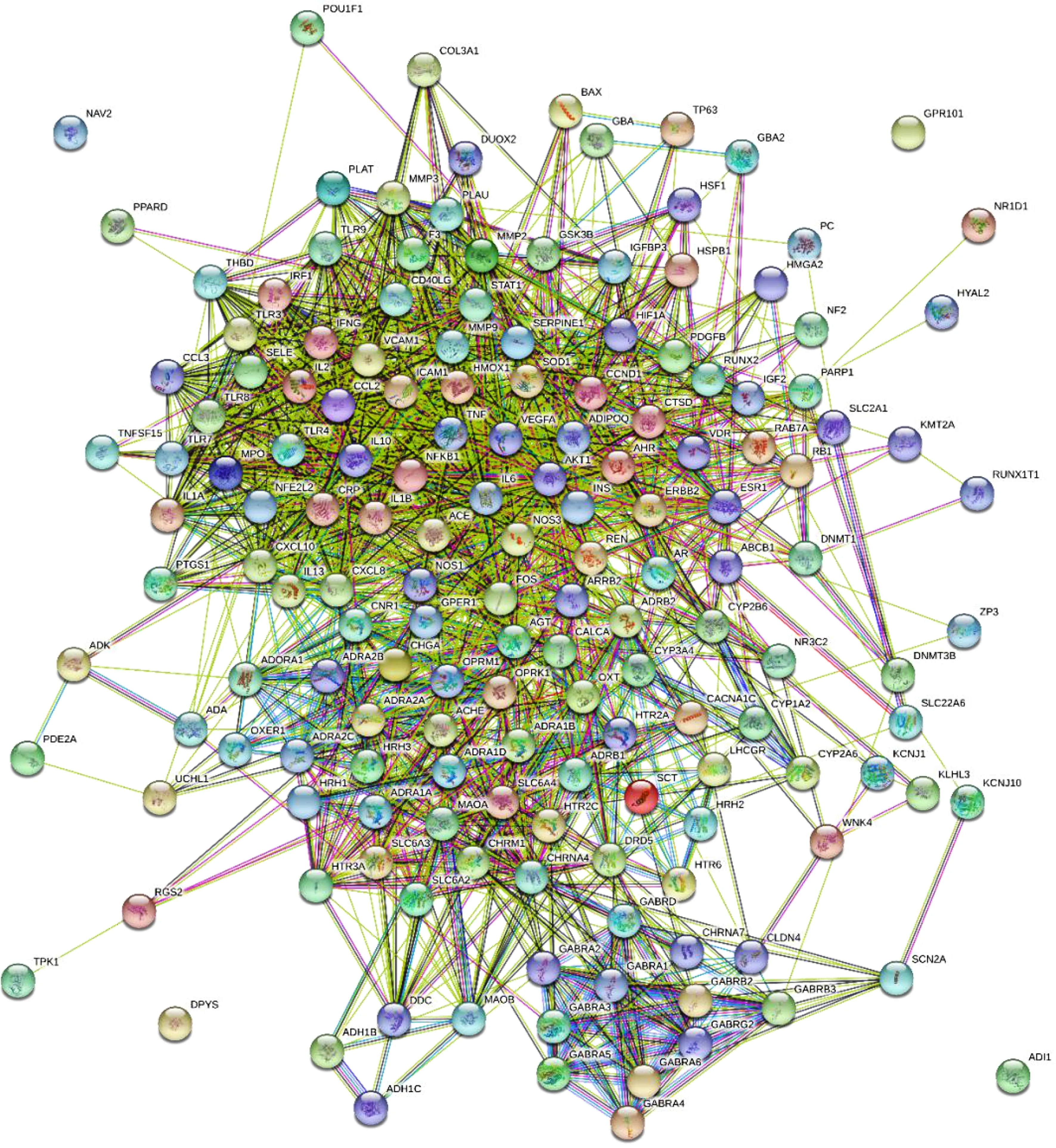
圖4 靶點相互作用PPI圖
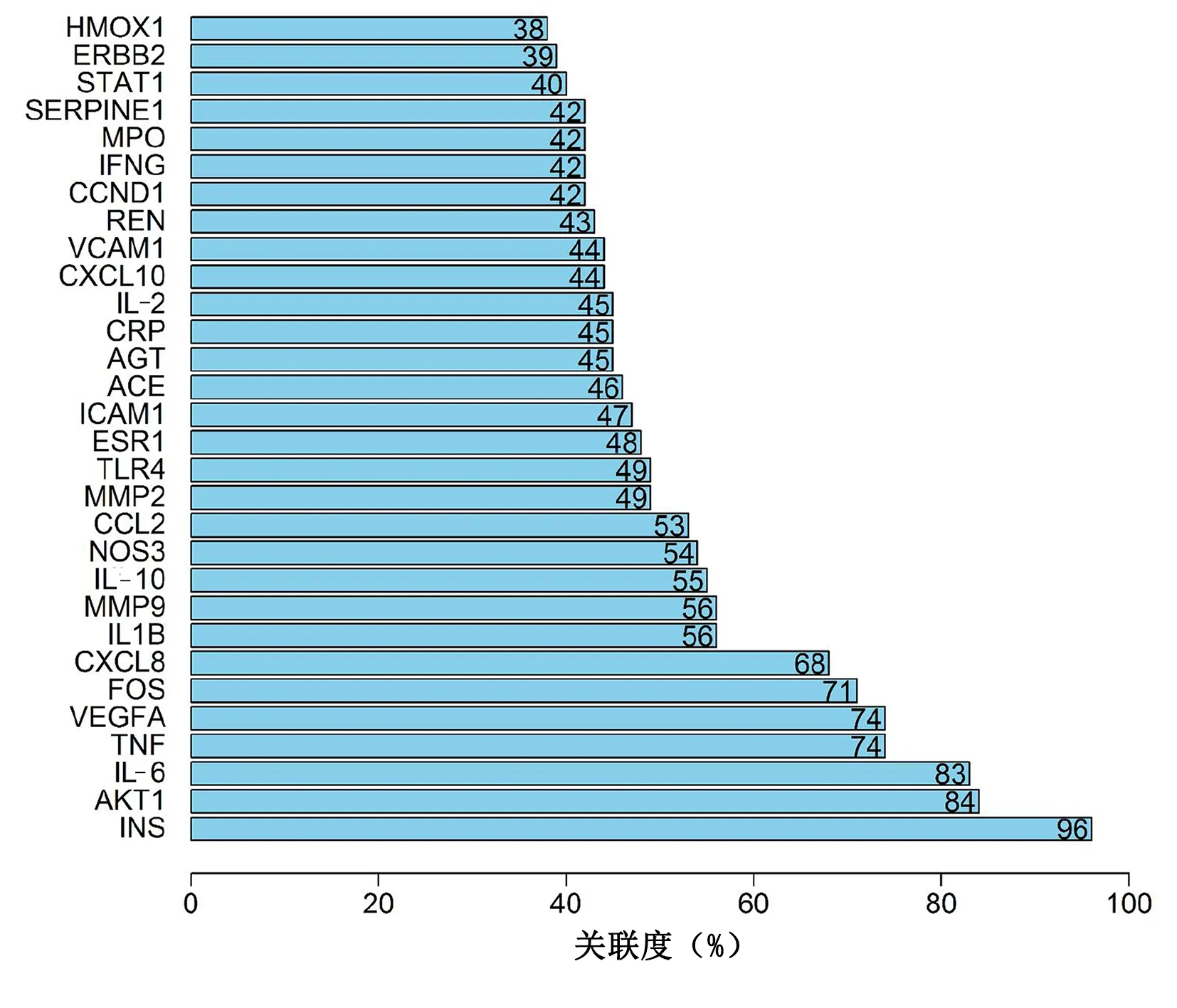
圖5 PPI圖中的靶點排序(排名前30位)
2.6 GO富集分析 將160個藥物-疾病共同靶點經R語言運行后GO分析選取生物學過程、細胞組分及分子功能3個部分。結果顯示,交集基因集合共富集至2 076條生物學過程(BP)通路中,其中,富集基因數目>20個的數目為78條,主要與第二信使介導的信號傳遞(second-messenger-mediated signaling),G蛋白偶聯受體信號傳導途徑、與環狀核苷酸第二信使偶聯(G protein-coupled receptor signaling pathway,coupled to cyclic nucleotide second messenger),對細菌起源分子的反應(response to molecule of bacterial origin),調節膜電位(regulation of membrane potential),調節炎癥反應(regulation of inflammatory response),肽分泌的調節(regulation of peptide secretion),對脂多糖的反應(response to lipopolysaccharide),循環系統中的血管過程(vascular process in circulatory system)等生物過程相關,表明交泰丸可能通過多個生物學過程發揮治療作用。詳見圖6。
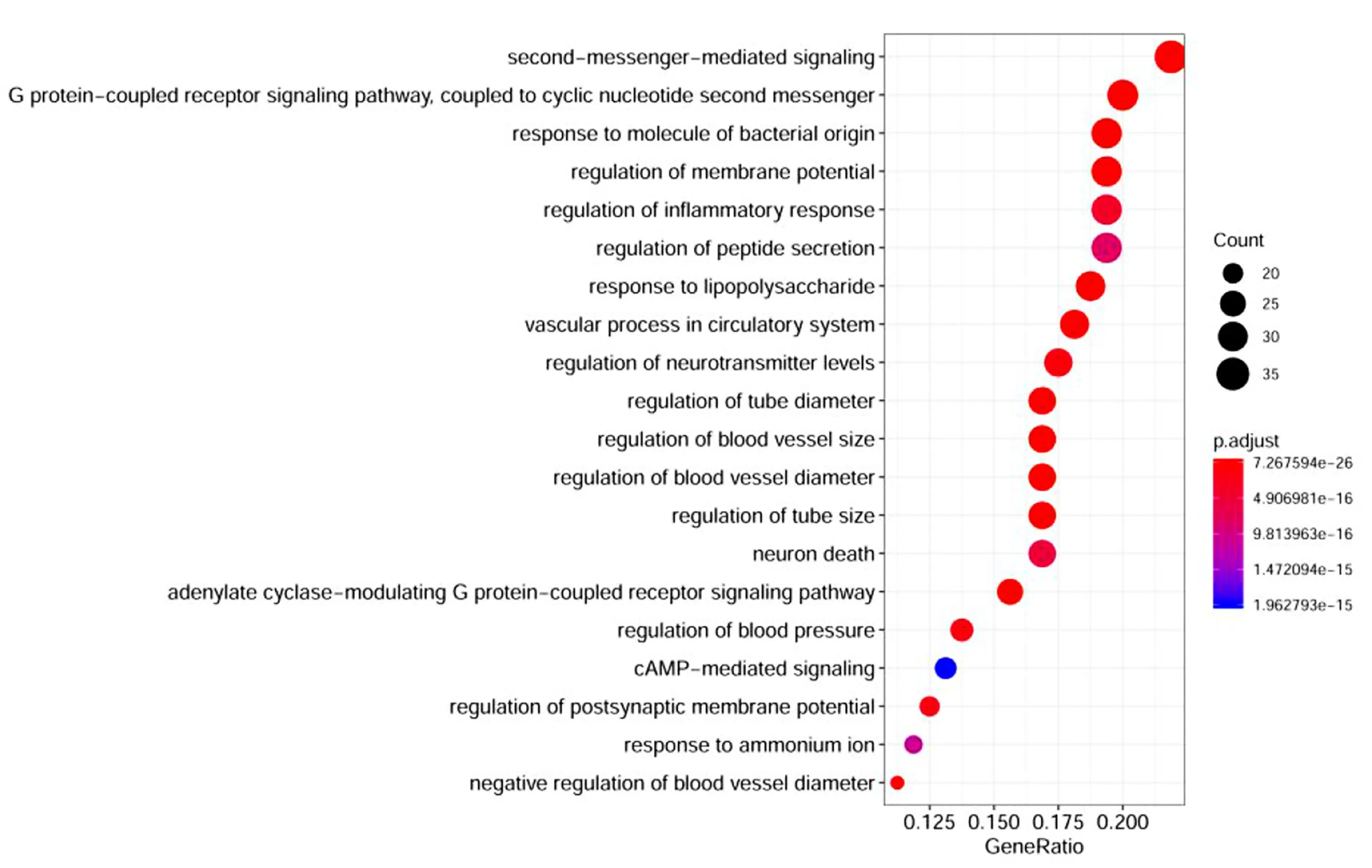
圖6 交泰丸治療失眠癥的GO富集分析
2.7 KEGG富集分析 將160個藥物-疾病共同靶點經R語言運行后共得到106條KEGG通路,前20位的結果形成KEGG功能富集的條形圖,P代表富集的顯著性,顏色越紅則顯著性越高。結果顯示,共同靶點主要富集于Toll樣受體信號通路(Toll-like receptor signaling pathway)、NF-κB信號通路(NF-kappa B signaling pathway)、環磷酸腺苷(cAMP)信號通路(cAMP signaling pathway)、γ-氨基丁酸(GABA)能突觸(GABAergic synapse)、TNF信號通路(TNF signaling pathway)、胰島素抵抗(Insulin resistance)、絲裂原活化蛋白激酶(MAPK)信號通路(MAPK signaling pathway)、環磷酸鳥苷-蛋白激酶(cGMP-PKG)信號通路(cGMP-PKG signaling pathway)等通路。表明交泰丸的活性成分靶點分布于不同的通路,可能通過多個通路協同發揮作用。詳見圖7。
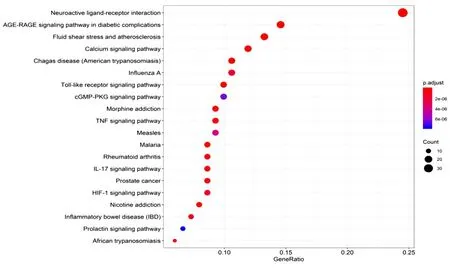
圖7 交泰丸治療失眠癥的KEGG富集分析
3 討 論
3.1 交泰丸的組方分析 交泰丸是中醫經典方劑,配伍精妙,出自清代王孟英《四科簡效方》,用于治療“心腎不交,怔忡無寐”,是臨床治療失眠常用方劑。中醫認為腎是人體之根本,心腎相交是人體正常的氣機升降,若腎陰虧虛,腎精不能上濟于心,心火不能下交于腎,則會出現病理的心腎不交證,水火不能相濟,使陽不入陰,陰不制陽,出現心神失養,夜不能寐,神志不安。交泰丸是治療心腎不交型失眠的經典方劑,由黃連和肉桂兩味藥物組成,黃連可清心之上浮之火,肉桂引心火下入于腎,使心腎相交,故能寐,現代常用于治療更年期失眠、頑固性失眠、抑郁性失眠[8-9]。按照中醫證型分類用于治療心腎不交型與陰虛火旺型失眠[10-11]。
3.2 交泰丸成分分析 通過分析得出交泰丸治療失眠的有效成分有10個,包括槲皮素、苯甲酸肉桂酯、乙酸肉桂酯、(R)-氫化小檗堿、茴香腦、反肉桂酸、肉桂酸乙酯、肉桂酸、肉桂醛等。其中槲皮素屬于黃酮類化合物,是交泰丸的主要活性成分。黃酮類化合物是一類低分子天然植物成分,大量實驗研究表明,黃酮類化合物有抗氧化、抗炎、鎮痛、調節免疫、抗衰老、降血脂作用,其作用機制可能與其抗自由基或抗氧化有關[12]。近年來黃酮類化合物對神經系統作用的研究成為熱點。有研究報道,黃酮類化合物可通過多種受體和信號通路對中樞神經系統發揮作用,機制十分復雜,具有抗抑郁、抗焦慮、中樞神經抑制、治療精神分裂癥、保護神經系統、鎮痛、改善記憶力和影響神經內分泌等多方面作用[13-16]。已有研究顯示,槲皮素具有抗癌、抗氧化、抗纖維化、抗炎、抗菌、抗衰老、抗抑郁癥、抗白血病、抗糖尿病等多種生物活性[17]。
現代藥理學研究表明,在交泰丸合方中,肉桂的肉桂醛(桂皮醛)具有鎮靜催眠、抑菌、鎮痛、擴管等多種功效;肉桂酸具有抗炎、升高白細胞、利膽、明顯對抗由二磷酸腺苷(ADP)和膠原誘導的血小板聚集等藥理作用[18]。黃連中的鹽酸小檗堿具有抗菌、降壓、擴張冠狀動脈及興奮平滑肌等作用[19]。小檗堿亦稱黃連素,是從中藥黃連中分離的主要有效成分。研究表明,黃連素對心血管系統具有調節蛋白激酶保護心肌、改善心肌缺血[20]、抑制血小板聚集[21]、調節鈣離子保護心肌[22]作用,尤其是降血脂作用對防治動脈粥樣硬化效果良好;對于神經系統具有促神經組織修復的作用,能夠通過影響大腦內神經遞質來達到抗焦慮作用[23-24]。以上實驗研究數據說明了本研究的可行性,但還有很多未被研究或證實,需進一步深入研究。因此,該方對于失眠的防治具有重要的作用,能夠緩解安眠藥帶來的不良反應和長期的依賴性,對進一步探討其治療失眠的機制具有非常重要的意義。
3.3 關鍵靶點分析 通過對交泰丸蛋白相關作用PPI關系網絡分析可以發現,交泰丸的有效成分可能通過INS、IL-6、IL-1β、TNF、VEGFA等重要靶點發揮治療作用,其中有96個化合物通過INS起作用。有研究表明,交泰丸具有改善睡眠、炎癥和胰島素敏感性的有益作用。其中INS敏感性與睡眠有著密切的關系[25]。失眠病人經常服用鎮靜催眠藥、抗精神病藥、抗抑郁藥和抗焦慮藥。與這些藥物有關的異常長睡眠時間可能引起胰島素抵抗的高風險,而慢性失眠通常與胰島素抵抗有關,交泰丸干預后可以使胰島素抵抗減弱。另有研究表明,失眠與某些炎癥基因表達的調節有關,如腫瘤壞死因子-α(TNF-α)、IL-1β和IL-6,交泰丸對于減輕大鼠的睡眠喪失相關炎癥具有有益的作用[26]。TNF是公認的對神經元有損傷作用的細胞因子之一,在正常腦組織中呈節律性表達,參與了睡眠生理調節作用。近年來研究發現,許多免疫調節物質均參與了睡眠的調節過程,如細胞免疫。有研究發現,TNF可以延長非快速動眼睡眠期的時間,減少快速動眼睡眠期的時間;當TNF含量超過一定量時,則抑制正常睡眠。可能是通過協同其他炎癥因子如IL-1β、IL-6等來改變神經內分泌的活動,增加某些神經遞質的釋放,引起大腦不同區域基因的激活,來維持人類自身基本的活動,如攝食、睡眠、學習和記憶等活動[27]。而當這一平衡遭到破壞時,就可能出現如睡眠障礙、學習記憶能力下降等日常生活紊亂[28]。亦有很多研究表明,睡眠剝奪與血管內皮生長因子(VEGF)的變化有密切關系[29],缺氧是VEGF水平升高的主要刺激因素,與心血管疾病的發生有關。睡眠呼吸暫停病人血液循環中的VEGF濃度升高,其升高的原因是由于合并心血管疾病或動脈粥樣硬化的亞臨床癥狀引起的,而不是由于呼吸系統疾病和低氧本身造成的,因此,降低VEGF濃度,對改善睡眠質量具有臨床意義[30]。說明交泰丸可能通過調節上述主要基因靶點的表達,從而改善失眠引發的胰島素敏感性、免疫反應,進一步達到改善癥狀的目的。
3.4 通路結果分析 KEGG通路分析結果可見,交泰丸有較多基因靶點富集在與炎癥相關的疾病和信號通路,這說明交泰丸可能通過作用于這些炎癥因子靶點,調節炎癥信號通路,抑制炎癥反應,改善胰島素抵抗,從而發揮治療失眠的作用。其中Toll樣受體信號通路、NF-κB信號通路、TNF信號通路都屬于炎癥相關通路,說明失眠與以炎癥為特征的疾病狀態有關。
目前研究表明,Toll樣受體信號通路中的Toll樣受體4(TLR4信號通路)響應已知與睡眠喪失相關的內源性和病原體相關配體而激活炎癥信號級聯反應,因此,TLR4可能是某些與炎癥相關的睡眠喪失影響的介質,越來越多的證據在評估TLR4作為睡眠剝奪細胞促炎反應介質的作用研究中,已經提供了令人信服的理由[31]。Toll樣受體對獲得性免疫應答類型具有調控作用,TLR4具有活化誘導免疫細胞合成和促炎細胞因子(TNF、IL-6及IL-1β)釋放的作用[32]。證明了TLR4及其在睡眠調節中激活的細胞內信號通路的重要性。
已有研究證明,睡眠與免疫力之間的相互作用,構成人體睡眠剝奪的主要組成部分是免疫功能基因,NF-κB是一種重要的轉錄信號因子,可調節多種免疫與炎癥相關的基因表達[33],在睡眠缺失情況下其在機體的水平明顯升高,NF-κB信號通路的下游成分,尤其是細胞因子[白介素-2(IL-2)、IL-6]對睡眠有重要的影響[34-35]。有研究發現,IL-2 和IL-6 作為細胞因子參與人體的睡眠和免疫功能的調節過程,慢性失眠常引起機體的慢性炎性反應以及免疫功能變化,而改變機體IL-2 和IL-6的分泌水平對失眠有重要調控作用[36]。
研究表明,睡眠剝奪會損害海馬cAMP信號傳導,并且cAMP傳導的失調與睡眠喪失具有重要作用[37]。睡眠剝奪過程中海馬興奮性神經元中瞬時增加的cAMP水平足以防止因睡眠喪失而導致的記憶鞏固不足。另外,睡眠剝奪會降低基礎條件下海馬中cAMP反應元件結合蛋白(CREB)的磷酸化,并防止CREB磷酸化[38]。
其次,TNF也是免疫系統重要的細胞因子,除參與炎癥反應外,還參與機體其他生理功能的調節,如影響睡眠、腦發育、食欲和內分泌功能等。腦內TNF的表達受到微生物代謝產物及晝夜節律的影響,動物血中單核細胞產生TNF的能力與睡眠-覺醒周期有關。TNF靜脈注射或腦室注入,可延長家兔、大鼠、小鼠的非快速眼動睡眠時間,說明TNF參與非快速眼動睡眠的調節。進一步研究發現,TNF可能通過促進大鼠、小鼠腦內5-羥色胺(5-HT)的合成而調節睡眠[39]。
另外GABA是中樞神經系統的主要抑制性神經遞質,對神經系統的神經元具有普遍的抑制作用,在興奮-抑制調節中起重要作用,具有抗焦慮、抗驚厥、鎮痛、調節內分泌等功能[40]。腦中GABA是通過谷氨酸經谷氦酸脫梭酶脫竣而成。GABA可存在于神經末梢胞漿,也可貯存在突觸囊胞中。GABA神經元興奮時,GABA被神經末梢釋放到突觸間隙,主要依靠突觸前膜的攝取,膠質細胞也可攝取GABA。用免疫組化技術顯示腦內GABA的分布,結果顯示,大腦中廣泛存在GABA能神經元,絕大多數都是短軸突中間神經元,主要分布在大腦皮層、海馬和小腦。黑質是腦中GABA濃度最高的腦區[41]。 有研究揭示,不同腦區的GABA、谷氨酸含量及其受體功能的改變參與睡眠覺醒過程及不同睡眠時相的轉換,在睡眠調節中發揮重要作用[42]。GABA含量的增加對興奮性和抑制性傳導的平衡起著關鍵作用,進而間接導致對睡眠產生特殊影響,目前已經公認的是GABA受體的活化有利于睡眠[43]。
目前研究已經明確,以上通路具有調節睡眠的作用,說明交泰丸有可能通過Toll樣受體信號通路、NF-κB信號通路、TNF信號通路、cAMP信號通路等,來抑制炎癥因子的產生,從而達到治療失眠的作用。
有學者研究了睡眠呼吸障礙與胰島素抵抗之間的關系,發現睡眠呼吸障礙對胰島素抵抗具有獨立的不良影響[44]。而失眠病人長期服用鎮靜催眠、抗精神病、抗抑郁和抗焦慮等藥物可能引起胰島素抵抗的高風險,特別是慢性失眠通常與胰島素抵抗有關,交泰丸干預后可能使胰島素抵抗減弱。
綜上所述,結合網絡藥理學的數據分析,可以推測交泰丸可能通過調節炎癥通路干預炎癥的發生發展以及改善胰島素抵抗來發揮治療失眠的作用,交泰丸可能通過作用于INS、VEGFA以及炎性細胞因子如TNF、IL-1β和IL-6等多個靶點,調節Toll樣受體信號通路、NF-κB信號通路、cAMP信號通路、GABA能突觸、TNF信號通路、胰島素抵抗等,作為研究交泰丸治療失眠分子作用機制的思路。本研究基于網絡藥理學深入探討交泰丸的作用機制,為交泰丸治療失眠提供新的思路和方法,也為交泰丸的臨床應用提供了參考價值。

