結腸癌中HRH3表達對細胞增殖的影響
朱劍軍,吳 昊
結腸癌的發病率和病死率均高居消化系統惡性腫瘤首位[1]。結腸癌的發生、發展是一個涉及多基因參與、多步驟的癌變過程。近年來,越來越多的文獻報道組胺與惡性腫瘤的發生、發展密切相關[2-3]。組胺能夠顯著增強乳腺癌細胞的放療敏感性,提示組胺能夠作為一種潛在的抗癌佐劑,提高腫瘤患者的放療效果[2]。作為一種具有生理活性的小分子物質,組胺通過與組胺受體結合,傳遞信號,在不同類型細胞中發揮不用作用[2]。組胺激活組胺1型受體,促進細胞增殖、胚胎發育和腫瘤生長[4]。激活組胺1型受體和組胺4型受體活性能夠顯著增強乳腺癌細胞的放療敏感性[2],提示組胺受體蛋白家族可能是治療惡性腫瘤的一組潛在作用靶點。組胺受體3(histamine receptor 3, HRH3)是一種7次跨膜蛋白,屬于G蛋白偶聯受體家族[5]。HRH3基因定位于染色體20q13.3,蛋白質由445個氨基酸組成,相對分子質量為48.6 KD。有研究報道HRH3與肝細胞肝癌、膽管細胞型肝癌、乳腺癌、前列腺癌等惡性腫瘤的生長與轉移有關[5-7]。但截至目前,關于HRH3在結腸癌生長過程中的作用尚未見相關報道。本實驗采用轉染siRNA片段的方式靶向沉默HRH3基因在結腸癌細胞中的表達,CCK-8和EdU法監測腫瘤細胞生長和增殖活性,qRT-PCR和Western blot法分析相關信號通路改變,明確HRH3基因在結腸癌細胞惡性增殖過程中的功能作用,探討相關分子機制,從而為闡明結腸癌的發病機制提供理論基礎,為結腸癌治療提供潛在作用靶點。
1 材料與方法
1.1 試劑DMEM培養液、胎牛血清(Hyclone公司,美國),CCK-8(碧云天公司,中國),EdU細胞增殖檢測試劑盒(銳博公司,中國),Lipofectamine 2000、TRIzol Reagent(Invitrogen,美國),cDNA合成試劑盒、TB Green Advantage qPCR Premix(Takara公司,日本),HRH3抗體、c-Myc抗體和CDKN1A抗體(Abcam公司,美國),β-actin抗體、二抗(三鷹公司,中國)。
1.2 細胞培養常規培養結腸癌Ls174T細胞和SW480細胞。用含10%胎牛血清的DMEM培養液于37 ℃、5%CO2細胞培養箱中培養。
1.3 siRNA轉染常規培養結腸癌細胞,將細胞接種于6孔板。24 h后,待細胞處于對數生長期時,進行細胞轉染。轉染步驟按照Lipofectamine 2000說明書進行。本課題實驗分3組:空白對照組(只加Lipofectamine)、陰性對照組(si-NC組,轉染陰性對照siRNA片段)、si-HRH3組(轉染si-HRH3片段)。si-HRH3片段正義鏈序列5′-GGAGGAGAAAUGUGC ACUCAU-3′,反義鏈序列3′-CCUCCUCUUUACACGU GAGUA-5′。siRNA片段和陰性對照序列由上海吉碼公司合成。
1.4 qRT-PCR常規培養結腸癌細胞,細胞轉染siRNA片段48 h后進行實時熒光定量PCR實驗。提取RNA、cDNA第一條鏈的合成步驟參照試劑盒說明書進行。采用TB Green qPCR Premix完成PCR擴增實驗。擴增程序如下:95 ℃預變性10 min;95 ℃ 10 s,58 ℃ 10 s,72 ℃ 10 s,共計40個循環;最后72 ℃延伸10 min。溶解曲線條件按照常規程序進行。采用2-△△Ct算法計算目的基因的相對表達水平。HRH3引物、c-Myc引物和CDKN1A引物序列見表1。
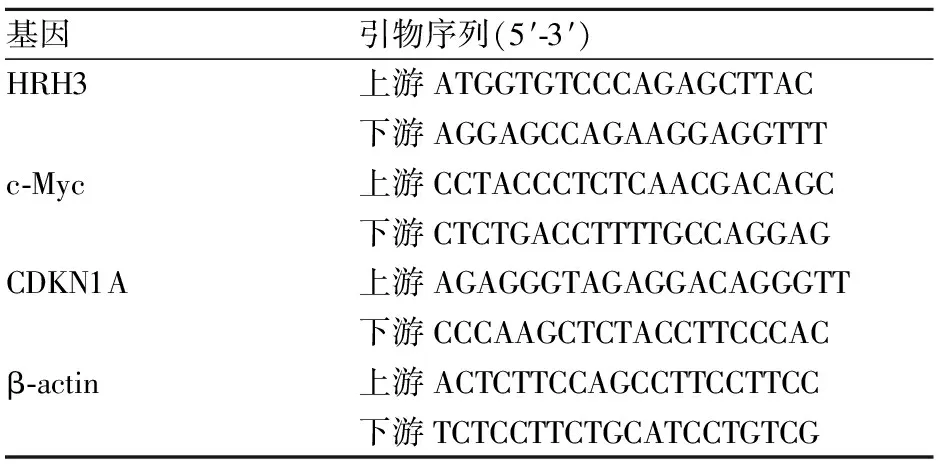
表1 qRT-PCR引物序列
1.5 Western blot常規培養結腸癌細胞,細胞轉染siRNA片段72 h后進行 Western blot實驗。RIPA裂解液裂解細胞,提取細胞總蛋白。BCA試劑盒進行蛋白定量。后續按照常規步驟進行SDS-PAGE垂直電泳、轉膜、封閉。常溫封閉1 h后,一抗孵育過夜。TBST沖洗后,二抗常溫孵育1 h。ECL發光液檢測蛋白條帶。HRH3和CDKN1A抗體工作濃度1∶1 000;c-Myc抗體工作濃度1∶2 000;二抗工作濃度1∶10 000。
1.6 CCK-8實驗常規培養結腸癌細胞。轉染siRNA片段6 h后將細胞接種于96孔細胞培養板。接種時間記為0 h。在0 h、24 h、48 h、72 h、96 h這5個時間點檢測細胞的生長狀態。CCK-8溶液孵育1 h后,于酶標儀450 nm處檢測。
1.7 EdU實驗常規培養結腸癌細胞。轉染siRNA片段48 h后進行EdU細胞增殖檢測實驗。加入適量EdU工作液,孵育2 h。后續經多聚甲醛固定、沖洗、EdU反應、Hoechst染色等步驟完成實驗。最后用倒置熒光顯微鏡拍照。

2 結果
2.1 轉染siRNA對結腸癌細胞中HRH3表達的影響采用轉染siRNA片段的方法沉默HRH3基因表達。在結腸癌Ls174T和SW480細胞中,與陰性對照組相比,轉染si-HRH3片段48 h后,si-HRH3組HRH3 mRNA表達水平降低,分別為82%±4.10%和75%±2.33%,差異均有統計學意義(P均<0.01,圖1)。與空白對照組相比,陰性對照組HRH3 mRNA表達無顯著變化(P>0.05)。Western blot結果進一步顯示,與陰性對照組相比,轉染si-HRH3片段72 h后,Ls174T和SW480細胞中HRH3蛋白水平均顯著降低(圖2)。上述研究表明,轉染si-HRH3能夠顯著沉默結腸癌細胞中HRH3表達水平。
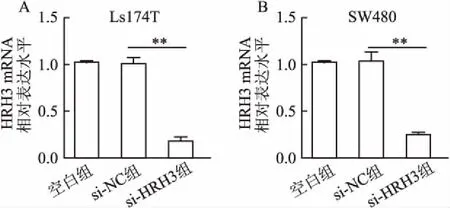
圖1 轉染si-HRH3對結腸癌細胞中HRH3 mRNA表達水平的影響:A.Ls174T細胞;B.SW480細胞;**P<0.01
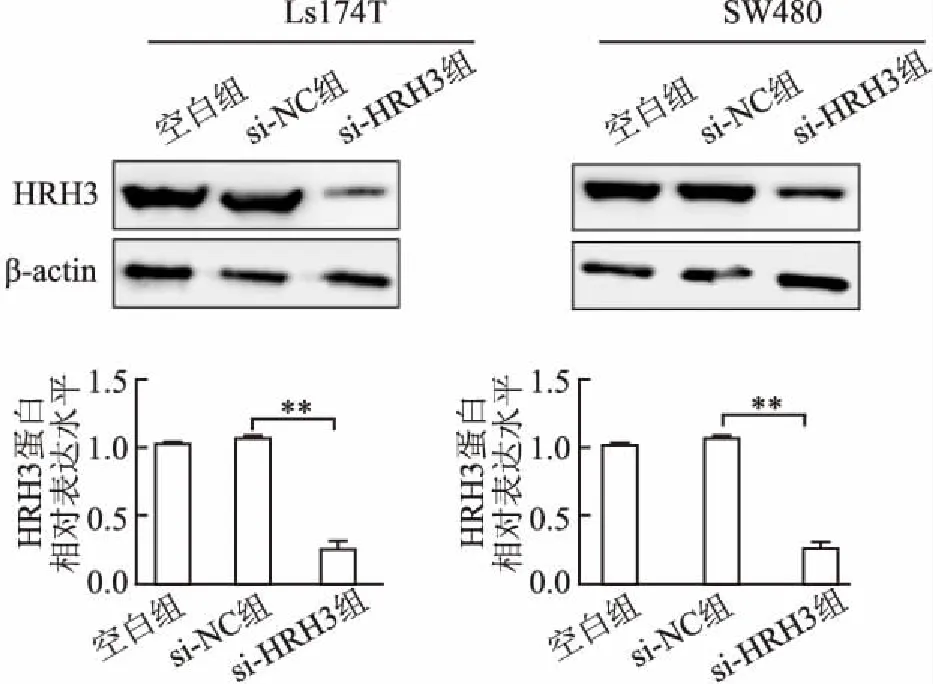
圖2 轉染si-HRH3對HRH3蛋白表達水平的影響:**P<0.01
2.2 HRH3對結腸癌細胞生長的影響為研究HRH3表達對結腸癌細胞生長的影響,本實驗首先通過CCK-8實驗檢測沉默HRH3后對結腸癌細胞生長的影響,結果顯示,在Ls174T和SW480細胞中,與陰性對照組相比,轉染si-HRH3片段后96 h,si-HRH3組細胞生長抑制率分別為39.00%±2.25%和35.54%±3.51%,其差異具有統計學意義(P均<0.01,圖3)。沉默HRH3后,結腸癌Ls174T和SW480細胞的生長明顯減慢。為進一步驗證HRH3對結腸癌細胞增殖的影響,本實驗采用EdU實驗檢測結果表明,在Ls174T細胞中,陰性對照組細胞的增殖率為52.68%±1.33%,si-HRH3組細胞增殖率為23.11%±0.89%,其差異具有統計學意義(P<0.01,圖4)。在SW480細胞中,陰性對照組與si-HRH3組的細胞增殖率分別為53.69%±2.57%、17.14%±1.46%,差異有統計學意義(P<0.01,圖4)。上述實驗結果表明,沉默HRH3表達能夠有效抑制結腸癌細胞的惡性生長。
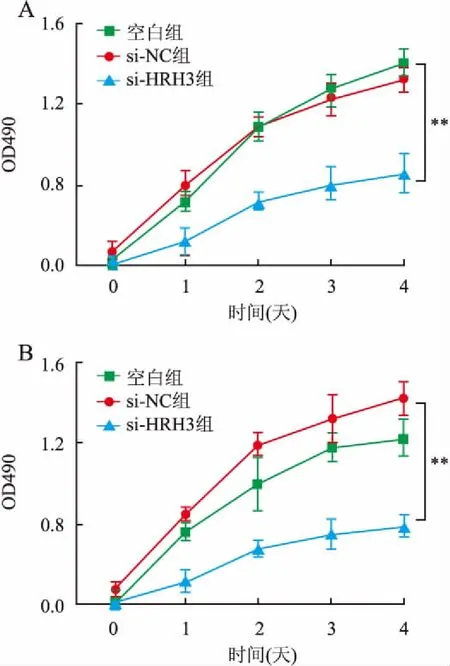
圖3 沉默HRH3對結腸癌細胞生長的影響:A.Ls174T細胞;B.SW480細胞;**P<0.01
2.3 沉默HRH3對細胞增殖關鍵分子表達水平的影響為深入研究沉默HRH3抑制結腸癌細胞增殖的具體分子作用機制,本實驗采用qRT-PCR和Western blot法檢測沉默HRH3后c-Myc和CDKN1A的表達水平。qRT-PCR實驗結果發現,在Ls174T和SW480細胞中,與陰性對照組相比,si-HRH3組c-Myc mRNA表達水平均顯著降低,分別為35.11%±1.52%和24.65%±1.80%,其差異均有統計學意義(P=0.025,P=0.030);與陰性對照組相比,si-HRH3組CDKN1A mRNA表達水平顯著升高,分別為56.73%±1.44%和55.39%±3.14%,其差異均具有統計學意義(P=0.0093,P=0.015,圖5)。與qRT-PCR結果一致,Western blot實驗結果顯示,沉默HRH3后,c-Myc蛋白水平降低(P<0.01),CDKN1A蛋白水平升高(P<0.01,圖6)。上述研究結果表明,HRH3可能通過調控c-Myc和CDKN1A表達水平,影響結腸癌細胞的惡性增殖。
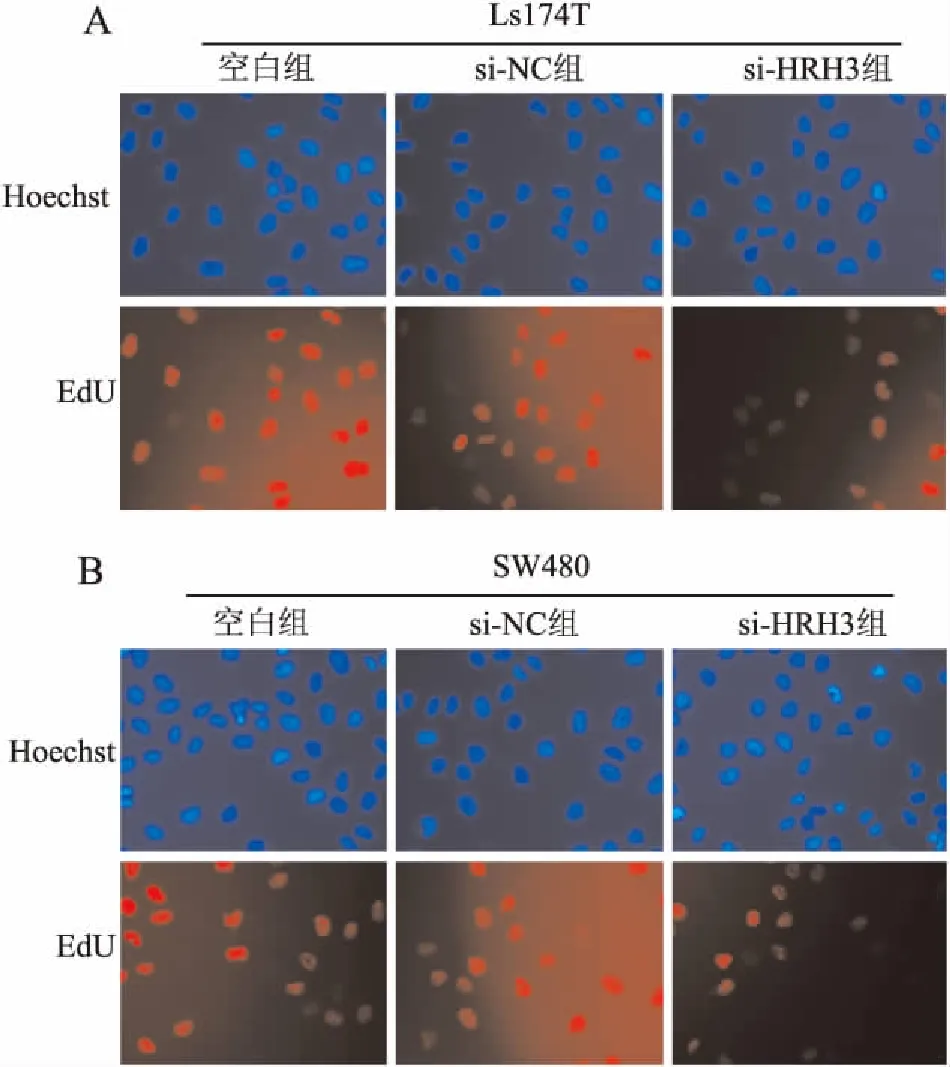
圖4 沉默HRH3對結腸癌細胞增殖的影響:A.Ls174T細胞;B.SW480細胞
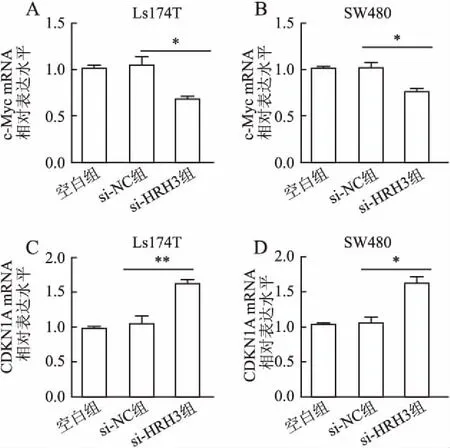
圖5 沉默HRH3對c-Myc和CDKN1A mRNA表達的影響:A.Ls174T細胞中c-Myc mRNA的表達;B.SW480細胞中c-Myc mRNA的表達;C.Ls174T細胞中CDKN1A mRNA的表達;D.SW480細胞中CDKN1A mRNA的表達;*P<0.05,**P<0.01
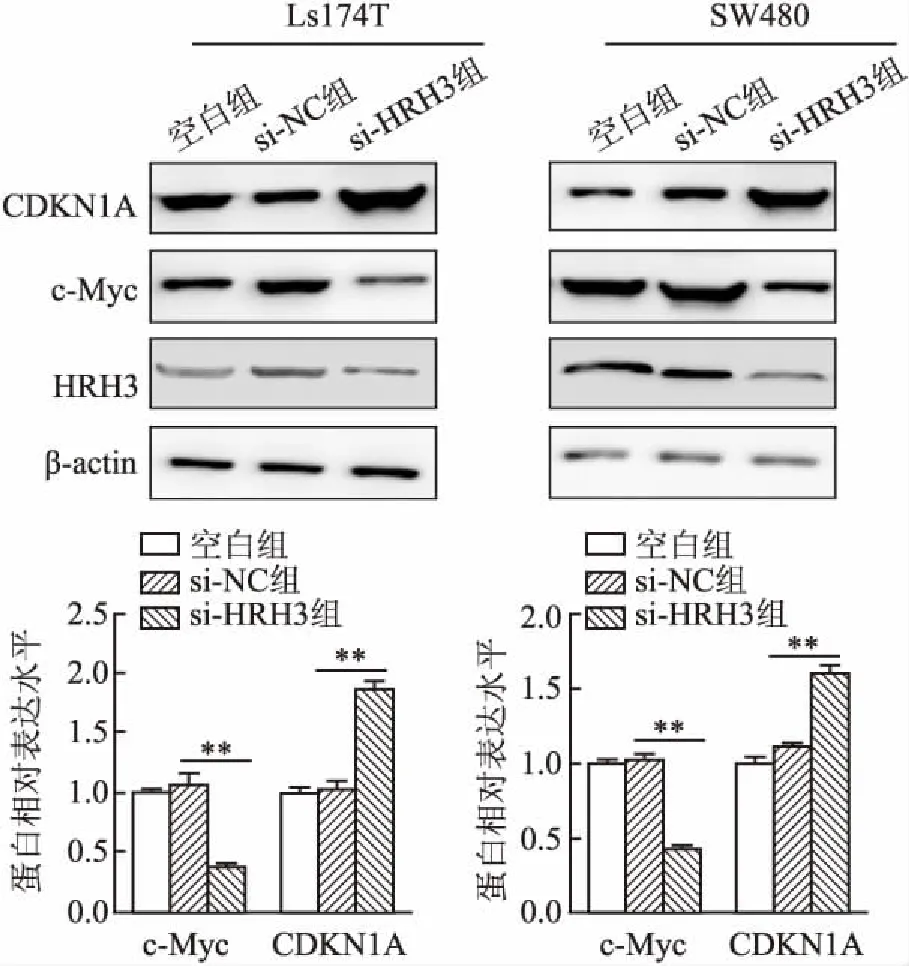
圖6 沉默HRH3對c-Myc和CDKN1A蛋白水平的影響**P<0.01
3 討論
結腸癌是一種常見的消化系統腫瘤,2018年全球新增結腸癌109萬余例,新增死亡55萬余例,其發病率居所有惡性腫瘤第三位,病死率高居所有惡性腫瘤第二位[1]。腫瘤的發生、發展與腫瘤微環境密切相關[8]。腫瘤微環境是由腫瘤細胞、間質細胞和其它非細胞成分(包括細胞因子、趨化因子等生理活性物質)共同組成[8]。組胺作為腫瘤環境中的重要一員,由組氨酸脫氫酶催化L-組氨酸脫羧形成,主要儲存于肥大細胞和嗜堿性粒細胞[3]。近年來,越來越多的研究證實,組胺和組胺受體在炎癥和惡性腫瘤形成過程中發揮重要作用[9]。
HRH3表達異常與多種惡性腫瘤的發生、發展密切相關[5,7]。Lin等[7]報道HRH3在惡性膠質瘤中呈高表達,抑制HRH3能夠顯著抑制惡性膠質瘤細胞生長、侵襲和上皮-間質轉化。Chen等[6]研究發現,抑制HRH3后前列腺癌的生長能力和侵襲活性減弱,細胞凋亡增加。本課題組前期研究發現,HRH3在肝細胞肝癌中呈顯著高表達,且激活HRH3后,肝癌細胞的增殖和遷移能力顯著升高[5]。與上述報道一致,本實驗通過轉染siRNA片段沉默HRH3表達發現,沉默HRH3后結腸癌細胞生長減慢,細胞增殖活性顯著降低,提示HRH3在結腸癌的發生進展過程中發揮促癌作用。然而,Francis等[10]在膽管細胞型肝癌細胞中發現,HRH3激動劑能夠顯著抑制肝癌細胞生長,提示HRH3在膽管細胞型肝癌細胞中發揮抑癌作用。基于此,作者推測HRH3在不同類型惡性腫瘤的發生進展過程中發揮不同作用,其作用機制有待深入研究。
目前,HRH3促進惡性腫瘤增殖和遷移的作用機制尚未完全闡明。Lin等[7]在神經膠質瘤中發現,HRH3通過調控PI3K/Akt和MEK/ERK信號通路,影響上皮-間質轉化關鍵分子的表達,如E-cadherin、ZO-1、vimentin和N-cadherin等,進而促進惡性膠質瘤細胞的侵襲轉移。Francis等[10]報道,HRH3通過調控PKCα依賴的ERK1/2去磷酸化抑制膽管細胞型肝癌細胞生長,提示ERK信號通路參與HRH3介導的膽管細胞型肝癌細胞生長。PI3K/Akt、MEK/ERK等信號通路通過激活下游靶基因,如c-Myc、CDKN1A等,在促進細胞生存和細胞周期進展方面發揮重要作用[11-14]。c-Myc在多種惡性腫瘤中異常高表達,且c-Myc表達水平與腫瘤細胞惡性增殖活性密切相關[15]。本實驗通過qRT-PCR和Western blot實驗檢測沉默HRH3后c-Myc的表達水平,結果顯示,沉默HRH3后,c-Myc mRNA和蛋白水平均顯著降低,提示HRH3可能通過激活c-Myc信號通路,促進結腸癌細胞惡性生長。
細胞周期失調是導致腫瘤細胞惡性增殖的一個重要始動因素[16]。Bai等[11]報道Akt通過調控CDK抑制因子CDKN1A,促進腫瘤細胞生存。本實驗發現,沉默HRH3后,CDKN1A mRNA和蛋白水平均顯著升高,提示HRH3可能通過調控CDKN1A表達水平,導致細胞周期紊亂,最終促進結腸癌細胞惡性增殖。然而,HRH3也能通過調控其它信號途徑影響腫瘤細胞生存[6]。例如,Chen等[6]在前列腺癌細胞中研究發現,敲除HRH3后,雄激素受體(androgen receptor, AR)表達水平降低,提示HRH3可能通過AR途徑抑制前列腺癌細胞生長、侵襲,促進細胞凋亡。上述研究結果提示HRH3可能通過激活不同信號通路,促進惡性腫瘤的發生、進展。
綜上所述,沉默HRH3表達后,結腸癌細胞的增殖活性減弱,c-Myc表達降低,CDKN1A表達升高。基于此,推測HRH3可能通過調控c-Myc和CDKN1A轉錄表達,促進結腸癌細胞惡性增殖。但是,HRH3是如何調控c-Myc和CDKN1A表達,PI3K/Akt、MAPK/ERK等信號途徑在HRH3介導的結腸癌細胞增殖過程中發揮怎樣的作用,這些問題有待進一步深入探討。

