石吊蘭HPLC 指紋圖譜的建立
員 浬,陳小秀,徐文芬,劉 趣,劉 嬌,馬敏龍,劉恩穩
(貴州中醫藥大學,貴州貴陽 550025)
石吊蘭為苦苣苔科吊石苣苔屬植物吊石苣苔Lysionotus pauciflorusMaxim.的干燥地上部分,廣泛分布于貴州、安徽、廣西等中國南部地區及臺灣地區,生于海拔300~2 000 m的丘陵、山地林中樹上或巖石上[1-2],其性溫,味苦,歸肺經,具有化痰止咳、軟堅散結的功效,常用于咳嗽痰多、瘰癘痰核等癥[3]。現代研究表明,石吊蘭主要含有黃酮類、揮發油類、苯乙醇苷類、菖蒲烷類等成分[4-8],具有明顯的抗結核菌、降壓、抗氧化、止咳化痰、抗粥樣動脈硬化、免疫調節作用[9-14],已作為益肺止咳膠囊原料藥材,對慢性支氣管炎引起的咳嗽咯痰及肺結核、淋巴結核等疾病療效顯著,臨床應用廣泛[15-17]。目前,石吊蘭雖已收載于2015 年版《中國藥典》,但在常規檢查的基礎上僅建立了以石吊蘭素為指標的含有量測定方法,這與中藥多成分、多靶點的特點,以及其市場需求量大這一現狀不匹配,同時該藥材多為野生資源,質量參差不齊,故全面評價其質量很有必要。
中藥指紋圖譜具有特征性、整體性、模糊性等特點,可充分反映出中藥復雜體系中各成分的整體狀況,是目前其質量控制較有效的手段之一,但目前對于石吊蘭的指紋圖譜僅見譚家華等[18]初步報道。本研究建立21 批石吊蘭的HPLC 指紋圖譜,運用聚類分析、主成分分析進行系統評價,以期為該藥材質量控制提供參考依據。
1 材料
1.1 儀器 Thermo Ulti Mate 3000 高效液相色譜儀(美國賽默飛世爾科技公司);SK5200H 超聲波清洗器(上海科導超聲儀器有限公司);AG135 天平(十萬分之一,瑞士Mettler-Toledo 公司);HH-S2 數顯恒溫水浴鍋(常州普天儀器制造有限公司)。
1.2 試藥 乙腈 (色譜純,國藥集團化學試劑有限公司);甲醇(色譜純,國藥集團化學試劑有限公司;分析純,天津市富宇精細化工有限公司);磷酸(優級純,天津市科密歐化學試劑有限公司)。石吊蘭素對照品(中國食品藥品檢定研究院,111555-200602,純度98.10%);采于貴州省各分布區,經貴州中醫藥大學孫慶文教授鑒定為苦苣苔科吊石苣苔屬植物吊石苣苔Lysionotus pauciflorusMaxim,具體見表1。
2 方法與結果
2.1 色譜條件 Thermo Hypersil GOLD-C18色譜柱(250 mm×4.6 mm,5 μm);流動相乙腈(A) -0.1%磷酸(B),梯度洗脫(0~6 min,13%~18%A;6~10 min,18%~20%A;10~26 min,20%~100%A);檢測波長334 nm;柱溫35 ℃;體積流量1 mL/min;進樣量10 μL。
2.2 對照品溶液制備 取石吊蘭素對照品0.10 mg,精密稱定,置于10 mL 量瓶中,85% 甲醇溶解稀釋至刻度,0.45 μm微孔濾膜過濾,即得(0.010 00 mg/mL)。
2.3 供試品溶液制備 取各批藥材粉末約0.5 g,精密稱定,置于具塞錐形瓶中,加入85%甲醇25 mL,超聲提取20 min,放冷至室溫,過濾,藥渣提取2 次,合并濾液,揮干,85%甲醇復溶并定容于25 mL量瓶中,0.45 μm 微孔濾膜過濾,即得。
2.4 方法學考察
2.4.1 專屬性試驗 精密吸取對照品、供試品、空白溶液,在“2.1”項色譜條件下測定,發現空白溶液在相應位置處未見色譜峰,供試品溶液色譜圖中石吊蘭素色譜峰的保留時間與對照品溶液一致。將藥材和對照品UV 光譜圖進行比對,見圖1,可知其峰純度較高,純度因子為1 000,分離度大于1.5,方法專屬性良好。

表1 樣品信息

圖1 各樣品UV 光譜圖
2.4.2 精密度試驗 取 “2.3”項下供試品溶液,在“2.1”項色譜條件下連續進樣6 次,以石吊蘭素為參照峰,測得其余各共有峰相對保留時間RSD 為0.070%~1.7%,相對峰面積RSD 為0.95~2.2%,表明儀器精密度良好。
2.4.3 穩定性試驗 取同一供試品溶液,于0、2、4、8、12、14、24 h 在“2.1”項色譜條件下進樣,以石吊蘭素為參照峰,測得其余各共有峰相對保留時間RSD 為0.079%~1.1%,相對峰面積RSD 為0.40%~2.3%,表明溶液在24 h內穩定性良好。
2.4.4 重復性試驗 取同一批藥材,按“2.3”項下方法平行制備6 份供試品溶液,在“2.1”項色譜條件下進樣,以石吊蘭素為參照峰,測得其余各共有峰相對保留時間RSD 為0.054%~1.9%,相對峰面積RSD 為0.93%~2.9%,表明該方法重復性良好。
2.5 HPLC 指紋圖譜建立 取21 批樣品,按“2.3”項下方法制備供試品溶液,在“2.1”項色譜條件下進樣,建立指紋圖譜,見圖2。由此可知,21 批樣品中標定12 個共有峰,12 號色譜峰的保留時間與對照指紋圖譜一致(圖3),而且其峰形及分離度較好,基線穩定,故作為參照峰計算相對保留時間、峰面積,見表2~3。

圖2 21 批樣品HPLC 指紋圖譜

圖3 藥材HPLC 對照圖譜
將21 批樣品HPLC 指紋圖譜導入相似度軟件,以S2 為參照圖譜,采用多點校正及自動匹配,時間窗寬度設為0.5,中位數法生成對照圖譜 (圖2),計算相似度,見表4。
由此可知,21 批樣品相似度為0.100~0.980,差異較大;S20 (安徽黃山)、S21 (安徽黃山) 相似度低,均小于0.600,可能與其氣候、土壤、地理環境等條件有關;S2 (貴州凱里) 為參考,S3 (貴州冊亨)、S4 (貴州冊亨)、S5 (貴州冊亨)、S6 (貴州安龍)、S7 (貴州安龍)、S8 (貴州安龍)、S9 (貴州興義)、S10 (貴州冊亨)、S11(貴州安龍)、S12 (貴州安龍) 藥材相似度均大于0.800,而S14 (貴州獨山)、S15 (貴州獨山)、S16 (貴州獨山)、S18 (貴州三都)、S19 (貴州三都) 藥材的相似度均小于0.800,即產地為黔西南布依族苗族自治州內的藥材相似度較高,而產地為黔南布依族苗族自治州的較低。結合表2~3,可知不同產地藥材成分類型較一致,但其含有量相差較大。

表2 21 批樣品共有峰相對保留時間

表3 21 批樣品共有峰相對峰面積

表4 21 批樣品相似度
2.6 聚類分析 采用SPSS 18.0 軟件對21 批樣品的量化峰面積進行系統聚類,采用組間距離法結合歐氏平方距離進行分析,樹狀圖見圖4。由此可知,當歐氏平方距離為25 時,21 批樣品可分為2 類,S1、S20、S21 聚為1 類,其他批次聚成1 類;當歐氏平方距離為20 時,其可分為4類,S1 為1 類,S20 和S21 聚成1 類,S2、S13、S4、S11、S7 聚為1 類,其余批次聚為1 類;當歐氏平方距離為15時,其可分為6 類,S1 為1 類,S2 為1 類,S13 為1 類,S20、S21 聚為1 類,S4、S7、S11 聚為1 類,其余聚為1類。取歐氏平方距離為20,可知產地為安徽省的2 批藥材聚為1 類,為黔南布依族苗族自治州的聚為1 類,為貴州遵義的單獨聚為1 類。S20、S21 與其他產地藥材存在一定差異,其2、3 號峰的相對峰面積明顯大于其他批次,可能是與其他批次樣品被聚為2 類的原因。
2.7 主成分分析 采用SPSS 18.0 軟件,導入21 批樣品12 個共有峰的量化峰面積,以主成分的特征值及貢獻率為參考依據進行主成分因子分析,計算累積方差貢獻率及綜合得分,得到總方差解釋變異量,見表5。采用正交性旋轉法,得到12 個共有峰在5 個主成分中的旋轉矩陣,見表6。
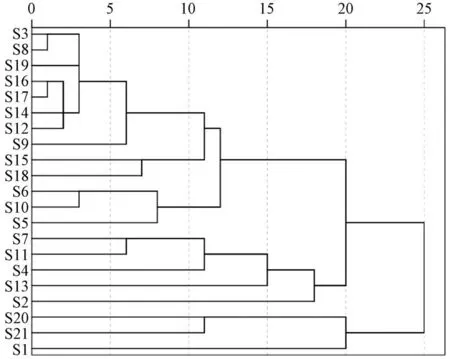
圖4 21 批樣品聚類分析樹狀圖

表5 主成分特征值及方差
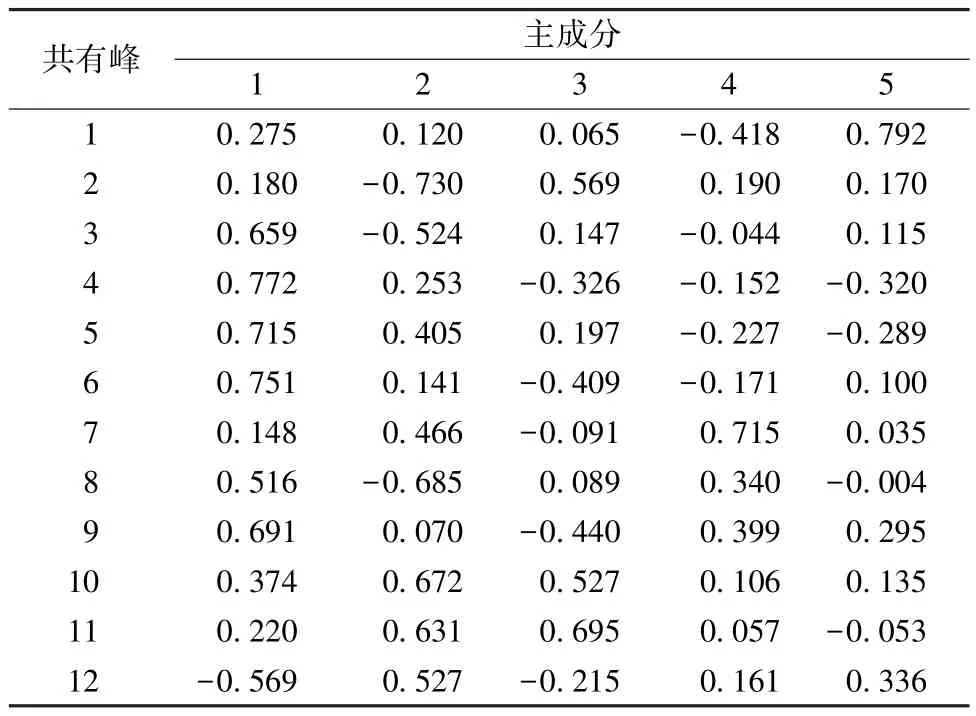
表6 各主成分矩陣
根據表6,以Z1、Z2、Z3、Z4、Z5分別代表主成分1、2、3、4、5,Z代表5 個主成分綜合值,X1~X12分別代表12 個共有峰峰面積的標準化數值,用于反映21 批樣品所表征的信息,得到線性組合表達式分別為Z1=0.275X1+0.180X2+0.659X3+0.772X4+0.715X5+0.751X6+0.148X7+0.516X8+0.691X9+0.374X10+0.220X11-0.569X12、Z2=0.120X1-0.730X2-0.524X3+0.253X4+0.405X5+0.141X6+0.466X7-0.685X8+0.070X9+0.672X10+0.631X11+0.527X12、Z3=0.065X1+0.569X2+0.147X3-0.326X4+0.197X5-0.409X6-0.091X7+0.089X8-0.440X9+0.527X10+0.695X11-0.215X12、Z4=-0.418X1+0.190X2-0.044X3-0.152X4-0.227X5-0.171X6+0.715X7+0.340X8+0.399X9+0.106X10+0.057X11+0.161X12、Z5=0.792X1+0.170X2+0.115X3-0.320X4-0.289X5+0.100X6+0.035X7-0.004X8+0.295X9+0.135X10-0.053X11+0.336X12。
將上述所得表達式加合,構建綜合評價函數,得到21批樣品的綜合得分,將其進行排序,結果見表7。
Z=0.833X1+0.379X2+0.353X3+0.227X4+0.801X5+0.412X6+1.274X7+0.255X8+1.015X9+1.813X10+1.550X11+0.240X12。Z值越大,表明藥材的綜合質量越高。
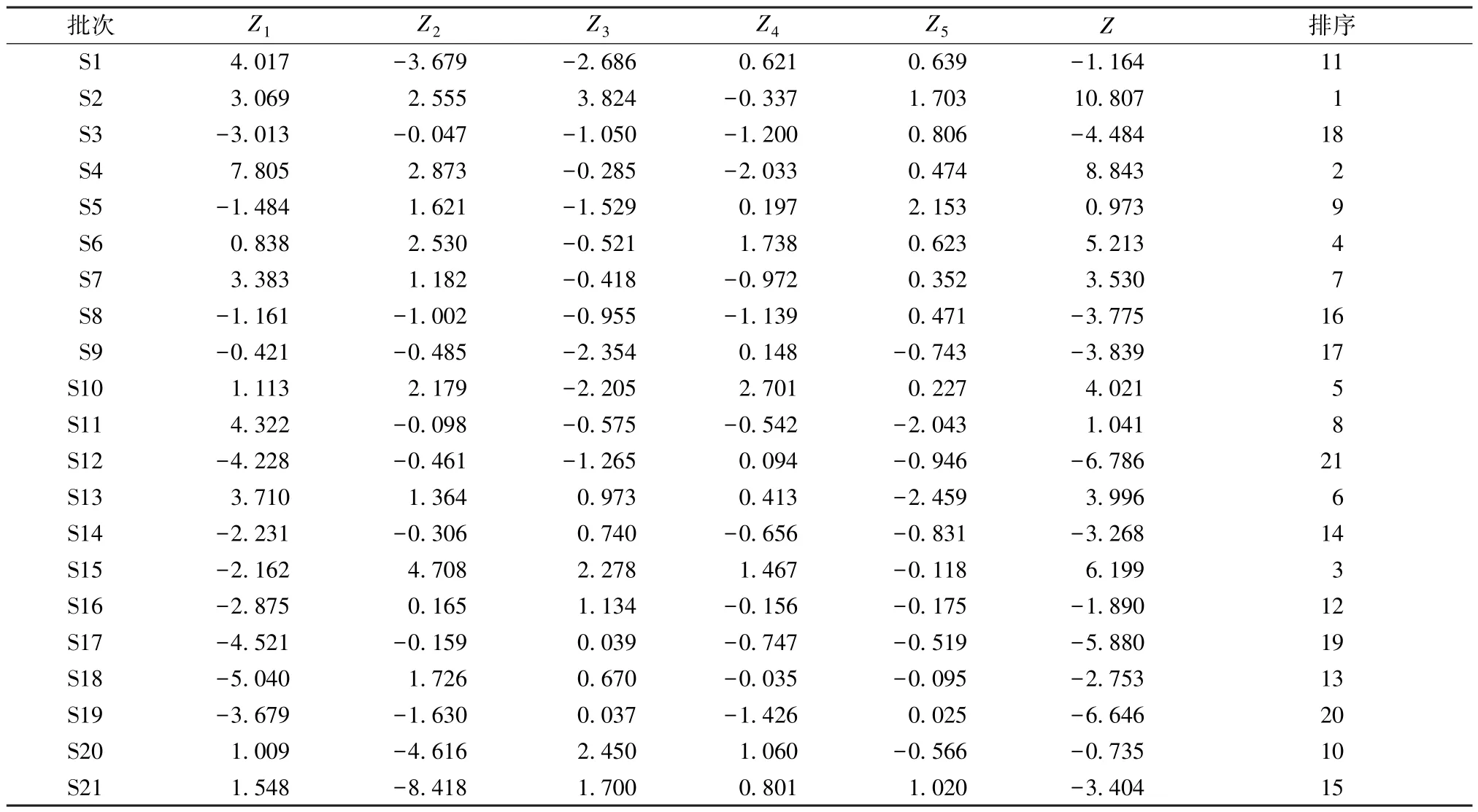
表7 各樣品主成分得分及排序
不同樣品綜合得分依次為S2>S4>S15>S6>S10>S13>S7>S11>S5>S20>S1>S16>S18>S14>S21>S8>S9>S3>S17>S19>S12,在排名前10 的藥材中,產地為黔西南布依族苗族自治州的占60%,為貴州省黔南布依族苗族自治州的占20%,為貴州省黔東南苗族侗族自治州的占10%,為安徽省黃山的占10%。
以主成分1、2、3 的得分值建立其三維坐標體系的散點圖,見圖5。由此可知,S1 距離較遠,聚為一類;S20與S21 距離較近,聚為一類;S2、S4、S7、S11、S13 距離較近,聚為一類;其余樣品聚為一類,結果與聚類分析、相似度評價一致。
3 討論

圖5 21 批樣品三維散點圖
本實驗對Thermo Hyperil GOLD-C18(250 mm×4.6 mm,5 μm)、Thermo Accucore-C18(150 mm×4.6 mm,2.6 μm)色譜柱進行考察,發現前者分離效果優于后者;對流動相(甲醇-水、甲醇-0.1% 磷酸、乙腈-0.1% 磷酸) 及柱溫(25、30、35 ℃) 進行考察,發現流動相為乙腈-0.1% 磷酸、柱溫為35 ℃時,色譜峰分離效果較佳。此外,對提取方法(超聲、回流)、提取溶劑(甲醇、乙醇) 及其體積分數 (55%、65%、75%、85%、95%、100%)、料液比(1∶30、1∶50、1∶70、1∶90、1∶110)、提取時間(10、20、30、40、50、60 min)、提取次數進行考察。最終,確定85%甲醇超聲提取3 次,每次20 min 作為最優提取條件。
S20、S21 與其余分布區的石吊蘭相似度低,即安徽省產的這2 批藥材與貴州省具有一定差異;在貴州省內,大部分黔南分布區產的藥材與其他產區相似度低。聚類分析將安徽省產的2 批藥材聚為1 類,貴州省內分布區產的聚為1 類,可能是由于地理環境、氣候的差異所致;貴州省遵義地區產的藥材被單獨分為1 類,可能是由于采收時間靠前、分布地區較其余批次遠、年均氣溫低于大部分地區等原因所致。
綜上所述,本研究建立了石吊蘭HPLC 指紋圖譜,并結合聚類分析、主成分分析對該藥材的質量進行綜合評價,可為其品種鑒別、種質篩選提供參考。

