先天性食管裂孔疝合并貧血圍手術期管理策略的對照研究1
周玲 姚海霞 顏景灝 李水學 姚虹
先天性食管裂孔疝是由于先天解剖因素導致的膈肌食管裂孔過大并伴有膈肌腳發育異常,導致腹腔臟器通過擴張的食管裂孔進入胸腔,形成的疝[1]。國外有關學者報道發病率約在4.7%~16%,國內有關學者報道發病率約為3%[2‐3]。目前先天性食管裂孔分為Ⅰ型滑動性食管裂孔疝(95%),Ⅱ型食管旁裂孔疝(5%),Ⅲ型混合型疝(10%),Ⅳ型復雜疝(0.5%)等四種類型。先天性食管裂孔疝合并貧血較為少見,患兒常常以貧血為首發癥狀就診于小兒內科,其原發病常常被忽視,使先天性食管裂孔延誤診治,加重患兒貧血情況,影響生長發育[4‐5]。國外有學者研究認為食管裂孔疝合并貧血的原因可能是由于胃疝入胸腔,胃壁反復摩擦后形成潰瘍,導致胃出血造成的貧血[6]。也有學者認為是由于胃疝入胸腔,造成胃酸分泌減少影響鐵吸收導致貧血[7]。目前,業界對先天性食管裂孔疝合并貧血的的病因不明確,圍手術期管理尚未達成統一,其中對先天性食管裂孔疝合并貧血圍手術期管理的研究尚屬空白。因此,本研究回顧性分析疆維吾爾自治區人民醫院先天性食管裂孔疝合并貧血的臨床資料,探討圍手術期管理食管裂孔疝合并貧血的治療策略。
資料與方法
一、一般資料
收集2008年7月至2018年4月就診于新疆維吾爾自治區人民醫院40例先天性食管裂孔疝合并貧血患兒的病例資料;A組患兒中有4例消化道出血癥狀,其中以嘔吐為主訴就診的10例,以貧血為主訴就診的10例;病理分型Ⅰ型14例,Ⅱ型4例,Ⅲ型2例;民族占比:維吾爾族8例,哈薩克族7例,漢族5例。B組患兒中5例有消化道出血癥狀,以嘔吐為主訴就診的12例,以貧血為主訴就診的8例,其中Ⅰ型15例,Ⅱ型3例,Ⅲ型2例,維吾爾族5例,漢族15例。兩組患者術前資料組間差異無統計學意義(P>0.05)(表1)。
二、納入與排除標準
1.納入標準:(1)經消化道造影明確診斷為先天性食管裂孔疝并且血紅蛋白(hemoglobin,Hb)<110g/L;(2)年齡<14歲。
2.排除標準:(1)合并患有其他可能導致貧血疾病的患兒。
三、術前準備
兩組患兒術前均行常規術前準備,完善鐵代謝檢查,均給予糾正貧血治療,A組患兒中18例18次接受輸血22 U懸浮紅細胞治療,B組患兒中有18例22次接受輸血22 U懸浮紅細胞治療;所有患兒均給予口服鐵劑治療,每日動態監測Hb變化,圍手術期管理策略不同點在于A組患兒Hb>70 g/L時行手術治療,B組患兒Hb>90 g/L時行手術治療。
四、手術方式
手術均由有腹腔鏡操作資質的小兒外科專科主任醫師主刀完成,全身麻醉生效后,患兒取合適體位;分別于臍上、左側腹、右側腹進入操作通道,其中左側腹進入腹腔監視器,臍上及右側腹進入操作器械。自患兒左側腹腔向對側分離肝脾韌帶,直至對側腹腔段食管,超聲刀解剖出食管后間隙,良好顯露膈肌腳,自右側腹腔向對側游離直至左側食管,血管阻斷帶將食管向后下方牽引,使腹段食管及對側膈肌腳充分暴露,間斷關閉食管裂孔,縫線材料使用不可吸收線。自左側向右側牽拉胃底包繞食360°,將胃底與胃前壁不可吸收線間斷縫合3~4針,形成Nissen胃底折疊術。胃底與胃前壁縫合松緊以通過腹腔鏡無損傷抓鉗為準。
五、術后處理
術后按照規定常規預防性應用抗生素,均不需放置引流管。術后復查消化道造影,于術后3個月及往后每年定期門診隨訪。
六、觀察指標
記錄A、B兩組患兒術前Hb數值、糾正貧血的時間、相關費用、手術時間、術中出血量、術后住院時間、并發癥發生、術后3個月的血紅蛋白等臨床情況。
七、統計學分析方法
應用SPSS 20.0統計軟件對數據進行處理。計量資料采用±s表示.定量數據間比較采用t檢驗,定性數據的比較采用卡方檢驗。以P<0.05為差異有統計學意義。
結 果
一、一般情況
所有患兒均順利完成腹腔鏡下食管裂孔疝修補術+Nissen胃底折疊術,手術順利無中轉開腹。兩組患者術前血紅蛋白水平A組患兒較B組患兒低,無統計學意義。年齡、性別、體重等一般資料上無統計學差異(P>0.05)(表1)。
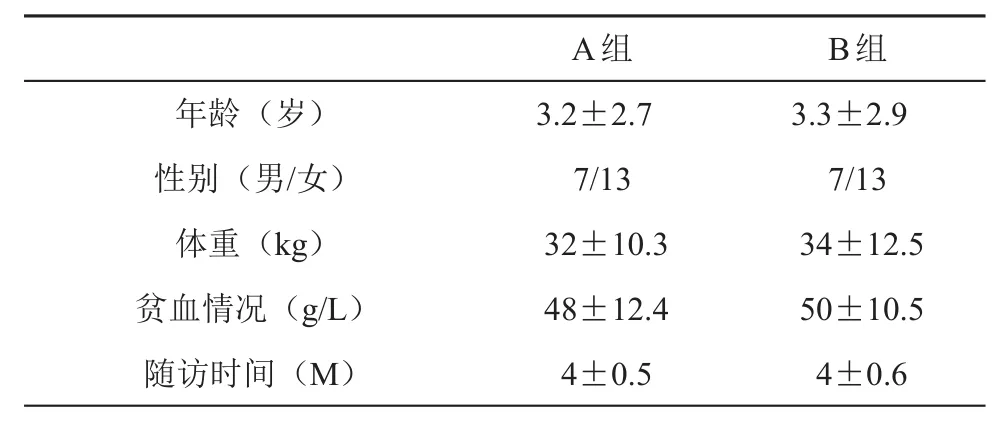
表1 一般情況
二、圍手術期情況
兩組患者術前糾正貧血的時間、相關費用、手術時間、術中出血量、術后住院時間、術后3個月的血紅蛋白等臨床資料(見表2)。A組糾正貧血時間及費用均明顯少于B組(P<0.05)。兩組手術時間、術中出血量、術后住院時間、術后3個月的血紅蛋白無統計學意義(P>0.05)。
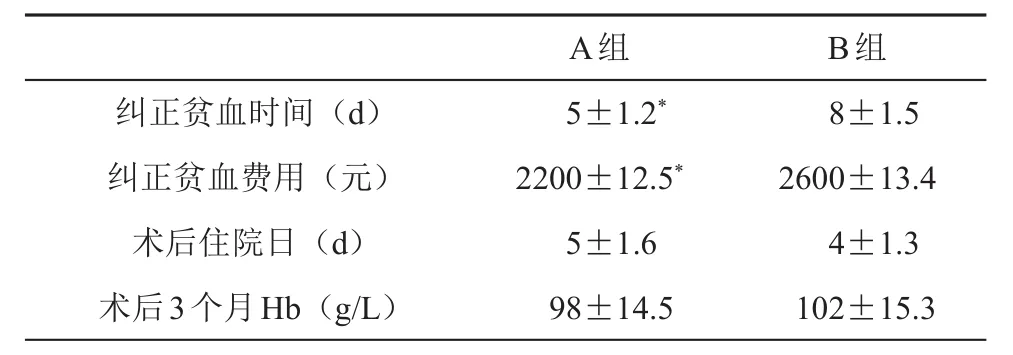
表2 兩組患者圍手術期的情況
三、影像學復查結果
兩組術后上消化道造影資料均可見食管裂疝消失。
四、并發癥發生情況
兩組共有7例(17.5%)出現不同并發癥。A組3例(5.4%),B組4例(2.7%)術后出現胃食管反流,給予對癥治療后,癥狀緩解。(見表3)。

表3 兩組患者術后并發癥發生情況
討 論
小兒先天性食管裂孔疝的主要癥狀常常是惡心、嘔吐,生發育延遲,合并貧血的患兒較為少見。但A組中有10例,B組中有8例是以貧血為首發癥狀就診小兒內科,小兒內科完善上消化道造影后明確診斷為先天性食管裂孔疝后轉診至我科。食管裂孔疝患者合并貧血的危險度2.9(95%CI=1.5~5.5)[8]。因此,食管裂孔疝是導致貧血的一個重要原因。成人食管裂孔疝合并貧血主要考慮原因與呼吸運動中胸腹壓力差使胃進入胸腔,造成胃壁充血腫脹,導致潰瘍的發生。隨著胸腹壓力的變化,胃進入胸腔的體積增大,更多的胃壁收到胸腔摩擦,降低胃酸的分泌,使患者對鐵離子的吸收能力下降,合并胃粘膜充血水腫導致胃潰瘍出血,所以引起的貧血也較重[9‐10]。但A組中有4例患兒出現消化道出血癥狀,B組患兒有5例有消化道出血癥狀,由于小兒的特殊性,尚不能用簡單的用成人經驗套用在小兒身上。飲食、生活習慣也影響著貧血的發生,A組貧血患兒中有15例、B組中有5例是生活在牧區的少數民族,長期無法獲得新鮮水果、蔬菜[14]以及豆類[15],對維生素C的攝取不足,造成鐵的吸收減少,影響血紅蛋白合成;同時由于保存條件的限制,食用的肉類主要以風干牛、羊肉為主,風干牛羊肉在制作過程中鐵離子大量流失造成鐵的攝入不足,鐵的吸收減少、攝入不足[16],有關學者認為小兒貧血可能具有地域或者民族聚居性[11],對此仍需要更進一步研究。同時,也應加強對兒內科醫生溝通與交流,A組患兒中有10例,B組患兒中有8例是糾正貧血為目的首診于兒內科,兒內科醫師在面對貧血患兒時應積極完善上消化道造影,排除由于先天性食管裂孔疝造成的貧血,尤其是在缺乏小兒外科專科醫生的基層醫院,往往缺少對先天性食管裂孔疝的認識,在面對無明顯消化道癥狀的食管裂孔疝造成的貧血;由于對疾病認識不足,造成對患兒診療延誤。
國外學者對先天性食管裂孔疝合并貧血患兒的患兒術前均給予常規糾正貧血治療即達到手術要求(Hg≥90 g/L),并在完成手術后3個月患兒貧血癥狀消失[12‐13]。本研究中A組與B組先天性食管裂疝合并貧血患兒按照年齡、性別、體重、術前Hb進行1:1配比,年齡、性別、體重、術前Hb均無差異,但在圍手術期糾正貧血過程中,因為最終治療的終點目標不一樣,糾正貧血的時間及費用A組少于B組,并且有統計學差異,說明在圍手術期糾正貧血過程中A組較B組患兒圍手術期糾正貧血的時間更短,費用也更低。
有國外研究者提出成人外科圍術期中自體輸血等技術是安全、可靠的,但兒童的圍手術期的輸血不良反應會增加患兒的死亡率,所以在兒童圍手術期管理中,減少輸血可能會降低患兒的死亡率[17]。兒童相較成人血液總量較少,而外科手術創傷大,術中、術后出血風險大,更易出現圍手術期失血性貧血[18]。失血性貧血所帶來的低血容量休克是導致小兒圍手術期中循環衰竭常見原因,故維持血容量非常重要[19]。圍手術期的貧血會導致機會性感染風險的增加,引發嚴重并發癥發生[20]。目前腹腔鏡下食管裂孔疝修補術+胃底折疊術可以有效的減少術中出血,降低圍手術期嚴重并發癥的發生[21]。尤其是Nissen胃底折疊術較其他胃底折疊術術后抗反流機制更為確切、有效[22]。本研究中對A組患兒適當的放寬手術指針,在糾正貧血的過程中積極準備微創手術治療,在Hg>70 g/L時就進行微創手術治療,B組患兒常規術前準備,在在Hg>90 g/L時才行微創手術治療,A組與B組患兒術中出血量、術后住院時間、術后3個月的血紅蛋白均無差異,A組20例患兒均順利完成腔鏡下食管裂孔疝修補術+Nissen胃底折疊術,術后隨訪3個月均無嚴重并發癥發生;說明對先天性食管裂空疝合并貧血的患兒適當的放寬手術指針(Hb>70 g/L),積極進行腹腔鏡下食管裂孔疝修補術+Nissen胃底折疊術治療先天性食管裂孔疝是安全可行,并不會因為術前Hb<90 g/L而造成圍手術期嚴重并發癥的發生。并且可以有效的縮短患兒的住院時間,減輕患兒家庭的經濟負擔,降低由于反復輸血增加的不良反應的發生概率[23‐24]。
但本研究由于是回顧性的病例對照研究,證據等級較低病例較少,隨訪時間較短,對Hb>70 g/L行手術治療的患兒未進行長期隨訪,遠期并發癥尚不能評估,先天性食管裂孔疝合并貧血的病因尚不能明確。
先天性食管裂孔疝合并貧血患兒在適當放寬手術指征(Hb≥80 g/L)的情況下,積極行腹腔鏡下食管裂孔疝修補術+Nissen胃底折疊術根治食管裂孔疝是安全、有效的;對于先天性食管裂孔疝合并貧血完成手術根治原發病是治療貧血的根本措施。

