山東某院耐碳青霉烯類腸桿菌科細菌臨床感染特征及耐藥基因分析
陸書華, 李曉哲, 劉凌云, 金呈強, 戈寧寧, 董海新
(濟寧醫學院附屬醫院,山東 濟寧 272000)
隨著碳青霉烯類抗菌藥物在臨床的廣泛應用,耐碳青霉烯類腸桿菌科細菌(carbapenemresistantEnterobacteriaceae,CRE)的分離率逐年增加。CRE的耐藥機制極為復雜,是臨床抗感染治療的難點。本研究旨在探討濟寧醫學院附屬醫院CRE的臨床感染特征、藥物敏感性及基因分型,為預防和治療CRE感染及醫院多重耐藥菌管理提供參考。
1 材料和方法
1.1 菌株來源
收集濟寧醫學院附屬醫院2017年7月—2018年12月CRE非重復臨床分離株,-80℃保存。質控菌株大腸埃希菌(ATCC 25922)和肺炎克雷伯菌(ATCC 700603)均由我國國家衛生健康委員會臨床檢驗中心提供。
1.2 方法
1.2.1 細菌鑒定及體外藥物敏感性試驗 菌種經復溫、增菌、培養后,根據《全國臨床檢驗操作規程》(第4版)要求進行分離培養。所有菌株經VITEK 2 Compact全自動微生物鑒定系統及配套革蘭陰性菌鑒定卡(法國生物梅里埃公司)進行細菌鑒定,并采用VITEK-MS全自動快速微生物質譜檢測系統(法國生物梅里埃公司)確證。采用稀釋法測定CRE最小抑菌濃度(minimum inhibitory concentration,MIC),抗菌藥物包括替加環素、頭孢唑啉、氨芐西林、氨芐西林-舒巴坦、替卡西林-克拉維酸、阿米卡星、頭孢曲松、亞胺培南、美羅培南、頭孢噻肟、哌拉西林、哌拉西林-他唑巴坦、厄他培南、氨曲南、復方磺胺甲噁唑、環丙沙星、左氧氟沙星、慶大霉素、頭孢吡肟、頭孢他啶、頭孢哌酮-舒巴坦、頭孢替坦、妥布霉素、四環素。頭孢哌酮-舒巴坦采用紙片擴散法測定抑菌環直徑,結果判定參照美國臨床實驗室標準化協會(the Clinical and Laboratory Standards Institute,CLSI)2018年版標準;替加環素采用E試驗試紙條(法國生物梅里埃公司)測定MIC,結果判定參照美國食品與藥品監督管理局(U. S. Food and Drug Administration,FDA)推薦的解釋標準,MIC≤2.0 mg/L為敏感,MIC=4.0 mg/L為中介,MIC≥8.0 mg/L為耐藥。
1.2.2 簡易碳青霉烯類滅活(simplified carbapenem inactivation method,sCIM)試驗 將過夜生長的大腸埃希菌(ATCC 25922)用肉湯調到0.5麥氏單位,直接涂布于M-H平板,將直接粘取待測CRE后的亞胺培南藥物敏感性試驗紙片放入涂有大腸埃希菌(ATCC 25922)的M-H平板,35 ℃培養16~18 h后,測量抑菌環直徑,抑菌環直徑<20 mm或為21~22 mm,環中大腸埃希菌菌落出現衛星現象為陽性;抑菌環直徑>25 mm為陰性;介于二者之間為不確定[1]。
1.2.3 Xpert Carba-R檢測 將大腸埃希菌(ATCC 25922)及待測菌株用0.9%氯化鈉溶液調至0.5麥氏單位,取2 mL菌液放入樣本處理液中,渦旋震蕩10 s,用新的移液管取2 mL液體加入試劑匣,然后放入儀器檢測,約1 h后讀取結果。
1.2.4 基因檢測 采用加熱煮沸法(100 ℃干浴10 min)提取菌株DNA模板,通過聚合酶鏈反應(polymerase chain reaction,PCR)擴增KPC、NDM、IMP、VIM和OXA-48基因序列,引物信息見表1,引物設計參考文獻[2-3]。擴增程序:95 ℃ 5 min預變性;95 ℃ 45 s變性;退火時間35 s,72 ℃ 50 s延伸,35個循環;72 ℃ 8 min再延伸。于2%瓊脂糖凝膠中擴增產物,用GelRed核酸染色劑染色,在Gel-Box凝膠成像系統中拍照并記錄結果。回收預期目的片段大小一致的PCR產物進行測序,所得堿基基因序列與美國國立生物技術信息中心(the National Center for Biotechnology Information,NCBI)數據庫中的已知序列進行比對,確證擴增產物的基因型別。
1.3 統計學方法
采用WHONET 5.4軟件進行數據處理與藥物敏感性試驗結果的統計學分析。

表1 碳青霉烯酶PCR引物信息
2 結果
2.1 CRE分離情況
2017年7月—2018年12月,濟寧醫學院附屬醫院送檢CRE的患者231例,有87例檢出CRE,其中6例患者不同部位的臨床樣本中同時檢出CRE。剔除同一患者相同部位的重復菌株,本研究納入CRE 93株。
2.1.1 CRE樣本來源 93株CRE臨床分離株中,有52株(55.91%)分離自痰液樣本,11株(11.83%)分離自血液樣本,8株(8.60%)分離自中段尿樣本,5株(5.38%)分離自肺泡灌洗液樣本,4株(4.30%)分離自分泌物樣本,膿液、膽汁樣本中各分離出3株(3.23%),腦脊液、穿刺液和引流液樣本中各分離出2株(2.15%),胸水樣本中分離出1株(1.07%)。
2.1.2 CRE科室分布 CRE主要分離自重癥監護病房(45株,48.39%),以下依次為:康復科(9株,9.68%),呼吸內科(6株,6.45%),血液科(5株,5.38%),肝膽科、創傷骨科、兒科各4株(4.30%),神經內科、急診科各3株(3.23%),神經外科監護病房、腎內科各2株(2.15%),泌尿科、燒傷科、神經外科、胃腸外科、手足外科、小兒外科各1株(1.08%)。
2.1.3 CRE菌種分布 93株CRE臨床分離株中,肺炎克雷伯菌59株(63.44%)、大腸埃希菌29株(31.18%)、陰溝腸桿菌4株(4.30%)、弗勞地檸檬酸桿菌1株(1.08%)。
2.2 體外藥物敏感性試驗結果
93株CRE對24種臨床常用抗菌藥物的耐藥率見表2。
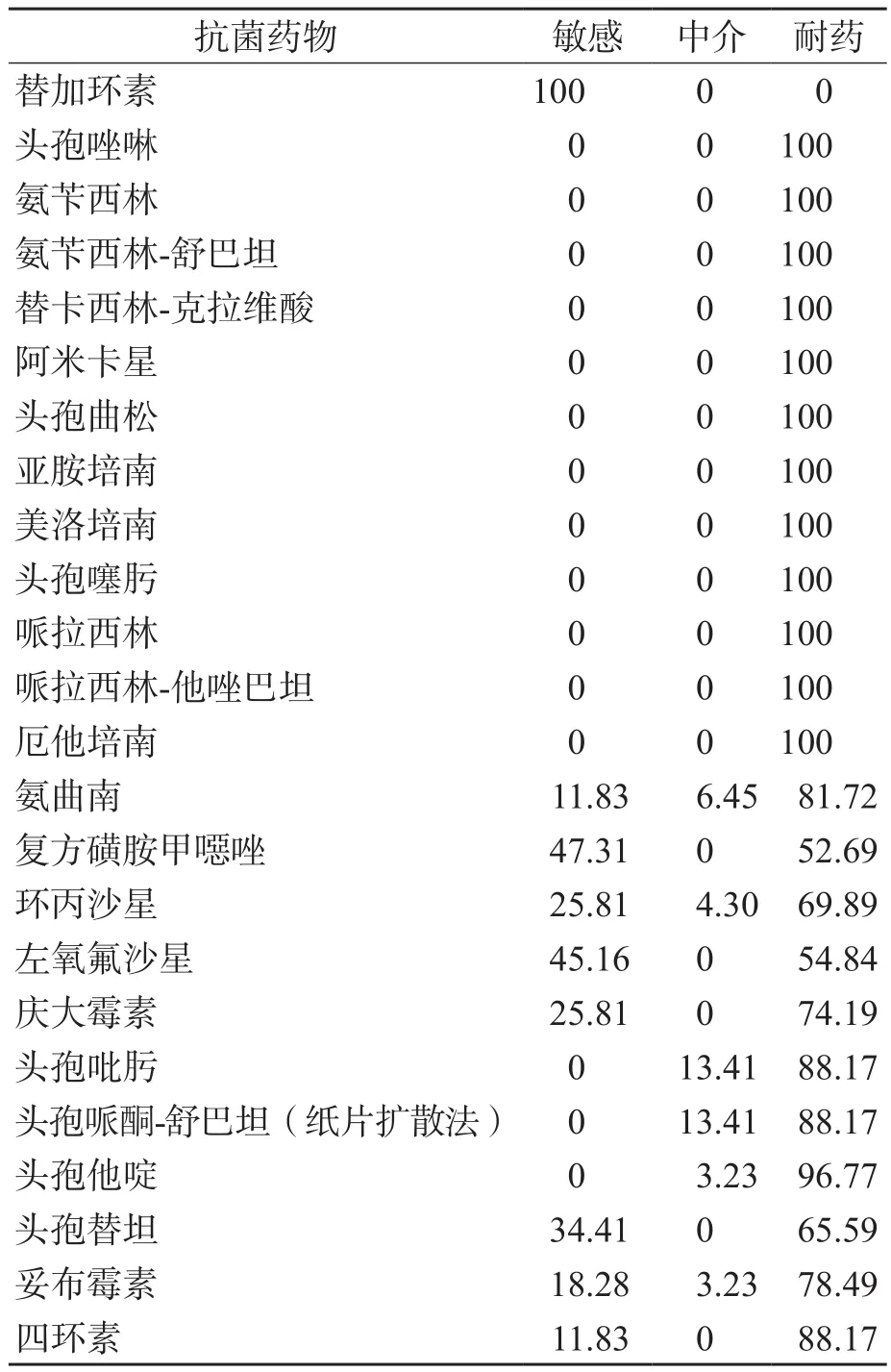
表2 CRE對24種抗菌藥物的耐藥率 %
2.3 sCIM試驗結果
93株CRE臨床分離株中,有79株(84.95%)產碳青霉烯酶,其中肺炎克雷伯菌52株、大腸埃希菌23株、陰溝腸桿菌3株、弗勞地檸檬酸桿菌1株。部分結果見圖1。
2.4 Xpert Carba-R檢測結果
79株產碳青霉烯酶CRE中,KPC基因陽性38株(48.10%),NDM基因陽性31株(39.24%),IMP基因陽性6株(7.59%),NDM+KPC基因陽性4株(5.06%),未檢出VIM及OXA-48 耐藥基因。
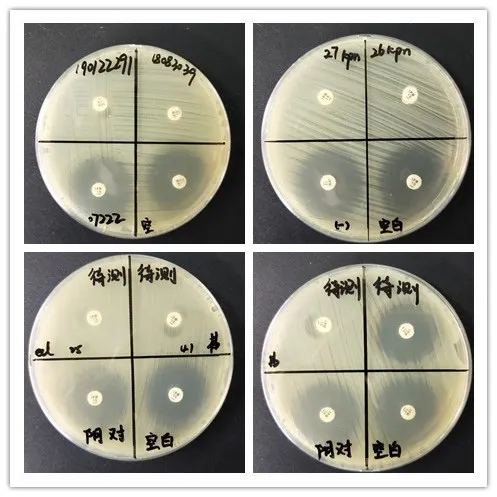
圖1 部分sCIM試驗結果
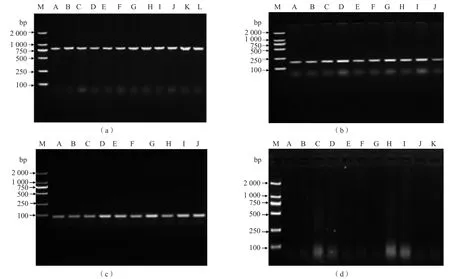
圖2 PCR產物瓊脂糖凝膠電泳圖譜
2.5 PCR基因擴增結果
52株肺炎克雷伯菌中,38株攜帶KPC耐藥基因,10株攜帶NDM耐藥基因,4株同時攜帶KPC和NDM耐藥基因。23株大腸埃希菌中,18株攜帶NDM耐藥基因,5株攜帶IMP耐藥基因。3株陰溝腸桿菌中,2株攜帶NDM耐藥基,1株攜帶IMP耐藥基因。1株弗勞地檸檬酸桿菌攜帶NDM耐藥基。有14株CRE未檢出本研究涉及的耐藥基因,未檢出VIM及OXA-48耐藥基因。擴增產物KPC測序結果與NCBI數據庫中的基因登錄號(KU680813.1)完全一致,即為KPC-2;擴增產物IMP測序結果與NCBI數據庫中的基因登錄號(KU051710.1)完全一致,即為IMP-4;擴增產物NDM測序結果與NCBI數據庫中的基因登錄號(JF826285.1 )完全一致,即為NDM-1。見圖2。
3 討論
近年來,CRE在世界范圍內散發或暴發流行,對全球的公共衛生構成了重大威脅[4],2017年,世界衛生組織將CRE列為21世紀最重要的耐藥病原菌之一。目前CRE分離率較高的國家除我國外,還包括希臘、意大利、巴西,以及美國和哥倫比亞[5-6]。有研究結果表明,2014—2015年,我國27個省市的肺炎克雷伯菌、大腸埃希菌的碳青霉烯類耐藥率分別為8%和2%;收集的999株CRE中,肺炎克雷伯菌、大腸埃希菌、腸桿菌科細菌所占比例分別為70%、16%和13%,其中92%的肺炎克雷伯菌和大腸埃希菌產碳青霉烯酶;KPC(63%)和NDM(34%)仍是主要的產酶類型,且有2%的菌株同時表達KPC和NDM基因[7]。
濟寧醫學院附屬醫院CRE的分離率也在逐年增加,2015年上報多重耐藥菌1 245株,其中CRE 24株(1.93%);2016年上報多重耐藥菌1 406株,其中CRE 30株(2.13%);2017年上報多重耐藥菌2 463株,其中CRE 100株(4.06%);2018年上報多重耐藥菌2 703株,其中CRE 166株(6.14%)。CRE主要分離自痰液樣本,其次是血液和尿液樣本,這與濟寧醫學院附屬醫院樣本結構有關。CRE主要分布在重癥監護病房,可能與重癥監護病房患者病因復雜且病情危重,高效廣譜抗菌藥物使用率高和有創操作治療較多有關[8]。
腸桿菌科細菌對碳青霉烯類耐藥的機制包括產碳青霉烯酶和非產碳青霉烯酶2類,其中產碳青霉烯酶是主要的耐藥機制。碳青霉烯酶基因常位于MDR質粒上,可在不同腸桿菌科細菌之間傳播。按照Ambler分子分類方法可將碳青霉烯酶分為A、B、D 3類,A類包括KPC、IMI、NMC、SME和GES等,B類也稱為金屬酶,包括IMP、VIM、NDM、SPM和GIM等,D類包括OXA-48、OXA-181、OXA-204和OXA-232。其中,A類酶中的KPC,B類酶中的NDM、VIM和IMP,以及D類酶中的OXA-48是腸桿菌科細菌中最常見的碳青霉烯酶。
實驗室可以通過碳青霉烯酶表型試驗或碳青霉烯酶耐藥基因的分子生物學試驗來檢測CRE。碳青霉烯酶表型檢測試驗包括改良Hodge試驗、Carba NP試驗、碳青霉烯類滅活(carbapenem inactivation method,CIM)試驗、乙二胺四乙酸-碳青霉烯類滅活(ethylenediaminetetraacetic acid-modified carbapenem inactivation method,eCIM)試驗等[9]。近年來也有研究者通過基質輔助激光解析電離-飛行時間質譜檢測碳青霉烯類抗菌藥物的水解來檢測碳青霉烯酶的活性。本研究采用一種新的碳青霉烯酶表型確證方法——sCIM,檢測腸桿菌科細菌碳青霉烯酶,sCIM與mCIM檢測原理相似,都是基于碳青霉烯酶能水解碳青霉烯類抗菌藥物,但sCIM操作方法較mCIM更簡單,更加適合臨床實驗室常規操作,在分析的93株CRE臨床分離株中,84.95%產生碳青霉烯酶,與ZHANG等[10]的研究結果基本一致。本研究采用Xpert Carba-R,48 min檢測KPC、NDM、VIM、OXA和IMP-1 5種碳青霉烯酶基因,是目前唯一可快速檢測并鑒別多種碳青霉烯酶基因的即時分子診斷方法,可直接檢測尿、拭子等臨床樣本,樣本處理只需簡單的3個步驟,耗時僅1 min,上機檢測后48 min即可獲得檢測結果,每種基因的檢測下限都可達102 CFU/拭子,可快速發現耐碳青霉烯酶菌株定植患者。Xpert Carba-R對應的敏感性及特異性分別為94.5%和100%,檢測時長僅48 min,為最快出結果的檢測方法。通過檢測及結果對比,sCIM試驗確證碳青霉烯酶表型與PCR金標準的符合率為100%,Xpert Carba-R碳青霉烯酶檢出率與PCR金標準的符合率為100%。綜合多種CRE檢測方法,本研究建議使用sCIM法簡便地確證腸桿菌科細菌碳青霉烯酶,對于急癥患者宜采用Xpert Carba-R檢測并鑒別碳青霉烯酶分型。
本研究測序驗證后的結果表明,93株CRE中有79株產碳青霉烯酶,其他為非產碳青霉烯酶菌株,可能為高產AmpC酶或超廣譜β-內酰胺酶合并外膜蛋白缺失以及外排泵過表達聯合外膜蛋白缺失所致。本研究中88%(52/59)的肺炎克雷伯菌,79%(23/29)的大腸埃希菌和75%(3/4)的陰溝腸桿菌攜帶碳青霉烯酶基因。肺炎克雷伯菌碳青霉烯酶耐藥基因主要為KPC型,大腸埃希菌主要為NDM型,與WANG等[11]的研究結果一致,可能是因為產KPC和NDM型耐藥基因均可由質粒介導,可通過菌株自身克隆以及不同菌種間水平轉移,導致耐藥菌株的廣泛傳播。
目前,碳青霉烯類抗菌藥物是唯一可選的治療產超廣譜β-內酰胺酶革蘭陰性細菌感染的抗菌藥物,然而CRE不但可以水解碳青霉烯類藥物,而且可以使頭孢菌素類、青霉素類等抗菌藥物失效,并對其他種類的抗菌藥物不同程度耐藥[12]。 使用單一抗菌藥物進行治療的成功率非常低,只有多種抗菌藥物聯合使用才能提高成功率。
綜上所述,CRE管理的核心問題在于:(1)快速甄別產碳青霉烯酶菌株,遏制其快速發展;(2)確定早期、快速篩查的方法,并結合全基因組測序等多種方法,對CRE感染快速溯源其傳播鏈條;(3)探索基于體外MIC的聯合方案下不同藥物組合[13]。臨床醫師需要準確掌握細菌耐藥情況,根據藥物敏感性試驗結果合理使用抗菌藥物,減少耐藥菌的產生。
本研究明確了濟寧醫學院附屬醫院CRE的臨床分布特征及耐藥基因,有助于及時遏制CRE的持續感染與流行,降低醫院CRE感染發生率,協助臨床醫師制定抗菌藥物使用策略,為醫院多重耐藥菌管理提供參考。

