丁苯酞軟膠囊聯合腦蛋白水解物對急性腦梗死患者NIHSS評分及Keap1-Nrf2/ARE信號傳導通路的影響
張立攀, 朱云亮
(濟寧醫學院附屬醫院, 山東 濟寧 272029)
急性腦梗死(Acute cerebral infarction,ACI)為臨床常見卒中類型,約占全部腦卒中60%~80%,且近年來,隨著我國人口結構改變,該病發病率逐年增長,受到臨床高度關注[1,2]。ACI后極易出現缺血性腦組織損傷,研究認為以核因子-E2相關因子2(Nrf2)為核心的Keap1-Nrf2/ARE信號轉導通路具有抗氧化應激、抗炎癥損傷、減輕鈣離子超載、抗細胞凋亡等多重作用,在維持腦組織細胞內氧化還原平衡狀態方面具有重要意義[3]。腦蛋白水解物作為腦血管輔助藥物,對ACI血小板活化抑制作用顯著,可緩解炎癥反應,減輕腦損傷,促進神經功能修復[4]。丁苯酞軟膠囊可阻斷ACI所致多個病理環節,維持腦缺血狀態下腦能量代謝、促進缺血區域腦血流量恢復,減少神經細胞凋亡,改善神經功能缺損癥狀[5]。本研究首次聯合采用丁苯酞軟膠囊、腦蛋白水解物治療ACI,分析其對患者神經功能(NIHSS)評分及Keap1-Nrf2/ARE信號傳導通路的影響。
1 資料與方法
1.1臨床資料:選取2016年8月至2019年7月我院93例ACI患者作為研究對象,納入標準:①符合依據《中國急性缺血性腦卒中診治指南2014》中ACI相關診斷標準[6],并經頭顱CT或MRI證實;②發病至入院時間<72h;③患者或其家屬自愿簽署本研究知情同意書;④本研究經我院醫學倫理委員會審核批準;排除標準:①伴有出血性傾向疾病者;②合并心、肝、腎等重要臟器功能障礙;③伴有免疫系統或血液系統疾病者;④發病前兩周內行重大手術者;⑤合并惡性腫瘤者;⑥過敏體質或對本研究所用藥物具有使用禁忌癥者。簡單隨機化分組,各31例。三組年齡、性別、發病時間、梗死部位、病情程度、合并癥等基線資料無明顯差異(P>0.05),見表1。
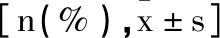
表1 三組臨床資料對比
1.2方 法
1.2.1治療方法:三組均根據《中國急性缺血性腦卒中診治指南2014》制定常規治療方案,包括穩定生命體征、控制血壓血糖、吸氧、糾正水電解質平衡等基礎治療,同時根據患者病情程度予以抗血小板聚集、改善腦功能、改善腦循環等藥物治療;于此基礎上,對照A組予以腦蛋白水解物(北京賽生藥業有限公司,國藥準字H11022185)治療,20mL腦蛋白水解物+250mL生理鹽水,靜脈滴注,60~120min滴完,1次/d;對照B組予以丁苯酞軟膠囊(石藥集團恩必普藥業有限公司,國藥準字H20050299)治療,200mg/次,3次/d;觀察組予以蛋白質水解物聯合丁苯酞軟膠囊治療,腦蛋白水解物、丁苯酞軟膠囊用法用量同對照A、B組。三組均連續治療14d。
1.2.2檢測方法:空腹狀態下抽取5mL肘靜脈血,高速離心處理(3000r/min,10min),留取血清待檢,采用酶聯免疫吸附法測定脂聯素(APN)、血管性假血友病因子(vWF)、白介素(IL)-8、IL-19、腫瘤壞死因子(TNF)-α,比色法測定血清超氧化物歧化酶(SOD)、丙二醛(MDA),試劑盒購自南京建成生物科技有限公司,嚴格按照試劑盒操作說明書進行;同時抽取外周血5mL采用免疫印跡法測定Keap1-Nrf2/ARE信號傳導通路相關蛋白表達,肝素抗凝后,分離出外周血淋巴細胞,提取PBMC,采用1640培養液洗滌2次,經重懸后收集至PBMC,加入細胞裂解液裂解,離心收集上層清夜取得總蛋白,BCA法測定并配平蛋白濃度,電轉移法轉移相應蛋白至PVDF膜上,以5%脫脂牛奶封閉液室溫下封閉2h,加入一抗4℃孵育過夜,次日TBST洗滌10min,共3次,加入經熒光標記的羊抗兔二抗孵育1h后洗膜,TBST洗滌10min,共3次,ECL發光顯影,采用QuantityOne軟件測定灰度值,計算蛋白條帶灰度值與內條帶灰度值比值表示目的蛋白相對表達水平。
1.3觀察指標:①臨床療效,參考《中國急性缺血性腦卒中診治指南2014》判斷患者治療后療效,基本控制:NIHSS評分下降>90%,病殘程度為0級;顯效:NIHSS評分下降46%~90%,病殘程度為1~3級;有效:NIHSS評分下降18%~45%;無效:NIHSS評分降低≤17或增加。總有效率=(基本控制+顯效+有效)/31×100%。②治療前、療程結束后神經功能及日常生活活動能力,以美國國立衛生研究院卒中量表(NIHSS)評分評估神經功能,分值越低,神經功能恢復越良好[7];Barthel指數評估日常生活活動能力,分值越高,日常生活活動能力越強。③治療前、療程結束后內皮功能指標APN、vWF水平。④治療前、療程結束后氧化應激指標SOD、MDA水平。⑤治療前、療程結束后血清炎性因子IL-19、IL-8、TNF-α水平。⑥治療前、療程結束后Keap1-Nrf2/ARE信號傳導通路相關蛋白表達。
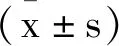
2 結 果
2.1臨床療效:觀察組臨床總有效率高于對照A、B組,差異有統計學意義(P<0.05),對照A、B組臨床總有效率相比,無明顯差異(P>0.0167),見表2。
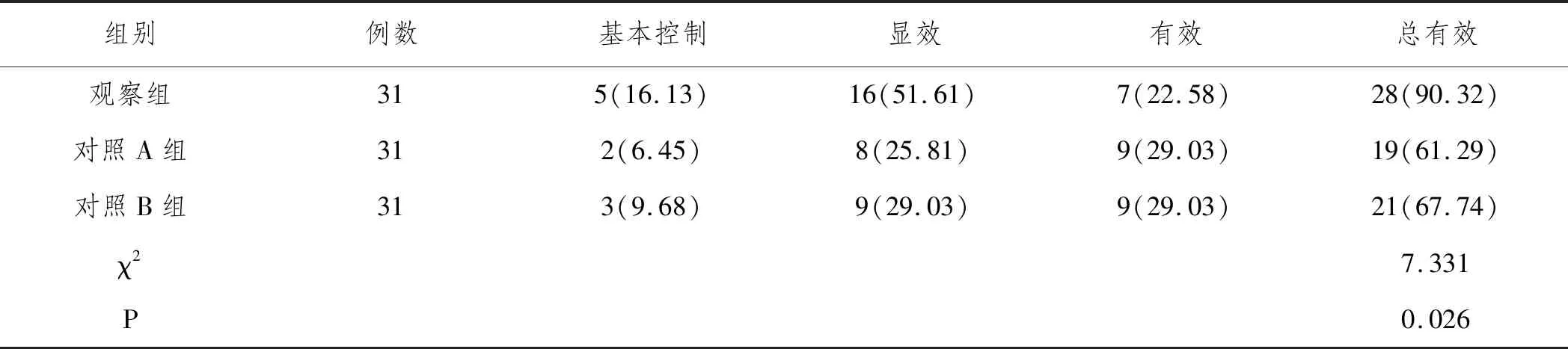
表2 三組臨床療效對比n(%)
2.2NIHSS評分、Barthel指數:三組NIHSS評分、Barthel指數組間、不同時間點的差異及組間·不同時間點交互作用均數有統計學意義(F1=12.314,F2=26.124,F3=19.052,F4=9.126,F5=25.134,F6=16.247,P<0.05),三組治療前NIHSS評分、Barthel指數相比,無明顯差異(P>0.05);療程結束后,觀察組NIHSS評分低于對照A、B組,Barthel指數高于對照A、B組(P<0.05),見表3。
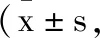
表3 三組NIHSS評分 Barthel指數對比分)
2.3內皮功能指標:三組APN、vWF水平組間、不同時間點差異及組間·不同時間點交互作用均有統計學意義(F1=10.125,F2=24.129,F3=19.742,F4=9.256,F5=25.175,F6=16.167,P<0.05),三組治療前血清APN、vWF水平相比,無明顯差異(P>0.05);療程結束后,觀察組血清vWF水平低于對照A、B組,APN水平高于對照A、B組(P<0.05)(P<0.05),見表4。
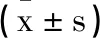
表4 三組內皮功能指標水平對比
2.4血清SOD、MDA水平:三組SOD、MDA水平組間、不同時間點差異及組間·不同時間點交互均有統計學意義(F1=9.745,F2=15.169,F3=13.256,F4=10.129,F5=27.141,F6=13.196,P<0.05),三組治療前血清MDA、SOD水平相比,無明顯差異(P>0.05);療程結束后,觀察組血清MDA水平低于對照A、B組,SOD水平高于對照A、B組(P<0.05),見表5。
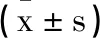
表5 三組血清SOD MDA水平對比
2.5血清炎性因子:三組IL-19、IL-8、TNF-α水平組間、不同時間點差異及組間·不同時間點交互均有統計學意義(F1=8.941,F2=16.174,F3=12.185,F4=11.254,F5=27.276,F6=14.251,F7=9.845,F8=24.312,F9=12.141,P<0.05),三組治療前血清IL-19、IL-8、TNF-α水平相比,無明顯差異(P>0.05);療程結束后,觀察組血清IL-19、IL-8、TNF-α水平低于對照A、B組(P<0.05)(P<0.05),見表6。
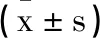
表6 三組血清炎性因子對比
2.6Keap1-Nrf2/ARE信號傳導通路相關蛋白:三組Keap1、NQO1、ARE、Nrf2表達水平組間、不同時間點差異及組間·不同時間點交互均有統計學意義(F1=8.172,F2=17.254,F3=14.135,F4=10.944,F5=25.126,F6=12.361,F7=8.125,F8=25.612,F9=15.141,F10=9.265,F11=24.756,F12=10.695,P<0.05),三組治療前Keap1、NQO1、ARE、Nrf2表達水平相比,無明顯差異(P>0.05);療程結束后,觀察組Keap1表達水平低于對照A、B組,NQO1、ARE、Nrf2表達水平高于對照A、B組(P<0.05),見表7。
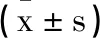
表7 三組Keap1-Nrf2/ARE信號傳導通路相關蛋白對比
3 討 論
ACI治療原則為抑制血栓擴展,縮小梗死范圍,盡快恢復缺血區域腦灌注,同時改善腦微循環,保護腦細胞,減輕缺血后再灌注損傷,防治腦細胞凋亡[8]。丁苯酞軟膠囊、腦蛋白水解物為腦血管疾病治療常用藥物,目前臨床多單一采用二者治療ACI,關于其聯合應用較為鮮見。本研究為進一步提高治療效果,聯合采用丁苯酞軟膠囊、腦蛋白水解物治療ACI,結果顯示療程結束后,觀察組NIHSS評分低于對照A、B組,Barthel指數高于對照A、B組,臨床療效優于對照A、B組,充分說明丁苯酞軟膠囊聯合腦蛋白水解物治療ACI,可顯著改善患者神經功能及日常生活活動能力,提高治療效果。此外,動脈硬化及血管內皮損傷的病理過程影響患者血清APN、vWF水平,血清APN、vWF水平可作為反映ACI患者腦血管受損程度及內皮功能[9]。本研究中,療程結束后,觀察組血清vWF水平低于對照A、B組,APN水平高于對照A、B組,提示丁苯酞軟膠囊聯合腦蛋白水解物可顯著改善患者血清APN、vWF水平,亦從血清層面進一步證實丁苯酞軟膠囊聯合腦蛋白水解物治療效果。原因在于①丁苯酞軟膠囊通過抑制谷氨酸釋放,解除微血管痙攣,抑制血小板聚集;保護血管內皮、加速血管生成,促進側支循環建立;減少線粒體電子傳遞鏈細胞色素C釋放,抑制神經元凋亡;保護線粒體功能,避免線粒體酶自我損傷,改善腦缺血再灌注引起的線粒體腫脹與功能異常;抑制氧化酶激活,防止脂質過氧化,發揮對缺血性神經元損傷的保護作用;②腦蛋白水解物可增加腦組織對氧利用率;增加腦組織無氧代謝時三磷酸腺苷生成;鈉離子拮抗,抑制鈣離子內流,降低氧自由基生成;調節腦內抑制性、興奮性物質平衡及有關激素生成,促進神經功能恢復;③丁苯酞軟膠囊、腦蛋白水解物作用機制不同,聯合應用,作用協同補充,進一步提高治療效果。
ACI后隨局部側支循環開放,受損腦組織缺血再灌注,致使大量自由基釋放,導致腦細胞膜脂質過氧化,產生微循環障礙及破壞腦細胞結構,為造成腦功能障礙的主要因素之一[10]。MDA為脂質過氧化反應中的代謝產物,可間接反應體內自由基水平,代表細胞受自由基損傷涉及脂質過氧化反應的程度;SOD作為體內自由基清除劑,可抑制氧自由基損傷腦細胞,減少缺血再灌注時腦組織過氧化產物生成,增加大腦皮層耐缺氧能力。此外,Keap1-Nrf2/ARE信號傳導通路作為一種氧化應激信號通路,在急性腦缺血后再灌注損傷中的作用可能是通過激活下游因子表達而發揮抗炎、抗氧化應激、抗凋亡等作用。本研究中,療程結束后,觀察組血清MDA、IL-19、IL-8、TNF-α、Keap1水平低于對照A、B組,SOD、NQO1、ARE、Nrf2水平高于對照A、B組,提示丁苯酞軟膠囊聯合腦蛋白水解物ACI,可降低患者血清MDA、IL-19、IL-8、TNF-α水平,提高SOD水平,調節Keap1-Nrf2/ARE信號傳導通路,從而達到抑制氧化應激反應目的。原因在于丁苯酞軟膠囊可加強自由基清除,抑制自由基產生,減少腦組織損傷后組織內有害物質增加,降低炎性反應,維護腦組織營養代謝;腦蛋白水解物具有鈣離子拮抗作用,可有效抑制鈣離子內流,減少氧自由基生成,抑制氧化應激反應,減輕ACI繼發性炎癥反應,二者聯合應用,可增強抗氧化應激能力,抑制炎性反應。
綜上所述,丁苯酞軟膠囊聯合腦蛋白水解物治療ACI,可明顯改善患者血管內皮功能,抑制氧化應激反應及炎癥反應,調節Keap1-Nrf2/ARE信號傳導通路相關蛋白,改善神經功能及日常生活活動能力,效果較為顯著。但本研究樣本量較小,還需臨床多中心、多渠道取樣,作進一步證實。

