應用CBCT評價CGF促進頜骨囊腫術后骨缺損修復的臨床研究
李欣,劉學,王楊,徐明
(華中科技大學協和深圳醫院 口腔科,廣東 深圳 518052)
0 引言
頜骨囊腫是口腔頜面外科的常見病與多發病,目前最常用的治療方法為手術摘除。但是,術后頜骨內遺留的骨腔易導致繼發感染、病理性骨折、種植牙骨量不足等并發癥的發生。為了促進骨缺損區的愈合,骨移植是目前治療頜骨囊腫術后骨缺損的主要方法。本研究應用錐體束CT(Cone Beam Computed Tomography,CBCT)評估濃縮生長因子(concentrated growth factors,CGF)聯合羥基磷灰石生物陶瓷及口腔修復膜應用于頜骨囊腫手術,促進骨缺損的愈合,取得了滿意的效果。
1 資料與方法
1.1 一般資料。病例收集2016年10月至2017年9月,于深圳市南山醫院口腔科就診,診斷頜骨囊腫并完成手術治療的病人60例,受試者年齡18-60歲,男女性別比近1:1。以相似年齡、性別分布平均分為3組(每組病患數20例),均采用徹底刮治的方法切除囊腫,所有手術均由第一作者主刀完成。納入標準:無不良煙酒嗜好及藥物過敏史;患者身體健康,無嚴重的全身系統性疾病;有較好的依從性。排除標準:不符合頜骨囊腫納入標準者;資料欠缺或不能配合手術者;骨質疏松患者;口腔衛生條件差者。
1.2 材料與設備。南山醫院口腔科手術患者自體血液;離心機(Silfradent 塞法登特公司,意大利);真空采血管;羥基磷灰石生物陶瓷(北京市意華健科貿有限責任公司,中國);口腔修復膜(煙臺正海生物技術有限公司,中國);CBCT Planmeca(Planmeca公司,芬蘭);手術器械(南山醫院口腔科)。
1.3 方法
1.3.1 CGF的制作:首先采集20-40 mL(2-4管)患者的靜脈血,注入試 管中,注滿后勿搖動,立即放入離心機的轉筒中。設定制備 CGF 程序,制備完成后,可見試管中分為三層,最上層為血清,中間為纖維蛋白層(CGF的主要載體),底層為紅細胞及血小板,留取纖維蛋白層及少部分底層的紅細胞層,并存儲在稀釋的抗菌溶液中備用。
1.3.2 手術方式:術前采用相同視野及拍攝參數拍攝CBCT,完善常規檢查,排除手術禁忌證,受累牙由同一位醫生行完善的根管治療或予以拔除。實驗組,手術采用口內角形或梯形切口,翻瓣、去骨,充分暴露囊腔并完整刮除囊腫;行根尖切除術,徹底搔刮根尖周圍及囊腔骨壁,球鉆修整骨創緣,生理鹽水沖洗;徹底止血后,將制備好的適量CGF剪碎至約1 mm大小顆粒,及羥基磷灰石生物陶瓷徹底混合,混合物填塞入缺損骨腔,適當加壓,平齊原骨創緣。后覆蓋海奧口腔修復膜,并將剩余的CGF材料壓制成膜,再以CGF膜覆蓋于海奧口腔修復膜之上表面,組織瓣對位縫合,關閉創口。術后應用抗生素3 d,復方氯己定含漱液漱口1周,7-10 d拆線。對照組,手術方式相同,只是未植入cgf。空白對照組,手術方式一樣,缺損骨腔內未植入任何材料。
1.3.3 術后隨訪:患者術后每隔3個月定期復診,臨床檢查創口愈合情況,相同視野及參數下拍攝CBCT。
1.4 測量方法。HU值:可反應出單位區域的平均骨礦物質含量,可作為骨缺損修復的重要指標。在植骨區和正常骨組織區截取相同面積的區域,分別測量HU值。HU差值=植骨區域平均HU值-正常區域平均HU值。HU差值越小說明植骨區與正常骨組織骨密度差距越小,骨愈合越快越好。選取骨缺損最長直徑對應的失狀面、冠狀面和軸面為測量平面,測量平面平均Hu值。同時測量頜骨對應正常位置相同面積平面的平均HU值。術后3個月、6個月分別測量。所有病例測量均由一人完成,且每個位置重復測量三次取平均值。
1.5 統計學分析。實驗數據采用SPSS 23.0統計軟件進行單因素方差分析,α=0.05。
2 結果
2.1 臨床檢查。術后觀察隨訪3-6個月。60例患者全身情況良好,口腔內術后傷口均達到一期甲級愈合,無感染、裂開,無膜暴露及骨粉溢漏,對應黏膜顏色、質地正常。
2.2 影像學觀察、測量數據分析。3個月、6個月時,組一(CGF+GBR)從失狀面、冠狀面及軸面三個面HU差值均優于組二(GBR)及組三(空白)。提示頜骨囊腫骨缺損區的愈合效果及愈合時間組一(CGF+GBR)最佳,并有顯著差異(P<0.05)。三組都可見到,術后6個月相比3個月骨缺損區域的愈合情況更好,詳情見表1、表2、表3。
表1 各時間段各組冠狀面HU差值及統計學分析(±s)
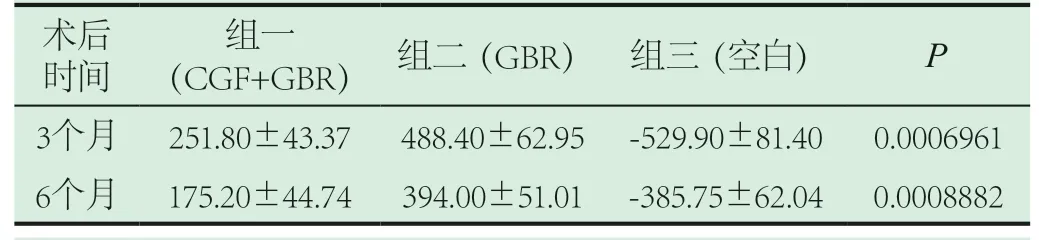
表1 各時間段各組冠狀面HU差值及統計學分析(±s)
?
表2 各時間段各組失狀面HU差值及統計學分析(±s)
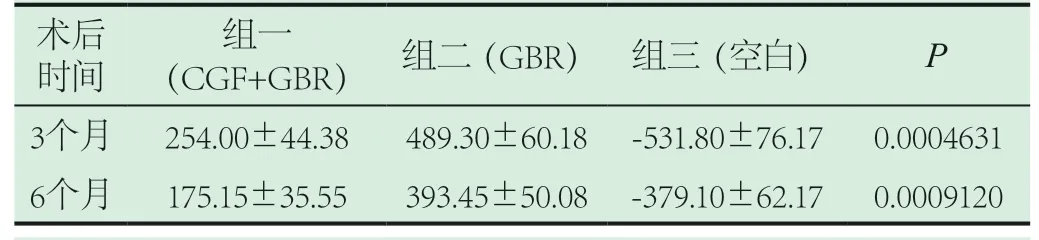
表2 各時間段各組失狀面HU差值及統計學分析(±s)
?
表3 各時間段各組軸面HU差值及統計學分析(±s)

表3 各時間段各組軸面HU差值及統計學分析(±s)
?
3 討論
Buser等在1993年提出了引導骨再生(GBR)的概念。現在,GBR技術已被廣泛應用在牙槽外科、牙周科和口腔種植領域[1]。在GBR技術中各種骨替代材料與血漿提取物的混合使用在目前的臨床應用中被廣泛使用。
濃縮生長因子(CGF)是Sacco首次開發出來的,由靜脈血分離制作而成[2]。是繼富血小板血漿(plateletrich plasma,PRP)和富血小板纖維蛋白(platelet-rich fibrin,PRF)之后的第三代血漿提取物,促進骨缺損修復和軟組織愈合[3-5]。
CGF技術是以患者自身靜脈血為原料,通過梯度密度離心的方法獲得,再單獨或聯合其他生物材料注入硬組織缺損或軟組織創傷處,從而修補缺損,誘導生長,加速局部創傷的愈合并提高愈合質量。其中的濃縮生長因子包含:骨形成蛋白(BMPs)、血管內皮生長因子(VEGF)、表皮生長因子(EGF)、轉移生長因子-β(TGF-β)、血小板衍生生長因子(PDGF)、類胰島素生長因子(IGF)、以及成纖維細胞生長因子(FGF)等,它們有促進細胞增殖、促進血管生成、移植物存活及誘導骨組織再生的作用[6],并具有修復促進和促進創口愈合的功能[7]。
有實驗表明,CGF與羥基磷灰石生物陶瓷聯合使用后,二者在骨再生方面表現為相互促進,發揮協同作用的效果,并加快了骨組織再生,比單獨應用羥基磷灰石生物陶瓷效果更佳[8]。
羥基磷灰石生物陶瓷,在骨增量手術中應用較廣泛。其結構呈多孔狀,對成骨細胞有支架作用,可維持或增加成骨空間。但HA無骨誘導性,僅起骨引導作用。本研究結果表明,采用CGF聯合HA骨粉、口腔生物膜進行GBR手術,完成頜骨缺損修復的治療,取得了滿意的效果。國內外部分研究也同樣支持CGF聯合骨替代用品,在修復頜骨缺損方面具有良好的效果。
CGF來源于自體本身,無毒性和免疫原性,操作提取簡單而費用低廉,臨床應用安全,因此其應用前景應十分廣闊。本研究通過測量比較組一(CGF+HA+修復膜)、組二(HA+修復膜)和組三(空白對照)術后3-6個月,經CBCT測量植骨區和正常骨組織密度的變化,對比說明不同方式對頜骨缺損修復的不同影響。結果顯示不同時間段組一和組二相對組三都取得了良好的骨愈合結果,而組一相比組二,在相同時間點上取得了更好的頜骨愈合情況。說明CGF同羥基磷灰石生物陶瓷以及口腔修復膜的聯合應用,對頜骨骨缺損的再生修復有明顯的促進作用,且再生所需時間短。
骨組織再生是一個極其復雜的過程,生長因子相互作用的機制還未完全明確。以及骨粉和CGF的混合比例、兩種混合物植入骨缺損區的松緊度等因素是否存在影響亦有待進一步研究。相信隨著相關基礎性研究和臨床試驗的不斷深入,CGF的應用前景必將更為廣闊。

