果膠-乳清蛋白混合比例和pH值對(duì)體系流變學(xué)特性的影響
白英,楊月嬌,謝瑞鵬
(內(nèi)蒙古農(nóng)業(yè)大學(xué) 食品科學(xué)與工程學(xué)院,內(nèi)蒙古 呼和浩特,010018)
由于具有明顯的凝膠特性,乳清蛋白(whey protein,WP)常被用做發(fā)酵乳制品加工中的增稠劑,提高發(fā)酵乳的持水力,改善組織狀態(tài),提高產(chǎn)品的蛋白質(zhì)含量。研究者將熱聚合乳清濃縮蛋白添加到發(fā)酵酸豆奶中,改善了產(chǎn)品的黏度和硬度,提高了產(chǎn)品的穩(wěn)定性[1]。通過(guò)添加變性乳清蛋白,改善發(fā)酵羊奶的穩(wěn)定性和脫水收縮作用[2]。以聚合乳清蛋白作為增稠劑,改善燕麥飲料的加工特性[3]。多糖是一種食品中常見(jiàn)的大分子組分,能夠影響蛋白凝膠的形成過(guò)程,從而影響食品的質(zhì)構(gòu)特性。果膠具有良好的膠凝特性,廣泛應(yīng)用于發(fā)酵乳及飲料制品的加工中,提高產(chǎn)品的穩(wěn)定性。分離乳清蛋白與甜菜果膠共價(jià)復(fù)合,可形成較穩(wěn)定的β-胡蘿卜素乳液[4]。聚合乳清蛋白與多糖相互作用形成絡(luò)合物,影響體系中乳清蛋白聚集體存在情況[5]。多糖的添加,增加了凝膠的孔隙度。導(dǎo)致持水能力的降低,同時(shí)改變了流變學(xué)特性[6]。但有研究顯示,明膠的添加并不會(huì)明顯增加凝膠的緊實(shí)度[7]。凝膠化過(guò)程是一個(gè)復(fù)雜的過(guò)程,受多種因素影響,如乳清蛋白初始濃度、多糖的添加量、加熱時(shí)間、加熱溫度、pH值和離子強(qiáng)度等。
本文以果膠-乳清蛋白凝膠體系為研究對(duì)象,對(duì)鈣離子誘導(dǎo)條件下,乳清蛋白濃度、果膠濃度和pH值對(duì)果膠-乳清蛋白體系凝膠形成及流變學(xué)特性的影響進(jìn)行了研究。
1 材料與方法
1.1 材料與試劑
恒天然乳清蛋白(蛋白含量80%),鄭州萬(wàn)博化工產(chǎn)品有限公司;食品級(jí)果膠(半乳糖醛酸含量66.7%),河南恒銳食品添加劑有限公司;CaCl2(分析純)、NaOH(分析純),國(guó)藥集團(tuán)化學(xué)試劑有限公司。
1.2 儀器與設(shè)備
Haake RS6000旋轉(zhuǎn)流變儀,Thermo Fisher 公司;HJ-6多頭磁力加熱攪拌器,江蘇杰瑞爾電器有限公司。
1.3 實(shí)驗(yàn)方法
1.3.1 乳清蛋白和果膠貯備液的制備
乳清蛋白溶液(200 g/L):稱(chēng)取20 g乳清蛋白粉緩慢加入超純水中,連續(xù)攪拌2 h,充分溶解后,待用。
果膠溶液(10 g/L):稱(chēng)取1 g果膠加入超純水中,加熱至50 ℃,保持?jǐn)嚢? h至完全溶解,待用。
以上溶液貯藏于4 ℃條件下,待用。
1.3.2 乳清蛋白-果膠混合液的制備
參照王翠娜[5]的方法,分別取20%的乳清蛋白溶液和1.0%的果膠混合,使最終混合體系中乳清蛋白質(zhì)量濃度40~100 g/L,果膠質(zhì)量濃度1~5 g/L,攪拌2 h充分溶解,制備果膠-乳清蛋白混合溶液。用0.5 mol/L NaOH調(diào)整體系pH值。85 ℃加熱30 min,冷卻至室溫。
試驗(yàn)中乳清蛋白體系質(zhì)量濃度分別為4%、8%和10%, pH值分別為7、8和9,果膠體系質(zhì)量濃度分別為1、2、3、4和5 g/L,CaCl2體系濃度分別為50、100、150和200 mmol/L。實(shí)驗(yàn)組設(shè)計(jì)如表1所示。
1.3.3 流變學(xué)特性的測(cè)定
參照白英等[8]的流變參數(shù),在 Haake RS6000 流變儀中以旋轉(zhuǎn)和振蕩模式進(jìn)行混合體系的初始黏度等流變學(xué)指標(biāo)檢測(cè)。通過(guò)在固定頻率(1 Hz)下的應(yīng)力掃描,測(cè)試確定線性黏彈性區(qū)域。在線性范圍內(nèi)的應(yīng)變(0.01%~100%)下評(píng)價(jià)儲(chǔ)能模量(G′)和損耗模量(G″)。

表1 實(shí)驗(yàn)組設(shè)計(jì)Table 1 Experimental design
2 結(jié)果與分析
2.1 聚合乳清蛋白液的初始黏度
如圖1所示,乳清蛋白溶液在85 ℃下,受熱30 min后,100 g/L乳清蛋白溶液黏度明顯高于未受熱100 g/L乳清蛋白溶液(100 g/L-NH)。蛋白質(zhì)的重組結(jié)構(gòu)以及蛋白質(zhì)分子之間的相互作用決定了乳清蛋白的凝膠特性。α-乳白蛋白存在半胱氨酸殘基,其熱變性與β-乳球蛋白相似[9]。研究表明,溫度大于60 ℃時(shí),乳清蛋白的球狀結(jié)構(gòu)發(fā)生改變,折疊結(jié)構(gòu)打開(kāi),巰基(—SH)外露。當(dāng)溫度達(dá)到75 ℃時(shí),隨著β-乳球蛋白折疊結(jié)構(gòu)的進(jìn)一步打開(kāi)[10]。當(dāng)溫度為85 ℃ 時(shí),超過(guò)了蛋白質(zhì)的耐受溫度,其結(jié)構(gòu)和生物活性或溶解度發(fā)生了改變,二硫鍵斷裂,分子內(nèi)疏水基團(tuán)暴露,α-螺旋內(nèi)部含有的半胱氨酸殘基暴露,易與其他分子交聯(lián)成二硫鍵[11]。而加熱引起的去折疊化β-乳球蛋白與α-乳白蛋白也能發(fā)生巰基-二硫化物交換反應(yīng),發(fā)生乳清蛋白間變性[12-13]。
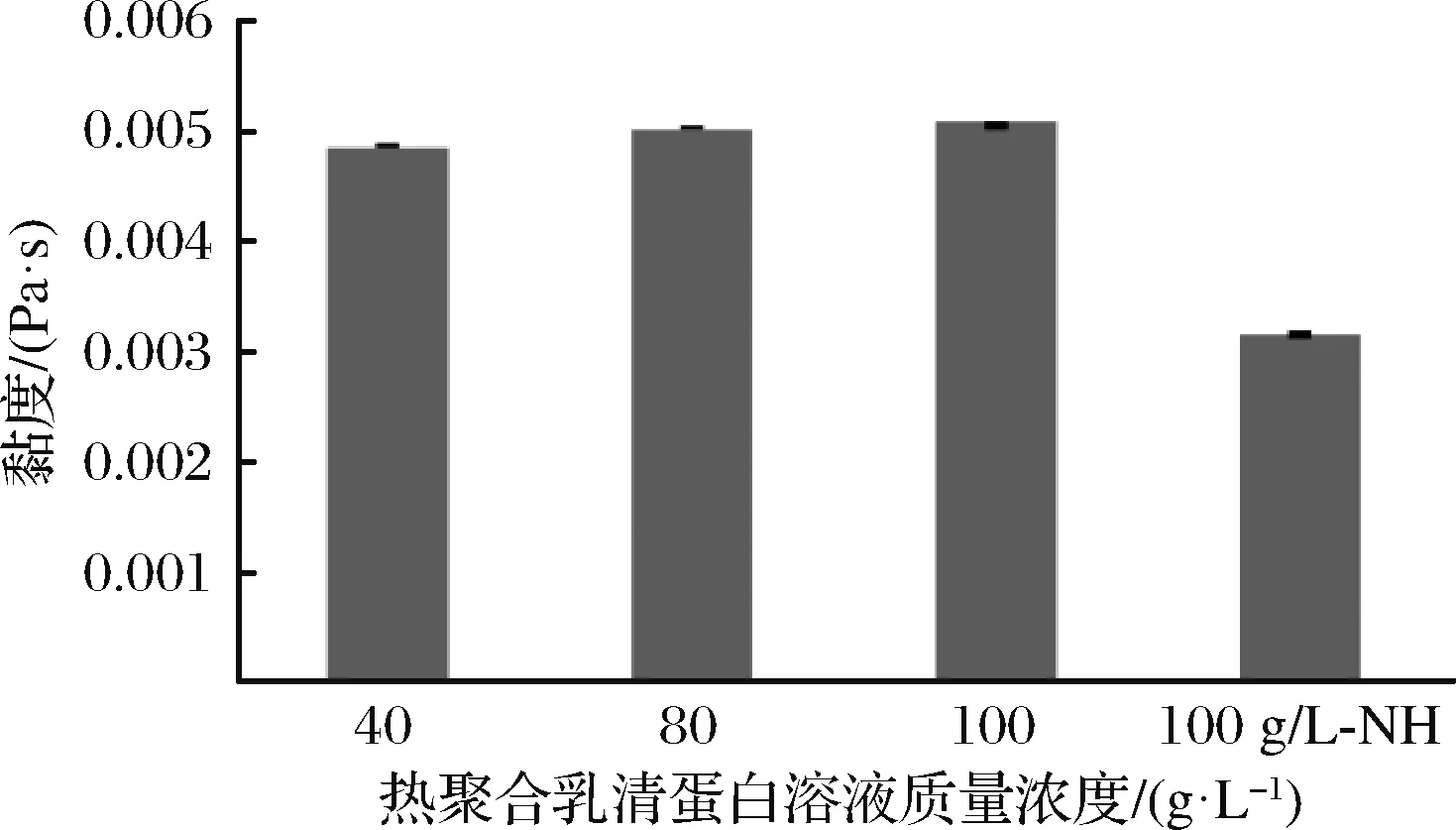
圖1 聚合乳清蛋白黏度Fig.1 Viscosity of polymerized whey protein
溶液中蛋白聚集體尺寸會(huì)隨著乳清蛋白濃度的升高而增加[14]。JU等[15]研究表明,隨著乳清蛋白濃度的增大,聚合乳清蛋白的平均粒徑也相應(yīng)增大從而導(dǎo)致熱聚合溶液黏度會(huì)隨著乳清蛋白濃度的增大逐漸增加。
2.1 果膠-乳清蛋白混合體系初始黏度的影響因素
果膠是一種帶有負(fù)電荷的陰離子多糖[16]。它可以與熱誘導(dǎo)聚合乳清蛋白(polymerized whey protein, PWP) 的陽(yáng)離子區(qū)域發(fā)生連接并形成堅(jiān)實(shí)的網(wǎng)狀結(jié)構(gòu)[17]。乳清蛋白濃度達(dá)到一定程度時(shí)才能形成熱誘導(dǎo)凝膠[18]。pH值影響聚合乳清蛋白溶液的形成以及熱誘導(dǎo)凝膠的特性。通常情況下,乳清蛋白在遠(yuǎn)離β-乳球蛋白等電點(diǎn)處進(jìn)行加熱聚合[19]。由圖2~圖4可看出,混合體系的初始黏度在不同pH值條件下,隨著果膠濃度的增加,呈現(xiàn)不同程度的增加。然而,隨著pH值的升高和乳清蛋白濃度的增大,混合體系的初始黏度呈下降趨勢(shì)。在pH=7時(shí),疏水性作用相對(duì)于堿性pH值小,混合液初始黏度值最大,為2.304 Pa·s。pH=8和pH=9時(shí),黏度較小且數(shù)值接近。在堿性條件下,靜電斥力較中性條件下大,阻礙了分子間的接近,進(jìn)而影響凝聚作用的發(fā)生。當(dāng)pH值較小破壞了蛋白聚合體的穩(wěn)定性,減少了乳體系中酪蛋白表面的靜電荷,最終導(dǎo)致了蛋白質(zhì)凝聚沉淀[20]。在適宜pH值下,蛋白質(zhì)分子才能相互接近到有利于分子間發(fā)生疏水性鍵結(jié)合的距離,形成分子間交聯(lián),生成不可逆性的蛋白質(zhì)凝膠[6]。

圖2 果膠-乳清蛋白體系初始黏度的變化曲線(pH=7)Fig.2 Curves of initial viscosity on mixed pectin- WP system (pH=7)
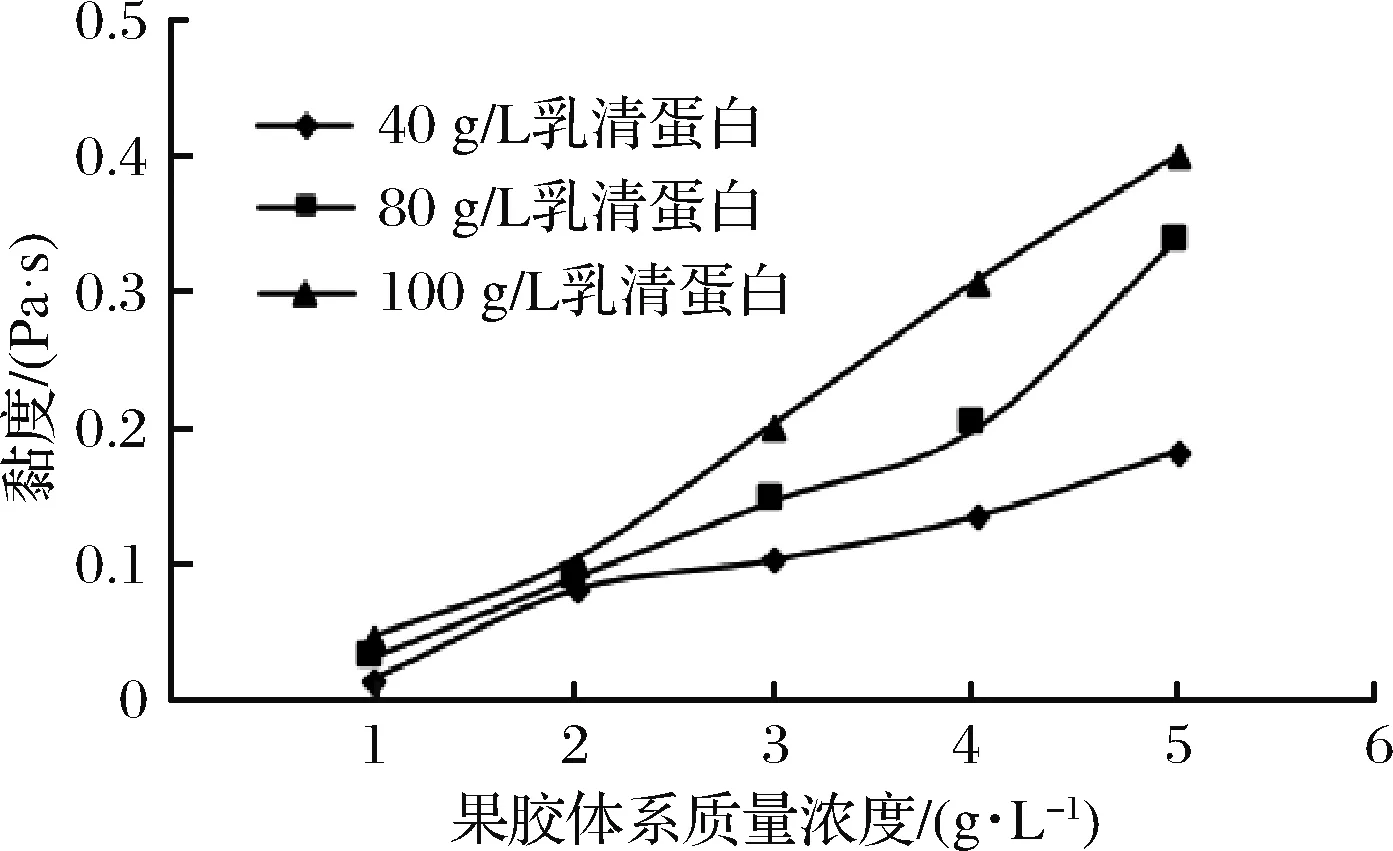
圖3 果膠-乳清蛋白混合體系初始黏度的變化曲線(pH=8)Fig.3 Curves of initial viscosity on mixed pectin- WP system (pH=8)

圖4 果膠-乳清蛋白體系初始黏度的變化曲線(pH=9)Fig.4 Curves of initial viscosity on mixed pectin- WP system (pH=9)
2.2 鈣離子對(duì)果膠-乳清蛋白體系黏度的影響
有研究表明,85 ℃及以上溫度進(jìn)行熱處理時(shí),蛋白構(gòu)象展開(kāi),活性氨基酸暴露,對(duì)鈣離子敏感的 ɑs-酪蛋白暴露,疏水作用增強(qiáng),與游離的鈣離子結(jié)合,從而減少表面電荷量,產(chǎn)生活性位點(diǎn),膠束平衡發(fā)生破壞,促進(jìn)乳清蛋白與鈣離子結(jié)合形成Ca2+-蛋白復(fù)合物,分子間的靜電斥力減小,溶液產(chǎn)生絮凝,乳清蛋白熱穩(wěn)定性降低[21]。40~100 g/L體系的純?nèi)榍宓鞍兹芤涸诘碗x子強(qiáng)度條件下,可以形成較小的聚集顆粒,但不會(huì)出現(xiàn)大規(guī)模的凝膠現(xiàn)象[22]。一般情況下,當(dāng)體系pH=7時(shí),離子強(qiáng)度為50 mmol/L NaCl或者10 mmol/L CaCl2時(shí),在較低濃度乳清蛋白條件下加熱即可形成熱誘導(dǎo)凝膠[23]。對(duì)于熱誘導(dǎo)凝膠,離子強(qiáng)度對(duì)凝膠強(qiáng)度的影響表現(xiàn)在,當(dāng)CaCl2濃度為11 mmol/L,而NaCl濃度為200 mmol/L 時(shí),凝膠強(qiáng)度達(dá)到最大值[24]。從圖5可以看出,在pH=7,乳清蛋白質(zhì)量濃度40 g/L的條件下,隨果膠濃度的增大,混合體系的初始黏度值逐漸增大。在較低的Ca2+濃度下,其誘導(dǎo)形成的凝膠主要是通過(guò)分子間電荷量的相互損耗作用,分子間結(jié)合的比較充分;較高的Ca2+濃度下,破環(huán)了分子間的電荷量平衡,分子間聚集的體系結(jié)構(gòu)不穩(wěn)定,從而導(dǎo)致黏度逐漸減小[25]。本實(shí)驗(yàn)結(jié)果顯示,在同一果膠濃度的條件下,當(dāng)Ca2+濃度為100 mmol/L時(shí),黏度值均達(dá)到最大值,隨著Ca2+體系濃度的繼續(xù)增大,黏度趨于平穩(wěn)。
2.3 pH值及果膠濃度對(duì)果膠-乳清蛋白混合體系剪切流變特性的影響
在以剪切速率為變量,添加果膠未影響40 g/L乳清蛋白體系濃度的果膠-乳清蛋白的流體類(lèi)型,混合體系表現(xiàn)出剪切稀變的特性(圖6~圖8)。在pH=7時(shí),體系黏度最大,說(shuō)明對(duì)于果膠-乳清蛋白混合體系來(lái)說(shuō),在溶液呈中性的條件下,溶液有最好的膠凝性。pH為8和9時(shí),黏度差異較小。隨著剪切速率的加大,果膠和乳清蛋白之間形成的微弱結(jié)構(gòu)被破壞,使溶液中的微小顆粒之間的摩擦作用變小,從而降低了黏度值[26]。在一定的pH值條件下,隨著剪切速率的增加,對(duì)于果膠-乳清蛋白混合體系中果膠的體系濃度越大,黏度變化越大,最終趨勢(shì)平緩。其中1 g/L果膠體系變化較小,因?yàn)楣z濃度低,與乳清蛋白之間分子斥力較小,結(jié)合充分,體系相對(duì)比較穩(wěn)定[27]。
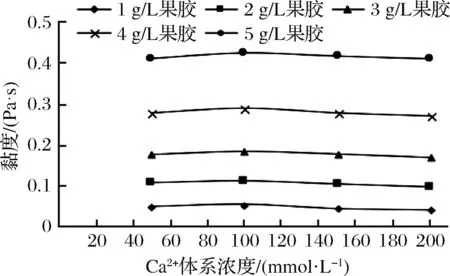
圖5 Ca2+濃度對(duì)果膠-40 g/L乳清蛋白混合體系黏度的影響Fig.5 Effect of Ca2+ concentration on viscosity of mixed pectin-40 g/L WP system

圖6 果膠質(zhì)量濃度對(duì)剪切黏度的影響(pH=7)Fig.6 Effect of pectin concentration on shear viscosity (pH=7)
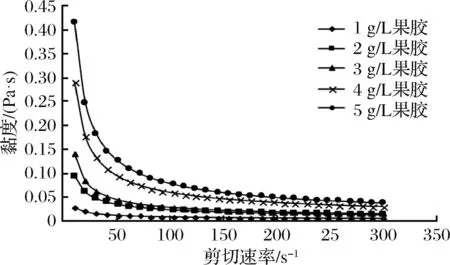
圖7 果膠質(zhì)量濃度對(duì)剪切黏度的影響(pH=8)Fig.7 Effect of pectin concentration on shear viscosity (pH=8)

圖8 果膠質(zhì)量濃度對(duì)剪切黏度的影響(pH=9)Fig.8 Effect of pectin concentration on shear viscosity (pH=9)
2.4 pH值及果膠濃度對(duì)果膠-乳清蛋白混合體系動(dòng)態(tài)流變特性的影響
物料體系在受到外力的作用下會(huì)發(fā)生形變,由于彈性(可逆)形變而儲(chǔ)存能量的大小叫作彈性模量(G′),又稱(chēng)儲(chǔ)能模量,以后可以恢復(fù);由于黏性形變(不可逆)而引起損耗能量的大小叫作黏性模量(G″),又稱(chēng)損耗模量,初始流動(dòng)所用能量轉(zhuǎn)變?yōu)榧羟袩幔划?dāng)彈性模量G′大于黏性模量G″時(shí),物料主要發(fā)生彈性形變,會(huì)表現(xiàn)出固態(tài)特性;反之,物料主要發(fā)生黏性形變,則會(huì)呈現(xiàn)液態(tài)特性[28]。為了考察果膠的添加量對(duì)果膠-乳清蛋白混合體系凝膠進(jìn)程的影響,對(duì)果膠-乳清蛋白混合體系進(jìn)行了動(dòng)態(tài)模量測(cè)定。不同pH值及果膠的添加量對(duì)40 g/L乳清蛋白體系G′和G″的影響如圖9~圖11所示,果膠含量對(duì)混合體系的損耗模量影響趨勢(shì)與彈性模量趨勢(shì)相類(lèi)似。在同等pH值條件下,隨著果膠體系質(zhì)量濃度的增大(1~5 g/L),果膠-乳清蛋白混合體系的彈性模量(G′)逐漸增加,體系黏度增大。隨著剪切時(shí)間的延長(zhǎng),所有樣品的損耗模量有明顯的上升趨勢(shì),這說(shuō)明果膠的濃度增加,樣品黏度增大,需更大的能量消耗,因此損耗模量(G″)變大。pH值的變化對(duì)模量有很大影響。由初始黏度可知pH值可改變體系的黏性,隨著pH值的增加,損耗模量先上升再下降。在pH=7的條件下,彈性模量遠(yuǎn)遠(yuǎn)大于損耗模量,混合體系的彈性遠(yuǎn)遠(yuǎn)大于樣品的黏性。在pH=8和pH=9時(shí),樣品損耗模量大于彈性模量,說(shuō)明此時(shí)樣品的黏性流動(dòng)性逐漸加強(qiáng)。由實(shí)驗(yàn)結(jié)果可知,隨著體系pH值的增加,混合體系的黏性流動(dòng)性加強(qiáng)。隨著果膠濃度的增大,出現(xiàn)明顯觸變環(huán)(圖11)。升速與降速剪切曲線所圍成的觸變環(huán)(又稱(chēng)滯后環(huán)),即物料在剪切作用下組織結(jié)構(gòu)會(huì)發(fā)生變化,撤去剪切作用后體系結(jié)構(gòu)需要滯后一段時(shí)間才會(huì)恢復(fù)到原來(lái)的狀態(tài)[29]。觸變環(huán)的面積大小表示破壞觸變結(jié)構(gòu)所需要能量的大小[30]。從觸變環(huán)面積可知,隨著果膠濃度的增加,破壞混合體系觸變結(jié)構(gòu)所需要的能量增大,體系穩(wěn)定性增強(qiáng)。
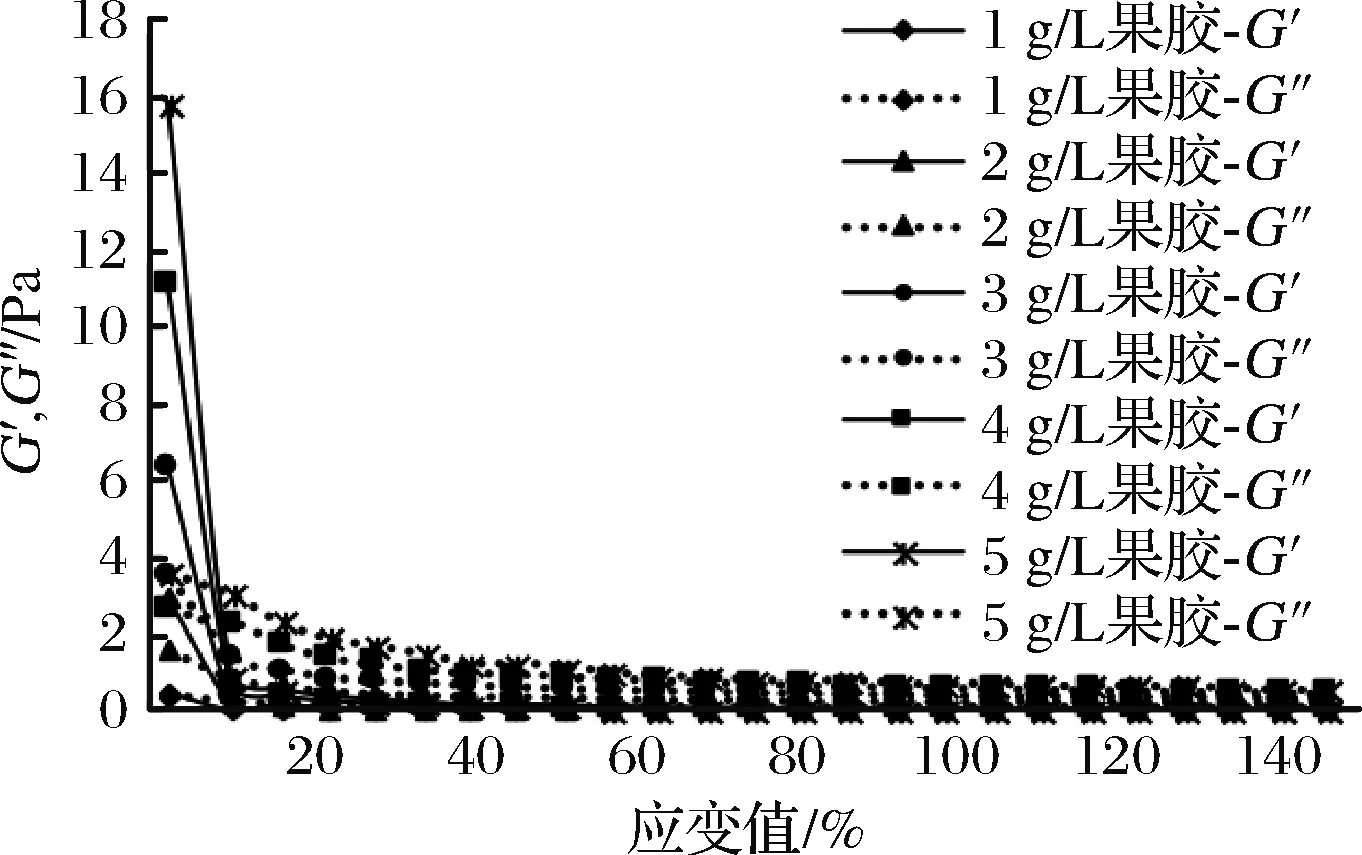
圖9 果膠質(zhì)量濃度對(duì)果膠-40 g/L乳清蛋白混合體系G′和G″的影響(pH=7)Fig.9 Effect of pectin concentration on G′and G″of mixed pectin-40 g/L whey protein system (pH=7)

圖10 果膠質(zhì)量濃度對(duì)果膠-40 g/L乳清蛋白混合體系G′和G″的影響(pH=8)Fig.10 Effect of pectin concentration on G′and G″of mixed pectin-40 g/L whey protein system (pH=8)

圖11 果膠質(zhì)量濃度對(duì)果膠-40 g/L乳清蛋白混合體系G′和G″的影響(pH=9)Fig.11 Effect of pectin concentration on G′and G″of mixed pectin-40 g/L whey protein system (pH=9)
3 結(jié)論
當(dāng)混合體系pH=7時(shí),Ca2+可誘導(dǎo)果膠-40 g/L乳清蛋白混合體系形成凝膠。果膠-乳清蛋白混合體系表現(xiàn)出剪切稀化的流體特征。在同等pH值條件下,隨著果膠體系濃度的增大,果膠-乳清蛋白混合體系的G′和G″都有明顯的上升趨勢(shì)。在pH=7的條件下,G′>G″;在pH=8和pH=9時(shí),樣品G′

