促紅細胞生成素對慢性腦缺血大鼠腦組織促凋亡相關(guān)蛋白表達水平的影響
嚴 澎,楊 斌,李文波,何玉清,阮春云
促紅細胞生成素(erythropoietin,EPO)又稱紅細胞因子與促紅素,為人體內(nèi)源性的糖蛋白激素,主要通過與其受體結(jié)合起作用,具有刺激紅細胞生成的功能[1]。既往研究顯示EPO不僅在胎兒的肝臟、成年人的腎臟中表達,也在非造血系統(tǒng)表達,如神經(jīng)元、血管內(nèi)皮細胞以及膠質(zhì)細胞。近年來,研究顯示EPO與腦缺血疾病的進展有關(guān),早期運用外源性的EPO對缺氧缺血性新生大鼠的腦損傷有神經(jīng)保護作用[2]。本研究通過雙側(cè)頸總動脈永久性結(jié)扎法建立慢性腦缺血大鼠模型,探討EPO對慢性腦缺血大鼠腦組織凋亡與促凋亡蛋白表達水平的影響,為臨床治療慢性腦缺血病人的藥物設(shè)計提供動物實驗理論依據(jù)。
1 材料與方法
1.1 主要試劑及儀器 兔抗鼠Caspase-3抗體(上海優(yōu)寧維公司生物科技有限公司),兔抗鼠Bax抗體(上海優(yōu)予生物科技有限公司),兔抗鼠Bcl-2抗體(上海恒斐生物科技有限公司),小鼠抗人Omi/HtrA2抗體(艾美捷科技有限公司),ECL試劑盒(上海經(jīng)科化學(xué)科技有限公司),末端脫氧核苷酸轉(zhuǎn)移酶介導(dǎo)的dUTP缺口末端標(biāo)記測定(TUNEL)試劑盒(江蘇凱基生物技術(shù)股份有限公司),丙二醛(MDA)、超氧化物歧化酶(SOD)酶聯(lián)免疫吸附實驗(ELISA)試劑盒(上海遠慕生物科技有限公司),過氧化氫酶(CAT)、谷胱甘肽(GSH)ELISA試劑盒(上海研謹生物科技有限公司),EPO(Theramabs),二甲基亞砜(DMSO,Sigma)。冷凍離心機3K15(Sigma),正置熒光顯微鏡FM-51D(上海繪統(tǒng)光學(xué)儀器有限公司),全自動輪盤式切片機(LEICA)。
1.2 實驗動物 無特定病原體(SPF)級健康雄性16~20周齡SD大鼠96只,體重250~300 g,購于武漢大學(xué)中南醫(yī)院動物實驗中心,許可證號:SYXK(鄂)2015-0025,購回飼養(yǎng)1周,再用于后續(xù)實驗,飼養(yǎng)溫度維持在20~25 ℃,空氣濕度為50%~55%,光照為人工光照,晝12 h、夜12 h,所有大鼠全天飲水自由。
1.3 模型制備與動物分組處理 采用雙側(cè)頸總動脈永久性結(jié)扎法建立慢性腦缺血大鼠模型,選取24只SD大鼠,隨機分為對照組與假手術(shù)組,每組12只,再選取30只SD大鼠作為建模組,用于建立慢性腦缺血模型。建模組大鼠于建模前12 h禁食,腹腔注射40 mg/kg 1%戊巴比妥鈉,頸部正中進行縱向切口,玻璃分針分離雙側(cè)頸總動脈,雙線結(jié)扎,電刀切斷頸總動脈防止復(fù)流,碘伏消毒,縫合切口,腹腔注射1×105U青霉素,防止感染,術(shù)后24 h內(nèi)蘇醒大鼠納入研究,未蘇醒大鼠剔除,本研究共剔除6只大鼠,剩余大鼠隨機均分為模型組與EPO組,每組12只。假手術(shù)組大鼠除不進行結(jié)扎血管,剩余操作與建模組大鼠相同,對照組不做任何處理。
造模成功0.5 h后,EPO組大鼠腹腔注射EPO 5 U/(g·d),連續(xù)注射2周,模型組、假手術(shù)組大鼠腹腔注射同體積的生理鹽水,對照組大鼠不予任何處理。連續(xù)給藥結(jié)束后,每組大鼠一部分用于神經(jīng)功能評分、學(xué)習(xí)記憶能力測試,剩余大鼠用于其他實驗指標(biāo)檢測。
1.4 觀察指標(biāo)
1.4.1 神經(jīng)功能評分 采用Longa 5級評分法評估藥物干預(yù)后大鼠神經(jīng)功能評分:無神經(jīng)缺損癥狀計0分;不能伸展右側(cè)前爪計1分;行走時向右側(cè)轉(zhuǎn)圈計2分;行走時向右側(cè)傾倒計3分;不能自發(fā)行走,意識喪失計4分。
1.4.2 Morris水迷宮實驗測定逃避潛伏期與空間記憶能力 每組隨機選取6只SD大鼠用于Morris水迷宮實驗,該實驗包括隱蔽平臺實驗與空間探索實驗。隱蔽平臺實驗每只SD大鼠訓(xùn)練量為每日3次,共5 d,觀察并記錄每只SD大鼠到達平臺時間(逃避潛伏期),訓(xùn)練3次的平均值作為該天的成績;隱蔽平臺實驗訓(xùn)練5 d后,撤去平臺,觀察并記錄每只SD大鼠在120 s內(nèi)穿過平臺次數(shù),用于檢測大鼠的空間記憶能力。
1.4.3 氧化應(yīng)激指標(biāo)檢測 末次給藥1 h后,采用1%戊巴比妥鈉麻醉處死大鼠,取出完整的腦組織,一部分用于腦勻漿制備,2 000 r/min、10 min,取上清液存儲于-80 ℃環(huán)境中,采用ELISA法檢測大鼠腦組織中的MDA含量及SOD、CAT、GSH活性,操作嚴格參照試劑盒說明進行。剩余腦組織一部分保存于-80 ℃環(huán)境中用于蛋白水平檢測,另一部分固定于4%多聚甲醛用于蘇木精-伊紅(HE)染色與TUNEL檢測。
1.4.4 HE染色與TUNEL檢測 處死大鼠,將腦組織置于4%多聚甲醛中固定,進行常規(guī)石蠟包埋,一部分用于HE染色,另一部分根據(jù)免疫組織化學(xué)試劑盒說明書操作用于TUNEL檢測,在顯微鏡下觀察并采集圖像。在TUNEL法檢測過程中,隨機選取10個視野,記錄100個細胞中陽性細胞數(shù),統(tǒng)計各組細胞凋亡率,細胞凋亡率=(陽性細胞數(shù)/總細胞數(shù))×100%。
1.4.5 蛋白免疫印跡法(Western-blot)檢測 提取各組大鼠腦組織總蛋白,采用Bradford調(diào)整蛋白濃度相同,經(jīng)十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE)、電轉(zhuǎn)膜至聚偏二氟乙烯(PVDF)膜,密封2 h,加入兔抗鼠Caspase-3、Bax、Bcl-2、Omi/HtrA2、β-actin一抗(1∶500)4 ℃孵育過夜,再用TBST緩沖液漂洗40 min,加入辣根過氧化物酶(HRP)標(biāo)記的二抗(1∶500)孵育1 h,參照ECL試劑盒操作說明觀察膜上蛋白條帶,收集影像。
2 結(jié) 果
2.1 各組神經(jīng)功能評分、逃避潛伏期及穿越平臺次數(shù)比較 與假手術(shù)組相比,模型組神經(jīng)功能評分增加(P<0.05);與模型組相比,EPO組神經(jīng)功能評分降低(P<0.05)。與假手術(shù)組相比,模型組逃避潛伏期延長(P<0.05),120 s穿越平臺次數(shù)減少(P<0.05);與模型組相比,EPO組逃避潛伏期縮短(P<0.05),120 s穿越平臺次數(shù)增加(P<0.05)。詳見表1。
表1 各組神經(jīng)功能評分、逃避潛伏期及穿越平臺次數(shù)比較 (±s)
2.2 各組大鼠腦組織SOD、CAT、GSH及MDA含量比較 與假手術(shù)組相比,模型組腦組織中SOD、CAT、GSH水平降低,MDA水平升高(P<0.05);與模型組相比,EPO組腦組織中SOD、CAT、GSH水平升高(P<0.05),MDA水平降低(P<0.05)。詳見表2。
表2 各組大鼠腦組織SOD、CAT、GSH及MDA含量比較 (±s)
2.3 各組大鼠腦組織細胞凋亡情況比較 對照組與假手術(shù)組大鼠腦組織神經(jīng)元結(jié)構(gòu)完整、排列整齊、細胞核大且圓;模型組大鼠腦組織中神經(jīng)元排列紊亂、核固縮、細胞體積減小且形狀不規(guī)則;EPO組大鼠腦組織中神經(jīng)元的形態(tài)結(jié)構(gòu)較模型組改善較多,細胞排列整齊,細胞核固縮較少。詳見圖1。對照組與假手術(shù)組大鼠腦組織TUNEL染色陽性細胞較少,其次為EPO組、模型組。詳見圖2。模型組大鼠腦組織細胞凋亡率高于對照組、假手術(shù)組及EPO組(P<0.05),對照組與假手術(shù)組大鼠腦組織細胞凋亡率比較差異無統(tǒng)計學(xué)意義(P>0.05)。詳見表3。
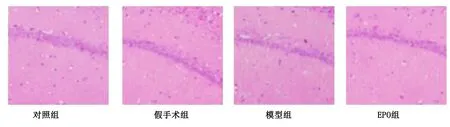
圖1 各組大鼠腦組織HE染色結(jié)果(×200)
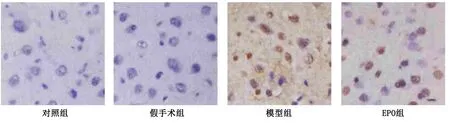
圖2 各組大鼠腦組織TUNEL檢測結(jié)果
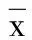
表3 各組大鼠腦組織細胞凋亡率比較 (±s) 單位:%
2.4 各組大鼠腦組織Caspase-3、Bax、Omi/HtrA2、Bcl-2蛋白水平比較 與假手術(shù)組相比,模型組大鼠腦組織中的Caspase-3、Bax、Omi/HtrA2蛋白水平均明顯升高(P<0.05),Bcl-2蛋白水平明顯下降(P<0.05),對照組與假手術(shù)組比較差異無統(tǒng)計學(xué)意義(P>0.05);與模型組相比,EPO組大鼠腦組織中的Caspase-3、Bax、Omi/HtrA2蛋白水平降低(P<0.05),Bcl-2蛋白水平升高(P<0.05)。詳見圖3、表4。
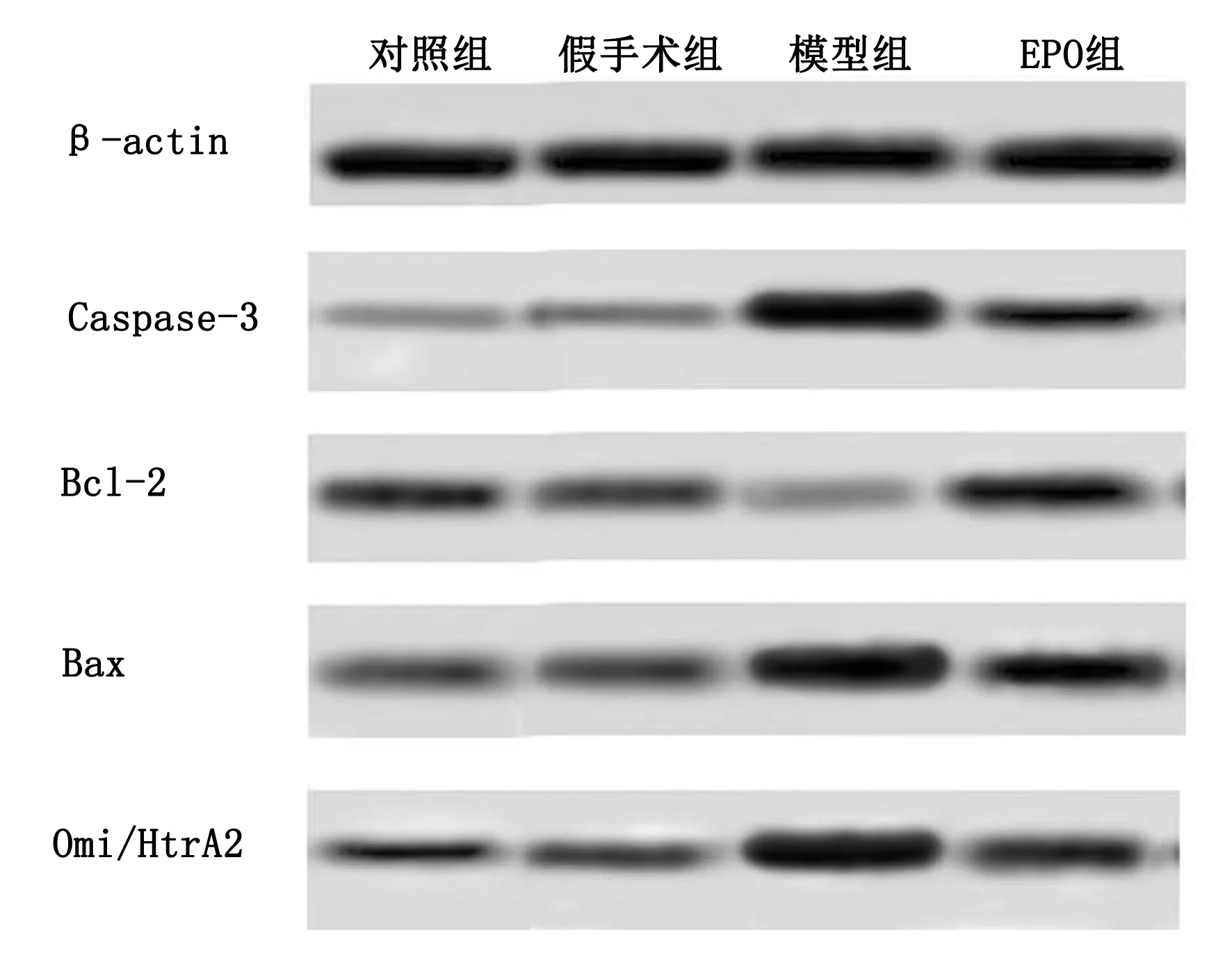
圖3 各組大鼠腦組織Caspase-3、Bax、Bcl-2、Omi/HtrA2蛋白凝膠成像結(jié)果
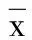
表4 各組大鼠腦組織Caspase-3、Bax、Bcl-2、Omi/HtrA2蛋白水平比較 (±s)
3 討 論
腦缺血是由多種因素引起的腦供血不足所致的神經(jīng)系統(tǒng)疾病,慢性腦缺血是其中常見的病理狀態(tài)之一,常伴發(fā)于多種神經(jīng)系統(tǒng)疾病進程中,如腦供血不足、皮質(zhì)下動脈硬化性腦病、缺血導(dǎo)致的腦白質(zhì)損害以及腦萎縮等[3]。EPO屬于造血細胞因子超家族成員,為含有唾液酸的酸性糖蛋白,主要由蛋白質(zhì)、糖類組成,有4個糖基化位點。EPO與其受體(EPOR)結(jié)合后使其構(gòu)象發(fā)生變化,能夠使JAK2絡(luò)氨酸激酶激活,使EPOR的多個絡(luò)氨酸殘基磷酸化,激活下游多個信號通路,包括磷脂酰肌醇3-激酶、有絲分裂原活化蛋白激酶(MAPK)以及Janus激酶2(JAK2)-信號轉(zhuǎn)導(dǎo)子等[4]。臨床研究顯示,EPO在開顱動脈瘤夾閉術(shù)后腦缺血治療中效果顯著,能夠幫助病人術(shù)后缺血腦組織微循環(huán)重建,改善腦缺血病人臨床癥狀,并對神經(jīng)功能有保護作用[5]。本研究通過雙側(cè)頸總動脈永久性結(jié)扎法建立慢性腦缺血大鼠模型以模擬成年人慢性腦缺血癥狀,并用EPO進行處理,結(jié)果顯示,EPO可以降低慢性腦缺血損傷大鼠的神經(jīng)功能評分,還可以提高大鼠的記憶能力。臨床研究顯示,在高壓氧治療的基礎(chǔ)上增加EPO治療能夠改善缺氧缺血性腦病患兒神經(jīng)行為,改善腦組織的代謝,并且安全性高[6]。本研究結(jié)果提示EPO對慢性腦缺血大鼠神經(jīng)功能有保護作用。
氧化應(yīng)激在神經(jīng)、血管性疾病中發(fā)揮著重要作用,慢性腦缺血存在慢性低灌注的特點,在此過程中細胞中的線粒體損傷,從而引起組織氧化應(yīng)激反應(yīng),活性氧物質(zhì)產(chǎn)生,脂質(zhì)發(fā)生過氧化反應(yīng),對機體的血腦屏障功能與腦實質(zhì)造成損傷[7]。同時在機體慢性缺血時,會抑制海馬突觸的可塑性、沉默信息調(diào)節(jié)因子(Sirt)活性,參與氧化應(yīng)激反應(yīng)以及認知受損過程[8]。本研究結(jié)果顯示,EPO可以降低慢性腦缺血大鼠腦組織中MDA含量,增加SOD、CAT、GSH水平。MDA是過氧化產(chǎn)物的主要成分之一,過量的自由基及脂質(zhì)過氧化產(chǎn)物會增加神經(jīng)細胞結(jié)構(gòu)損傷程度,導(dǎo)致腦組織損傷程度加重;SOD具有清除自由基的能力[9-10];CAT主要是催化過氧化氫分解成為水和氧;GSH由谷氨酸、半胱氨酸及甘氨酸組成,具有抗氧化以及解毒作用。SOD、CAT、GSH共同組成了機體抗氧化的防御系統(tǒng),其活性均能反映機體的抗氧化應(yīng)激能力。石境懿等[11]研究顯示,重組人促紅細胞生成素(rhEPO)可以降低新生兒缺氧缺血性腦病導(dǎo)致的氧化應(yīng)激損傷。本研究結(jié)果表明,EPO可以降低慢性腦缺血大鼠腦組織的氧化應(yīng)激反應(yīng),減少神經(jīng)組織損傷。
慢性腦缺血后腦組織會出現(xiàn)損傷,氧化應(yīng)激增強,調(diào)控細胞凋亡的特定蛋白水平表達上調(diào)。細胞核、線粒體是影響細胞凋亡的重要因素,線粒體損傷使活性氧(ROS)大量產(chǎn)生,影響B(tài)cl、Bax比例,細胞色素C先后與凋亡酶激活因子、Caspase-9結(jié)合,激活Caspase-3,破壞細胞核內(nèi)的DNA修復(fù)酶促進細胞凋亡[12-13]。本研究結(jié)果顯示,EPO可以降低慢性腦缺血大鼠腦組織的細胞凋亡率,還可以降低Caspase-3、Bax、Omi/HtrA2蛋白水平,增加Bcl-2蛋白含量。Bcl-2是線粒體途徑凋亡通路中的重要成員,其高表達可以抑制多種因素導(dǎo)致的細胞凋亡,而Bax屬于促細胞凋亡基因,兩者比值大小可以直接反映細胞凋亡情況。Omi/HtrA2是新型的促凋亡蛋白,當(dāng)細胞處于正常的生理代謝時,其主要分布于線粒體膜間隙,當(dāng)細胞收到凋亡信號時,會通過自我加工(去N端的殘基)穿過線粒體膜以進入胞質(zhì),通過與其相關(guān)因子結(jié)合,激活下游的Caspase-3蛋白水平[14]。李晉娜等[15]研究顯示,rhEPO可以促進Bcl-2上調(diào)、Bax下調(diào),改善慢性缺血大鼠的神經(jīng)細胞凋亡。鄒禮樂等[16]研究顯示,EPO可以通過抑制腦組織Omi/HtrA2表達而減少神經(jīng)細胞凋亡,實現(xiàn)對腦損傷的保護作用。本研究結(jié)果表明,EPO可以通過調(diào)節(jié)Caspase-3、Bax、Bcl-2、Omi/HtrA2蛋白水平抑制慢性腦缺血大鼠腦組織細胞凋亡。
綜上所述,EPO可以降低Caspase-3、Bax、Omi/HtrA2蛋白水平,增加Bcl-2蛋白含量,降低大鼠MDA含量,增加SOD、CAT、GSH活性,降低大鼠腦組織細胞凋亡,增強抗氧化應(yīng)激能力,從而減輕腦組織損傷。本研究只是通過大鼠模型實驗來進行探討,而在臨床上是否存在相似凋亡相關(guān)蛋白水平變化,還需要進一步研究。

