淋巴結清除范圍與腹腔鏡根治性膀胱切除術后并發癥和再入院的相關性研究
李前進 馬惠斌 王文光 馬 濤
根治性膀胱切除術+盆腔淋巴結清掃一直以來是肌層浸潤性膀胱癌和高危非肌層浸潤性膀胱癌的標準手術方式[1]。隨著腹腔鏡外科的不斷發展,腹腔鏡下根治性膀胱切除術(laparoscopic radical cystectomy,LRC)在臨床上應用越來越廣泛,一些大型三甲醫院已經逐步取代了傳統開放式膀胱切除術。在盆腔淋巴結清掃范圍方面,業內一直存在爭議,尚未形成統一的意見。2004年歐洲泌尿外科學會(EAU)關于膀胱癌的指南僅推薦含閉孔間隙的局部淋巴結清掃,但隨著臨床實踐的增多,越來越多的研究表明若僅采用此種方式進行淋巴結清掃,將有約63%~77%的陽性淋巴結被遺漏[2,3]。2018年版的中國膀胱癌診療規范中列舉了標準淋巴結清掃和擴大淋巴結清掃兩種術式,但對于兩種術式的優劣性業內尚無確切的報道[4]。另外,國外研究證實,癌癥患者術后再入院手術會增加患者死亡風險和醫療資源過度利用[5]。但目前關于影響患者出院后再入院的相關因素尚無深入研究,明確膀胱癌患者再入院手術的相關因素對于提高醫療質量具有重要意義。
資料與方法
1.臨床資料:(1)納入標準:①術前經膀胱鏡取活檢病理確診為膀胱尿路上皮癌;②經CT/MRI/彩超等影像學檢查符合手術指征;③臨床資料完整;④術后規律進行放化療。(2)排除標準:①其他類型惡性腫瘤轉移至膀胱者;②合并嚴重的心臟、肝臟、肺臟、腎臟功能障礙無法耐受手術者;③合并遠處轉移者;④存在血液或凝血系統疾患。共納入2012年1月~2017年4月因膀胱癌在新疆醫科大學第一附屬醫院行腹腔鏡根治性膀胱切除術的患者160例,其中,男性133例,女性27例,患者年齡31~65歲。根據術中淋巴結清掃范圍分為ePLND組(73例)和sPLND組(87例),兩組患者基線資料比較,差異無統計學意義(P>0.05),詳見表1。
2.手術方法:所有患者均完善術前檢查,查無手術禁忌證后開始實施腹腔鏡根治性膀胱切除術;腹腔鏡操作嚴格按照《腹部創傷腔鏡診療規范專家共識》[6]中的操作規范進行;盆腔淋巴結清掃范圍參考文獻[7,8]。標準淋巴結清掃范圍清掃至近端髂總血管分叉處,外側至生殖股神經外側,遠端至旋髂靜脈和Cloquet淋巴結,后方至髂內血管,包括閉孔、髂內、髂外淋巴結及骶骨前淋巴結;擴大淋巴結清掃范圍在標準淋巴結清掃范圍基礎上向上擴展至腹主動脈分叉處,包括腹主動脈分叉區域的所有淋巴結,骶前和髂血管交叉輸尿管內側,髂總血管、腹主動脈遠端及下腔靜脈周圍淋巴脂肪組織;部分病例淋巴結清掃范圍延伸到腸系膜下動脈水平。根治性切除術與淋巴結清掃術同時進行,清除雙側清掃范圍內的所有淋巴脂肪組織。尿路重建根據患者不同情況分別采用回腸通道術(Bricker術)、原位回腸新膀胱術(Studer術)或輸尿管皮膚造口術。
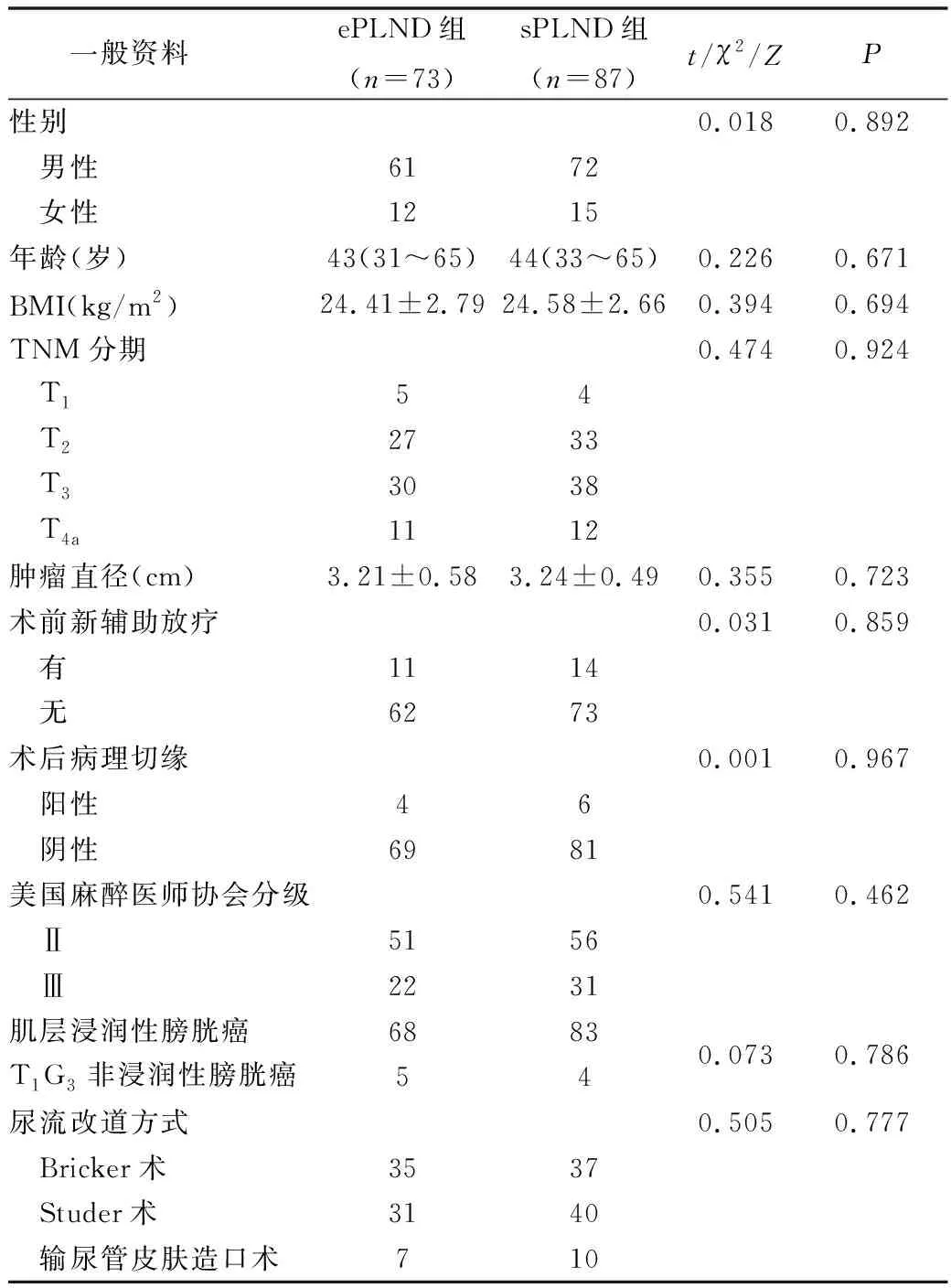
表1 兩組患者一般資料比較
3.觀察指標:記錄兩組患者術后出現低蛋白血癥(Alb<3.5g/dl)、泌尿系感染(腎盂腎炎、腎積膿)、腸梗阻、腸瘺、切口脂肪液化、下肢深靜脈血栓、肺部感染等并發癥發生情況。無進展生存期和總生存期:通過再入院記錄、患者預留聯系方式對術后再入院和預后進行分析,預后資料主要分析術后24個月的疾病進展和總生存情況。
結 果
1.兩組患者并發癥及再入院率比較:術后并發癥發生率ePLND組為28.77%,sPLND組為22.99%,兩組比較差異無統計學意義(P>0.05);出院后90天內兩組患者共有19例再入院治療,其中ePLND組8例,sPLND組11例,兩組比較差異無統計學意義(P>0.05),詳見表2。

表2 兩組患者并發癥及再入院率比較[n(%)]
2.影響患者再入院的COX回歸分析:低蛋白血癥(HR=15.098)、腸瘺(HR=11.068)、切口脂肪液化(HR=12.710)是導致患者再入院的獨立危險因素(P均<0.05),詳見表3。
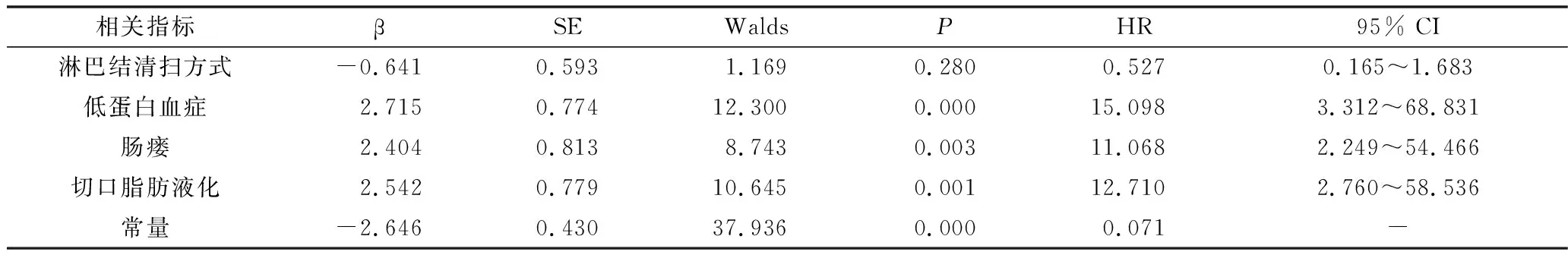
表3 影響患者再入院的COX回歸分析
3.兩組患者隨訪PFS和OS比較:病例記錄顯示在聯系患者過程中,ePLND組有3例發生失訪,sPLND組有5例出現失訪。術后24個月兩組患者均未達到中位PFS和OS,其中ePLND組2年PFS 率為80.00%(56/70),sPLND組為64.63%(53/82),兩組比較差異有統計學意義(Log-Rankχ2=5.201,P=0.023),詳見圖1; ePLND組2年OS率為87.14%(61/70),sPLND組為78.05%(64/82),兩組比較差異無統計學意義(Log-Rankχ2=2.624,P=0.105),詳見圖2。
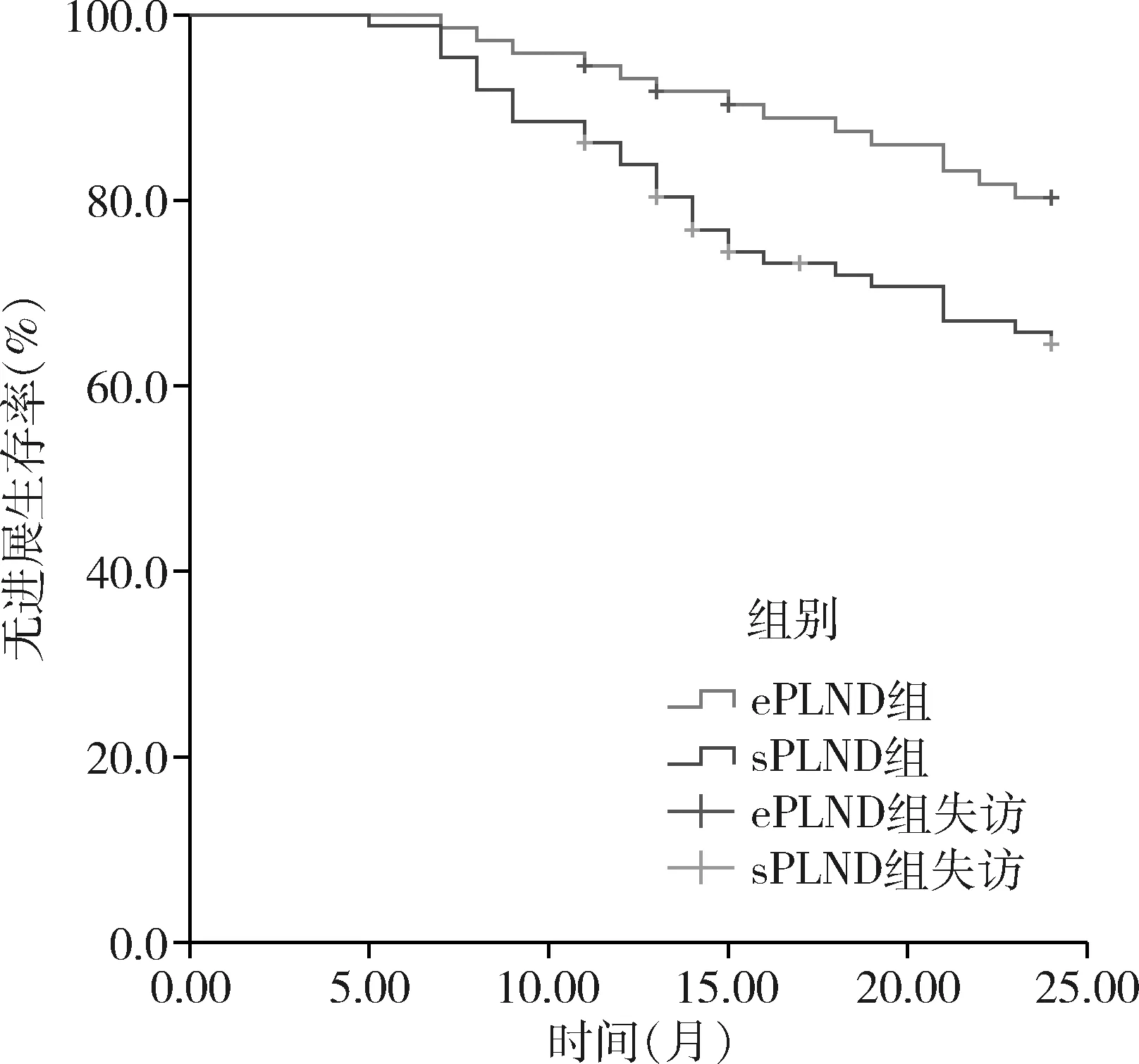
圖1 兩組患者2年PFS比較
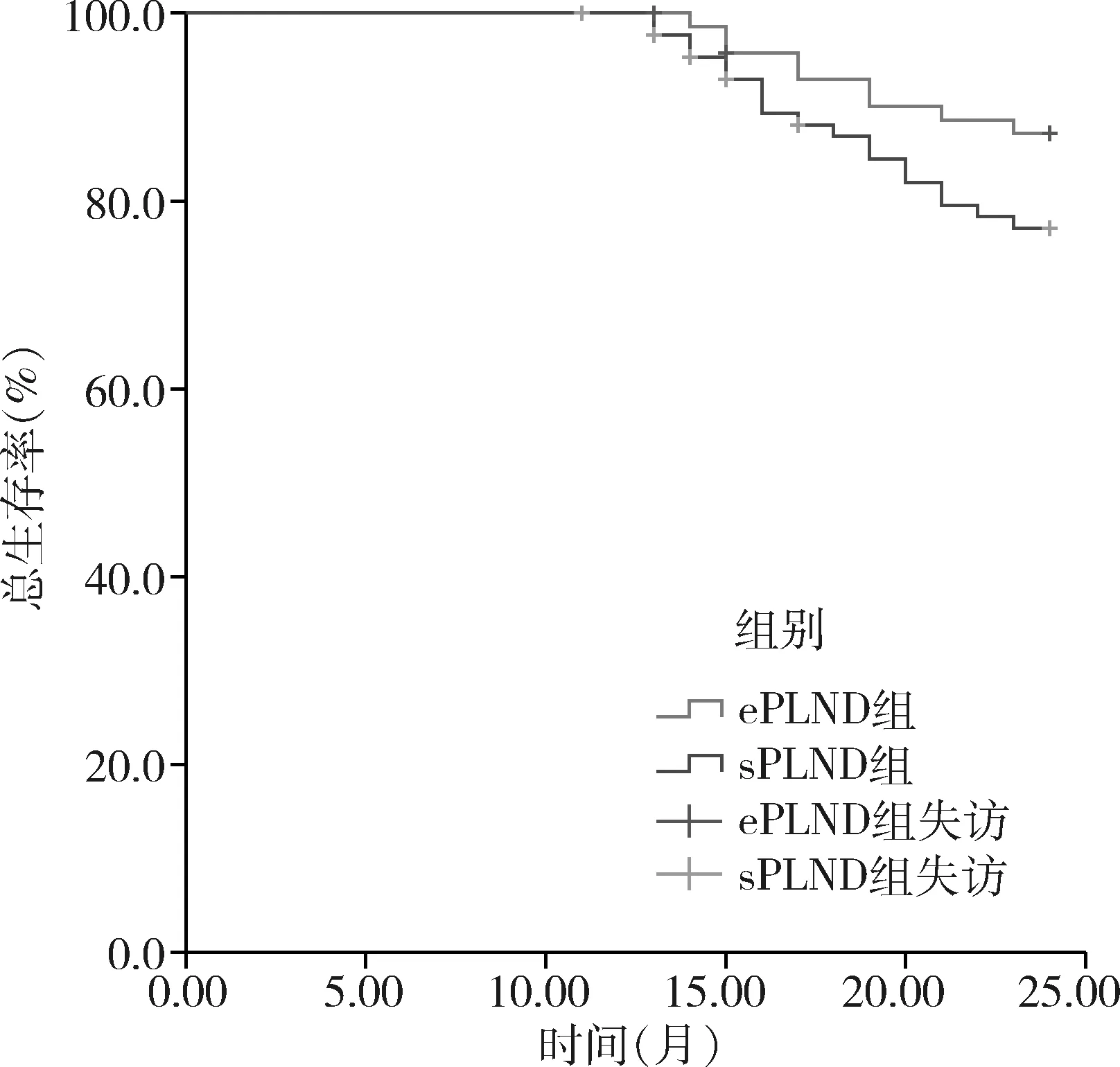
圖2 兩組患者2年OS比較
討 論
膀胱癌是我國泌尿系統腫瘤中最常見的類型,其中90%為移行細胞癌,而這中間有約25%的病例會發展為浸潤性膀胱癌[9]。隨訪研究顯示,對于無遠程轉移的膀胱癌5年生存率可達65.5%~74.7%[10]。治療上根治性膀胱癌切除術為首選方式,一直以來臨床上為了提高膀胱癌患者生存率,也開展了許多新嘗試,如術前新輔助放療、術后放化療、術前淋巴結清掃等。自20世紀下半葉開始,臨床治療上將盆腔淋巴結清掃納入膀胱癌根治術的操作范圍,用以預防膀胱癌淋巴結轉移。相關研究表明,術前未檢查出淋巴結轉移的患者術后發生淋巴結轉移的概率可達25%[11]。雖然盆腔淋巴結清掃在臨床上應用時間已久,但對于清掃范圍一直存在爭議,尚未達成統一標準。
近年來,研究者逐漸認識到雖然大多數淋巴結位于盆腔,但實踐中膀胱癌的淋巴結轉移范圍非常廣泛。有研究顯示,約有41%的淋巴結轉移位于標準淋巴結清掃范圍之外,由此誕生了擴大淋巴結清掃的概念,將清掃范圍上移至腹主動脈分叉處乃至腸系膜下動脈水平[12]。但關于不同淋巴結清掃范圍對于患者預后及并發癥的影響相關報道并不多,且結論各異,無法提供有效參考。另一方面,外科領域一直將患者出院后的再入院率作為評估醫療質量的一項重要標志,在癌癥切除領域的應用也相當廣泛,過多的再入院率說明外科醫療質量低下且對患者遠期預后產生負面影響[13]。
對于腹腔鏡根治性膀胱切除術后的并發癥發生率國內外文獻報道并不多,國外一項應用Clavien-Dindo分級系統評價ePLND和sPLND的手術并發癥發生率,發現二者差異無統計學意義[14]。本研究的結果也進一步支持了這一結論。在本研究中,并發癥發生例數排在前3位的是低蛋白血癥、腸瘺和切口脂肪液化,其中ePLND組發生5例低蛋白血癥,4例腸瘺和3例脂肪液化,而sPLND組發生6例低蛋白血癥、5例腸瘺和5例脂肪液化。筆者分析認為,低蛋白血癥的發生原因可能與盆腔淋巴結清掃有關,淋巴結清掃使得大量淋巴液漏出,淋巴液中含有大量蛋白質,若術后補充不及時則會導致低蛋白血癥;而脂肪液化也與機體營養缺乏和炎性反應有關,營養狀況低下及炎性反應呈現亢進狀態會影響切口愈合,增加脂肪液化的發生。上述并發癥中有部分病例經對癥處理后好轉,未再入院治療,而部分病例則需要再入院治療,出院后90天內共有19例患者因圍術期相關疾病導致再入院,再入院率為11.87%,略高于國外報道(7.3%~9.0%)[15]。進一步對再入院病例進行多因素COX風險分析顯示,低蛋白血癥、腸瘺和切口脂肪液化是導致患者再入院的獨立危險因素,筆者分析認為,再入院率作為手術質量度量的一項指標被臨床上廣泛應用,低蛋白血癥與營養缺乏和全身炎性反應有關。動物實驗研究顯示,低蛋白血癥的小鼠免疫應答遲鈍,這一現象有助于解釋為什么營養不良患者切口愈合較慢且更易發生術后感染[16]。
研究表明,圍術期加強免疫營養補充有助于降低切口感染率,且對于減少術后再入院率具有積極影響,雖然這一結論尚未進行大樣本隨機對照研究,但筆者持支持態度[17]。關于切口脂肪液化前文已經講到,筆者在這里著重要說明的是雖然腹腔鏡手術中取出膀胱標本僅需要一個較小的切口,但仍需要注意切口感染的可能。國外有研究者報道了機器人腹腔鏡根治性膀胱切除術后發生再入院的研究,結果發現有6%的患者再入院的原因是由于切口裂開引起的[18]。考慮到本研究樣本量較小的緣故,切口脂肪液化與再入院的相關性尚需要進一步論證。腸瘺是腹部和盆腔手術領域一類較為常見和嚴重的并發癥,輕度的腸瘺可以通過禁食、胃腸減壓促進其愈合,對于營養狀況較差、經胃腸減壓、禁食后遲遲不愈合的患者則需要再入院行手術修補,既降低了醫療質量,也增加了患者負擔。
關于腹腔鏡根治性膀胱切除術中淋巴結清掃范圍與患者預后關系方面,既往研究觀點認為,淋巴結清掃數目越多,患者預后越好[19]。且國外有研究針對1260例膀胱癌淋巴結轉移的患者進行生存分析后發現,淋巴結清掃數目>10枚則患者的5年總生存率更高[20]。但也有文獻報道持不同看法,認為清掃淋巴結數目與腫瘤相關病死率無明確相關性[21]。目前尚無指南對根治性膀胱切除術中需要清掃最少的淋巴結數目進行明確規定,但筆者認為適當擴大清掃淋巴結數目越多可以在一定程度上提高陽性淋巴結的發現概率,對于術后進一步治療的指導價值更大。在本研究中,ePLND組在2年PFS率方面高于sPLND組,但兩組2年OS率比較,差異無統計學意義,考慮可能與隨訪時間較短有關。國內關于ePLND和sPLND預后比較的文獻報道較少,僅有個別回顧性研究報道ePLND患者的局部無復發生存率高于sPLND組,側面論證了本研究的結論,但其也指出采用ePLND方式并不會延長患者總生存率[22]。可見關于ePLND和sPLND的預后比較尚需進一步研究。
綜上所述,腹腔鏡根治性膀胱切除術中采用擴大淋巴結清掃并不會增加術后并發癥發生率,且能夠提高患者無進展生存率,加強術后營養支持對于減少患者再入院手術具有積極意義。

