CRISPR-Cas9基因編輯的歷史
我們都知道保持自然界豐富多彩的生物學基礎是遺傳和變異,遺傳可以讓物種一代一代的穩定存在,而變異又可以讓物種變得多姿多彩,使物種內的個體不會一模一樣。而遺傳和變異的基礎是DNA或RNA。DNA的變異可能產生有益基因,也可能會產生有害基因,導致不良性狀的產生。因此生物學家們一直夢想可以在細胞內對遺傳物質或者叫基因進行精準的修改。作為農業科學工作者或者育種家,當需要把某個優良基因導入到栽培品種中時,在基因編輯時代之前,通常采用的方法是雜交育種、誘變育種等。要把優良基因導入栽培品種,需要育種家一年又一年的田間篩選工作,往往從青年熬到中年,即便如此,能夠培育出較突出的優異品種的也是鳳毛麟角。對育種人來說真的太難了。而基因編輯技術出現后,只需要對目標基因進行修改,一兩年內就可以獲得一系列理想中的品種。
1 基因編輯的定義及基本元素
所謂基因編輯,是指在細胞內對遺傳物質進行修改。目前常用的基因編輯主要是CRISPR/Cas9(Clustered Regularly Interspaced Short Palindromic Repeats(CRISPR) and CRISPRassociated(Cas)9)系統,它主要由兩部分組成,一是Cas9蛋白,該蛋白含有核定位信號,可以將表達的Cas9蛋白轉運到細胞核內;另一部分是sgRNA(Single guide RNA),包括5’端20個堿基的引導RNA和3’端的頸環結構,20個堿基通過序列互補識別目標基因,頸環結構被Cas9識別,二者結合形成復合體(圖1)。Cas9蛋白與sgRNA形成復合體后,可以快速的對基因組內的NGG位點(PAM位點)進行掃描,一旦找到與引導RNA(20個堿基)互補的基因組DNA,Cas9/sgRNA復合體就會停止移動,Cas9蛋白就會對基因組進行剪切,在DNA修復過程中就會產生各種變異,從而達到對靶標基因進行編輯的目的[1]。
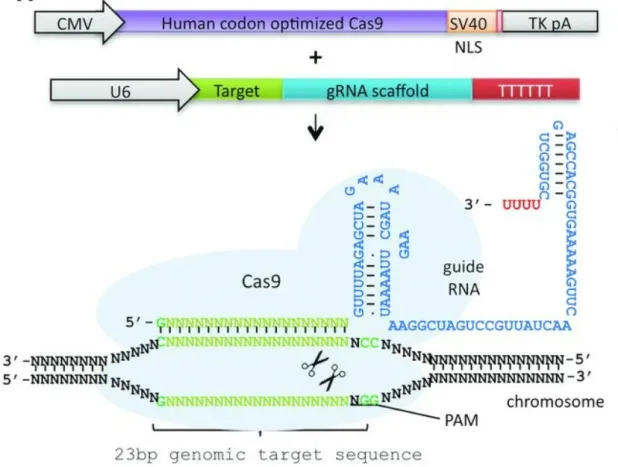
圖1 CRISPR/Cas9系統的組成單元[1]
2 基因編輯的歷史發展
基因編輯從誕生起,就對生物領域產生了廣泛的影響,它在疾病治療、農業生產、藥物開發等多個方面具有巨大的應用價值。在農業上,基因編輯可以極大地推動基因功能研究,而基因功能的清晰明了可以進一步促進農作物的按需改造,培育優質高產、抗逆、抗病和環境友好型的基因編輯農作物。
從1987年發現CRISPR/Cas9的第一個元件開始,到2012年CRISPR/Cas9系統開始應用到細菌中,再到隨后幾年相關研究的爆發性增加,我們還在驚嘆它的迅猛勢頭和強大功能之時,很多相關技術卻已經成為了歷史。
2.1 間隔重復回文序列的發現
1987年,日本的Nakata科研團隊對大腸桿菌iap基因進行測序時,發現在該基因終止子后存在一串間隔重復回文序列(圖2),由于可以形成串聯的二級結構,他們推測該序列可能和mRNA穩定有關[2]。
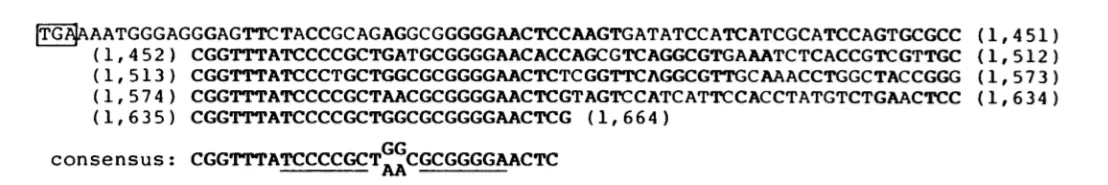
圖2 基因iap序列中的間隔重復回文序列[2]
1995年,讀博士的Mojica在幾種古細菌中也發現了類似的序列(圖3)[3],他對這種有規律的序列十分好奇,他推測與細菌的繁殖有關。但是重復序列在基因組中實在太常見了,沒有多少人在意這些看似沒有功能的序列。隨著測序技術的發展,2000年,Mojica收集了更多的類似序列,他發現40%的細菌和90%的古細菌都有這種短的間隔重復回文序列(圖3)[4]。

圖3 細菌和古細菌中的間隔重復回文序列[3-4]
2.2 Cas基因及CRISPR的由來
2002年,Jansen等發現,這類間隔重復回文序列相鄰的區域,都存在著比較保守的基因(圖4),這些基因現在統稱為Cas基因[5]。Jansen和Mojica一起命名了CRISPR(Clustered regularly interspaced short palindromic repeats)和Cas gene(CRISPR-associated gene )。
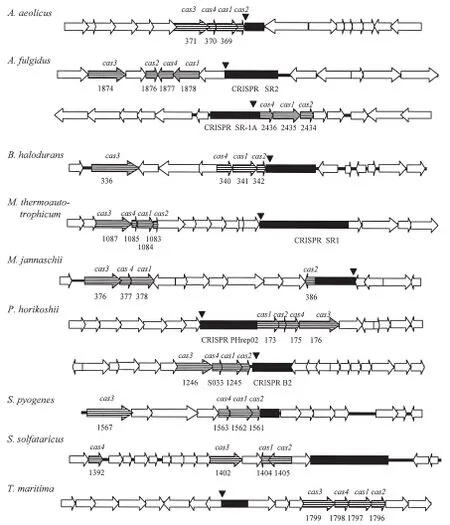
圖4 間隔重復回文序列相鄰的Cas基因[5]
2.3 重復回文序列之間的間隔序列的來源
2005年,生物學家Bolotin對間隔重復回文序列之間的間隔序列產生了興趣,他們把間隔序列與DNA數據庫進行比對分析,結果令人十分震驚,原來這些間隔序列大部分來自于噬菌體。學者Mojica也發現這些序列來自于噬菌體或質粒,他們都推測這些間隔序列可能和細菌防御外來遺傳物質侵染有關[6]。同年,Pource等進一步發現這些間隔序列的排列具有一定的規律性,越是古老的序列,位置離轉錄起始越遠[7]。由此他們提出CRISPR可能參與細菌的免疫功能的假說。
2.4 CRISPR系統與細菌的免疫
2007年,Horvath課題組的Barrangou博士首次證明了CRISPR系統是細菌的免疫系統:當噬菌體侵染細菌時,在細菌的CRISPR處獲得了新的來源于噬菌體的間隔序列,同時新的菌株能對噬菌體產生抗性;另外,Cas基因的突變使細菌喪失了抗性(圖5)[8]。
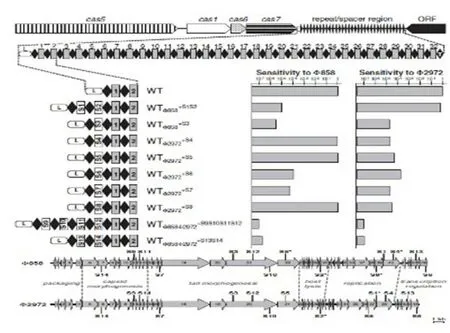
圖5 CRISPR系統是細菌的免疫系統[8]
2.5 外源DNA的剪切
既然CRISPR系統與細菌的免疫系統有關,當噬菌體入侵細菌遺傳系統后,細菌就會對外源DNA進行剪切,從而產生抗性。2008年,Deveau等發現了Cas蛋白剪切位點(PAM位點)具有保守性[9]。2011年,Charpentier教授剛工作不久,也對這類系統產生了十分濃厚的興趣,她找了個碩士研究生Deltcheva進行相關研究,他們發現一段非編碼RNA介導了DNA的剪切(圖6)[10],研究結果發表在頂尖級學術雜志Nature上。
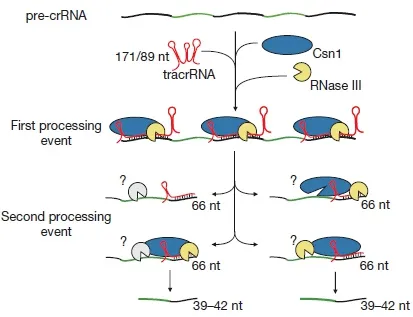
圖6 非編碼RNA介導DNA的剪切[10]
2.6 CRISPR/Cas作為細菌的免疫防御系統的作用機制
至此,CRISPR/Cas作為細菌的免疫防御系統的作用機制已大致清晰:當外來DNA入侵細菌時,CRISPR/Cas可以捕獲外來DNA片段到CRISPR的間隔區,該序列表達后與tracRNA互補與Cas9結合形成復合體,從而對外來DNA進行剪切(圖7)[11]。同樣,作為基因編輯系統的幾個重要要素都已清晰,包括Cas9蛋白,sgRNA,PAM位點,tracRNA等[12]。
2012年9月,Siksnys首次在細菌內表達Cas9和RNAs,實現了對細菌基因組DNA的剪切(圖8)[13]。2012年4月6日Siksnys將手稿投遞給Cell雜志,6天后該雜志通知其拒稿。Virginijus Siksnys于當年5月21日將該稿投給PNAS雜志并于9月4日在線發表。
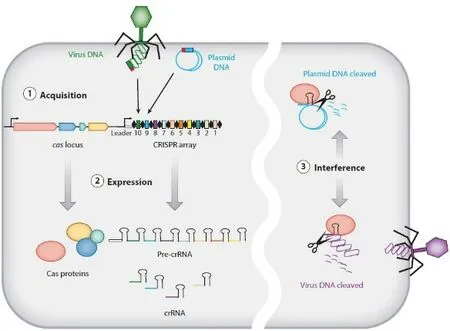
圖7 CRISPR/Cas9作為細菌的免疫防御系統的作用機制[11-12]
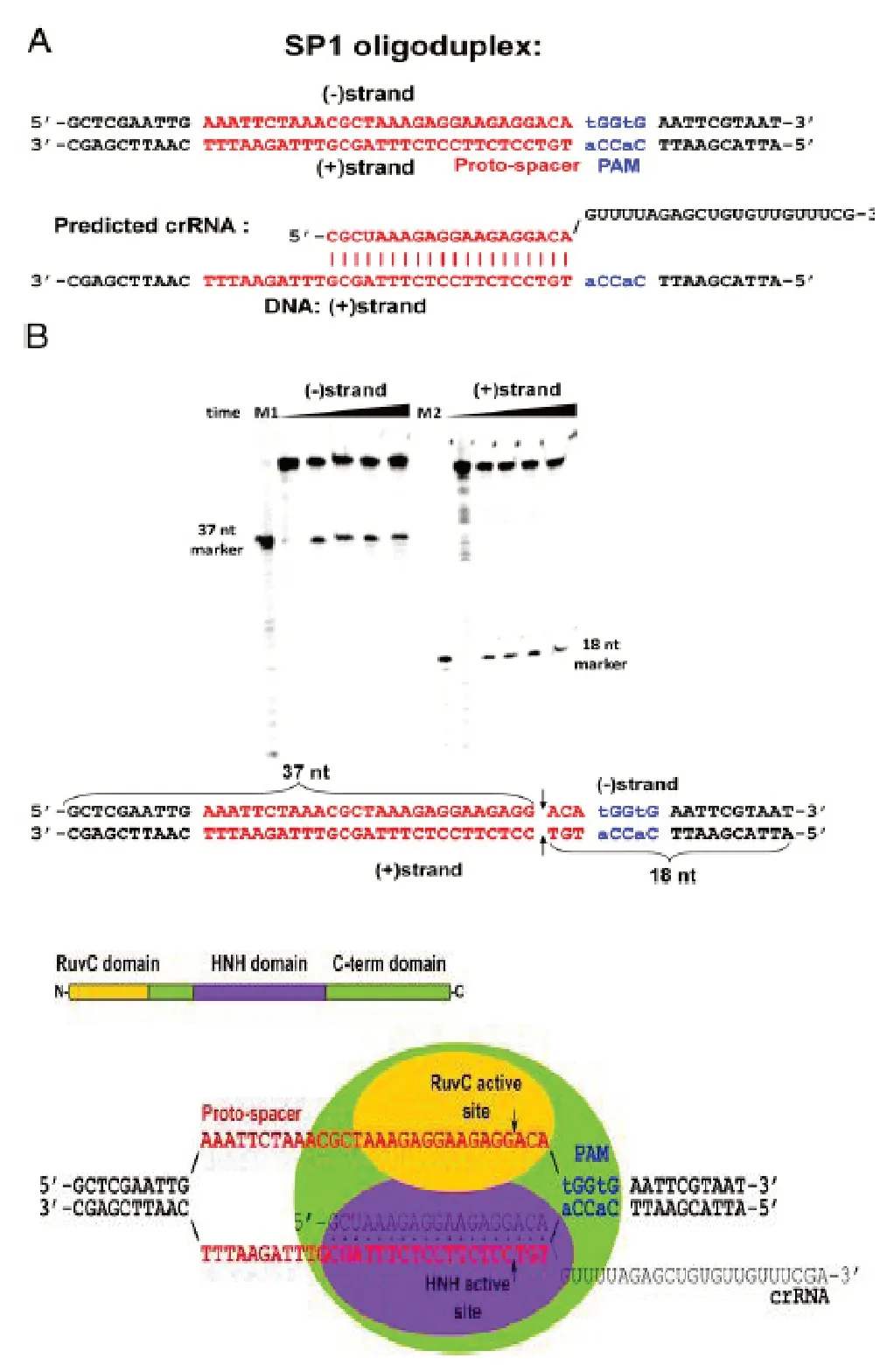
圖8 細菌內表達Cas9和RNAs實現對細菌基因組DNA的剪切[13]
同年7月,來自加州大學伯克利分校的結構生物學家詹妮弗·杜德納(Jennifer Doudna)和瑞典于默奧大學的埃馬紐埃爾·卡彭蒂耶(Emmanuelle Charpentier)合作將tracRNA和crRNA整合成一條RNA,并發現只需Cas9和人工sgRNA在細菌內就能對DNA進行剪切(圖9)[14]。2012年6月8日將論文投與Science雜志,并于6月28日發表。她們的研究證明了在雙鏈RNA指導下切割雙鏈DNA斷裂的內切酶家族并揭示了CRISPR/Cas系統在RNA指導下進行基因編輯的巨大潛力。
2.7 CRISPR系統在動植物中編輯功能的實現
2013年2月,Science背靠背發表了麻省理工學院博德研究所的張鋒課題組和來自于哈佛大學醫學院的George Church課題組關于CRISPR系統在動物細胞系中的編輯功能(圖10)[15-16]。加州大學舊金山分校系統及合成生物學中心的華人齊磊(Lei S.Qi)實驗室,同年也成功將CRISPR/Cas系統應用到哺乳動物細胞中,研究結果發表在Cell雜志上[17]。隨后,人們實現了對果蠅、線蟲、大鼠、豬、羊、等多種動物的基因編輯。同時,基因編輯技術在醫學領域如癌癥治療,胚胎編輯,干細胞等方面的應用在中美兩國像展開競賽一樣,只要有人通過創新領先一步,其他人就會奮起直追。
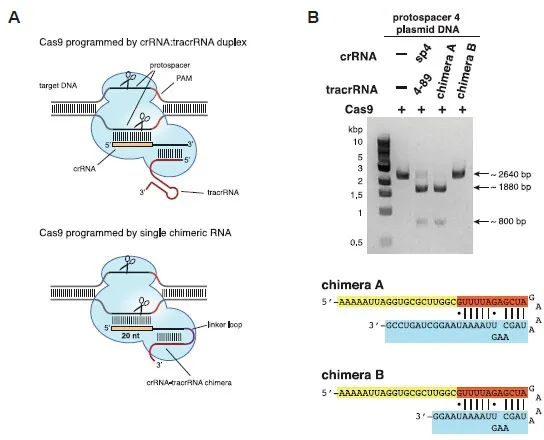
圖9 Cas9和人工sgRNA在細菌內表達實現對細菌DNA的剪切[14]

圖10 CRISPR系統在動物細胞系中實現基因編輯[15-16]
同年,在植物中也有了相關報道。其中中國科學院遺傳所的高彩霞老師開發了多種基因編輯工具,用于植物的基因編輯,極大地推動了植物的基因編輯的發展[18-19]。且高彩霞老師課題組創建了首個具有應用價值的基因編輯農作物,抗白粉病的面包小麥(圖11)[20]。

圖11 基因編輯的抗白粉病面包小麥的創制[20]
2.8 基因編輯技術在農業領域的應用及監管
基因編輯技術在農業領域的應用也展露頭角。除了上面提到的基因編輯的抗白粉病小麥,還有像花束一樣的基因編輯西紅柿,美國冷泉港實驗室通過對控制株型緊湊快速開花的基因SP5G和終止生長,提前成熟的基因SP進行基因編輯,創制出早花早熟,果實成束,顏色多彩的城市西紅柿(圖12)[21]。日本的筑波大學通過對花青素合成酶基因DFR-B進行基因編輯和修飾,得到了色彩斑斕的牽牛花(圖12)[22]。而賓夕法尼亞大學的白蘑菇也只是對一個多酚氧化酶基因PPO進行了編輯就實現了多酚氧化酶活性降低30%,從而減少了白蘑菇在空氣中的褐化(圖12)。而且,據nature news報道這種基因編輯蘑菇已經不在美國農業部監管范圍內[23]。歐洲對轉基因比較保守,甚至影響了基因編輯作物的發展。數據顯示,從2007年到2011年,35%的基因編輯的科學出版來自歐洲,但之后被美國超過。也有科學家呼吁歐盟放松作物基因組編輯監管[24]。中國雖然在研究水平上處于世界領先地位,但由于公眾輿論壓力大,即便是基因編輯領域的專家也是小心謹慎,我們也只能從一些學術會議上聽到科學家們呼吁我國應該放松對基因編輯作物的監管的“建議”。
短短幾年時間,基因編輯系統深刻的改變了生命科學研究。當我們還在驚嘆于系統內某項新技術功能強大之時,它已經被更絕妙的方法所替代,而上一項技術已然成為了歷史。基因編輯技術在醫學、農業等領域的應用以及由此而產生的基因編輯產品也是讓人目不暇接,似乎只有如何監管已經成為了一個被追著跑的問題。

圖12 基因編輯西紅柿,蘑菇和牽牛花[21-23]

