輸尿管軟鏡鈥激光碎石術與微創經皮腎鏡碎石術治療2~3cm腎結石的療效比較
梁鎮鋒, 黃荏釗, 張增強, 盧建軍, 李志雄, 莫俊華, 羅道升
(廣東省東莞市人民醫院泌尿外科, 廣東 東莞 523000)
腎結石是泌尿外科常見疾病,在泌尿系統結石中40%~50%為腎結石,如何在保證理想結石清除效果同時避免損傷腎實質與周圍器官是臨床不斷探索的課題[1]。長期臨床實踐認為微創經皮腎鏡碎石術(Mini-percutaneous nephrolithotomy, MPCNL)為治療直徑≥2 cm腎結石的首選方法,MPCNL術有創傷小、術后恢復快等特點,且結石清除率相對較高,但隨MPCNL術逐漸應用,發現該技術存在大出血、腎功能損害等并發癥[2]。輸尿管軟鏡鈥激光碎石術(flexible ureteroscopy, FURSL)系經自然腔道進行體內碎石,有術中出血量少、對組織損傷小、安全性好、并發癥發生風險低等優勢,國內推薦其用于處理≤1.5 cm的腎結石。而隨著經驗積累及設備更新,FURSL術的適應證正在擴大,可以處理較大的腎結石,成為治療腎結石的新手段。本文在既往研究基礎上,進一步分析FURSL術與MPCNL術治療2~3cm腎結石的療效:
1 資料與方法
1.1一般資料:選取東莞市人民醫院2018年1月至2019年1月期間泌尿外科收治的腎結石患者160例作為研究對象。納入標準:①經腹部X線、CT、B超檢查確診為腎結石,并且結石最大徑2~3cm;②行體外沖擊碎石定位困難、碎石效果不理想者;③所有患者均知情且簽署手術知情同意書。排除標準:①既往曾行MPCNL術或已知輸尿管狹窄、嚴重畸形、腎臟解剖異常者;②同時存在尿路感染、腎積膿、重度腎積水、凝血功能障礙者;③合并嚴重心肺功能不全,無法耐受手術者。按入院順序編號后,采用隨機數字表以簡單隨機分組法將其分為FURSL組、MPCNL組各80例,兩組一般資料有均衡性(P>0.05),詳見表1。
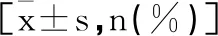
表1 兩組一般資料對比
1.2方法:FURSL組行FURSL術:所有患者術前3~4周均預置入雙J管。全麻下手術。取平臥、膀胱截石位。輸尿管鏡下拔除預先留置的雙J管,自輸尿管鏡向輸尿管開口插入黑泥鰍導絲并觀察輸尿管條件,于導絲引導下將F14/16擴張鞘置入至輸尿管上段UPJ水平下方1cm處并固定。經輸尿管擴張鞘置入Olympus電子輸尿管軟鏡進入腎盂,觀察腎盂及各盞情況,尋找結石。經軟鏡插入200μm鈥激光光纖,抵住結石,不斷調整角度將結石碎片化或粉末化,術中以注射器手工灌注生理鹽水維持術野清晰,根據結石的CT值調整激光參數,決定是否碎片化還是粉末化結石,對于3~4mm結石碎片尤其是下盞結石碎片以Frl.9取石籃(COOK)取出。碎石取石完畢后,將軟鏡退至鞘內,邊退鏡邊退鞘,觀察輸尿管是否損傷及損傷程度。重新置入黑泥鰍導絲,留置F4.8雙J管一根,留置尿管,手術完畢。術后1d復查腹部平片(KUB),若發現有意義的殘石則行二次FURSL術。MPCNL組行MPCNL術:采用硬膜外麻醉。取截石位,逆行插入F5輸尿管導管至輸尿管,留置導尿管。后俯臥,采用小枕將腰腹部墊高,逆行注水(經輸尿管導管)以形成人工腎積水,于B超引導對目標腎盞(11肋間、腋后線與肩胛下角線間)進行穿刺,拔除針芯有尿液引出,將黑泥鰍導絲置入后“一步法”擴張至F18或F20,經外鞘置入經皮腎鏡硬鏡觀察外鞘與腎結石位置,使用氣壓彈道或鈥激光擊碎結石并自經皮腎通道經水流沖出結石碎片,用異物鉗將較大殘石取出,結合術前CT檢查與術中超聲結果,評估結石是否清除干凈。術后留置F4.8雙J管和F16腎造瘺管,術后3~4d復查KUB片,若發現仍有殘石則予以二期MPCNL術,若未見殘石則拔除腎造瘺管。
1.3觀察指標:①比較兩組術中與術后指標,包括手術時間、術中出血量、住院時間、住院費用、血紅蛋白下降值、一期與二期結石清除率;②取術前、術后2d清晨空腹靜脈血3mL,測定血尿素氮(BUN)、血肌酐(Scr),同時測定感染性指標降鈣素原(PCT);③采用疼痛視覺模擬評分(VAS)評估兩組術前、術后1d、術后2d疼痛度,該表滿分0~10分,得分越高疼痛越嚴重;④比較兩組術后3個月內手術相關并發癥發生率,包括≥2級的發熱、血尿、感染、腎周血腫等。
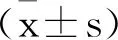
2 結 果
2.1兩組術中與術后指標比較FURSL組術中出血量、住院時間、住院費用、血紅蛋白下降值、一期結石清除率低/短于MPCNL組(P<0.05),手術時間較對照組延長(P<0.05),兩組二期結石清除率比較差異無顯著性(P>0.05),詳見表2。
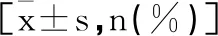
表2 兩組術中與術后指標比較
2.2兩組BUN、Scr、PCT變化比較:兩組術后2d BUN、Scr、PCT呈明顯升高趨勢(P<0.05);FURSL組術后2d BUN、PCT及其治療前后差值低于MPCNL組(P<0.05),兩組術后2d Scr比較差異無統計學意義(P>0.05),詳見表3。

表3 兩組BUN Scr PCT變化比較
2.3兩組VAS評分比較:與術前比較,兩組術后VAS評分呈下降趨勢(P<0.05),且FURSL組術后1d、術后2d VAS評分低于MPCNL組(P<0.05),詳見表4。
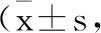
表4 兩組VAS評分比較分)
2.4兩組并發癥發生率比較:FURSL組術后3個月內并發癥發生率低于MPCNL組(P<0.05),詳見表5。

表5 兩組并發癥發生率比較
3 討 論
2~3cm腎結石患者的治療方案是臨床研究熱點,MPCNL治療雖然提高了治療效率,使結石得以有效清除,但MPCNL需穿刺及擴張腎實質建立通道,不可避免損傷腎實質與周圍器官[3]。近年來輸尿管鏡取石術逐漸在上尿路結石中開展應用,其中FURSL術因有鏡體纖細柔軟、能有效降低對腎盂與輸尿管黏膜的損傷等優勢而在臨床廣泛應用。隨輸尿管軟件技術與輔助碎石設備的研發、手術經驗積累,FURSL術適應證不斷擴大,在臨床實踐中較多醫生開始將其應用于2~3cm腎結石的治療[4,5]。
本研究中,FURSL組術中出血量、住院時間、住院費用、血紅蛋白下降值均優于MPCNL組,表明相比于MPCNL術,FURSL術風險小,可減輕創傷與患者醫療負擔,促進其術后康復,可能是因為FURSL術主要經自然腔道置入腔鏡,更符合“無創”原則,且FURSL術后早期可進行下床活動,這有利于促進結石碎片排出,而MPCNL術中需一或多處穿刺,術后也需保留造瘺管,這不利于患者術后康復進程[6]。我科輸尿管軟鏡手術均采用二期手術,一期先留置雙J管3~4周,二期使用F14/16擴張鞘,加強灌注液引流,有效避免術中加壓灌注致腎內壓過高,降低腎損傷程度及感染風險。FURSL組手術時間較MPCNL組延長,可能原因有:①為進一步提高結石清除效果和避免石街現象,FURSL術中需粉碎結石至直徑≤2mm,而MPCNL術碎片可經穿刺通道自然地經水流沖出,無需粉碎結石即可達到這一目的;②對于體積較大結石如鹿角形腎結石者,在FURSL術中需以鈥激光將結石碎片化,并采用套石籃取石,這可能延長手術時間。結石殘余是復雜性腎結石復發的主要原因,本研究FURSL組的一期結石清除率低于MPCNL組,表明FURSL術一期清除效果不及MPCNL術,但是兩組二期結石清除率比較差異無統計學意義。但再次手術可能導致治療周期延長,加重患者經濟負擔,因此對于經濟條件欠佳、術后療效預期較高的患者應謹慎推薦FURSL術,與既往孫懿等[7]的研究論點相符。本研究中兩組術后2d BUN、Scr、PCT呈明顯升高趨勢,說明兩種術式均可能對患者腎功能造成損傷,且引起感染,但FURSL組術后2d BUN、PCT及其治療前后差值低于MPCNL組,提示FURSL術后近期腎損傷程度及感染風險小于MPCNL術,這與王炳衛等[8]的報道結果一致。此外本研究中FURSL組術后1d、術后2d VAS評分低于MPCNL組,說明FURSL術造成的疼痛較MPCNL術輕,這可能與輸尿管軟鏡經人體自然腔道進入腎臟集合系統而進行碎石有關,目前臨床常采用電子輸尿管軟鏡,其單側彎曲極限可達270度,當插入鈥激光光纖等設備后彎曲度也可達185~270度,能輕松抵達腎盂及各腎盞位置,聯合鈥激光碎石操作,避免腎盂黏膜與腎實質損傷[9]。
FURSL組術后3個月內并發癥發生率低于MPCNL組,表明FURSL術可降低并發癥風險。FURSL術直接經自然通道到達腎內位置,無需建立人工通道,可進入腎盂及腎盞碎石,避免術中腎臟創傷,減少腎臟出血風險,而MPCNL術需建立通道,對腎臟造成創傷,存在出血、感染等風險[10]。
綜上所述,FURSL術治療2~3cm腎結石較MPCNL術創傷小、術后恢復快,可減輕腎損傷小、疼痛、感染及并發癥風險,但FURSL存在診治周期長,手術時間延長,一期結石清除率低等缺點。因而對于經濟條件差、術后療效預期較高的患者應推薦行MPCNL術;但對于MPCNL術存在恐懼心理,害怕有穿刺創傷而經濟條件、時間允許的患者,則可推薦選擇FURSL術。

