希特林蛋白缺陷病并自身免疫性溶血1例及文獻復習
段金濤 鄧成俊 李娟
【摘要】 目的 對1例臨床診斷為新生兒肝內膽汁淤積癥(NICCD)合并自身免疫性溶血的患兒及家系進行SLC25A13基因突變分析, 以達到早確診早治療的目的。方法 結合患兒的臨床特點及靶向捕獲二代測序(NGS)檢測結果總結患兒的遺傳特點進行確診。結果 患兒表現為皮膚、鞏膜黃染等癥狀, 伴血乳酸、甲胎蛋白等明顯升高, 臨床診斷為NICCD。基因檢測結果提示患兒SLC25A13基因5號外顯子及5號內含子存在長片段純合變異, 父母均為攜帶者。結論 NICCD合并自身免疫性溶血病患臨床上較為罕見, 本文報告了該疾病致病基因新的突變形式, 為日后疾病的及時診療提供案例參考。
【關鍵詞】 希特林蛋白缺陷病;SLC25A13;肝內膽汁淤積癥
DOI:10.14163/j.cnki.11-5547/r.2020.29.077
【Abstract】 Objective ? SLC25A13 gene mutation analysis was performed on a child and family with a clinical diagnosis of neonatal intrahepatic cholestasis caused by citrin deficiency (NICCD) combined with autoimmune hemolysis to achieve the purpose of early diagnosis and early treatment. Methods ? Combined with the clinical characteristics of the children and the results of Next generation sequencing (NGS) detection, the genetic characteristics of the patients were summarized for diagnosis. Results ? The children presented with symptoms such as skin and sclera yellow staining, accompanied by a significant increase in blood lactic acid and alpha-fetoprotein, and was clinically diagnosed as NICCD. The results of genetic testing indicated that there were long homozygous mutations in exon 5 and intron 5 of SLC25A13 gene, and both parents were carriers. Conclusion ? NICCD combined with autoimmune hemolytic disease is clinically rare. This article reports a new mutation form of the disease-causing gene, which provides a case reference for timely diagnosis and treatment of the disease in the future.
【Key words】 Citrin deficiency; SLC25A13; Neonatal intrahepatic cholestasis caused by citrin deficiency
希特林蛋白缺陷病(citrin deficiency, CD)是一種由于SLC25A13基因缺陷導致希特林蛋白表達異常的功能缺陷性疾病, 為常染色體單基因隱性遺傳疾病[1]。致病基因位于染色體7q21.3, 含18個外顯子和17個內含子, 由675個氨基酸組成, 全長約200 kb, 主要在肝細胞內表達。目前已報道CD具有3種年齡依賴性臨床表型:希特林缺陷導致的新生兒肝內膽汁淤積癥(neonatal intrahepatic cholestasis caused by citrin deficiency, NICCD)、成人發病瓜氨酸血Ⅱ型(adult-onset type Ⅱ citrullinemia, CTLN2)、希特林缺陷導致的生長發育落后和血脂異常(failure to thrive anddyslipidemia caused by citrin eficiency, FTTDCD)[2]。其中NICCD是目前CD兒科主要的臨床表型, 本研究對1例合并自身免疫性溶血的NICCD患兒進行分析及文獻復習, 報告如下。
1 臨床資料
患兒女, 2月6天, 彝族, 因“皮膚黃染1月余, 加重4 d”入院。患兒生后1周出現皮膚、鞏膜黃染, 當地醫院先后予藍光箱等治療效果不佳, 4 d前家長發現患兒黃疸較前加重就診。近1周無發熱, 無嗜睡、抽搐, 無咳嗽、嘔吐, 否認白陶土樣大便。查體:皮膚、鞏膜黃染, 無皮疹及瘀斑、淤點, 腹膨隆, 肝右肋下3 cm, 劍突下1.5 cm可及, 脾未及腫大。輔助檢查:血型AB型, RhD陽性。血常規檢測:白細胞計數 13.97×109/L, 紅細胞計數3.12×1012/L, 血紅蛋白 77.00 g/L, 網織紅細胞百分比5.36%, 紅細胞形態:成熟紅細胞輕度大小不等, 中心淺染區擴大。Coombs試驗:直接抗人球蛋白試驗:+;間接抗人球蛋白試驗:+;抗IgG:陽性;抗C3:陰性。肝功能:谷丙轉氨酶 67 U/L, 谷草轉氨酶 122 U/L, 總膽紅素 209.3 μmol/L, 間接膽紅素 74.5 μmol/L, 直接膽紅素 134.8 μmol/L, 總膽汁酸 166.7 μmol/L, 總蛋白49.9 g/L, 白蛋白27.9 g/L。
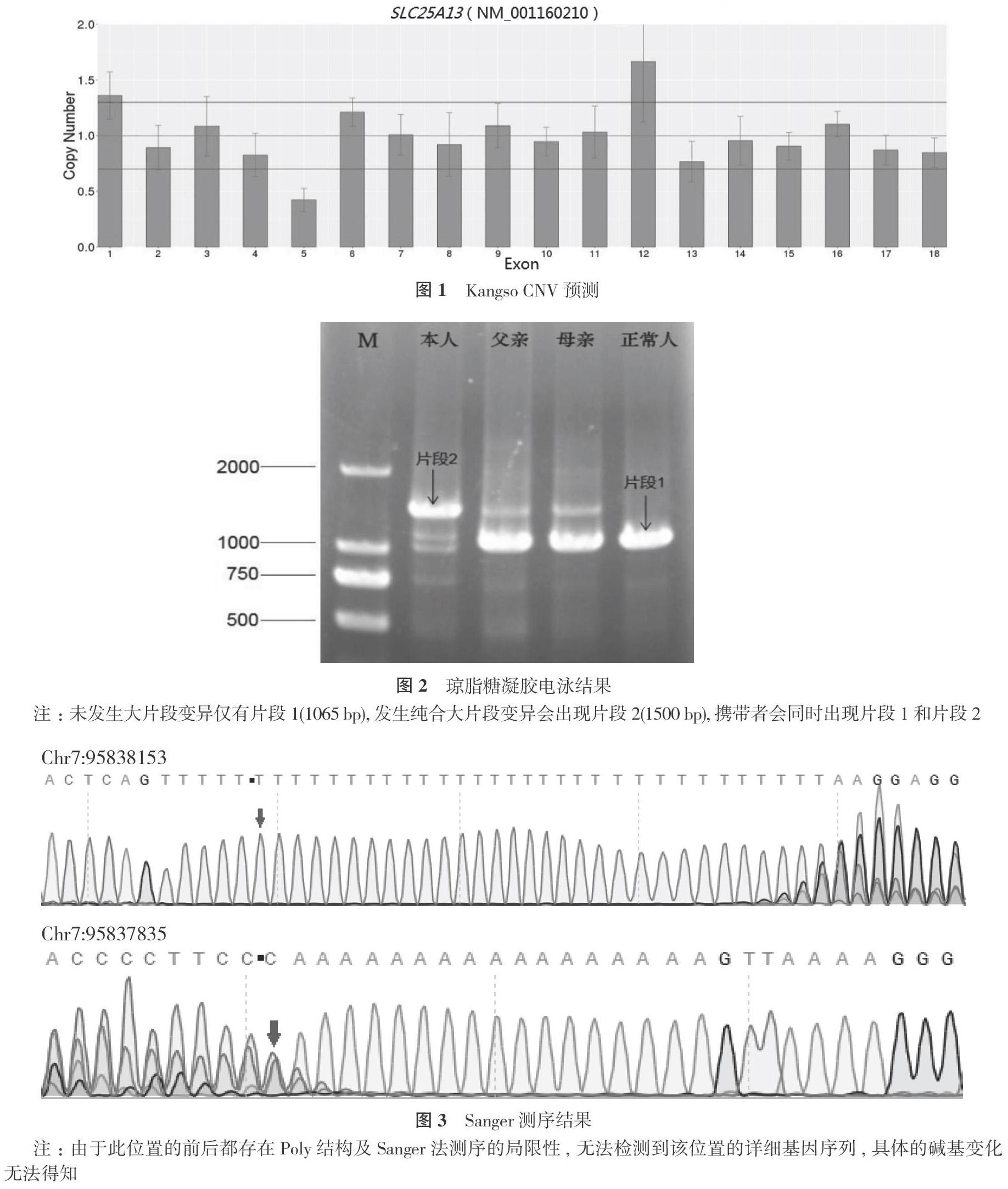
血氣分析:pH 7.445, 堿剩余(BE) -8.1 mmol/L, 乳酸濃度3.2 mmol/L。甲胎蛋白 60500 ng/ml。空腹血糖2.2 mmol/L。血串聯質譜檢測為瓜氨酸102.64 mmol/L、甲硫氨酸119.66 mmol/L、酪氨酸 66.04 mmol/L、瓜氨酸/苯丙氨酸比值2.96、甲硫氨酸/苯丙氨酸比值3.45, 谷氨酸/瓜氨酸比值0.91。結合患兒血乳酸、甲胎蛋白等明顯升高, 有低蛋白、低血糖等表現, 臨床診斷為NICCD, 予無乳糖和富含中鏈甘油三酯的配方奶粉喂養2周, 復查血串聯質譜檢測瓜氨酸、甲硫氨酸、酪氨酸等均降至正常范圍, 3個月后檢查肝功能、膽紅素基本正常。臨床診治過程中, 經昆明市兒童醫院醫學倫理委員會審核批準, 遵循家屬意見并簽署知情同意書后, 采集患兒及父母外周血2 ml, 送北京康旭醫學檢驗所進行全外顯子檢測, 重點關注希特林蛋白缺陷病, 并根據拷貝數變異(CNV)預測結果, 進一步完善SLC25A13基因檢測, 結果提示SLC25A13基因Exon5的全部或部分可能存在變異(見圖1), 后采用Sanger法測序及瓊脂糖凝膠電泳, 證明患兒SLC25A13基因5號外顯子及5號內含子(chr7:95837835-95838153位置)存在長片段純合插入變異(見圖2, 圖3), 其父母為長片段變異的攜帶者(雜合變異, 見圖2)。
2 討論
Citrin蛋白是一種由SLC25A13基因編碼的線粒體內鈣結合蛋白, 其功能是將線粒體內的天冬氨酸轉運至胞質內, 參與尿素、蛋白及核苷酸的合成, 將還原型煙酰胺腺嘌呤二核苷酸(NADH)轉變為煙酰胺腺嘌呤二核苷酸(NAD+), 而NADH/NAD+比值是維持部分細胞生化代謝途徑的重要因素[3, 4]。Citrin功能缺陷可導致細胞質內NADH堆積, 蛋白質與核酸合成受到抑制, 引起一系列生化代謝紊亂。
NICCD臨床相對少見, 其發病率為1/34000~1/17000,?男女比例無明顯差異, 多數新生兒期起病[3-5], 主要的臨床表現為黃疸、肝大、脂肪肝、生長發育遲緩等;生化檢查可見肝酶異常、膽汁淤積、低蛋白血癥及低血糖, 部分患兒存在凝血功能異常, 血氨、甲胎蛋白、乳酸升高或血脂異常[3, 6]。目前缺乏公認的臨床或生化診斷標準, 基因分析存在2個SLC25A13等位基因純合或復合雜合突變可確診。
本例患兒以皮膚黃染加重就診, 入院經血液、生化檢查發現存在“自身免疫性溶血”, 對癥治療后溶血停止, 但患兒同時伴有谷丙轉氨酶、谷草轉氨酶、直接膽紅素、總膽汁酸、甲胎蛋白、血乳酸等升高, 白蛋白和空腹血糖降低, 自身免疫性溶血不能完全解釋患兒臨床表現, 結合血串聯質譜檢測結果及予無乳糖和富含中鏈甘油三酯的配方奶喂養后病情明顯好轉, 臨床診斷NICCD, 進一步完善SLC25A13基因檢測, 發現5號外顯子及5號內含子存在長片段純合插入變異, 其父母為變異攜帶者, 符合常染色體隱性遺傳方式, 確診患者為NICCD合并自身免疫性溶血, 這在臨床比較罕見, 既往相關文獻未見報道[4, 5, 7, 8]。
目前, 全世界已發現100余種SLC25A13基因突變, 我國以c.851-854del4(58.1%)、c.1638-1660dup23(8.85%)、IVS6+5G>A(8.41%)和IVSl6ins3kb(7.52%) 4種突變最為常見, 占80%以上[9, 10], 但隨著新的檢測方法在臨床的應用, 新的突變位點不斷報道[11], 同時, 部分確診的患兒也發現存在一些之前未被發現的特殊臨床表現[12, 13]。本研究檢出的突變位點既往在人類基因突變數據庫(HGMD)、EnSembl數據庫、千人基因組數據庫中均未見報道, 對于完善我國SLC25A13基因突變數據庫具有重要意義, 但目前尚不能肯定新突變與臨床表現的相關性, 還需通過動物模型或蛋白功能表達等研究進一步證實。同時, 在臨床工作中, 當臨床醫師在遇到無法用一種疾病解釋病情時, 需要醫生仔細結合病史、查體及輔助檢查, 及時進一步完善相關檢查, 避免漏診、誤診, 也能夠為患兒臨床早期遺傳咨詢及明確病因提供參考。
參考文獻
[1] Zhang ZH, Lin WX, Zheng QQ, et al. Molecular diagnosis of citrin deficiency in an infant with intrahepatic cholestasis: identification of a 21. 7kb gross deletion that completely silences the transcriptional and translational expression of the affected SLC25A13 allele. Oncotarget, 2017, 8(50):87182-87193.
[2] Okano Y, Ohura T, Sakamoto O, et al. Current treatment for citrin deficiency during NICCD and adaptation/compensation stages: Strategy to prevent CTLN2. Mol Genet Metab, 2019, 127(3):175-183.
[3] Lu CT, Shi QP, Li ZJ, et al. Blood glucose and insulin and correlation of SLC25A13 mutations with biochemical changes in NICCD patients. Exp Biol Med (Maywood), 2017, 242(12):1271-1278.
[4] Ohura T, Kobayashi K, Tazawa Y, et al. Clinical pictures of 75 patients with neonatal intrahepatic cholestasis caused by citrin deficiency (NICCD). J Inherit Metab Dis, 2007, 30(2):139-144.
[5] Oh SH, Lee BH, Kim GH, et al. Biochemical and molecular characteristics of citrin deficiency in Korean children. J Hum Genet, 2017, 62(2):305-307.
[6] Saheki T, Inoue K, Tushima A, et al. Citrin deficiency and current treatment concepts. Molecular Genetics & Metabolism, 2010, 100(supp-S):S59-S64.
[7] 彭曉康, 劉希, 劉攀, 等. Citrin缺陷導致的新生兒肝內膽汁淤積癥32例臨床特點分析. 中華實用兒科臨床雜志, 2019, 34(5):377-380.
[8] 白欣立, 張亞男, 楊亭亭, 等. Citrin缺陷導致新生兒肝內膽汁淤積癥患兒臨床特點及SLC25A13基因分析. 中國婦幼保健, 2017, 32(19):4748-4751.
[9] Song YZ, Zhang ZH, Lin WX, et al. SLC25A13 gene analysis in citrin deficiency: sixteen novel mutations in East Asian patients, and the mutation distribution in a large pediatric cohort in China. PloS one, 2013, 8(9):e74544.
[10] Zhang ZH, Lin WX, Deng M, et al. Clinical, molecular and functional investigation on an infant with neonatal intrahepatic cholestasis caused by citrin deficiency (NICCD). PloS one, 2014, 9(2):e89267.
[11] Lin WX, Zeng HS, Zhang ZH, et al. Molecular diagnosis of pediatric patients with citrin deficiency in China: SLC25A13 mutation spectrum and the geographic distribution. Sci Rep, 2016(6):29732.
[12] Lipiński P, Jurkiewicz D, Ciara E, et al. Neonatal cholestasis due to citrin deficiency: diagnostic pitfalls. Acta biochimica Polonica, 2020, 67(2):225-228.
[13] 張建玲, 舒賽男, 蔡在勝, 等. 以肝硬化腹腔積液為特征表現的Citrin蛋白缺陷所致新生兒肝內膽汁淤積癥1例報告. 臨床肝膽病雜志, 2019, 35(2):372-375.
[收稿日期:2020-06-24]

