茉莉花實時熒光定量PCR內參基因的篩選與驗證
齊香玉,陳雙雙,馮 景,王華娣,鄧衍明,
(1.江蘇省農業科學院 休閑農業研究所,江蘇省高效園藝作物遺傳改良重點實驗室,江蘇 南京 210014;2.江蘇大學 生命科學學院,江蘇 鎮江 212013)
實時熒光定量PCR(qRT-PCR)是研究基因表達的一項重要技術,通過對內參基因的檢測從而達到對目的基因表達情況的實時監測[1]。qRT-PCR技術具有靈敏度高、特異性強和重復性好等優點,得到了廣泛應用。但該技術對樣品RNA的質量、反轉錄的效率、內參基因選擇及引物特異性等都有著非常嚴格的要求[2]。其中,qRT-PCR分析結果準確可靠的前提是合適內參基因的選擇。常用的內參基因包括EF1α(Elongation factor 1 alpha)、Actin(Actin-7)、GAPDH(Glyceraldehyde-3-phosphate dehydrogenase)、PP2A(Protein phosphatase 2A)、TIP41(TIP41-like family protein)、UPL7(E3 ubiquitin-protein ligase UPL7)、PEPKR1(Phosphoenolpyruvate carboxylase-related Kinase 1)、SAND(SAND family protein)和TUB(Tubulin)等[3-4]。理想的內參基因在植物不同生長發育階段、不同組織中均能穩定表達,不受環境影響[5]。但研究表明,在不同植物中、不同時間及處理條件下,內參基因表達穩定性存在較大差異,如Actin在側柏各組織中有較好的穩定性表達[6],但其表達穩定性在柚木各組織中卻較差[7];18SrRNA在黃山欒樹不同組織中表達穩定性較好[8],但在珙桐各器官中表達穩定性較差[9]。如直接使用未經篩選的內參基因,會導致試驗數據出現偏差,影響目的基因表達水平的分析[10]。因此,為了確保qRT-PCR分析結果可靠準確,針對不同植物、組織、生長發育階段及試驗條件等因素,應對內參基因表達穩定性進行評價從而篩選出適宜的內參基因。
茉莉花(Jasminumsambac(L.)Aiton)又名茉莉、茶葉花,為木樨科(Oleaceae)素馨屬常綠灌木。茉莉花原產于印度、巴基斯坦等地,在1 700多年前的漢代傳入我國,最早在東南沿海地區栽培,然后漸次北上直到長江流域,現主要分布在廣西、福建、四川、廣東等地,是“一路一帶”經濟植物開發與應用的重要成員之一[11]。茉莉花具有較高的觀賞、茶用和藥用價值,歷來受到我國人民的喜愛,被譽為“天下第一香”、“花樹中的珍品”[12]。茉莉花因馥郁及優雅的香氣而被稱為“精油之王”,廣泛用于花茶和香精加工產業。目前,對茉莉花分子生物學方面的研究日益增多,基因表達分析已被應用于茉莉花香氣基因調控網絡的研究中[13],如JsDXR和JsTPS在花發育不同階段及花不同部位的表達水平[14]、α-法呢烯合成相關的HMGS、HMGR、FPPS、TPS基因在茉莉花不同花期的表達情況的研究[15]等。研究茉莉花香氣合成代謝通路中的關鍵基因,明確其調控分子機制將有助于對香氣成分進行調控。茉莉花基因表達的研究必須要有合適的內參基因作為參照,但目前關于茉莉花內參基因的研究尚未見報道。因此,本研究選取8個常用候選內參基因(EF1α、GAPDH、Actin、PP2A、TIP41、UPL7、PEPKR1和SAND),研究其在茉莉花不同組織和花發育不同時期的表達水平,并借助geNorm、NormFinder、BestKeeper和RefFinder軟件對這些內參基因表達的穩定性進行評價,進一步利用目的基因對篩選獲得的內參基因的穩定性和可靠性進行驗證。本研究結果為后續茉莉花基因表達、功能及調控等相關研究奠定基礎。
1 材料和方法
1.1 試驗材料
供試材料為多年生雙瓣茉莉花,種植于江蘇省農業科學院茉莉花種質資源圃。不同組織樣品分別取自根、莖、嫩葉、成熟葉和花;花發育不同階段樣品取樣參照Deng等[16]分別取階段Ⅰ(幼蕾期)、階段Ⅲ(膨大花蕾期)、階段Ⅴ(最長花蕾期)和階段Ⅵ(初綻期)4個時期。每個樣品設置3個生物學重復,液氮速凍后置-80 ℃冰箱保存。
1.2 試驗方法
1.2.1 RNA提取及cDNA合成 用RNA提取試劑盒(TaKaRa, 日本)提取樣品總RNA。總RNA樣品用DNaseⅠ(TaKaRa, 日本)消化去除基因組DNA污染。利用ND-1000 spectrophotometer(NanoDrop, Wilmington,DE)和1.0%的瓊脂糖凝膠電泳檢測總RNA濃度、純度和完整性。取各樣品1 000 ng的RNA為模板,按照PrimeScript 1st strand cDNA synthesis kit(TaKaRa, 日本)的操作方法反轉錄合成cDNA,cDNA置于-20 ℃保存。
1.2.2 候選內參基因選擇及引物設計 根據繡球與宿根花卉研究室前期茉莉花轉錄組數據,選擇較常見的8個候選內參基因:EF1α、GAPDH、Actin、PP2A、TIP41、UPL7、PEPKR1和SAND。根據候選內參基因序列及引物設計原則,運用軟件Primer Premier 5.0設計內參基因的引物(表1),并由南京思普金生物科技有限公司合成。

表1 茉莉花候選內參基因引物序列
1.2.3 候選內參基因引物特異性分析 用內參基因qRT-PCR引物,以茉莉花各樣品cDNA等量混合為模板進行PCR擴增。PCR反應的體系為25.0 μL:cDNA模板1.0 μg、上下游引物(10 μmol/L)各1.0 μL、TaKaRa Taq(5 U/μL)0.2 μL、10× PCR Buffer 2.5 μL、dNTP(2.5 mmol/L each)2.0 μL,加水至25.0 μL。PCR反應條件為:94 ℃預變性5 min;94 ℃變性30 s,60 ℃退火30 s,72 ℃延伸30 s,35個循環;72 ℃延伸7 min。通過2%的瓊脂糖凝膠電泳對引物的特異性進行檢測。
1.2.4 內參基因的qRT-PCR分析 qRT-PCR擴增采用TaKaRa公司的TB Green Premix Ex Taq(Tli RNaseH Plus)試劑盒,具體操作按說明書進行。cDNA稀釋10倍作為模板,反應體系20 μL:cDNA模板2.0 μL、TB Green Premix Ex Taq(Tli RNaseH Plus)(2×)10 μL、上下游引物(10 μmol/L)各0.4 μL、ROX Reference Dye Ⅱ(50×)0.4 μL、ddH2O 6.8 μL。反應在實時熒光定量PCR儀ABI 7500上進行,反應程序:95 ℃預變性30 s;95 ℃變性5 s,60 ℃退火34 s,40個循環;95 ℃變性15 s,60 ℃退火1 min,95 ℃變性15 s。每個樣品設3個生物學重復和3次技術重復。
1.2.5 數據處理和分析 qRT-PCR后得出Ct值,分別利用geNorm[17-18]、NormFinder[19]和BestKeeper[20]軟件對Ct值進行分析,對8個內參基因表達的穩定性進行比較,并從中選擇最適內參基因。使用RefFinder程序對以上3種軟件的分析結果進行綜合分析,選出最適于茉莉花不同組織和花發育不同階段的內參基因[21]。
1.2.6 內參基因穩定性驗證 通過對茉莉花花香氣形成過程中的5-磷酸脫氧木酮糖合成酶(DXS,Deoxyoxylulose-5-phosphate synthase)基因JsDXS和苯丙氨酸解氨酶(PAL,phenylalanine ammonia lyase)基因JsPAL2在花發育不同階段的表達模式進行分析,從而對篩選的內參基因穩定性和可靠性進行驗證。基因JsDXS和JsPAL2qRT-PCR分析的引物序列分別參考孫君等[22]、熊青等[23]文獻報道中的引物序列。
2 結果與分析
2.1 總RNA質量檢測及引物特異性分析
NanoDrop檢測各樣品總RNA的OD260/280均在1.95~2.13,OD260/230均大于2.0,說明總RNA的純度較好。通過1.0%的瓊脂糖凝膠電泳檢測樣品總RNA完整性,所有樣品28S rRNA和18S rRNA條帶清晰完整,說明總RNA的完整性較好,達到后續試驗的需求。
以各樣品cDNA等量混合為模板,對8個內參基因進行PCR擴增。凝膠電泳結果顯示,8個候選內參基因均擴增出單一條帶,無非特異擴增及引物二聚體,且擴增條帶大小符合預期(圖1),說明設計的引物特異性好,可用于qRT-PCR試驗。

圖1 茉莉花8個候選內參基因PCR產物
將各樣品cDNA等量混合后,稀釋10倍作為模板,分別用8個候選內參基因引物進行qRT-PCR擴增,結果如圖2所示。各候選內參基因溶解曲線均只有明顯的單一峰,說明8個候選內參基因引物擴增特異性強,符合qRT-PCR試驗要求,可用于后續候選內參基因穩定性的分析。

圖2 茉莉花8個候選內參基因qRT-PCR溶解曲線
2.2 候選內參基因表達分析
分別以茉莉花不同組織和花發育不同階段cDNA為模板,進行qRT-PCR分析。結果如圖3所示,8個候選內參基因在茉莉花不同樣品中的Ct值均有一定的變化,變化的趨勢各有不同。EF1α在不同樣品的Ct值在19.09~23.27,GAPDH的Ct值在17.89~31.26,Actin的Ct值27.88~29.20,PP2A的Ct值在22.16~34.03,TIP41的Ct值在22.31~33.51,UPL7的Ct值在23.47~31.39,PEPKR1的Ct值在26.96~29.98,SAND的Ct值在25.54~31.20。除Actin外,其他所有候選內參基因在花中的Ct值均高于其他組織,即在花中的表達量均最低。因各候選內參基因的Ct值(除Actin)在花與其他組織中的差異較大,對后期結果影響較大,故在候選內參基因穩定性評價中,將不同組織分為“有花組”(包含根、莖、嫩葉、成熟葉、花)和“無花組”(包含根、莖、嫩葉、成熟葉)進行分析。8個候選內參基因平均Ct值為21.53~28.68,其中EF1α的Ct值最小,說明其表達豐度較高(圖4)。

Ⅰ.幼蕾期;Ⅲ.膨大花蕾期;Ⅴ.最長花蕾期;Ⅵ.初綻期。圖7同。

箱體內的線表示中位數;箱體下、上邊分別表示25%,75%的百分位數;箱體上、下豎線分別表示最大值與最小值。
2.3 候選內參基因表達的穩定性分析
2.3.1 geNorm分析 geNorm軟件依據計算的每個基因表達穩定性M值來進行排序,M值越小穩定性越好,反之則穩定性越差,M<1.5時認為是理想內參。geNorm軟件分析結果顯示,在有花組中,EF1α、SAND、PEPKR1、UPL7的M值小于1.5,說明這些內參基因表達穩定性較好,表達的穩定性由高到低排序依次為:EF1α=SAND>PEPKR1>UPL7>TIP41>PP2A>Actin>GAPDH(圖5-A);在無花組中,各候選內參基因M值均小于1.5,說明8個內參基因均具有良好的穩定性,表達穩定性由高到低排序依次為:GAPDH=UPL7>TIP41>EF1α>PP2A>SAND>PEPKR1>Actin(圖5-B);在花發育不同階段,各基因M值均小于1.5,說明8個內參基因均具有良好的穩定性,表達穩定性由高到低排序依次為:EF1α=Actin>PEPKR1>GAPDH>SAND>TIP41>UPL7>PP2A(圖5-C)。

A.不同組織(有花組);B.不同組織(無花組);C.花發育不同階段。圖6同。
geNorm通過對配對差異分析(Vn/Vn+1)得出最佳內參基因個數,軟件默認的Vn/Vn+1閾值為0.15,Vn/Vn+1比值小于0.15時,最適內參基因為n個;大于0.15時,最適內參基因為n+1個。對候選內參基因的配對差異值分析發現,在有花組中,Vn/Vn+1值均大于0.15,此時不能依靠閾值(0.15)來決定最適內參基因的個數,評估目的基因在茉莉花不同組織中的表達水平時,選取2~3個穩定性強的內參基因即可(圖6-A);在無花組中,V2/V3=0.087<0.15,說明最適內參基因個數為2(圖6-B);在花發育不同階段,V2/V3=0.126<0.15,說明采用2個內參基因即可(圖6-C)。

圖6 geNorm分析確定候選內參基因數目
2.3.2 NormFinder分析 NormFinder軟件通過方差分析對候選內參基因進行篩選,利用ΔCt法計算候選內參基因表達穩定值(S),從而對內參基因表達的穩定性進行評價,S值越小,基因越穩定。NormFinder分析結果顯示,在有花組中,UPL7(S=0.172)和SAND(S=0.221)表達最穩定,GAPDH(S=0.898)表達最不穩定;在無花組中,UPL7(S=0.037)和GAPDH(S=0.072)表達最穩定,Actin(S=0.201)表達最不穩定;在花發育不同階段,Actin(S=0.036)、PEPKR1(S=0.077)和GAPDH(S=0.077)表達最穩定,PP2A(S=0.350)表達最不穩定;是否有花,對GAPDH的穩定性排名有重要影響(表2)。
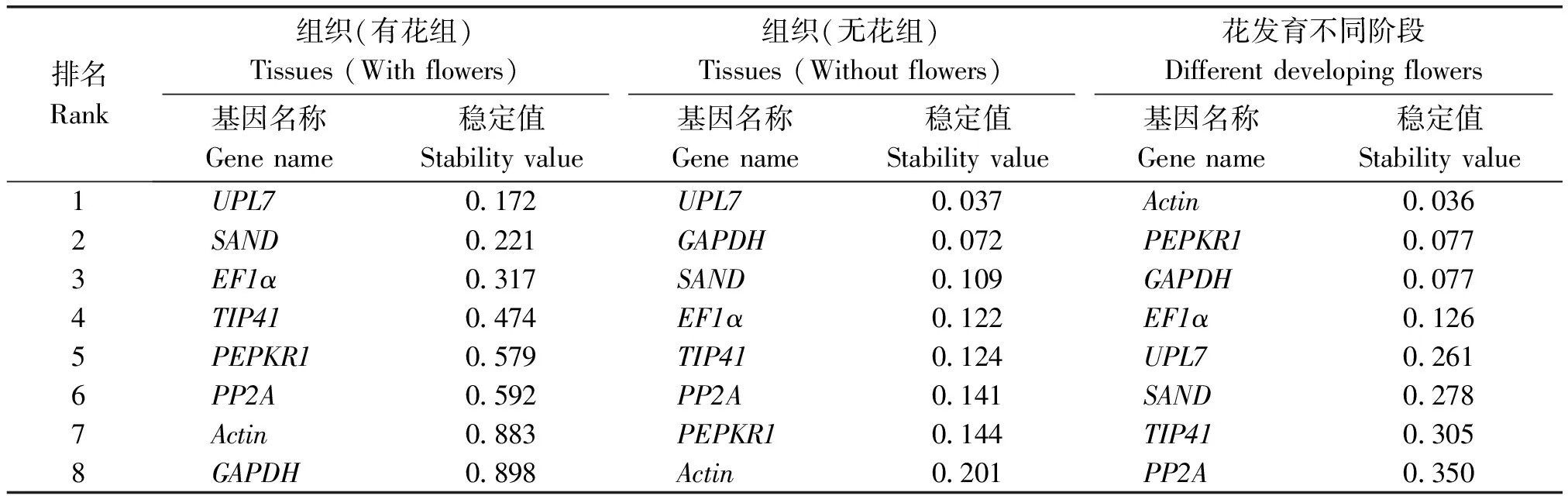
表2 NormFinder分析候選內參基因表達穩定性排名
2.3.3 BestKeeper分析 BestKeeper通過計算不同樣品間候選內參基因Ct值產生配對的變異系數(CV)、標準差(s)的大小來對各內參基因表達的穩定性進行評價。CV和s越小,說明該內參基因的穩定性越好;若s>1,則說明該內參基因表達不穩定。BestKeeper軟件分析結果顯示,在有花組中,Actin(s=0.42)和PEPKR1(s=0.78)s值小于1,說明這2個候選內參基因的表達穩定性較好;在無花組中,8個候選內參基因的s值均小于1,說明各內參基因的表達均為穩定,穩定性由高到低進行排序為:UPL7>SAND>GAPDH>PP2A>TIP41>EF1α>Actin>PEPKR1;在花發育不同階段中,8個內參基因的s值均小于1,說明各基因的表達均為穩定,穩定性由高到低進行排序為:EF1α>Actin>PEPKR1>GAPDH>UPL7>TIP41>SAND>PP2A(表3)。
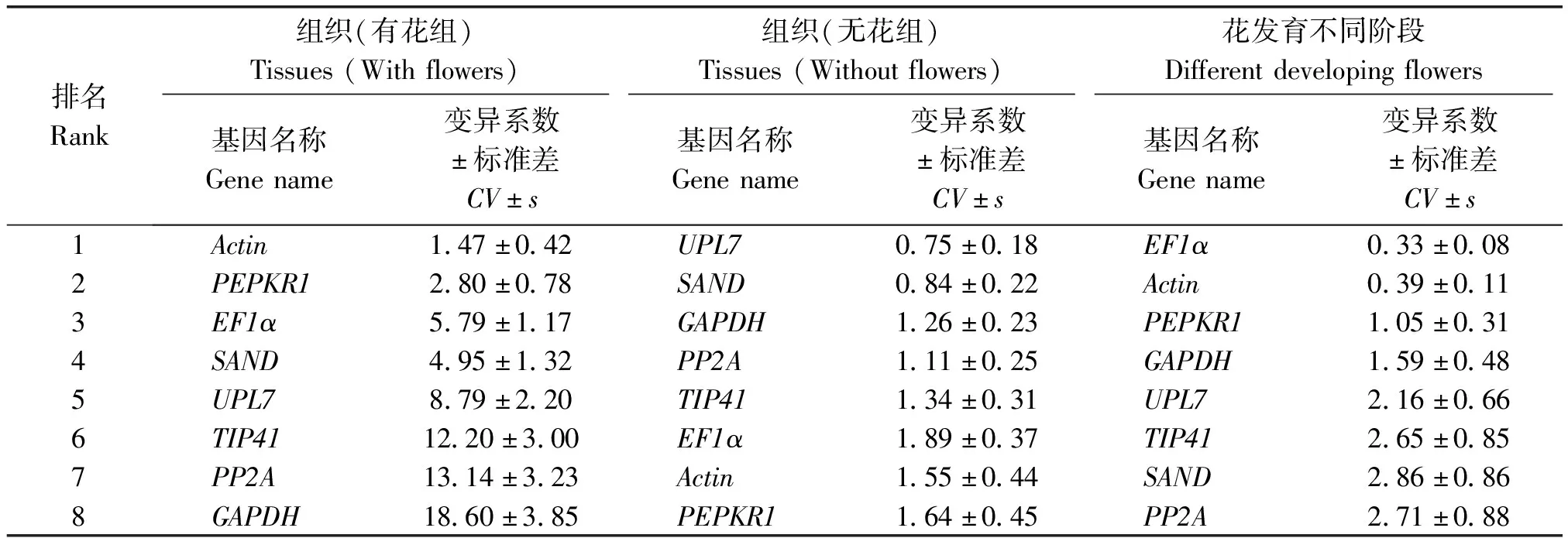
表3 BestKeeper分析候選內參基因表達穩定性排名
2.3.4 RefFinder綜合排名分析 由于各個軟件算法原理不同,3個軟件獲得的最穩定的內參基因排名有差異,最后使用RefFinder對8個候選內參基因穩定性進行綜合分析,幾何平均值越小,其表達穩定性越好。結果顯示,在有花組中,8個候選內參基因中表達的穩定性由高到低依次為:SAND>UPL7>EF1α>PEPKR1>Actin>TIP41>PP2A>GAPDH;在無花組中,內參基因的穩定性由高到低依次為:UPL7>GAPDH>SAND>TIP41>EF1α>PP2A>PEPKR1>Actin;花發育不同階段中內參基因的穩定性由高到低依次為:Actin>EF1α>PEPKR1>GAPDH>SAND>UPL7>TIP41>PP2A(表4)。
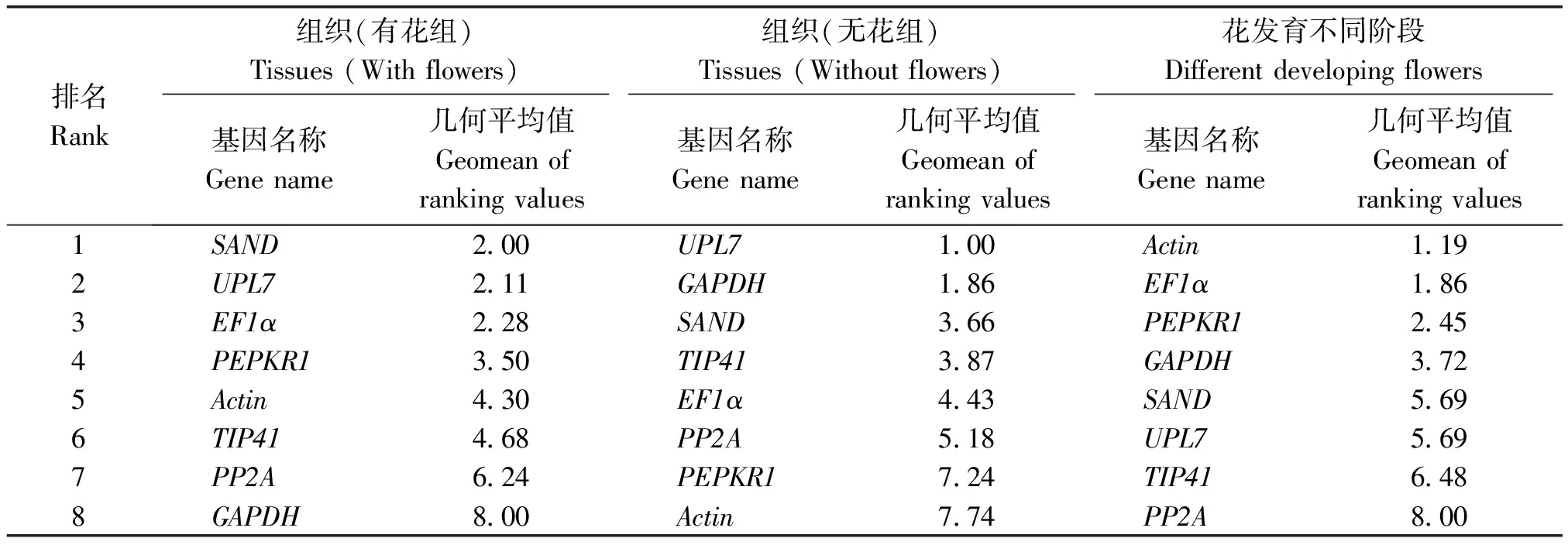
表4 候選內參基因表達穩定性綜合排名
2.4 內參基因表達穩定性驗證
為驗證篩選的內參基因表達穩定性,分別用穩定性排名最高的2個內參基因Actin、EF1α及Actin+EF1α組合,以最不穩定的內參基因PP2A為對照,對花發育不同階段的JsDXS和JsPAL2的表達水平進行分析。結果顯示,以穩定性好的內參基因Actin、EF1α及Actin+EF1α組合為參照時,JsDXS基因在花發育不同階段的表達水平的變化趨勢基本一致,而用最不穩定的內參基因PP2A為參照時,花發育不同階段的表達水平的變化趨勢不一致(圖7-A);同樣,以Actin、EF1α及Actin+EF1α組合為參照時,JsDXS在花發育不同階段的表達水平的變化趨勢基本一致,而用PP2A為參照時,花發育不同階段的表達水平的變化趨勢不一致(圖7-B)。
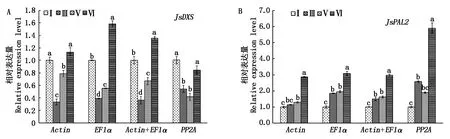
圖7 不同內參基因或組合分析茉莉花花發育不同階段JsDXS和JsPAL2表達水平
3 討論與結論
qRT-PCR是目前在轉錄水平上研究基因表達最為普遍的技術,具有靈敏度高、特異性強、快速高效和重復性好等優點,常用于相對定量分析生物體不同組織間、不同生長發育時期、不同試驗條件下基因表達的變化,而qRT-PCR對目的基因進行表達水平分析的前提是選擇表達穩定的內參基因[4, 24]。試驗中常選擇管家基因作為內參基因,因為這些基因在生物體各組織和不同生長階段表達水平較為穩定。近年來研究發現,這些管家基因在不同植物、組織、生長發育時期及環境下表達的水平并非穩定[25]。如非生物脅迫處理的海濱雀稗草中,內參基因U2AF和GAPDH在鎘處理的葉和冷處理的根中穩定性最好,U2AF和FBOX在鎘處理的根和冷處理的葉中穩定性最好,SAND和CACS在鹽處理的葉中穩定性最好[4];火龍果果實不同發育期樣本中,內參基因YLS8和TBP2穩定性最好[26];在水稻稻瘟病菌的發病機理研究中,Edf和TI是最穩定的內參基因,而常見的管家基因18SrRNA和UBQ5是最不穩定的內參基因[27]。本研究也有類似發現,同一基因在不同組織中穩定性存在較大差異,如GAPDH在不同組織(有花組)中是最不穩定的內參基因,而在不同組織(無花組)中是穩定的內參基因。由此可見,不只在不同物種間內參基因的表達存在差異,即便同一物種,若研究的組織、生長階段和環境等不同,內參基因表達的穩定性也存在差異。因此,做目的基因表達分析之前,必須對具體條件下內參基因表達的穩定性進行篩選及驗證。
geNorm、NormFinder和BestKeeper是目前對內參基因穩定性進行評價中最常用的3種軟件。本研究中,發現3種軟件的內參基因穩定性排名有所不同,其中,茉莉花不同組織(有花組)中,Actin在BestKeeper中的穩定性最好,但是其在geNorm和NormFinder中的穩定性都較差;SAND和UPL7在BestKeeper中的穩定性不好,但其在geNorm和NormFinder中的穩定性都較好。該現象在柑橘(Citrusreticulata)[28]、鳳丹[29]的內參基因的篩選中也有報道,推測可能與計算機內置統計學算法不同有關,geNorm和NormFinder都是利用各內參基因Ct值換算成Q值進行分析,而BestKeeper直接用Ct值進行分析[30]。在實際選用內參基因時,為避免因軟件分析差異帶來的誤差,通常利用幾何平均法對不同軟件得到的結果進行分析得出綜合排名,該排名在一定程度上可以說明各內參基因的穩定性趨勢[9]。本研究利用RefFinder對8個候選內參基因穩定性進行綜合分析,從而篩選出了在不同樣品中表達最為穩定的內參基因。geNorm分析發現,在茉莉花不同組織(有花組)中,Vn/Vn+1值均大于0.15,在榛[31]、梨[32]內參基因的篩選中也發現了類似現象,這可能是由于試驗材料來自不同組織,跨度較大而導致變異系數均大于0.15。
在對目的基因表達水平進行分析時,不僅要求所用內參基因表達穩定,而且要求其表達量與目的基因的表達量相近[33]。本研究中,茉莉花不同組織(無花組)、花發育不同階段最優內參基因中,GAPDH、EF1α表達豐度高,適合作為分析較高表達豐度目的基因時的內參;UPL7、Actin表達豐度低,適合作為分析較低表達豐度目的基因時的內參。本研究發現茉莉花發育不同時期最適內參基因為Actin和EF1α,這與已有研究中常用Actin作為內參基因一致[15, 22, 34],說明Actin基因適合做花的內參基因。利用最適內參基因Actin和EF1α對目的基因JsDXS和JsPAL2的表達水平進行分析,結果進一步說明篩選出來的Actin和EF1α穩定性較好。
總之,本研究對茉莉花的內參基因進行了篩選,不同組織(有花組)的最優內參基因為SAND和UPL7;不同組織(無花組)的最優內參基因為UPL7和GAPDH;花發育不同階段的最優內參基因為Actin和EF1α。本研究結果為茉莉花基因表達分析提供了可選擇的內參基因,為后續基因表達、功能及調控等相關研究奠定了基礎。

