過(guò)渡金屬型錳基低溫NH3-SCR脫硝催化劑研究綜述
馮 晴,曾賢君,張利杰,李 賀,孟廣瑩,孫彥民
(1.中海油天津化工研究設(shè)計(jì)院有限公司,天津300131;2.天津市煉化催化技術(shù)工程中心)
為了滿足工業(yè)日益增長(zhǎng)的能源需求,不可再生的化石燃料仍然是工業(yè)生產(chǎn)、 發(fā)電廠和機(jī)動(dòng)車(chē)輛的主要能源。然而大量化石燃料的燃燒所排放的尾氣中,主要的污染產(chǎn)物為氮氧化物(NO、NO2和N2O 及其衍生物),并因此導(dǎo)致酸雨、光化學(xué)煙霧、臭氧消耗和水資源富營(yíng)養(yǎng)化等一系列問(wèn)題[1-2],減少氮氧化物的排放對(duì)環(huán)境保護(hù)至關(guān)重要。目前高效去除氮氧化合物的方法,是利用催化材料對(duì)氮氧化合物進(jìn)行催化還原轉(zhuǎn)化為氮?dú)狻F渲校琋H3選擇性催化還原NOx(NH3-SCR)的反應(yīng),以其較高的NOx去除率而得到了廣泛的應(yīng)用[3]。通常情況下,工業(yè)煙氣的排放溫度低于300 ℃,因此要求NH3-SCR 催化劑須在低溫下(100~300 ℃)保持良好的催化活性。目前已經(jīng)商業(yè)化的NH3-SCR 催化劑V2O5-WO3(MoO3)/TiO2是 一種典型的中溫NH3-SCR 催化劑[4]。但該類(lèi)催化劑存在著工作溫度窗口窄且溫度高(350~400 ℃)、氮?dú)膺x擇率低等不足。因此,更多的研究人員將研發(fā)方向集中在開(kāi)發(fā)低溫高活、性能穩(wěn)定、成本低、環(huán)境友好的NH3-SCR 催化劑。
目前,根據(jù)低溫脫硝催化劑的活性組分來(lái)分主要有貴金屬催化劑、過(guò)渡金屬催化劑兩大類(lèi)。貴金屬催化劑主要以Pt、Pd、Rh 等[5]貴金屬為活性組分,雖然具有較好的低溫脫硝活性,但N2選擇性較差,且易SO2中毒,再加之成本較高,該類(lèi)催化劑未能在燃煤煙氣等固定源脫硝領(lǐng)域得到廣泛應(yīng)用。相對(duì)而言,過(guò)渡金屬催化劑因選擇性好、轉(zhuǎn)化率高、抗硫抗水性較好[6]、成本低成為目前低溫NH3-SCR 脫硝技術(shù)中研究及應(yīng)用最為廣泛的催化劑類(lèi)型。
過(guò)渡金屬元素的價(jià)層電子軌道大多在d 層和ds層,因d 層電子更易于向NH3和O2轉(zhuǎn)移電子,在低溫下誘導(dǎo)促進(jìn)NH3-SCR 反應(yīng)的進(jìn)行,因而表現(xiàn)出優(yōu)良的氧化還原性能。除此以外,與貴金屬催化劑相比,過(guò)渡金屬元素兼具價(jià)格低和熱穩(wěn)定性高的優(yōu)勢(shì),因此被研究者廣泛地應(yīng)用到低溫NH3-SCR 反應(yīng)中[7]。在早期的實(shí)驗(yàn)中,研究了很多過(guò)渡金屬元素,如Fe、Cu、Mn、Cr、Co、Ni 等[8-9],由于Mn 元素價(jià)態(tài)多變,氧化還原性能優(yōu)良引起研究者廣泛關(guān)注。研究發(fā)現(xiàn)錳系催化劑在低溫段表現(xiàn)出良好的脫硝性能,但是極易被煙氣中的SO2影響導(dǎo)致失活,脫硝率急劇下降且失活過(guò)程大多不可逆,低溫下煙氣中的水蒸氣也會(huì)對(duì)NH3-SCR 催化劑的活性造成影響。因此,對(duì)Mn 基低溫脫硝催化劑進(jìn)行改性,增強(qiáng)其低溫活性、 提高抗硫毒和水抑制能力的新型Mn 基催化劑是近些年研究的重點(diǎn),主要體現(xiàn)在兩方面:一是引入一種或多種過(guò)渡金屬氧化物來(lái)修飾錳基催化劑,形成過(guò)渡金屬?gòu)?fù)合氧化物,通過(guò)元素間誘導(dǎo)協(xié)同作用來(lái)增強(qiáng)反應(yīng)的活性位點(diǎn)[10-11];二是合成復(fù)合載體材料,分散過(guò)渡金屬基氧化物,通過(guò)金屬-載體相互作用提高活性[12-13]。
本文系統(tǒng)地綜述了近幾年國(guó)內(nèi)外低溫NH3-SCR 反應(yīng)中過(guò)渡金屬M(fèi)n 基催化劑的研究進(jìn)展,較為全面地總結(jié)了該系列催化劑Mn 元素及其他過(guò)渡金屬元素在不同組合結(jié)構(gòu)中對(duì)催化劑性能的影響,分析了過(guò)渡金屬M(fèi)n 基催化劑在低溫NH3-SCR 反應(yīng)中的脫硝活性機(jī)理及抗SO2、H2O 的性能機(jī)理。
1 二元過(guò)渡金屬M(fèi)n 基氧化物催化劑
由于Mn 的單一金屬氧化物的比表面積小、熱穩(wěn)定性差,研究者們更多地將Mn 系低溫脫硝催化劑的性能提升放在多金屬組合的氧化物上。最常用的方法是通過(guò)摻雜其他金屬,比如Sn、Cr、Co、Fe、Cu、Ni、Ce 等[14-16]過(guò)渡金屬,改善Mn 單一金屬氧化物,使其具有良好的催化性能而被廣泛用于低溫NH3-SCR 反應(yīng)。
Tang 等[17]采用氧化還原共沉淀法制備出的MnOx-SnO2復(fù)合氧化物具有較高的脫硝活性,可能是由于其含有高價(jià)態(tài)Mn4+或高價(jià)態(tài)Sn4+,實(shí)驗(yàn)結(jié)果證實(shí)Mn 元素不同價(jià)態(tài)的脫硝活性由大到小順序?yàn)椋篗nO2、Mn5O8、Mn2O3、Mn3O4。經(jīng)分析得知,在低溫NH3-SCR 反應(yīng)中,L 酸位是其催化活性高的關(guān)鍵,MnOx-SnO2復(fù)合氧化物中Sn4+比Mn4+表現(xiàn)出更強(qiáng)的L 酸位,因而對(duì)NH3具有更強(qiáng)的吸附作用。當(dāng)NH3吸附在Sn4+上,更易與MnOx中的晶格氧反應(yīng)生成氨氧基中間產(chǎn)物,經(jīng)過(guò)Eley-Rideal 途徑最終生成N2和H2O,因而極大提高了催化活性。Chen 等[18]研制出一種CrMn1.5O4尖晶石相的復(fù)合氧化物,使其在低溫120 ℃脫硝轉(zhuǎn)化率可達(dá)98%以上,顯著降低了NH3-SCR反應(yīng)的還原溫度。在抗硫性實(shí)驗(yàn)中,SO2通入后催化劑活性有所降低,但停止通SO2后脫硝活性迅速恢復(fù),表現(xiàn)出優(yōu)異的抗硫可逆性,主要是由于CrMn1.5O4尖晶石相形成了Cr-Mn 高氧化還原電位對(duì),促進(jìn)了Cr與Mn 之間的電子傳遞,從而加速了催化劑活性的恢復(fù),對(duì)SO2導(dǎo)致的催化劑失活能有效再生。
Zhang 等[19]通過(guò)金屬和有機(jī)溶劑合成了立方狀空心MnxCo3-xO4納米顆粒催化劑,見(jiàn)圖1。在150~300 ℃的NH3-SCR 反應(yīng)中,通過(guò)對(duì)比分析金屬比例相同的空心MnxCo3-xO4納米顆粒和實(shí)心納米顆粒,發(fā)現(xiàn)空心納米顆粒的脫硝活性為100%且呈現(xiàn)出更高的N2選擇性。在175 ℃時(shí),同時(shí)通入H2O 和SO2,空心納米顆粒的性能均優(yōu)于實(shí)心納米顆粒,且在抗硫性測(cè)試中,空心納米顆粒在停止通入SO2后,幾乎恢復(fù)到原來(lái)的脫硝活性。究其原因,空心MnxCo3-xO4納米顆粒具有較好的低溫脫硝活性和抗硫性能,歸因于催化劑的空心結(jié)構(gòu)及有層次的多孔結(jié)構(gòu),為反應(yīng)氣體的吸附和活化提供了更大的比表面積和更多的活性中心,同時(shí),Co 和Mn 離子之間的協(xié)同作用能夠抑制催化劑表面硫酸鹽的形成。

圖1 利用Mn3[Co(CN)6]2·nH2O 納米前驅(qū)體合成中空結(jié)構(gòu)的MnxCo3-xO4 納米顆粒[19]
Li 等[20]在Mn2O3中摻雜Fe2O3制備出尖晶石晶相的均勻六角微片結(jié)構(gòu)催化劑。此種Fe2O3-Mn2O3催化劑表現(xiàn)出很好的脫硝活性,在200 ℃時(shí)NO 轉(zhuǎn)化率高達(dá)98%,H2O 對(duì)其影響為可逆抑制。此外,在抗硫性測(cè)試中,脫硝活性僅下降了10%,停止通入SO2氣體后NO 轉(zhuǎn)化率最終恢復(fù)到90%以上。分析發(fā)現(xiàn),Mn 元素嵌入Fe2O3的六方晶格中,在內(nèi)部結(jié)構(gòu)中Mn和Fe 兩種離子之間形成協(xié)同作用,Mn 的摻雜不僅產(chǎn)生了更多的化學(xué)吸附氧,見(jiàn)圖2a,還能提高整個(gè)氧化還原循環(huán)中活性金屬離子的含量,從而增強(qiáng)脫硝的催化能力。此外,由圖2b 可看出,F(xiàn)e2O3中摻雜微量Mn2O3形成的復(fù)合晶體結(jié)構(gòu),尺寸均勻、表面光滑,不利于硫酸鹽附著,也是增強(qiáng)其抗硫性的重要原因。Fang 等[21]利用浸漬法制備出尖晶石相的CuMn2O4催化劑,在180 ℃時(shí)脫硝活性接近100%,也是由于尖晶石內(nèi)部Cu-Mn 離子之間強(qiáng)烈的協(xié)同作用,有利于內(nèi)部電子轉(zhuǎn)移,從而增強(qiáng)脫硝催化活性。

圖2 NH3 與NO 在Mn(0.2)-FeOx 六方晶片上的反應(yīng)機(jī)理(a)及Mn(0.2)-FeOx 六方晶片的SEM 圖(b)[20]
Han 等[22]采用溶劑熱法制備出獨(dú)特的NiMn2O4三殼空心球,由于其特殊的3 層殼結(jié)構(gòu),所制備的NiMn2O4催化劑表現(xiàn)出優(yōu)越的低溫脫硝活性,在較寬的脫硝溫度100~225 ℃范圍內(nèi)氮氧化合物去除率達(dá)到90%以上。分析其原因是由于三層空心殼結(jié)構(gòu)使其具有極高的比表面積,從而提供了更多的Mn4+活性位點(diǎn)。在抗水性和耐硫性檢測(cè)中,水對(duì)NiMn2O4催化劑的活性影響較小且為可逆過(guò)程,但通入SO2后催化劑的活性下降較明顯,停氣后活性雖然會(huì)上升,但不能完全恢復(fù)至最初狀態(tài)。
Gao 等[23]采用檸檬酸法制備出微介孔尖晶石相CrMn2O4催化劑,在100~225 ℃脫硝轉(zhuǎn)化率接近100%,200 ℃的抗硫抗水實(shí)驗(yàn)中,20 h 脫硝轉(zhuǎn)化率為72%±3%。CrMn2O4催化劑優(yōu)異的脫硝活性得益于微介孔尖晶石結(jié)構(gòu)產(chǎn)生了更大的比表面積,增加了Mn3+/Mn4+的活性位點(diǎn),加快Cr5++2Mn3+?Cr3++2Mn4+之間的電子傳遞,進(jìn)而提高脫硝活性。他們認(rèn)為微介孔尖晶石相CrMn2O4催化劑具有耐硫性的原因,一方面是Cr3+對(duì)Mn 起到一定的保護(hù)作用,另一方面催化劑表面生成的-HSO3和SO42-向H…SO42-的轉(zhuǎn)變過(guò)程中,產(chǎn)生了新的B 酸性位點(diǎn),引發(fā)NO2與NH4+快速反應(yīng)生成NH4NO2,分解為N2和H2O,進(jìn)而增強(qiáng)催化劑在SO2中的脫硝活性。
二元過(guò)渡金屬氧化物在增強(qiáng)脫硝催化活性方面,一是可以轉(zhuǎn)化為尖晶石結(jié)構(gòu),誘導(dǎo)加強(qiáng)過(guò)渡金屬離子與Mn 之間的協(xié)同作用,促進(jìn)電子轉(zhuǎn)移,提高催化劑再生活性; 二是通過(guò)改變復(fù)合氧化物的結(jié)構(gòu)形貌,增大比表面積,可以增加活性位點(diǎn),進(jìn)而提高脫硝轉(zhuǎn)化率。
2 多元過(guò)渡金屬M(fèi)n 基氧化物催化劑
在Mn 基兩種金屬氧化物的基礎(chǔ)上繼續(xù)改進(jìn),可以引入其他過(guò)渡金屬元素形成多元過(guò)渡金屬M(fèi)n基復(fù)合氧化物而加強(qiáng)各項(xiàng)性能。如表1 所示,通過(guò)引入多種過(guò)渡金屬進(jìn)而產(chǎn)生更多的化學(xué)吸附氧,加強(qiáng)活性元素之間的電子傳遞,來(lái)提高脫硝活性和抗硫抗水性引發(fā)新的反應(yīng)機(jī)理[24-31]。
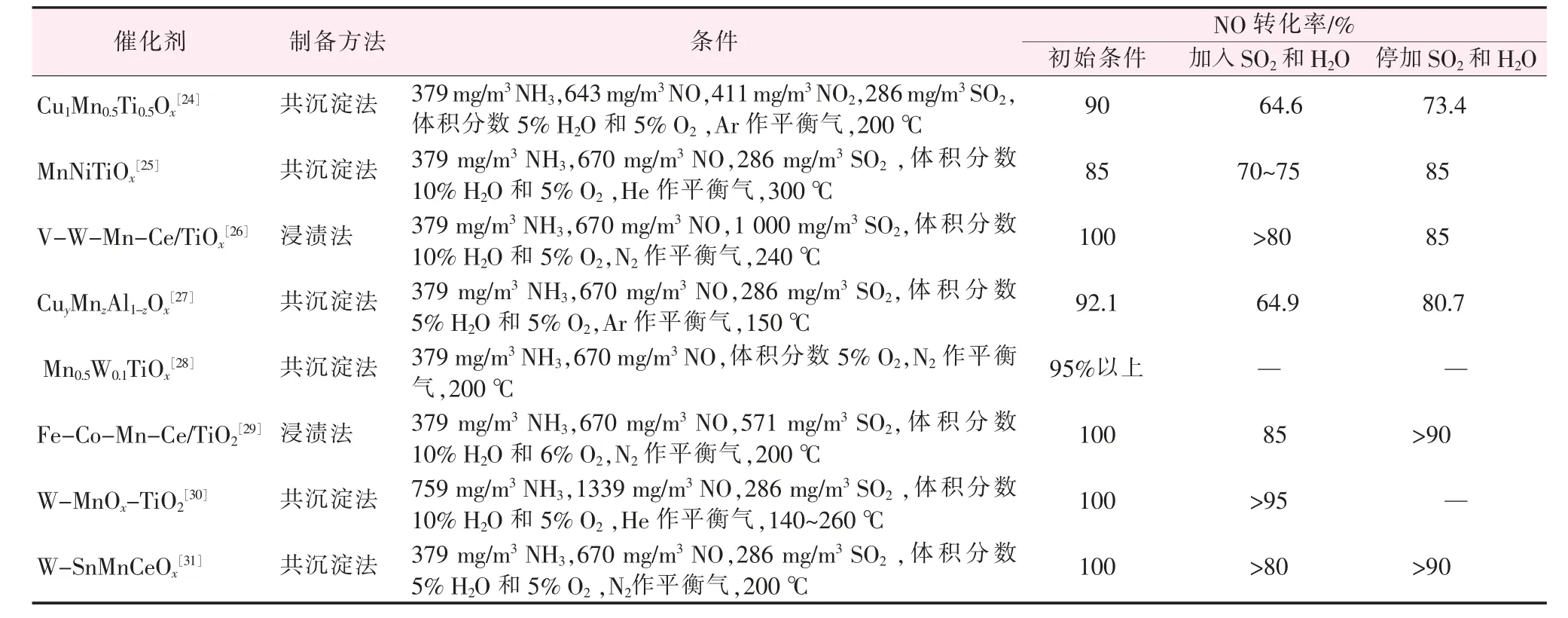
表1 引入多種過(guò)渡金屬對(duì)催化劑脫硝活性和抗硫抗水性的影響
France 等[32]以混合金屬鹽溶液蒸干制備的Ce-Fe-MnOx復(fù)合氧化物,在NH3-SCR 反應(yīng)中可形成穩(wěn)定的化學(xué)吸附態(tài)的氮物種,從而抑制了硫酸鹽的形成,提高了抗硫性能。Liu 等[33]利用水熱法制備的Mn0.2Ce0.1Ti0.7Ox復(fù) 合 氧 化 物,在150 ~350 ℃的NH3-SCR 反應(yīng)中,脫硝活性超過(guò)90%,N2的選擇性在此溫度范圍內(nèi)達(dá)到100%,在通入H2O 和SO2之后,脫硝活性依然在90%以上,停止H2O 和SO2進(jìn)氣后,脫硝活性基本完全恢復(fù)。這是由于Mn0.2Ce0.1Ti0.7Ox復(fù)合氧化物中含有高比例的Ce3+和Ti3+,在催化劑表面會(huì)產(chǎn)生更多的化學(xué)吸附氧,促進(jìn)了氣相氧的吸附和活化,同時(shí)復(fù)合氧化物中的Mn4+有利于在催化劑上形成NH4+從而增強(qiáng)催化劑的脫硝活性。
Gao 等[34]以碳酸銨為沉淀劑,將Cu、Co、Cr、Ni、Fe、Sn、Mg 元 素 與Mn、Ce 元 素 進(jìn) 行 共 沉 淀 制 備M1Mn4Ce5Ox(M=Cu、Co、Cr、Ni、Fe、Sn、Mg),在進(jìn)料相同、摻雜不同金屬催化劑的脫硝實(shí)驗(yàn)中,Co、Ni 摻雜的催化劑活性最高。分析發(fā)現(xiàn),Co、Ni 摻雜的催化劑具有更高的比表面積、更多的化學(xué)吸附氧和活性中心而且活性位點(diǎn)中n(Ce4+)/n(Ce3+)更高,因此使其具有更高的脫硝性能;在抗硫性能上,經(jīng)Co1Mn4Ce5Ox和Ni1Mn4Ce5Ox上吸收NOx,首先形成的是不受SO2影響的雙齒硝酸鹽,進(jìn)而轉(zhuǎn)化為單齒硝酸鹽,產(chǎn)生新的B 酸位再生成NH4+,因此具有良好的抗硫性。
Fang 等[35]利用共沉淀法制備出Fe0.3Mn0.5Zr0.2Ox復(fù)合氧化物,在200~360 ℃時(shí)NO 脫除率能達(dá)到100%且保持80 h;在200 ℃通入SO2時(shí),催化劑的脫硝活性為98%保持了24 h;當(dāng)SO2增加一倍時(shí),脫硝活性為95%保持了25 h,由此可見(jiàn)催化劑有非常強(qiáng)的抗SO2能力。據(jù)其分析,非晶態(tài)的MnO2和Fe2O3均起到表面活性位點(diǎn)的作用,而載體ZrO2和活性組分可通過(guò)Fe、Mn 和Zr 之間的協(xié)同作用加快電子轉(zhuǎn)移,F(xiàn)e 與Mn 之間較強(qiáng)的相互作用促使部分電子更傾向于從Fe 向Mn 的轉(zhuǎn)移,產(chǎn)生的高氧化態(tài)的Mn更容易被還原。低溫時(shí)價(jià)態(tài)較低的Mn 很容易將電子轉(zhuǎn)移到吸收的O2上,這導(dǎo)致表面晶格氧(O)的儲(chǔ)存和遷移增加,F(xiàn)e、Mn 和Zr 之間通過(guò)協(xié)同作用不僅提高了脫硝活性,而且使SO2不易在催化劑表面轉(zhuǎn)化成硫酸鹽沉積[36]。
Yao 等[37]采用一步共沉淀法合成CeO2-MnOx-Al2O3復(fù)合氧化物。結(jié)果顯示,在CeO2-MnOx混合氧化物中加入少量的Al 元素,有助于減小復(fù)合氧化物的晶粒尺寸增大其比表面積,繼而增加了作為活性中心的Ce3+和Mn4+的總數(shù)量。Lee 等[38]采用浸漬法制備出不同n(Ce)/n(Mn)的Ce/Mn-TiO2催化劑,Ce/Mn-TiO2催化劑與Mn-TiO2相比脫硝活性明顯提升,這是由于催化劑僅為Mn-TiO2兩種組分時(shí),部分MnO2顆粒易進(jìn)入到TiO2的孔道內(nèi),而無(wú)法發(fā)揮表面催化氧化的作用,不利于NH3-SCR 反應(yīng)的進(jìn)行;當(dāng)摻雜適量CeO2之后,由于CeO2遮擋住了TiO2的孔道,導(dǎo)致MnO2無(wú)法進(jìn)入孔道而均勻分散在TiO2的表面,增強(qiáng)了表面催化氧化活性;但CeO2的添加過(guò)量時(shí),金屬氧化物之間發(fā)生強(qiáng)烈的相互作用,導(dǎo)致MnO2聚集結(jié)塊不能均勻分布在TiO2的表面,使其催化活性降低。
多元過(guò)渡金屬摻雜的復(fù)合氧化物,在增強(qiáng)脫硝活性方面,主要依據(jù)金屬離子之間的協(xié)同作用,加快不同元素之間電子的轉(zhuǎn)移,從而產(chǎn)生更多的金屬活性中心和表面晶格氧,加快NH3-SCR 反應(yīng)的進(jìn)行。此外,多金屬之間的強(qiáng)協(xié)同作用,還能有效抑制SO2在催化劑表面產(chǎn)生沉積硫酸鹽,增強(qiáng)其抗硫性能。
3 負(fù)載型多元過(guò)渡金屬M(fèi)n 基催化劑
對(duì)于依賴表面催化氧化的NH3-SCR 反應(yīng),催化劑的比表面積的大小決定了活性位點(diǎn)的多少,研究者為改善過(guò)渡金屬氧化物本身比表面積小的問(wèn)題,引入了比表面積大的載體,合成負(fù)載型過(guò)渡金屬催化劑。由于活性組分在載體表面具有良好的分散性,以及活性組分與載體之間的協(xié)同作用,使得載體催化劑的性能優(yōu)于未加載體的過(guò)渡金屬氧化物。因此,通過(guò)將過(guò)渡金屬氧化物分散在不同的載體材料上以增強(qiáng)脫硝性,獲得越來(lái)越高的關(guān)注度。目前,常見(jiàn)載體有Al2O3、TiO2、SiO2、分子篩和納米管材料等。
3.1 以Al2O3 為載體
Wang 等[39]配制金屬混合鹽溶液,通過(guò)噴霧干燥法制備MnO2-CeO2-Al2O3,由于噴霧干燥過(guò)程中水快速蒸發(fā),球形顆粒分布著大量的塌陷孔隙,比表面積增大,活性元素分散均勻,反應(yīng)活性增強(qiáng),在150 ℃下脫硝轉(zhuǎn)化率為97.4%,氮?dú)獾倪x擇性為94.5%。Smirniotis 等[40]研究了包含Al2O3在內(nèi)的不同載體負(fù)載過(guò)渡金屬催化劑,在低溫NH3-SCR 反應(yīng)中Mn/銳鈦 礦TiO2活 性>Mn/金 紅 石TiO2活 性>Mn/γ-Al2O3活性>Mn/SiO2活性,經(jīng)過(guò)表征分析,載體對(duì)催化劑表面的Lewis 酸性位及其Mn4+的表面濃度的影響,對(duì)提升低溫脫硝反應(yīng)性能有重要意義。Schill 等[41]采用浸漬法和共沉淀法分別制備Mn0.75-Fe0.25/Al2O3和Mn0.75-Fe0.25/TiO2兩種催化劑,并進(jìn)行性能的對(duì)比。研究發(fā)現(xiàn),共沉淀法制備的兩種催化劑脫硝活性均高于浸漬法,共沉淀法所制備催化劑的活性在180 ℃時(shí)與工業(yè)催化劑在220 ℃的活性基本一致。此外,陳煥章等[42]采用共沉淀法制備的Mn-Fe/γ-Al2O3催化劑,γ-Al2O3載體介孔結(jié)構(gòu)豐富,比表面積大,活性組分MnOx、FeOx以無(wú)定形結(jié)構(gòu)高度分散于載體的內(nèi)外表面,所形成的催化劑具有良好的低溫活性。孟劉邦等[43]以分步共混法制備Mn-Ce/TiO2、Mn-Ce/SiO2及Mn-Ce/Al2O33 種均質(zhì)整體式催化劑,3 種催化劑比表面積從大到小依次為Mn-Ce/TiO2、Mn-Ce/SiO2、Mn-Ce/Al2O3,表面上酸量從大到小依次為Mn-Ce/TiO2、Mn-Ce/SiO2、Mn-Ce/Al2O3,在低溫80~100 ℃時(shí)Mn-Ce/TiO2和Mn-Ce/SiO2的脫硝活性均大于Mn-Ce/Al2O3,但N2選擇性Mn-Ce/TiO2大于Mn-Ce/SiO2,可見(jiàn),載體的比表面積和表面酸量大小是影響脫硝活性的關(guān)鍵因素。
3.2 以TiO2 為載體
Pena 等[44]嘗試?yán)枚喾N過(guò)渡金屬元素(V、Cr、Mn、Fe、Co、Ni 和Cu) 分別負(fù)載在TiO2上用于低溫脫硝反應(yīng),其中Mn/TiO2催化劑脫硝活性最高、抗水性最強(qiáng)。劉納等[45]以氧化沉淀-浸漬法制備Fe-Mn/TiO2催化劑,F(xiàn)e 元素的摻入能有效改善Mn-TiO2的微觀結(jié)構(gòu),降低團(tuán)聚,增大比表面積,更利于氣體的吸脫附。Liu 等[46]采用溶膠凝膠法制備的Mn/TiO2和Mn-Eu/TiO2催化劑具有高脫硝活性。在對(duì)Mn/TiO2和Mn-Eu/TiO2催化劑的硫化實(shí)驗(yàn)中發(fā)現(xiàn),在SO2存在下Mn-Eu/TiO2催化劑上的NH3-SCR 過(guò)程是通過(guò)Langmuir-Hinshelwood 途 徑 進(jìn) 行,Mn-Eu/TiO2催 化劑能有效抑制表面硫酸鹽的生成。Xu 等[47]采用浸漬法制備的Ce-Mn/TiO2催化劑以不同負(fù)載量的Ce 元素為考察對(duì)象。180 ℃下Ce(20)-Mn/TiO2脫硝率為99.7%,通入SO2的5 h 后,Ce(20)-Mn/TiO2的脫硝率仍維持在94%,在停止通入SO2后,催化劑能快速恢復(fù)到之前的活性。催化劑表面廣泛分布的Mn 和Ce元素使硫酸鹽無(wú)法沉積在催化劑表面,是其具有良好抗硫性的重要因素。此外,Xu 等[48]還將Fe 元素以浸漬法負(fù)載在Ce-Mn/TiO2催化劑上,100 ℃時(shí)其脫硝率為96%,120~160 ℃脫硝率達(dá)到100%,F(xiàn)e 元素的加入極大地降低了NH3-SCR 的反應(yīng)溫度。Xu 等[49]以含TiO2高爐渣為載體采用浸漬法制備了一系列MnOx-CeO2/TiO2催化劑,結(jié)果顯示,元素Mn、Ce 和含TiO2的高爐渣之間存在強(qiáng)烈的相互作用,使活性組分以非晶態(tài)形式分散在表面,使其比表面積增大,孔容孔徑適中。同時(shí),Ce 元素?fù)饺胧惯€原峰向低溫偏移,降低脫硝溫度,Mn 元素增加了強(qiáng)酸位點(diǎn)的數(shù)量,增強(qiáng)了氧化還原能力,由于高爐渣本身的結(jié)構(gòu)特性,能有效阻斷H2O 對(duì)活性的影響,增強(qiáng)了抗水性。
3.3 以分子篩為載體
分子篩的種類(lèi)繁多,是目前催化劑中常用的一種多孔材料。Li 等[50]以粉煤灰衍生的SBA-15 分子篩為載體,采用水熱-浸漬兩步法制備了Fe/Mn-SBA-15 催化劑。結(jié)果顯示,兩種金屬?gòu)?fù)合負(fù)載的催化劑脫硝活性明顯高于單一金屬負(fù)載的催化劑。200~250 ℃時(shí)Fe/Mn-SBA-15 催化劑脫硝轉(zhuǎn)化率超過(guò)90%,其高活性的原因是Fe 和Mn 離子之間形成協(xié)同作用加快電子轉(zhuǎn)移形成新的金屬活性中心,且在催化劑表面形成的硝酸雙齒配合物可以轉(zhuǎn)化成新的酸性中心,從而提高氮氧化合物的脫除率。黃增斌等[51]采用浸漬法以β、ZSM-5 和USY 分子篩為載體制備了Mn-Ce 負(fù)載型催化劑。低溫下3 種負(fù)載型催化劑中Mn-Ce/USY 的脫硝活性最為優(yōu)異。一方面原因是催化劑表面弱酸對(duì)低溫NH3-SCR 反應(yīng)起主要作用,弱酸量從大到小順序?yàn)镸n-Ce/USY、Mn-Ce/β、Mn-Ce/ZSM-5;另一方面由于Mn-Ce/USY 催化劑表面n(Mn4+)/n(Mn3+)最大,且吸附氧表面濃度也最高,因而該催化劑具有最高的低溫脫硝活性。Zhou 等[52]通 過(guò) 溶 液 浸 漬 法 制 備Fe-Ce-Mn/ZSM-5脫硝催化劑,在200 ℃時(shí)脫硝活性達(dá)到96%以上,增加浸漬液中錳元素的含量,催化劑的低溫脫硝活性有明顯提升。從紅外實(shí)驗(yàn)中可知Mn 元素的引入增加了催化劑表面的B 酸位,有利于反應(yīng)中NH3的吸附,添加Fe、Ce 元素可提高表面晶格氧,促進(jìn)Mn2O3向MnO2轉(zhuǎn)化,兩者協(xié)同促進(jìn)低溫下NH3的氧化。通過(guò)紅外實(shí)驗(yàn)結(jié)果提出來(lái)兩種可能的反應(yīng)途徑: 一種是NO2在B 酸位上與NH4+反應(yīng)形成NO2[NH4+]2再與NO 反應(yīng)生成N2和H2O; 另一種是吸附的NH3與NO/HNO2反應(yīng)生成不穩(wěn)定中間體NH4NO2和NH2NO,分解為N2和H2O。
3.4 以其他材質(zhì)納米管為載體
Boningari 等[53]采用水熱法和浸漬法合成了一系列過(guò)渡金屬氧化物負(fù)載的二氧化鈦納米管M/TNT(M=Mn、Cu、Ce、Fe、V、Cr 和Co)催化劑。Mn/TNT催化劑對(duì)NO 有著非常好的低溫脫硝活性,在100~250 ℃脫硝率均能達(dá)到100%。與傳統(tǒng)TiO2負(fù)載Mn相比,Mn/TNT 催化劑具有更高的脫硝活性,主要是由于其表面分布著豐富的Mn4+有利于低溫脫硝反應(yīng)的發(fā)生。Zhang 等[54]采用改性浸漬法在碳納米管(CNT)負(fù)載的MnOx和CeOx納米顆粒(NPS)上涂覆介孔TiO2層,獲得了具有高催化活性的核-殼結(jié)構(gòu)催化劑。一方面多孔結(jié)構(gòu)的特性為吸附反應(yīng)提供了更大的比表面積,增加了活性位點(diǎn),提高脫硝活性,同時(shí)具有介孔結(jié)構(gòu)的TiO2膜作為一個(gè)天然的屏障,能有效抑制金屬氧化物的聚集,增強(qiáng)其熱穩(wěn)定性;另一方面MnOx、CeOx、氧化鈦涂層和CNT 之間的相互作用不僅避免了硫酸銨鹽在表面的沉積,而且抑制催化劑活性位點(diǎn)產(chǎn)生硫酸錳,從而增強(qiáng)了抗硫性。Lee 等[55]采用共沉淀法將Mn 和Fe 元素分別負(fù)載在TNT 和TiO2粉末上,對(duì)比兩者的性能發(fā)現(xiàn)Fe-Mn/TNT 的抗硫性明顯優(yōu)于Fe-Mn/TiO2的主要原因是n(Mn4+)/n(Mn3+)高及比表面積大,此外,TiO2的晶相和金屬顆粒在TNT 上的良好分散增加了催化劑表面B 酸位的數(shù)量,有利于NH3的吸附及后續(xù)氧化反應(yīng)的發(fā)生。
4 結(jié)束語(yǔ)
目前,以NH3為還原劑的NH3-SCR 低溫脫硝技術(shù)中,錳基催化劑因其低溫高效的特點(diǎn),適用于低塵低硫的環(huán)境。但由于反應(yīng)溫度窗口的降低,煙氣中SO2轉(zhuǎn)化的硫酸鹽不易分解,且與Mn 活性位點(diǎn)結(jié)合后失活不可逆,是當(dāng)前錳基低溫脫硝催化劑技術(shù)的一個(gè)瓶頸。本文通過(guò)對(duì)過(guò)渡金屬錳基催化劑進(jìn)行綜述,分析不同過(guò)渡金屬元素助劑對(duì)錳基低溫脫硝催化劑的結(jié)構(gòu)、脫硝活性及抗硫性能的影響,得出未來(lái)低溫脫硝催化劑的研究方向主要為: 對(duì)于過(guò)渡金屬?gòu)?fù)合氧化物可轉(zhuǎn)化成規(guī)則的晶型結(jié)構(gòu),誘導(dǎo)加強(qiáng)過(guò)渡金屬離子與Mn 之間的協(xié)同作用促進(jìn)電子轉(zhuǎn)移增加表面晶格氧,抑制硫酸鹽沉積,提高低溫下催化劑抗硫再生活性;另一方面可以通過(guò)調(diào)整制備工藝,改變催化劑結(jié)構(gòu)形貌和酸位,增大比表面積,增加活性位點(diǎn)數(shù)且使其呈高度分散,進(jìn)而增強(qiáng)低溫脫硝活性;再者可以通過(guò)摻雜更多新的助劑引發(fā)新的脫硝機(jī)理。盡管催化劑在抗硫抗水方面取得了顯著進(jìn)展,但在低溫環(huán)境、SO2和H2O 同時(shí)存在下,大多數(shù)過(guò)渡金屬基催化劑的抗硫抗水性較低,耐久性仍有待提高,SO2和H2O 的抑制機(jī)理尚不清楚。因此,研究人員應(yīng)不斷探索過(guò)渡金屬基混合氧化物和活性過(guò)渡金屬/金屬?gòu)?fù)合載體的不同組合,以待開(kāi)發(fā)出更好的低溫NH3-SCR 抗硫抗水的催化劑。

