妊娠晚期孕婦D-二聚體水平異常升高的因素分析*
李昀暉,徐 暢,張 文,王秋實
中國醫科大學附屬盛京醫院:1.檢驗科;2.輸血科,遼寧沈陽 110000
妊娠是一個特殊的生理過程,隨著孕周的進展和胎兒的生長發育,孕婦體內凝血、抗凝及纖溶系統等均存在不同程度的改變。D-二聚體是纖維蛋白單體活化交聯后,經纖溶酶水解的產物,可作為判斷體內高凝狀態和血栓形成的重要標志物之一[1-2],D-二聚體水平異常升高反映了繼發性纖溶亢進。為了維持妊娠期凝血與纖溶系統的動態平衡,機體纖溶活性增加,使孕婦D-二聚體水平高于非孕女性,且隨著孕周的進展逐漸升高[1]。目前臨床應用的D-二聚體參考區間是根據健康人群建立的,若以此判斷孕婦凝血狀態,有可能將處于生理狀況的孕婦歸于病理性妊娠,不利于臨床的判斷和醫療成本的節約[3]。本研究檢測妊娠晚期孕婦D-二聚體水平,探討引起D-二聚體水平異常升高的生理性及病理性因素,現報道如下。
1 資料與方法
1.1一般資料 連續納入2019年1-3月于中國醫科大學附屬盛京醫院產科住院并分娩的妊娠晚期孕婦457例。納入標準:(1)孕周≥28周;(2)分娩信息完整。排除標準:(1)有嚴重肝、腎系統疾病;(2)不愿 配合本研究。根據檢驗項目參考區間制訂的相關要求[4],以納入人群中健康孕婦第95%位點的D-二聚體的水平作為最佳臨界值,>此水平的為異常升高組,≤此水平的為對照組。健康孕婦納入標準:(1)1周內未服用影響凝血功能的抗凝藥物或抗血小板藥物;(2)無獲得性或先天性凝血障礙病史;(3)無肝、腎系統疾病;(4)無妊娠相關疾病;(5)無產后出血、新生兒疾病等不良妊娠結局;(6)自然受孕并分娩。排除標準:不愿配合本研究。所有納入的研究對象均經本院倫理委員會批準。
1.2方法
1.2.1標本采集 用含0.2 mL的枸櫞酸鈉真空抗凝管采集靜脈血1.8 mL混勻,3 000×g離心10 min,分離出的血漿采用濁度法用于D-二聚體水平的檢測。
1.2.2觀察指標 收集孕婦生理性及病理性資料,生理性資料包括孕周、孕齡、體質量指數(BMI)、孕產次等。病理性資料包括是否患有妊娠期糖尿病、妊娠期高血壓、前置胎盤(包括邊緣性前置胎盤、中央性前置胎盤、兇險性前置胎盤)、復發性流產史、羊水過少等,同時收集纖維蛋白原(FIB)、膽固醇、三酰甘油、血小板等指標。
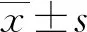
2 結 果
2.12組一般資料統計 連續納入457例孕婦為研究對象,其中健康妊娠晚期孕婦共163例,第95%位點D-二聚體的水平為1 319 μg/L。以D-二聚體水平>1 319 μg/L為異常升高組(60例),D-二聚體≤1 319 μg/L為對照組(397例)。
2.22組D-二聚體影響因素的比較 與對照組比較,異常升高組妊娠期高血壓、雙胎妊娠、體外受精-胚胎移植術后、復發性流產史的發生率及三酰甘油的水平升高;FIB的水平降低,差異均有統計學意義(P<0.05)。見表1。
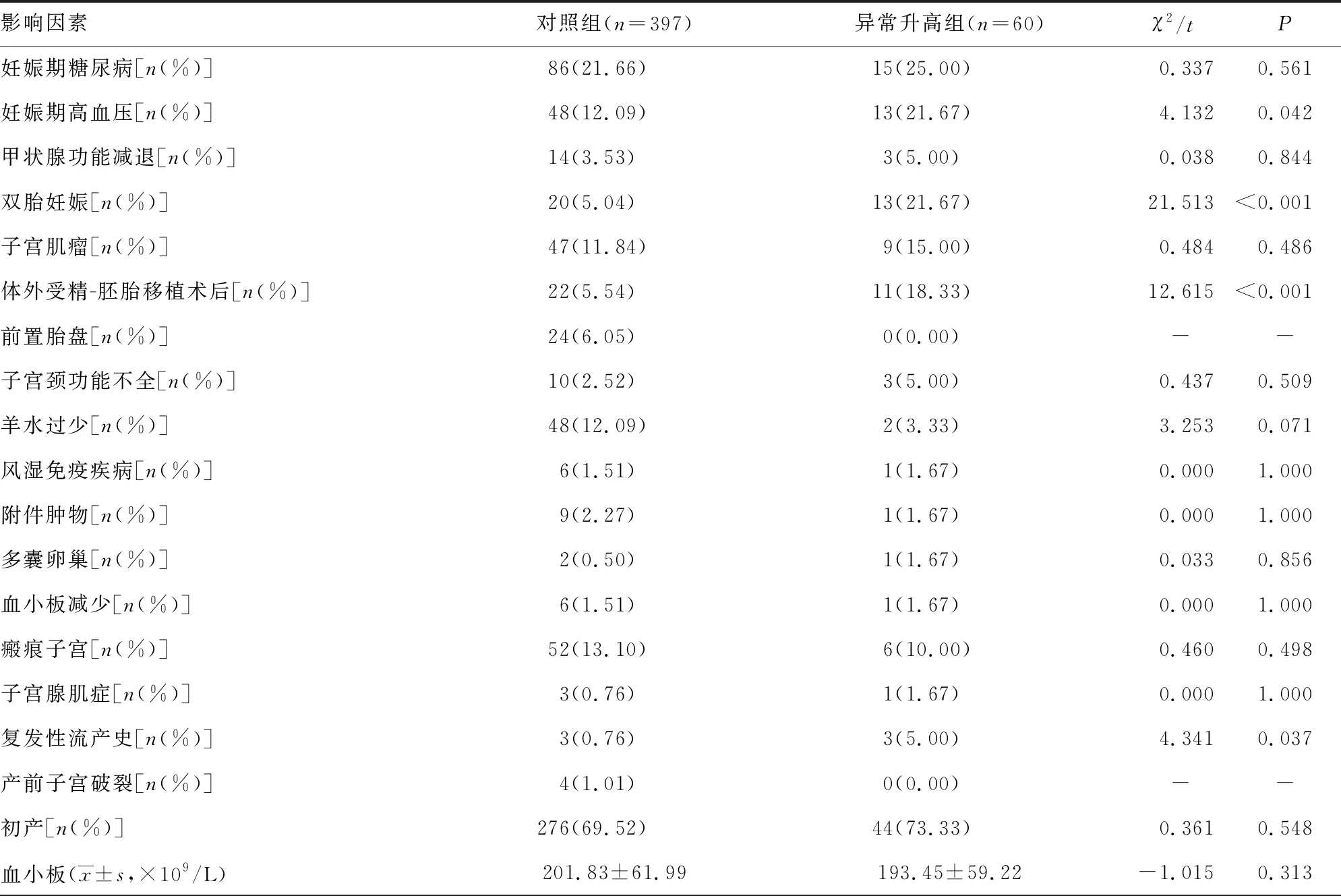
表1 2組D-二聚體影響因素比較
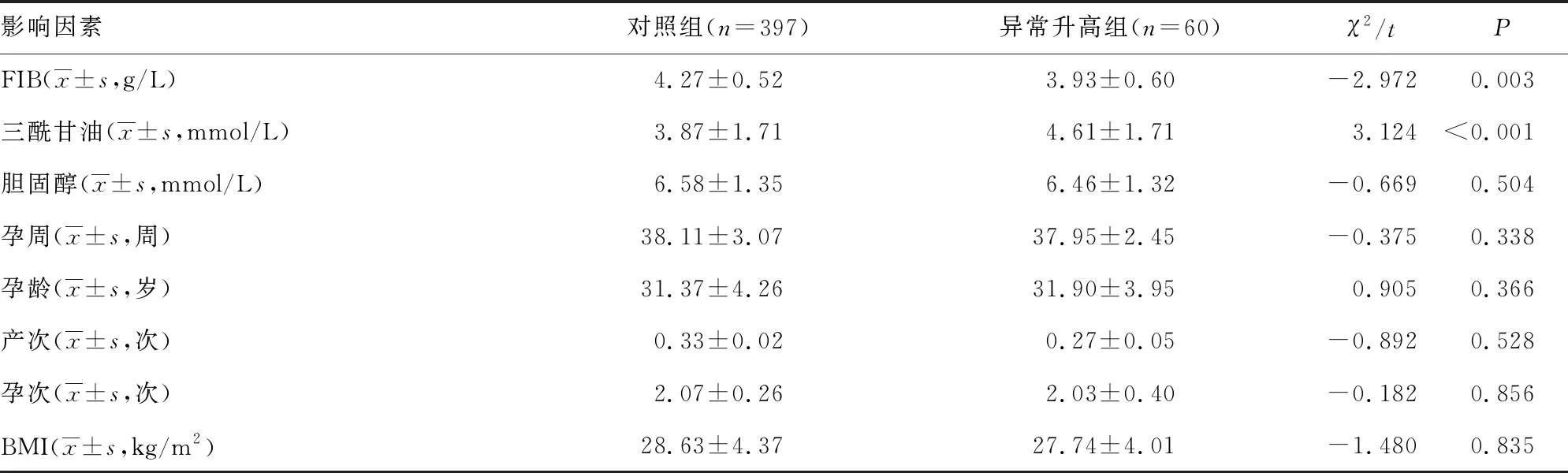
續表1 2組D-二聚體影響因素比較
2.3異常升高組的多因素Logistic回歸分析 單因素分析中,妊娠期高血壓、雙胎妊娠、體外受精-胚胎移植術后、復發性流產史,以及FIB、三酰甘油的水平為影響D-二聚體水平異常升高的因素(P<0.05)。以此6個因素作為自變量,D-二聚體為因變量,進一步進行多因素Logistic回歸分析。結果顯示:雙胎妊娠(P<0.001,OR=5.262)、復發性流產史(P=0.044,OR=6.115)是引起D-二聚體水平異常升高的獨立危險因素。低水平的FIB(P<0.001,OR=0.262)是獨立保護因素。其中復發性流產史是引起D-二聚體水平異常升高最重要的影響因素,其次是雙胎妊娠與FIB的水平。見表2。
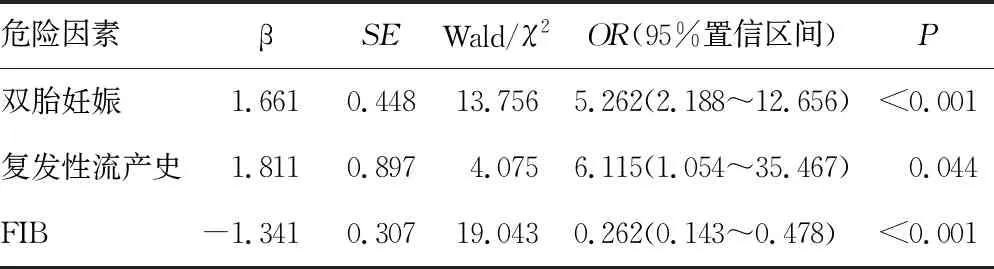
表2 異常升高組的多因素Logistic回歸分析
3 討 論
妊娠女性血液呈高凝狀態,這一生理改變為產后快速有效的止血提供物質基礎。孕婦體內凝血途徑的激活,往往伴隨著纖溶系統的啟動,從而使體內D-二聚體水平逐漸升高。D-二聚體水平升高的原因主要分為兩類,一是凝血與纖溶途徑受到影響,如機體的高凝狀態、血管內皮細胞的損傷、繼發性纖溶亢進等;另一方面是D-二聚體的排出量下降,如腎功能異常等[5]。臨床一旦忽視D-二聚體水平異常升高孕婦的篩查,則會增加不良妊娠結局的發生風險。
本研究中健康妊娠晚期孕婦第95%位點的D-二聚體的水平為1 319 μg/L,與國內外研究結果一致[2,6],即妊娠晚期孕婦D-二聚體的水平是正常未孕女性的4~5倍(正常未孕女性第95%位點的D-二聚體的水平為224 μg/L)。若以傳統的D-二聚體水平最佳臨界值(500 μg/L)診斷孕婦血栓栓塞性疾病,可能導致結果的假陽性率偏高。因此,臨床常規使用的D-二聚體參考區間不適用于妊娠晚期孕婦。本研究發現妊娠期高血壓、雙胎妊娠、體外受精-胚胎移植術后、復發性流產史、三酰甘油及FIB與D-二聚體水平異常升高有關(P<0.05)。多因素Logistic回歸分析結果顯示:雙胎妊娠(OR=5.262)、復發性流產史(OR=6.115)是引起D-二聚體水平異常升高的獨立危險因素。
與單胎妊娠孕婦比較,妊娠晚期雙胎孕婦凝血和纖溶狀態更為亢進[7-8],表現為D-二聚體水平升高,FIB水平降低。雙胎平均血容量較單胎多,加上胎盤重量和體積的增加,使得胎盤中凝血酶的活性增強[7],FIB在凝血酶的作用下形成不溶性纖維蛋白單體,此時,纖溶活性增強,D-二聚體水平異常升高。
復發性流產史是引起D-二聚體水平異常升高的另一個獨立危險因素。既往研究表明,有復發性流產史的孕婦本身即為產科高危人群,多次流產和流產刮宮的病史是胎盤增生的高風險因素,引起胎盤功能不良[9]。此外復發性流產的患者具有異常的免疫細胞功能和細胞數量,導致子宮螺旋動脈異常重建,血流阻力增大,血管內皮細胞功能發生障礙。劉勁松等[10]研究發現復發性流產患者凝血酶原時間、活化部分凝血活酶時間縮短,FIB、D-二聚體水平升高,抗凝血酶水平降低,這些結果表明上述病理性因素激活凝血系統,導致微血栓形成,纖溶系統隨之也被啟動,機體處于高凝易栓狀態。研究指出血栓前狀態是導致復發性流產的重要指標,且D-二聚體水平越高,患者再次流產的風險就越大[11]。
有研究表明,妊娠期高血壓患者的D-二聚體水平升高,且升高的幅度與疾病的嚴重程度有關[12-13]。妊娠期高血壓與全身小動脈痙攣及血管內皮細胞功能損傷有關。血管內皮細胞無法被替代,子宮動脈血流受阻,出現胎盤缺血和絨毛壞死等癥狀。脫落的滋養葉碎片進入血液循環,并不斷被溶解,釋放大量凝血活酶,引起D-二聚體水平升高。此外,D-二聚體水平升高可能與妊娠期高血壓患者腎功能異常導致其排出量下降有關。
體外受精-胚胎移植術后孕婦D-二聚體水平的升高,可能與自身患有的不孕疾病如多囊卵巢綜合征等有關[14],多囊卵巢綜合征是一種內分泌代謝異常疾病,多合并血糖與血脂的紊亂,易引發機體血管內皮細胞損傷。其次,還可能與治療過程中的醫療干預有關[15],包括大劑量促排卵藥物造成凝血和纖溶系統的異常。接受胚胎移植的孕婦與自然受孕的孕婦比較,發生不良妊娠的風險明顯增加[16]。提示未來在輔助生殖工作中,應加強孕婦產前監護及管理,關注孕婦胎盤的功能,尤其是有復發性流產史的孕婦。
妊娠期孕婦體內雌、孕激素水平升高,肝脂酶活性增加,妊娠晚期三酰甘油水平升高,在脂肪酶的作用下分解為甘油和脂肪酸,游離的脂肪酸可能損傷血管內皮細胞,產生炎性反應,激活凝血途徑,導致D-二聚體水平升高。
本研究發現D-二聚體水平異常升高組FIB水平低于對照組(P<0.05)。FIB是凝血系統的中心蛋白質,在凝血酶的作用下形成不溶性纖維蛋白單體,D-二聚體是纖維蛋白單體活化交聯后,經纖溶酶水解的產物。所以,D-二聚體水平異常升高的孕婦FIB水平呈現消耗性降低。此外,FIB水平持續降低是產后出血預后不佳的標志之一。FIB<2.0 g/L對嚴重產后出血的陽性預測價值為100%[17]。因此,應加強D-二聚體水平異常升高孕婦的產前監測,關注產后出血的風險。
綜上所述,妊娠期高血壓、雙胎妊娠、體外受精-胚胎移植術后、復發性流產史等病理性因素使妊娠晚期孕婦D-二聚體水平異常升高,臨床應制訂針對妊娠晚期孕婦的參考區間用于產前監測。本研究建議加強妊娠晚期D-二聚體水平>1 319 μg/L孕婦的管理,關注FIB水平持續降低導致產后出血的風險,以進行早期干預,盡可能避免不良妊娠的發生,保護母嬰健康。

