雙循環戰略促進后新冠疫情時期的生物醫藥創新發展*
劉昌孝
(天津藥物研究院·釋藥技術與藥代動力學國家重點實驗室·天津濱海食品藥品監管科學研究中心,天津 300301)
2020年是國家“十三五”的收官之年。面對錯綜復雜的國際環境和艱巨繁重的國內改革發展穩定任務,中國共產黨團結帶領全國各族人民頑強拼搏、開拓創新,奮力開創了黨和國家事業發展新局面,中國經濟實力、科技實力、國防實力、國際影響力又上了一個大臺階[1]。“十三五”的成就為迎接“十四五”開局奠定了穩定發展的基礎。
2020年也是全球新型冠狀病毒肺炎(COVID-19)傳染病大流行年。疫情的大暴發是近百年來人類所遭遇的最嚴重的公共衛生危機,給人類的生命安全和全球經濟帶來了全方位沖擊,全球“抗疫”形勢更趨復雜。世界衛生組織(WHO)2020年9月10日公布的數據顯示,全球單日新增COVID-19確診病例再創新高[2]。全球疫情反彈凸顯團結合作的重要性。引發COVID-19的病毒是人類的共同威脅,全球疫情防控形勢惡化,說明各國采取的防控舉措存在問題。最近,WHO總干事指出:“這場大流行遠未結束,我們需要調整一切努力,使之適合長期實施,將強有力的領導與整個政府、整個社會參與的方法結合起來,將有助于持續作出一致、有力的應對。”[3]各國科學家和醫藥學工作者從科學角度開展大量科學和臨床研究,為防控疫情貢獻了力量[4-18]。
在黨的領導下,我國堅持把國家、人民和集體利益放在首位,彰顯了人民和整體利益置于首位的制度優勢,是社會主義制度堅持人民至上、生命至上的中國表達。“抗疫”期間,堅持全國一盤棋,舉全國之力調動各方,全國各條戰線、各個領域都緊急行動起來,迅速投入到這場沒有硝煙的戰斗中,彰顯了堅持人民主體地位的制度優勢。中國之所以在比較短時間里迅速有效地控制住疫情,就是因為廣泛發動和依靠人民群眾,凝聚人民力量,構筑起了群防群控的嚴密防線,這是最終打贏這場疫情防控阻擊戰的決定性因素。
我國醫藥戰線在抗疫斗爭中肩負著重要使命和責任。這次疫情對公共衛生體系的發展和改革帶來了一定促進作用。疫情發生使得醫療醫藥行業的下游需求相對剛需,調整結構,緊急防控疫情之需,疫情防護、疾病治療、重癥監護等產品的需求在疫情期間快速增長。在中國“戰疫”過程中,中醫藥發揮了重要作用,特別是“三藥三方”功不可沒[19]。隨著COVID-19疫情在全球蔓延,一段時間以來,國內外對中醫藥參與“戰疫”的需求和關注也在增加。但從整個醫藥行業發展來看,其發展同樣面臨各種各樣的挑戰與困難。
COVID-19疫情對全球供應鏈造成了極大的沖擊和破壞。在供給端,制造業停工停產,影響國際往來和貿易,進而又影響到其他國家的貨物生產。在需求端,隨著疫情在全球蔓延,居家隔離,外出消費減少;企業大幅削減員工;世界總體需求開始下降。這種同時對供求兩端均造成破壞的情況復雜且少見,無疑對貨幣和財政政策的制定帶來更大挑戰。在疫情暴發期間,持續完善公共衛生服務體系、疫情防控體系與能力的一次大考中,既有經驗,也有教訓。初期多部門、多層次的有效聯動機制與體系尚未健全,在人民“戰疫”中,在國家大財政的支持下進行運作才得以勝利。無論是原材料、生產加工、配送與包裝材料的使用等,人們對健康提出了更高質量的要求,注重消費特色與品牌產品。
1 COVID-19疫情對醫藥產業創新發展的影響
1.1 國際醫藥產業發展的影響
世界治療COVID-19藥物需求明顯增長,目前尚無有效藥物問世,幾種“神藥”也被WHO宣布“無效”。WHO于2020年7月4日宣布停止羥氯喹和洛匹那韋/利托那韋兩個試驗,與標準治療相比,COVID-19住院患者病亡率幾乎或完全沒有下降[20]。美國食品藥物管理局(FDA)撤銷氯喹、羥氯喹治療COVID-19的緊急使用授權[21]。NEJM的文章認為,羥氯喹不能降低COVID-19住院患者死亡風險[22]。疫苗研發是戰勝病毒的關鍵,時間緊、難度大且充滿不確定性,因此,成功研發仍需時日。暫停海外檢查可能會影響全球藥品的供應和安全問題。FDA曾警告稱,若疫情持續數月,美國多種藥物將出現短缺。疫情讓美國和歐洲都看到并開始反思對中國原料藥的依賴,下一步或將采取措施逐漸擺脫這種供應關系。
由此,可以看到供給與需求的價值體現關系。以醫藥產業來說,全球2 000多種原料藥中的1 500多種靠中國供應,發達國家所需大部分(75%以上)由中國供給,但由于質量話語權不在我方,就體現不了技術價值。在以技術輸出和服務輸出為主的西方國家,特別是隨著疫情的發展,國外意識到存在明顯的原料藥中國依賴,原料藥離不開中國,也離不開中國制造。圖1為以企業鏈-供應鏈-空間鏈為核心的價值鏈維度關系。如何發揮價值鏈的影響力,還有許多問題值得探討和重視。

圖1 以企業鏈-供應鏈-空間鏈為核心的價值鏈維度關系Fig.1 The dimension relationship of value chain w ith the core of enterprise chain-industry chain-space chain
隨著COVID-19疫情的影響在全球范圍內擴大,生物制藥公司正在密切監控世界各地的生產企業點(鏈)和供應點(鏈)。根據鈕達發布的《COVID-19對全球生物制藥供應鏈的影響》,對于仿制藥行業,利潤的回升將是一個巨大的勝利,因為仿制藥行業近年來在美國面臨著價格壓力,并且利潤微薄。諾華(Novartis)的Sandoz業務2019年僅增長1%,而輝瑞(Pfizer)的Upjohn業務2019年的降幅高達16%。
誠思行業發布《COVID-19藥物行業現狀調研分析及發展趨勢預測報告(2020)》,研究了全球與中國COVID-19藥物的現狀及未來發展趨勢,分別從生產和消費角度分析COVID-19藥物的主要生產地區、主要消費地區及主要生產商。重點分析全球與中國主要廠商的產品特點、產品類型,不同類型產品的價格、產量、產值,以及全球和中國主要生產商的市場份額,報告重點分析全球及中國重要的、代表性企業,主要產品、服務、商業模式、市場定位、市場規模、市場份額及未來發展計劃等,分析了對全球近40家主要企業的影響。
以下是3家跨國醫藥企業發布的2020年第三季度財報,所顯示的數據應有一定代表性。諾華制藥(Novartis)季度銷售額為122.59億美元,同比增長1%;營業利潤為24.14億美元,同比增長2%;凈利潤19.32億,同比降低5%。賽諾菲(Sanofi)季度凈銷售額為94.79億歐元,同比下降0.2%;普通藥品銷售額為36.08億歐元,同比下降6.4%;疫苗銷售額為20.77億歐元,同比增長13.6%;消費者保健部門(CHC)銷售額為10.41億歐元,同比下降1.1%。葛蘭素史克(GSK)季度銷售額為86.46億英鎊,以實質匯率計同比下降8%;制藥部門銷售額為42億英鎊,同比下降7%;疫苗銷售額為20億英鎊,同比下降12%;CHC銷售額為24億英鎊,同比下降4%;總營業利潤為18.58億英鎊,同比下降13%。
1.2 國內醫藥產業的業績和影響
“十三五”期間,中國生物醫藥成果顯著。面對未來,挖掘最具潛力的科技創新企業,推動我國經濟高質量發展是醫藥產業的重任。自主創新能力顯著增強。完善以企業為主體的技術創新體系、企業研發投入較快增加、全面提高原始創新、集成創新能力,有利于產品結構優化升級。到2020年,生物制藥、現代中藥、醫療器械估計還會保持正增長。“十三五”規劃中提出的“優化和完善創新藥物優先評審和快速審批政策,強化審批檢驗人員隊伍的擴充”已經顯著改善,國務院《關于改革藥品醫療器械審評審批制度的意見》的細化落實,大大提高了保障新藥審批、新藥研發審批的速度。國際社會也積極評價中國“十三五”時期的經濟社會發展成就。根據科技部有關報告,我國創新能力基本體現在:(1)新藥臨床前研究和評價與國際接軌水平提高;(2)初步建成國家藥物創新技術體系;(3)人才隊伍與管理水平不斷提升;(4)重大品種創新的現代化、國際化成果顯著;(5)全國中藥資源普查為掌握我國資源發展和利用提供了科學依據;(6)新藥創制專項促進醫藥產業穩步發展應對供給側改革。
2020年后新冠疫情時期的到來,引起了衛生防疫和醫療體系的巨變,藥物研究、開發、經營發展也必然面臨著諸多風險。實際上,疫情防控和治療所產生的挑戰只是醫藥領域的一個方面,在醫療設備領域、醫藥冷鏈運輸領域及一些審批審核環節,都還有諸多方面要完善。
一是環境錯綜復雜:醫藥經營環境錯綜復雜,醫藥工業總產值增速放緩,再加上行業監管持續強化,衛生防疫和醫改政策不斷深化,醫藥企業在研發、環保、資金等方面的成本和風險上升,研發、生產、經營面臨壓力和挑戰。知識產權和技術封鎖等國外挑戰因素也不可忽視。
二是結構調整任務艱巨:國家基本藥物目錄調整、用藥結構、病種治療費用控制、藥品注冊審評審批流程優化、一致性評價成本投入與銷售收入空間壓縮,以及“4+7”城市藥品集中帶量采購等政策落地帶來醫藥企業經營模式的改變,整個醫藥行業機遇不確定性與挑戰嚴重性并存,面臨經營環境和模式的轉型壓力,許多企業的體制機制、結構調整、營銷創新改革艱巨。國內企業、外資企業和國際合作的競爭格局均面臨問題。
三是醫藥行業改革因素復雜:國家醫藥行業改革、多項產業政策出臺實施導致醫藥產品價格持續走低。同時,受國內環保標準不斷提高、藥品質量監管趨嚴等因素影響,藥品研發受創新能力、知識產權、專利保護、生產原材料成本上升、高端人才引入困難、人力資源成本和流動無序、能源和動力等制約,以及環保治理投入不斷加大,進一步壓縮了企業的利潤空間,加大了企業運營風險。
四是醫藥研發風險繼續延伸:行業的藥品研發存在高投入、高風險、周期長等特點,研發過程中存在諸多不可預測因素;藥品的市場推廣也會因為行業、市場環境及競爭等因素的不確定性受到影響,使得藥品研發投入與收益存在不匹配風險。
1.3 我國“十三五”生物醫藥發展的認識
近年來,我國藥品監管科學得到國家藥品監督管理部門的高度重視,在監管創新、法規建設、完善體系建設、監管能力提升和新藥審評審批等方面,其改革創新的主要成績有:(1)加快推進藥品監管科學發展;(2)加強藥品法律法規建設,加快推進藥品監管法制進程;(3)加快推進藥品標準體系完善,標準是科學管理的基本尺度;(4)持續推進藥械審批改革,深化藥品審評審批改革;(5)持續強化產品風險防控;(6)持續加強監管能力建設;(7)全力加強新冠疫情防控。這些成績的取得,除了政府引導實施得力外,在全球化、信息化的大時代背景下,與信息用于產業、用于經濟、用于監管等分不開。信息的共享和擁有程度,已經體現在視野開闊、能力提高、科學監管水平的提高上。
細讀《中國共產黨第十九屆中央委員會第五次全體會議公報》,全會提出了“十四五”時期經濟社會發展指導思想和必須遵循的原則,以及經濟社會發展的主要目標。“堅持黨的全面領導,堅持和完善黨領導經濟社會發展的體制機制,堅持和完善中國特色社會主義制度,不斷提高貫徹新發展理念、構建新發展格局能力和水平,為實現高質量發展提供根本保證。堅持以人民為中心,堅持新發展理念,堅持深化改革開放,堅持系統觀念”。全會提出:“加快發展現代產業體系,推動經濟體系優化升級。堅持把發展經濟著力點放在實體經濟上,堅定不移建設制造強國、質量強國、網絡強國、數字中國,推進產業基礎高級化、產業鏈現代化,提高經濟質量效益和核心競爭力。要提升產業鏈供應鏈現代化水平,發展戰略性新興產業,加快發展現代服務業,統籌推進基礎設施建設,加快建設交通強國,推進能源革命,加快數字化發展。”[1]國家“十四五”規劃落實任務艱巨,服務于民生的醫藥產業在加快發展產業體系和強國目標中的地位不可動搖。全會提出:“改善人民生活品質,提高社會建設水平。堅持把實現好、維護好、發展好最廣大人民根本利益作為發展的出發點和落腳點,盡力而為、量力而行,健全基本公共服務體系,完善共建共治共享的社會治理制度,扎實推動共同富裕,不斷增強人民群眾獲得感、幸福感、安全感,促進人的全面發展和社會全面進步。要提高人民收入水平,強化就業優先政策,建設高質量教育體系,健全多層次社會保障體系,全面推進健康中國建設,實施積極應對人口老齡化國家戰略,加強和創新社會治理。”[1]改善人民生活品質,不斷增強人民獲得感、幸福感、安全感,均離不開醫藥產業的健康發展。
2 發展監管科學推進生物醫藥創新發展
2.1 發展監管科學
監管科學是一門新興學科,其旨在研究開發新理論、新技術、新方法、新工具和新標準來評估受監管產品的安全性、有效性、質量和性能,是監管決策的基礎,是用于人用藥和獸用藥整個生命周期中評估其質量、安全性和有效性的科學。其發展需要政府、企業界和科學界的合作和協調。
本人作為國內早期研究監管科學的藥學工作者,先后以6篇論文系統介紹該新生學科發展的歷史,分析其進展[23-28]。認為近10年來主要有五方面的發展:(1)通過前沿創新醫藥科學發展,推進生物醫藥創新,為保障全球食品和醫藥產品供應鏈安全等方面取得了巨大成就;(2)在推進醫藥產品安全性和有效性方面,人用藥新監管措施和保障藥品供應鏈的規定,繼續加速藥品審評的速度和效率;(3)基于風險的機制,為確保患者安全,保證供應商能夠用安全、準確、可靠的測試結果指導治療決策服務;(4)在醫藥產品中心的個性化醫療時代,可以根據患者的腫瘤遺傳特征,選擇藥物的可能性;(5)重視監管科學發展,利用新理論、新科技、新方法、新標準和新工具作為安全有效的新藥及新療法之間的紐帶,為保障公眾健康和促進產業發展的平衡方面積累了豐富的經驗與成就。美國FDA組織召開了第一屆全球藥品監管科學峰會,此后每年一屆,每屆峰會均有來自各國藥監部門、制藥行業和學術機構三方面的官員及專家參加。強調監管不應該是產業發展的障礙,而是實現有意義和持久創新的切實路徑。
2.2 掌握治療藥物的新進展、共同關注的藥物發展
本人是國際藥物信息學會(Drug Information Association,DIA)的老會員,20世紀90年代在中國還沒有其分支機構時就直接加入了該協會。DIA是一個全球知名的科研型專業協會,涉及藥物發現、藥物開發、藥事法規、監管及藥品市場開拓等領域。該組織1964年成立于美國馬里蘭州,其前身由學術界及制藥界的30名專業人員創建,到2005年已發展成為擁有來自80多個國家的2.3萬名會員的跨學科組織。為促進全球藥品行業的不斷發展,中國醫藥國際交流中心與美國藥物信息協會于2009年11月1日至3日在北京共同舉辦了“第一屆藥物信息協會(DIA)中國年會”,吸收會員,舉行相關主題的報告會和研討會。以后每年舉行1次中國年會。
過去的10多年間,中國的藥物研發環境發生了巨大變化。監管機構的各項改革和監管能力的提升引人注目且成效卓著,生物醫學研發領域的領軍人物們信心滿滿、充滿活力,加上政府支持和各種投資融資機會,使得生命科學創新生態系統在中國呈現愈發蓬勃的生機。
2020年是ICH(InternationalCouncilonHarmonization)成立30周年。2015年,ICH在成立25年后進行組織改革,將International Conference on Harmonization(國際協調會議)改為International Council on Harmonization(國際協調咨詢理事會),成為國際藥品技術要求協調組織,從三方協調組織變成全球化的非營利協調機構。這30年里,ICH在各國藥監機構的合作下,取得了巨大成就[29-31]。ICH指南使全球藥物開發以患者為中心,避免了不必要的重復試驗和注冊流程,快速實現創新藥品在各國獲批上市。
在2014年11月的里斯本會議上,原國家食品藥品監督管理總局(CFDA)國際合作司向ICH管理委員會傳遞了加入ICH的積極愿望。2017年6月,國家藥品監督管理局正式加入ICH。進入ICH 3年,基本實現了各項指導原則在中國的實施,還有個別正加緊轉化,目標是引入ICH各項指導原則,保證技術要求與國際指導原則體系全面接軌。中國快速、精準地轉化落地ICH技術指導原則的過程,對于提高評價和評審效率產生了積極作用。
國家藥品監督管理局藥品審評中心(CDE)為完善國內指導原則體系,為滿足業界研發需求和鼓勵創新,制定國際先進技術標準、藥品技術指導原則共100多個《藥品注冊管理辦法》配套文件和技術指導原則等。ICH指導原則轉化實施標準,遵循了ICH指導原則的所有相關要素、概念及原則[31]。
2020年10月在蘇州舉行了2020年DIA藥物信息年會。會議公眾號發布最新ICH動態,了解最智能的新興技術,捕捉最具影響的話題和討論,掌握疾病治療藥物的新進展,探討共同關注的藥物發展問題等內容。這對于我國藥物規范研究開發,特別是認真理解ICH的M文件、Q文件、E文件和S文件內涵十分重要[29-31]。
3 構建國內國際雙循環互促生物醫藥發展新格局
3.1 “雙循環”新發展格局的建設
研究表明,人體免疫系統對新型冠狀病毒的反應與流感病毒及其他能引起感冒的冠狀病毒類似,即無法產生永久抗體。這再次印證了世界衛生組織的說法:新型冠狀病毒或將與人類長期共存。還有研究發現,新型冠狀病毒抗體水平下降的情況在所有年齡段都有出現。此外,無癥狀感染者體內的新型冠狀病毒抗體水平降幅高于有癥狀者。因此,有人估計,疫情影響可能會持續3~5年。為此,必須以新模式規劃產業發展的戰略和策略。
雙循環發展格局下,中國醫藥行業內需有望進一步被激活,醫藥創新有望提速。雙循環發展格局強調以國內大循環為主體,龐大的醫藥內需市場需要有大而高質量的供給端與其匹配。在我國醫藥領域已有深厚積淀的基礎上,顯著提升生產制造力,消除外資壟斷并不排斥外資合作,雙循環發展格局預計會促進國內企業發展。
“雙循環”的新發展格局建設必須面對逆全球化負面因素。我國在世界醫藥產業的份額極低(6%左右),仿制藥是“大國”,而不是“強國”。中國醫藥產業要繼續堅持高舉經濟全球化大旗,積極參與國際經濟大循環,實現由仿制藥“大國”向創新強國的轉變中產生世界影響;未來的發展進程不能僅僅依靠、依賴和利用國際市場,需要更加注重利用自己的內需優勢,向構建具有中國特色的醫藥保障和安全供給體系邁進,以此構建獨立的國內經濟循環體系;在高質量發展背景下,急需改革開放,不搞封閉發展,設法參與和帶動國際經濟循環,把國內國際循環統籌起來,相互影響、相互促進,形成不同于過去的新的醫藥產業與醫藥商業的發展新格局。
我國構建國內國際雙循環互促新格局的關鍵著力點,在于提升產業基礎高級化和產業鏈現代化水平。其具體路徑包括以下幾個方面:(1)以動態比較優勢理論為指導,推進本土企業實現市場價值和技術的雙重追趕,且必須“揚長補短”;(2)以國內價值鏈為依托,培育本土的“鏈主”企業和“隱形冠軍”企業;(3)以現代化產業集群為載體,實現產業鏈與創新鏈的融合發展;(4)以“互聯網+”數字經濟為契機,促進存量優化和增量創新相結合的產業結構調整,重塑整個產業鏈上下游生態;(5)以“一帶一路”建設為紐帶,塑造以中國制造、中國創造為關鍵技術譜系的國際生產體系。在全球產業鏈中,緊緊抓住與疫情防控有關的醫藥產業和產品的國際需求和合作機遇。
3.2 關注創新要素,提高創新研發能力,建設中國特色的醫藥產業體系
“雙循環”戰略將反映在2021年開局的“十四五”規劃中,有兩個經濟循環,一個在國內,一個在國外。中國希望減少對出口的依賴,希望通過國內消費來刺激經濟。生物醫藥應著重利用本國產業和自我技術擴展的產業政策,在臨床需求和強國需求的產品方面降低對外國的依賴。
1)重視COVID-19疫情全球大流行的大變局演化,提高對新一輪科技革命和產業變革深入發展的認識。
當今世界正經歷百年未有之大變局,2020年COVID-19疫情全球大流行使得這個大變局加速演化。新一輪科技革命和產業變革深入發展,國際力量對比深刻調整,經濟全球化遭遇逆流,保護主義、單邊主義加劇,疫情引發的問題和激化的矛盾將長期存在。要堅持人民至上、生命至上,立足國內需要,建立中國特色的衛生健康體系,實現以人民為中心的健康中國目標,落實從治療向預防轉變、從城市向基層轉變、從大規模向高質量轉變,我國生物醫藥發展必須適應三大轉變的需求,轉向高質量發展。在完成“十三五”規劃全面建成小康社會的基礎上,踏上第二個百年奮斗目標的新征程,繼續發展具有多方面優勢和條件,但發展不平衡不充分問題仍然突出,生物醫藥創新能力還不適應需求轉變的形勢和高質量發展的要求,以及科技強國和科技強醫藥的要求。
生物醫藥從研發到臨床試驗的全過程,最后的目標是應用于患者,因此醫藥產品的市場回報才最終形成完整的循環。這一過程受到政策和法規的指引和影響,包括其中的審批環節、準入環節、市場供給體系、醫療體系、醫保體系等的支持、保障與改革。
2)生物醫藥產業轉型中,人才結構與人才成本問題突出。
高端知識和人才的短板,導致中國的產業轉型能力與人才動力不足。中國的產業結構轉型進程仍處于起步推廣階段,人才隊伍和結構難以達到預期的創新效果,支撐產業轉型的高端人才與前沿知識庫存有限,使其發展軌跡仍然受到廉價人才、廉價知識成本的約束,這種慣性導致中國醫藥產業(特別是國有醫藥企業)結構轉型艱難。建設良好的中國生物醫藥生態圈,需要打通科研和工業界人才流動的壁壘,加強人才特別是領軍人才的培養;需要強調科學創新,企業、大學、科研機構協作,加速科研的產業化轉換;需要專業的投資,規范整個行業的競爭。期待借力于多樣的生態圈,打造中國的旗艦企業和研發團隊,為早日走向世界做好準備。
3)制定生物醫藥創新發展規劃,從跟風中走出來。
2015年以來,由于中國藥政改革,醫藥市場發生了很大變化,新藥獲批速度明顯加快,國外新藥進入中國的速度也大幅加快,這樣既惠及中國患者,也對國內制藥企業提出了新挑戰。目前,進入國家醫保談判的新藥數量大幅增加,藥價快速下降,但新藥研發成本卻越來越高。因此,企業內部形勢和外企的壓力都在促使中國藥企走創新之路。
如國內抗腫瘤藥物研發同質化嚴重,追逐熱門靶點,跟風最為明顯。近幾年雖然國內生物藥獲批數量逐年上升,但基本無原始創新成果,創新度不足,創新藥研發仍以熱門靶點為主。有些熱門靶點(如PD-1,PD-L1,BTK等)多家企業都在做,擠在一個賽道,有相當的盲目性。實際上,可供選擇的靶點非常多,抗體分子就有約1 500個靶點,其中近400個靶點已有藥物開展臨床試驗,國內企業在做的靶點可能不足40個。
藥物創新開發又是一個漫長的過程,創新度越高風險越大,選擇藥效已經得到充分驗證的熱門靶點壓力也巨大。應選擇全新的道路,具體結合公司實際狀況和發展戰略綜合考慮,選擇適合自己的路。同時,還要根據人力、財力和創新力的競爭因素考慮企業的戰略布局。
4)重視傳承精華、守正創新的經典名方開發。
世界藥物大多屬于由化學藥物和生物技術藥物組成的兩個方隊。而中國歷史傳承下來的中醫藥對人民健康起著不可替代的顯著作用,形成了特有的化學藥物、中藥和生物技術藥物組成的3個方隊。在疫情防控中,中醫藥的“三藥三方”彰顯的作用獲得世界認可。在COVID-19全球大流行暴發期缺乏有效治療藥物的情況下,中醫藥發揮了有效作用。其優勢在于:(1)在世界醫學史上,從來沒有像今天這樣如此重視中醫;(2)在世界醫學領域,中醫是唯一能與西醫并存的醫學;(3)在解決西醫難題中,中醫具有不可替代性;(4)在未來世界醫學發展中,中醫是重要貢獻者。而且,這種優勢和特點已經得到國際學者的認同[19]。
古代經典名方是歷代流傳下來的祖國醫藥瑰寶,至今仍廣泛應用、療效確切,具有明顯特色與臨床優勢。國家藥品監督管理局和國家中醫藥管理局為切實貫徹落實習近平總書記關于中醫藥發展的系列重要指示精神,先后出臺了《中醫藥法》《藥品管理法》《藥品注冊管理辦法》《中藥注冊分類及申報資料要求》等政策措施。《中醫藥法》明確規定,來源于古代經典名方的中藥復方制劑,申請藥品批準文號時可以僅提供非臨床安全性研究資料。最近又出臺了《中藥注冊分類及申報資料要求》等措施,此次修訂是深刻總結中藥審評審批實踐經驗,尊重中藥研發規律,堅持以臨床價值為導向,簡化審批程序,深化中藥注冊領域改革。將古代經典名方發揚光大,造福廣大群眾,是新時期傳承創新中醫藥的切入點和突破口。為提高經典名方開發的效率,國家政策規定,將這類中藥開發分為兩類,即3.1類(完全免臨床試驗的經典名方品種)和3.2類(需要臨床試驗驗證)中藥新制劑。
應研究明確“傳承精華、古為今用、古今銜接、凝聚共識”的關鍵信息考證總體原則,制訂基原、炮制、劑量、功能主治的考證細則,解決考證過程中可能涉及的具體問題。考證原則是能用歷史和發展的角度認識經典名方的關鍵共性問題,使經典名方關鍵信息考證提供示范效應,這在科技界和企業界必將引發強烈反響。以臨床價值為導向的高品質中藥制劑研發,已逐漸走上高質量發展科學道路,期待把握其研發契機,突破中藥質量瓶頸。
開展經典名方研發,強調研發的基礎傳承性、共識性、質量穩定性,以及技術和產業化的可行性,需要開展監管科學和科學監管問題研究[26],為經典名方全生命周期監管做好頂層設計。為此,需要遵循3個原則:一是制定政策、法規、技術指南-評價規則,考慮中藥發展的歷史依據,即基于臨床經驗和歷史積累的方劑進行研發。二是傳承的方藥組成、劑量和制備方法原則,區別現有藥典收載品種。建立以“中藥質量標志物”為抓手的中藥全產業鏈的質量體系[32-34],通過“指紋成分-工藝過程可重現性”“生物學、有效性、安全性”“中藥功效-作用機制關聯性”“質量物質可測性”“質量標準穩定性”等質量標志物5元素貫穿經典名方開發的全過程,形成質量和風險的全過程質量追溯系統。三是基于循證醫學原則進行療效再評價研究,形成循證醫學的臨床有效性評價基礎[26](圖2),對于不能免臨床試驗的3.2類制劑需要根據循證醫學原則開展臨床研究。基于上述原則,結合經典名方研發、評價、監管所存在的問題,從組織、協調和戰略方面制訂計劃,組織監管科學立項研究,制訂科學規范的經典名方制劑的質量標準、評價指導原則和技術指南,為科學監管提供依據,實現藥典品種和市場產品的質量和臨床有效性及質量可追溯性,有利于經典名方制劑示范開發。

圖2 遵循循證醫學的監管科學與科學監管的關系[26]Fig.2 The relationship between regulatory science and scientific supervision according to the evidence-based m edicine
5)充分利用大數據、互聯網、生物信息和人工智能(AI)技術。
大數據、互聯網、生物信息和AI等技術已經越來越深入生物醫藥多個領域,面對復雜系統和復雜問題,特別是AI是現階段正在積極深入產業的新興技術,并且努力謀求與自身匹配的布局,將給生物醫藥的發展帶來實現設計、評價、工藝、質量控制的基礎和方向。
在臨床試驗中,依據個體的測試結果,Al可以分析試驗者對藥物的反應及藥物反應的歷史患者數據。AI還能夠開發個性化的藥物治療方案。一是確定臨床試驗候選人。除幫助理解臨床試驗數據外,制藥行業中,AI的另一用途是為試驗尋找參與者。二是預測治療結果。AI應用能夠節省更多的時間和成本,可使藥物干預措施與個體患者匹配,從而減少先前涉及反復試驗的工作。三是預測性生物標志物。完成生物標志物的開發在藥物發現和開發過程中也是一項重要任務。四是確保用藥依從性和劑量。制藥公司為確保臨床研究的自愿參與者遵守藥物研究方案,可通過AI使在藥物研究中的患者必須執行相關規定,以防止影響藥物研究結果。五是加強循證醫學指導的臨床研究的風險評估[26](圖3),保證臨床結論的真實性、科學性和可用性。
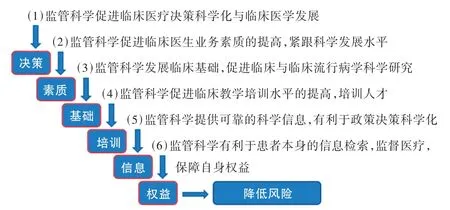
圖3 監管科學促進循證醫學發展中的作用[26]Fig.3 The role of regulatory science in promoting the development of evidence-based medicine
6)先進研發基礎理論和技術是發展的基礎。
生物醫藥研發是一個龐大的技術體系,相應的配套產業也應緊緊跟上,比如上游的原料、生產藥品的儀器設備,等等。未來需要持續加強我國自主創新能力建設,研發出越來越多的國產配套產品,為藥物研發提供更多高技術、新技術支撐。如微生物反應器技術可以大大提高產量和質量。21世紀興起的合成生物學使直接在基因和代謝水平對細胞的改造變得越來越方便,而相應的后續新工程化技術研究卻比較缺乏,反應器相關研究也未得到高度重視。這種狀況反過來又導致現有裝備不能滿足對通過合成生物學技術得到的大量菌種、細胞進行篩選和工藝優化的需要。這種上、下游脫節的現象制約了我國現代生物技術產品的產業化,生物制造產業的健康發展和產業升級也受到了限制。同時,在以大數據和AI為代表的第四次工業革命到來之際,傳統的實驗室規模生物反應器產生數據的速度和質量遠遠不能滿足機器學習、大數據挖掘等新技術的需要。
7)構建臨床數據大平臺,有利于循證醫學指導下臨床新藥的真實科學評價。
我國“十三五”期間的藥物研發不論從新藥種類還是從研發條件方面都有很大提高,越來越接近國際化水平。但是對比其他發達國家,目前國內的原研能力不足,臨床研發人才和管理人才缺乏國際化視野和經驗。應加強新生態下的監管科學能力建設,并呼吁研究機構要與藥企攜手建設發展共同體,以此整合技術平臺,在藥監部門的領導下實現信息互通共享,以服務于創新藥物研發。可以循證醫學指導的真實世界數據的新藥臨床科學評價為抓手,構建基于“信息化+AI+大數據”的國家藥品臨床大數據平臺,構建專科臨床試驗聯合體,做到規范共享、數據共享、資源共享、倫理互認。還可以推動藥物臨床試驗規范、藥物審評規范及藥物應用指南一體化和聯動化,推進臨床試驗人才高質量培訓向集約化、數字化、智能化方向發展,讓中國的新藥研發具有世界影響力。
4 結語
2020年是極不平凡的一年,COVID-19疫情對全球經濟的影響深遠,中國生物醫藥行業面臨不確定性和前所未有的一系列挑戰。未來5年,將是中國生物醫藥轉型升級的關鍵機遇期。中國醫藥創新與投資既要重視市場和資源要素的內循環,更要用好中國元素和中國優勢,在雙循環發展戰略指引下大力推動國內國際合作開放來促進醫藥創新,把握機會,同心協力,為全球生物醫藥領域的創新貢獻中國力量。
近日公布的《中共中央關于制定國民經濟和社會發展第十四個五年規劃和二○三五年遠景目標的建議》[35]指出:“形成強大國內市場,構建新發展格局。堅持擴大內需這個戰略基點,加快培育完整內需體系,把實施擴大內需戰略同深化供給側結構性改革有機結合起來,以創新驅動、高質量供給引領和創造新需求。”結合本文所討論的問題,認為應建立順應促進生物醫藥發展需求的國內國際雙循環格局,立足于滿足人民健康需求的醫藥產業結構的國內大循環,發揮比較優勢,協同推進強大國內醫藥市場和醫藥貿易發展,以國內大循環吸引全球資源要素。同時,改善政府監管體制和企業管理水平,推進醫藥健康產品的高質量、高效率發展。

