糖尿病腎病患者血清CTRP3、CTRP9水平及與血管鈣化的關系
楊會娜 王莉 陸靖 譚文彬
糖尿病腎病是以腎功能衰竭、血糖和血脂代謝紊亂為臨床癥狀的代謝疾病,發展到終末期階段多出現血管鈣化等并發癥,是引起患者死亡的重要原因[1]。臨床上一般用24 h尿微量清蛋白排泄率作為糖尿病腎病診斷指標,但是敏感度較低。研究表明,糖尿病腎病患者中出現血管鈣化并發癥者病死率相對較高,且血管鈣化可在糖尿病腎病初期檢測出,因此可用血管鈣化作為糖尿病腎病的預測指標,對其進行早期檢測,確定鈣化部位,以便實施干預治療[2,3]。作為貯存能量器官的脂肪組織,近年來被證明可分泌脂聯素、腫瘤壞死因子-α等脂肪因子,參與到內分泌系統中,影響血糖和血脂水平,抑制炎性反應,起到保護心血管的作用[4-6]。C1q/腫瘤壞子因子相關蛋白3(C1q/TNF-related protein3,CTRP3)和C1q/腫瘤壞子因子相關蛋白9(C1q/TNF-related protein9,CTRP9)均是新發現的脂肪因子,與脂聯素具有相似的調脂水平,同源度較高[7]。CTRP3通過抑制磷酸烯醇式丙酮酸羧化激酶、6-磷酸葡萄糖酶及轉化生長因子-β1表達,降低血糖水平,減少血管外膜成纖維細胞的增殖和表型轉換,防止血管鈣化發生;同時能夠調節細胞炎性因子水平,發揮抗炎作用[8]。CTRP9在心血管疾病方面顯示出與脂聯素極為相似的生物學功能,可以保護血管內皮細胞,具有抗炎、影響胰島素代謝的作用[9]。目前對于CTRP9的研究多是在動物體內,在人體內研究相對較少。本研究對糖尿病腎病患者和健康者血清中CTRP3、CTRP9水平及血管鈣化情況進行檢測,旨在探討CTRP3、CTRP9對糖尿病腎病發生發展的影響,明確CTRP3、CTRP9表達水平與糖尿病腎病嚴重程度及血管鈣化之間的關系。
1 資料與方法
1.1 一般資料 選取2017年2月至2019年3月濟寧市第一人民醫院收治的糖尿病腎病患者135例(患者組)為研究對象,其中男72例,女63例;年齡26~64歲,平均年齡(42.17±6.52)歲;病程7個月~10年,平均(5.22±2.49)年。根據糖尿病腎病臨床分期分為尿毒癥組48例,非尿毒癥組87例;根據24 h尿微量清蛋白排泄率分為高量尿蛋白組(>300 mg/24 h)42例,微量尿蛋白組(30~300 mg/24 h)53例,尿蛋白正常組(<30 mg/24 h)40例。同時另選取60例體檢健康志愿者為對照組,其中男30例,女30例;年齡25~68歲,平均年齡(41.38±5.29)歲。受試者年齡、性別比方面差異無統計學意義(P>0.05),具有可比性。受試者同意配合研究,簽署知情同意書。本研究經醫院倫理委員會審批通過。
1.2 納入與排除標準
1.2.1 納入標準:①首次確診為糖尿病腎病患者;②未進行血液透析患者。
1.2.2 排除標準:①腎臟活檢結果為非糖尿病腎病的其他腎臟疾病患者;②自身嚴重炎性性疾病患者;③惡性腫瘤患者。
1.3 方法
1.3.1 實驗室檢查:受試者空腹靜脈取血,檢測血清白蛋白(Alb)、膽固醇(TC)、空腹血糖(FPG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、血清鈣(Ca2+)、血清磷(P3+)及C-反應蛋白(CRP)等指標。
1.3.2 血管鈣化檢測:采用X線片對受試者的手指動脈、股動脈、胸主動脈及腹主動脈血管鈣化情況進行檢測,由3名經驗醫師根據檢測結果判定是否為血管鈣化。
1.3.3 血清CTRP3、CTRP9水平檢測:采用酶聯免疫法測定受試者血清中CTRP3、CTRP9水平,試劑盒購自江蘇江萊生物科技有限公司。
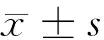
2 結果
2.1 2組血管鈣化結果比較 糖尿病腎病患者的血管鈣化率顯著高于對照組,差異有統計學意義(P<0.05)。見表1。

表1 2組血管鈣化結果比較 例(%)
2.2 2組臨床生化指標結果比較 患者組Alb值顯著低于對照組(P<0.05),患者組FPG值、CRP值、血磷值及血鈣磷乘積值顯著高于對照組(P<0.05),2組TC、HDL、LDL和血鈣值差異無統計學意義(P>0.05)。見表2。
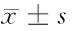
表2 2組臨床生化指標結果比較
2.3 2組血清中CTRP3、CTRP9水平比較 糖尿病腎病患者血清中CTRP3水平顯著高于對照組(P<0.05),CTRP9水平顯著低于對照組,差異有統計學意義(P<0.05)。見表3。

表3 2組血清中CTRP3、CTRP9水平比較
2.4 血清CTRP3、CTRP9水平與糖尿病腎病患者臨床病理及血管鈣化的關系 糖尿病腎病患者血清中CTRP3水平與患者性別無相關性(P>0.05),與患者年齡、病程長短、臨床分期、24 h尿微量清蛋白排泄率及血管鈣化率顯著相關(P<0.05);CTRP9水平與患者性別、年齡無相關性(P>0.05),與患者病程長短、臨床分期、24 h尿微量清蛋白排泄率及血管鈣化率顯著相關(P<0.05)。見表4。

表4 血清CTRP3、CTRP9水平與糖尿病腎病患者臨床病理及血管鈣化的關系
2.5 影響糖尿病腎病患者血管鈣化發生的危險因素分析 單因素分析顯示,病程時間、臨床分期、尿蛋白排泄率、CTRP3水平和CTRP9水平均是影響糖尿病腎病患者血管鈣化的危險因素。多因素分析顯示,CTRP3和CTRP9水平是影響糖尿病腎病患者血管鈣化的獨立危險因素(HR=3.731,95%CI為1.628~8.551;HR=3.508,95%CI為1.774~6.935,P<0.05)。見表5。

表5 影響糖尿病腎病患者血管鈣化危險因素分析
3 討論
糖尿病腎病患者血糖和血脂代謝異常,血清中血磷含量及血鈣磷乘積較高,因此患者極易出現血管鈣化癥狀。血管鈣化是鈣化抑制因素與促進因素之間調節不平衡的結果,是基因與蛋白介導主動調節過程[10]。安玉等[11]研究表明年齡、高磷血癥或體內攝入過多鈣劑均可增加患者血管鈣化的風險。糖尿病腎病患者體內胰島素分泌不足,脂肪代謝異常,脂質分解進程得不到控制,致使血液中脂質分解產物增多,造成高血脂和高血糖。病程發展到后期時,患者腎臟功能出現嚴重障礙,對磷的清除能力減弱,而且一般出現蛋白尿癥狀,從而使Alb含量下降,血磷含量升高,鈣磷乘積增加,增加患者血管鈣化的風險。本研究結果顯示糖尿病腎病患者的Alb值顯著低于對照組(P<0.05),患者組FPG值、CRP值、血磷值及血鈣磷乘積值顯著高于對照組(P<0.05),2組TC、HDL和LDL值之間差異無統計學意義(P>0.05)。
研究發現,脂肪組織能夠分泌一系列脂肪因子,參與到免疫調節、血管功能和脂肪代謝中,影響高血脂血糖等糖尿病腎病疾病的發展進程[12]。CTRP家族是新發現的脂肪因子,與脂聯素具有高度同源性,能夠調節體內代謝和能量平衡,其中以CTRP3和CTRP9與血管關系最為緊密。CTRP3蛋白由246個氨基酸序列構成,人體編碼CTRP3基因共有兩種表達亞型,CTRP3A和CTRP3B,并以其C-末端球狀C1q結構域為主要生物學功能結構域,與其他蛋白或受體發生相互作用[13]。動物學實驗表明,CTRP3能夠抑制肝臟糖異生過程,降低正常小鼠及胰島素代謝異常小鼠血糖水平,但是對血清中脂聯素及胰島素水平無影響[14],即CTRP3發揮作用的方式獨立于胰島素,不依賴胰島素減少來控制血糖。CTRP3對脂肪代謝的影響是通過促進脂聯素分泌和表達以及對3T3-L1細胞系胰島素敏感性的改善作用來實現的,它可以增加葡萄糖轉運子表達,降低炎性因子表達。Zhou等[15]研究表明,CTRP3除在血糖血脂中的代謝作用外,在由腎臟疾病引起的血管鈣化中也具有高表達,且和鈣化部位之間存在共定位。CTRP3可以加劇β-甘油磷酸誘導的血管平滑肌細胞鈣結節生成,但是CTRP3只能促進由高血磷引起的血管鈣化,自身無法導致血管鈣化。CTRP9蛋白有333個氨基酸序列構成,含有4個不同的結構域,同樣以C-末端球狀C1q結構域為主要生物學功能結構域,與其他蛋白或受體發生相互作用[16]。相關動物學試驗研究表明,CTRP9通過蛋白激酶B等途徑調節糖脂代謝,當敲除小鼠CTRP9基因后,會導致小鼠促進食欲的神經肽水平升高,食物攝入增多,胰島素敏感性降低,抵抗性增加[17]。CTRP9多在脂肪組織中表達,在血漿中含量很低,但是在成年鼠心臟組織中含量很高,提示CTRP9可能參與調控心臟功能,影響心血管疾病的發生發展過程。CTRP9可以對蘇氨酸蛋白激酶進行激活,抑制人體動脈內皮細胞凋亡,減少基質金屬蛋白酶-2分泌,減輕炎性反應,改善血管內皮細胞,降低血管鈣化率[18,19]。本結果顯示,糖尿病腎病患者血清中CTRP9水平顯著低于對照組,CTRP3水平、血管鈣化率顯著高于對照組,提示CTRP3可能對糖尿病腎病的發展有促進作用,CTRP9水平可能對糖尿病腎病的發展有減緩作用。進一步分析結果顯示糖尿病腎病患者血清中CTRP3水平與患者年齡、病程長短、臨床分期、24 h尿微量清蛋白排泄率及血管鈣化率顯著相關;CTRP9水平與患者病程長短、臨床分期、24 h尿微量清蛋白排泄率及血管鈣化率顯著相關,提示糖尿病腎病患者血清中CTRP3、CTRP9水平與患者病程、病理分期、尿蛋白排泄率及血管鈣化形成有關。多因素分析顯示,CTRP3、CTRP9水平是影響糖尿病腎病患者血管鈣化的獨立危險因素,提示CTRP3和CTRP9可能通過某種機制參與糖尿病腎病疾病發展,并對血管鈣化產生影響。
綜上所述,CTRP3在糖尿病腎病患者血清中高表達,CTRP9低表達,與患者病程、臨床分期、24 h尿微量清蛋白排泄率及血管鈣化情況有關,是影響血管鈣化的獨立危險因素。推測CTRP3和CTRP9可能通過某種方式參與糖尿病腎病及血管鈣化的發生發展。

