CYP17A1聯合FGF5基因多態性與高血壓的相關性評價
刁曉艷 何燕
(1.貴州醫科大學附屬醫院心血管科,貴州 貴陽 550004;2.貴州醫科大學分子生物學教研室,貴州 貴陽 550004)
原發性高血壓(EH)是當今社會的最常見疾病之一,它的發病機制一直處于研究和探討之中,它是由遺傳因素與環境因素相互作用所致的復雜性疾病[1]。基因的研究不斷進展,但仍眾說紛紜。近年來研究認為細胞色素p450c17alpha蛋白(CYP17A1基因)多態性及成纖維細胞生長因子5(FGF5基因)多態性與EH的發病的有一定的相關性,但結論不一致[2-6,8-12]。本研究選擇貴州省貴陽市部分漢族人群作為研究對象,探討他們的基因多態性與EH的發病關系,現報告如下。
1 資料與方法
1.1研究對象 EH組:選擇在貴州醫科大學附屬醫院心內科門診或住院部高血壓患者191例,血壓診斷標準按中國高血壓指南(2010年)標準;排除繼發性高血壓、瓣膜疾病、心肌病及肝、腎衰竭,孕婦、哺乳期婦女以及精神疾病史或濫用藥物者等;患者中男86例,女105例,平均年齡(58.86±11.67)歲。對照組:選擇在貴州醫科大學附屬醫院門診的健康體檢者196例,無高血壓家族史,無各類心血管、腦血管、腎、內分泌等方面疾病的健康人群;患者中男85例,女111例,平均年齡(55.07±11.08)歲。兩組性別差異無統計學意義(P>0.05),年齡差異有統計學意義(P<0.05)。兩組均為貴州籍漢族人,且互相均無血緣關系。
1.2方法
1.2.1生化指標測定 清晨空腹抽取靜脈血檢測血脂(包括甘油三酯、總膽固醇)、血糖和尿酸。
1.2.2體質量指數(BMI)計算 采用國際標準化方法測量身高、體重。BMI=體重/身高2(kg/m2)。
1.2.3基因分型 按經典常規法(酚-氯仿法)抽提白細胞DNA,溶于TE;紫外吸收法定量后標化為30 ng/μL,-40℃備用。應用TaqMan 實時熒光定量PCR技術對CYP17A1基因和FGF5基因進行基因分型。PCR反應為10 μL體系:DNA(濃度為30 ng/μL)1.5 μL,通用TaqMan PCR Master Mix 5 μL,雙蒸水3.25 μL,20×基因分型探針及引物0.25 μL。其中TaqMan PCR Master Mix、基因分型探針及引物均購自美國ABI公司,探針分別用FAM、VIC染料標記。反應條件為:95℃ 10 min活化AmpliTaq金牌酶后,95℃ 15 s,60℃ 1 min 20 s,共55個循環。儀器采用美國ABI公司生產的Step one Plus PCR儀,讀取FAM/VIC熒光判斷基因分析結果。FAM熒光探針識別T等位基因,VIC熒光探針識別C等位基因。每塊96孔板設3孔陰性對照,并隨機抽取5%樣本復測,一致性為100%。
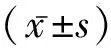
2 結 果
2.1一般資料及臨床生化指標比較 兩組年齡、血糖、甘油三酯及BMI比較,差異有統計學意義(P<0.05)。見表1。
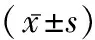
表1 一般資料及臨床生化指標比較
2.2基因型和等位基因頻率分布 兩組CYP17A1 C/T基因型及FGF5 T/A基因型的分布均符合Hardy-Weinberg遺傳平衡(P>0.05)。經χ2檢驗CYP17A1 C/T兩組間基因型分布差異有統計學意義(P<0.05),兩組間等位基因頻率分布差異有統計學意義(P<0.05)。兩組間FGF5 T/A基因型及等位基因型差異無統計學意義(P>0.05)。見表2。

表2 兩組CYP17A1 C/T與FGF5 T/A基因型和等位基因頻率比較[n(%)]
2.3原發性高血壓的患病風險分析 去掉性別、身高、體重、尿酸等混雜因素(P>0.05)進行Logistic回歸分析,年齡、FGF5 TT基因型、CYP17 A1 TT基因型和空腹血糖高于正常標準的人群具有更高的患病風險,特別是當空腹血糖高于正常標準時較對照組患病風險提高4倍。見表3。

表3 高血壓的患病風險分析
3 討 論
原發性高血壓的發病具有相當的遺傳因素,但至今候選基因仍很多。近年發現4q21區域的FGF5(成纖維細胞生長因子5)基因內的rs16998073位點主要是與鹽敏感性相關,該基因遺傳變異與血壓可能相關[7,12]。迄今為止,鹽敏感性高血壓的發病機制仍有爭論。有研究[11]認為FGF5可以促進細胞生長和在多種細胞增殖,包括心肌細胞,能夠促進心臟血管形成。然而,現在沒有證據證明這個基因與高血壓發病機理的關系。目前有研究[8]表明在韓國人中FGF5(rs16998073)遺傳變異與鹽敏感性密切相關。全基因組關聯分析(GWAS)研究認為8個與血壓相關基因變異,其中包括FGF5(rs16998073)為一個可能性的因素。在日本人中認為FGF5是與高血壓發病關系最明顯的基因位點。FGF5在日本人群中對收縮壓和舒張壓的影響是歐洲人群中1.4倍[10]。
CYP17A1基因編碼細胞色素P450c17alpha蛋白,影響類固醇17alpha-羥化酶和17,20 裂解酶活性,在類固醇的生存途徑的調控中起著重要的作用。CYP17A1rs11191548位點的突變可導致17alpha-羥化酶/17,20 裂解酶缺陷癥,從而損害腎上腺和性腺中類固醇激素的合成,刺激腎上腺皮質增生和17-脫氧類固醇前體如孕酮、孕烯醇酮、脫氧皮質酮、皮質酮等發揮鹽皮質激素功能,引起水鈉潴留,血壓增高[9]。近年來很多研究致力于rs11191548與高血壓相關性,但是結論有所爭議,C.Newton-Cheh[2]在歐洲家系及印度—亞洲家系的樣本進行研究中認為位于10q24.3的CYPl7A1基因的rs11191548與收縮壓(SBP)相關。K.W.Hong[3]等選擇了7 551例韓國人,發現CYPl7A1基因rs11191548位點攜帶C最小等位基因能顯著降低SBP、舒張壓(DBP)及高血壓的患病風險。而X.M.Li[5]研究結果表明CYPl7A1基因rs11191548位點攜帶C最小等位基因的能增加高血壓的患病風險。Y.H.Lin[6]與先前的歐洲人群和中國漢族人群不同,在畬族人群中未發現rslll91548突變與高血壓有顯著的相關性。
本研究結果顯示,CYPl7A1基因C/T基因型與等位基因頻率在貴州省漢族的EH組和對照組中差異有統計學意義(P<0.05),均明顯高于對照組組。提示CYPl7A1基因C/T基因型與高血壓的發病可能相關。雖然本研究未得出FGF5基因多態性與高血壓的明顯關系,但在多元回歸分析中提示FGF5 TT基因型可能患高血壓的風險較大(P<0.05),而且CYPl7A1 TT基因型 FGF5 TT基因型在高血壓的風險分析中同時具有統計學意義,提示兩種基因型同時存在時可能會增加高血壓的發病。在兩組FGF5的基因型和等位基因比較中也可看到TT基因型和T等位基因在EH組中較多,但無統計學意義,目前對FGF5基因與高血壓的關系大部分集中在與鹽敏感性的關系上,故推測是否與入組病人中鹽敏感性高血壓類型少有關。
目前對上述兩種基因與高血壓的關系仍無定論,本研究結果顯示,年齡、空腹血糖、甘油三酯、體重指數是高血壓發病的危險因素,但如果加入基因多態性的影響,就只顯示年齡和血糖與高血壓患病風險更高。總的看來高血壓的發病機制很復雜,遺傳、環境及獲得性因素對高血壓發病均有關系。本研究也進一步提示對高血壓的基因研究還存在很多復雜性,包括神經體液因素對高血壓的發病機制的影響。

