伏立康唑血藥濃度監測及其在血液系統腫瘤患者用藥指導中的應用
張文娟,姚 瑤,強 瓊,楊 樂,劉琳娜(中國人民解放軍空軍軍醫大學第二附屬醫院藥劑科,陜西 西安 710038)
伏立康唑是新一代三唑類抗真菌藥物,其抗菌譜廣,抗菌作用強,越來越多的用于曲霉菌、新型隱球菌、念珠菌等真菌感染的治療,被各大指南推薦作為侵襲性曲霉菌病的首選藥物。伏立康唑的療效、不良反應與血藥濃度相關,研究[1-3]表明,食物、年齡均可影響其血藥濃度,且伏立康唑治療窗較窄,藥物暴露量與CYP2C19的基因多態性具有顯著相關性,又與多種藥物之間存在相互作用,這些都可影響其療效和安全性。伏立康唑具有非線性動力學特征,同一劑量下患者的血藥濃度會有不同,因此對其實施血藥濃度監測具有重要意義。近年來,多個指南均推薦對伏立康唑進行血藥濃度監測,以達到臨床安全有效的目的,基于此,我們建立了運用反相高效液相色譜法測定血清中伏立康唑藥物濃度,對我院2017年7月 -2019年11月血液科460例住院患者的611個標本進行了伏立康唑血藥濃度的監測和分析,旨為臨床安全合理用藥提供參考。
1 儀器與試劑
1.1 儀器
LC-2030液相色譜儀(日本島津儀器公司),Inertsil ODS-3色譜柱(日本 GL Sciences公司),MX-S旋渦混合器[大龍興創實驗室儀器(北京)有限公司],MiniSpin離心機(德國Eppendorf公司),KH5200PV型超聲儀(昆山禾創超聲儀器有限公司),電子分析天平(十萬分之一)(德國Sartorius公司),Milli-Q Advantage A10超純水機(德國默克密理博公司)。
1.2 試劑
伏立康唑對照品(中國藥品生物制品檢定所,批號:100862-201402);酮康唑對照品(中國藥品生物制品檢定所,批號:100294-201203);甲醇和乙腈(色譜純,Fisher公司);冰醋酸為分析純(天津市富宇精細化工有限公司);三乙胺為分析純(天津市科密歐化學試劑有限公司)。空白血清由唐都醫院輸血科提供。
2 方法與結果
2.1 色譜條件
色譜柱Inertsil ODS-3柱(250 mm×4.6 mm,5 μm);流動相為乙腈 : 冰醋酸-三乙胺緩沖液 = 45∶55(v/v),流速1.0 mL·min-1;進樣量20 μL;室溫25 ℃;紫外檢測波長255 nm。
2.2 標準溶液和內標溶液的配置
2.2.1 伏立康唑標準溶液的配制精密稱定伏立康唑標準品77.59 mg,以甲醇定容至50 mL容量瓶中,儲備液于4 ℃保存備用。
2.2.2 內標溶液的配制精密稱定酮康唑對照品107.61 mg,以甲醇定容至50 mL容量瓶中,儲備液于4 ℃保存備用。
2.3 血清樣品處理方法
取血清450 μL,加入不同濃度的伏立康唑工作液30 μL和內標溶液20 μL,漩渦30 s混勻,加入乙腈溶液500 μL,漩渦3 min,13 000 r·min-1離心10 min,取上清液20 μL進樣。
2.4 方法學驗證
2.4.1 專屬性考察患者血清按照“2.3”項下方法進行預處理,進樣得色譜圖。伏立康唑和血清雜質及內標之間分離良好。詳見圖1。

圖1 HPLC色譜圖A-空白血清,B-空白血清 + 伏立康唑標準品 + 內標,C-患者血清;1-伏立康唑,2-酮康唑(內標)Fig 1 HPLC chromatogramA-blank serum, B-blank serum + voriconazole standard + internal standard, C-serum of patients; 1-voriconazole, 2-ketoconazole(internal standard)
2.4.2 標準曲線線性關系考察取空白血清450 μL,共7份,分別加入不同濃度的伏立康唑標準溶液,使伏立康唑的藥物濃度分別為0.097、0.58、1.46、2.93、5.85、11.69、23.38 μg·mL-1,按“2.3”項下方法處理。按照“2.1”項下方法測定。測定結果以伏立康唑濃度(X)為橫坐標,伏立康唑與內標峰面積的比值(Y)為縱坐標,用最小二乘法作線性回歸,得到血清中伏立康唑濃度回歸方程:Y= 0.029 5X-0.003 8,r= 0.999 0。血清中伏立康唑在0.097~23.380 μg·mL-1的濃度范圍內呈良好的線性關系。
2.4.3 回收率試驗取濃度分別為0.58、5.85、23.38 μg·mL-1伏立康唑工作液各5個樣品。按“2.3”項下方法處理后進樣分析。取含量相同的伏立康唑工作液直接進樣分析,計算伏立康唑在血清中的提取回收率,用回歸方程計算方法回收率,詳見表1。

表1 回收率試驗結果Tab 1 Results of recovery test
2.4.4 精密度試驗配制上述回收率考察試驗中的3個濃度伏立康唑血清樣品,分別在同日內不同時間點和不同日處理后進樣分析,計算日內精密度和日間精密度,低、中、高三個濃度的日內和日間精密度分別為0.89%~4.47%和0.72%~4.22%。
2.4.5 穩定性試驗1)血清樣本室溫放置穩定性:配制伏立康唑濃度分別為0.58、5.85、23.38 μg·mL-1血清樣品,于室溫下放置,分別在配制后的2、4、6、8 h處理后進樣分析。伏立康唑低、中、高三種濃度血清樣本,室溫放置穩定性的RSD為0.96%~1.22%。2)血清樣本凍融穩定性:配制伏立康唑濃度分別為0.58、5.85、23.38 μg·mL-1血清樣品,于-20 ℃冰箱冰凍保存,分別在第0、3、7、14 d解凍測定,考察伏立康唑低、中、高3種濃度血清樣品,凍融穩定性的RSD為1.16%~8.42%。
2.4.6 重復性考察取低、中、高三個濃度血清樣品,按“2.3”項下方法平行處理后分別連續進樣分析5次。結果顯示伏立康唑和酮康唑峰面積比值的RSD為0.12%~8.37%。
2.5 血液腫瘤患者伏立康唑血藥濃度測定結果
應用上述方法對2017年7月- 2019年11月在我院血液科住院的460例患者的611個標本進行了伏立康唑血藥濃度測定。460例患者中男性比例為55.65%,女性比例為44.35%,臨床診斷包括急慢性淋巴細胞白血病、急慢性粒細胞白血病、多發性骨髓瘤以及再生障礙性貧血。給藥方式包括口服(164例次)和靜脈滴注(447例次),所有用藥均用于預防或治療肺部真菌感染,藥物未區分生產廠家。相關指南[4]指出,監測穩態谷濃度具有良好的臨床意義,伏立康唑給予負荷劑量時第3天達穩態血藥濃度,未給予負荷劑量的則在第5~7天達穩態血藥濃度。本實驗所有標本均嚴格按照要求,在血藥濃度達穩態后的第一次給藥前30 min內采集,本監測結果表明血藥濃度能夠達到指南推薦的1.0~5.5 μg·mL-1的患者比例為67.10%(表2);男性血藥濃度與女性相比相差不大(表3,P> 0.05);大于60歲老年患者血藥濃度總體水平較高(表4),這可能與老年人代謝緩慢有關;口服給藥和靜脈給藥血藥濃度有顯著性差異,靜脈給藥血藥濃度總體水平較高(表5,P< 0.01)。

表2 血藥濃度分布情況Tab 2 Distribution of serum drug concentration
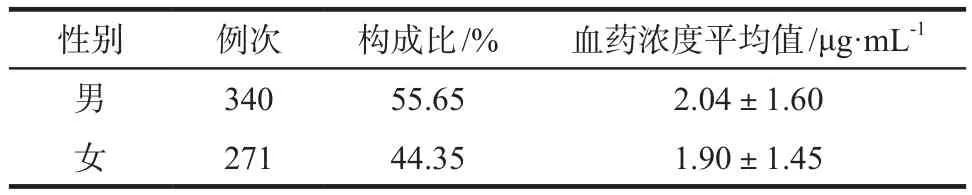
表3 不同性別患者血藥濃度情況Tab 3 Serum drug concentration in different gender

表4 不同年齡組血藥濃度情況Tab 4 Serum drug concerntration in different age groups

表5 不同給藥方式血藥濃度情況Tab 5 Serum drug concerntration of different ways of administration
3 討論
目前,國內外進行伏立康唑血藥濃度監測的方法有超高液相、串聯質譜、固相萃取-HPLC法、酶免疫放大法等[5-9],超高液相以及串聯質譜的速度、靈敏度和分離度都較高,非常適合復雜組分及微量元素的測定,但這兩種儀器的固定資產投入較大,不利于臨床推廣;固相萃取技術作為樣品前處理方法,已普遍應用于實驗中,能有效的將標的物質與雜質分離,但該法相對于蛋白沉淀法耗時過長。以服務臨床為目的,不僅要做到高效、準確,還要做到快速和便于推廣,故本研究選擇了高效液相色譜法。
在方法學建立過程中,筆者比較了應用甲醇沉淀蛋白、乙腈沉淀蛋白的提取方法,乙腈沉淀蛋白處理的組織樣品無雜質,藥物提取回收率高。此外還考察了血清與血漿中內源性物質對伏立康唑濃度監測的影響,發現血漿樣品中內源性物質對伏立康唑有明顯干擾,導致二者分離度差,所以采用血清樣本進行測定。
伏立康唑的分子結構中含有三唑環、吡啶環等堿性基團,在流動相中加入一定比例的三乙胺,不僅可以調節流動相的pH值,還可作為掃尾劑,防止色譜峰的拖尾,改善峰形[10]。
本研究所測定的患者血樣為血液腫瘤患者樣本,此類患者用藥最突出的特點就是合并用藥多,采用本研究建立的方法分離度好,能夠很好的排除合并用藥的干擾,使得目標藥物與內標的分離度良好。因此本研究建立的方法具有實用性強、操作簡便、數據準確、靈敏度高、重復性好的特點,可作為伏立康唑血藥濃度日常監測方法,為臨床合理安全用藥提供有力的保障。目前國內外研究結果表明,伏立康唑藥動學個體差異大,且臨床療效和不良反應與血藥濃度顯著相關[11-17],故指南建議,在給藥4~7 d后應監測伏立康唑血藥谷濃度,以指導劑量調整,使谷濃度水平達到有效治療范圍[17],根據國外指南推薦伏立康唑可能的安全濃度范圍為1.0~5.5 μg·mL-1,研究表明,當谷濃度高于1 μg·mL-1時,療效增加,當谷濃度≥4 μg·mL-1,神經毒性增加,谷濃度≥ 5 μg·mL-1,肝毒性增加,因此谷濃度范圍在1.0~5.5 μg·mL-1可以實現療效最大化、不良反應最小化,本研究測定的標本67.10%谷濃度達到該范圍,對于未達標的原因還應做更進一步的探索。血液腫瘤患者免疫功能低下,病原菌及感染灶不明確,臨床上通常采用經驗性治療。經驗用藥使患者獲益的同時也存在風險,如抗感染效果欠佳,不良反應發生率升高等。因此,建議臨床應結合病原學檢查結果及時調整抗菌藥物的使用,并根據血藥濃度優化給藥策略,實現精準治療[18-20]。

