ABO 血型不相容親屬活體腎移植病人的精細化護理
柴 榕,暢秋月,吳曉英
1.山西省第二人民醫院,山西030012;2.北京大學人民醫院
腎移植是治療各種終末期腎病的最佳方法。近年來,供腎逐漸緊張、器官資源短缺是束縛器官移植發展最重要的原因,擴大標準供者、心臟死亡器官捐獻、腦死亡器官捐獻、供腎交換和邊緣供腎是解決當前供腎短缺的有效途徑[1]。親屬活體腎移植為移植病人提供了一種新的解決供體短缺的有效方法。國外統計資料顯示,在潛在的活體供者中,約有30% 的供者與受者ABO 血型不相容(ABOi),即供者血型和受者血型不符合輸血原則[2]。我院于2016 年4 月―2019 年11 月共實施了9 例ABO 血型不相容親屬活體腎移植術,現將我院對病人的圍術期精細化護理總結如下。
1 資料與方法
1.1 一般資料 9 例親屬活體供者各項檢查結果均達到手術要求,未發現手術禁忌證。9 例親屬活體受者完成血液生化、心電圖、心臟彩超、胸片、腹部B 超及雙側髂血管B 超等檢查,確定無移植禁忌證,供受者間錯配2~4 個。9 例親屬活體供、受者基本情況見表1。

表1 9 例親屬活體供者、受者一般資料
1.2 術前預處理 ABO血型不相容腎移植術(ABOi-KT)通過術前脫敏治療有效解決了血型不配所導致的超急性排斥反應,大大提高了人腎遠期存活率。我院脫敏方案為:①術前1 個月給予利妥昔單抗靜脈輸注免疫誘導;②定期復查血型抗體滴度(靜脈輸注利妥昔單抗前后,以后每周1 次);③每周化驗B 細胞(CD3-CD19+)比例,目標范圍為0.1 左右;④術前3 周開始口服三聯免疫抑制劑;通常為他克莫司0.05~0.10 mg/(kg·d),霉酚酸酯1~2 g/d或霉酚酸鈉1.44 g/d,甲潑尼龍20~80 mg/d;⑤術前根據抗體滴度水平行血漿置換或雙重濾過血漿置換。脫敏治療后定期復查肝、腎功能及凝血、血常規等,預防感染;及時協調相關輔助科室緊密配合。受者均病情穩定,血型抗體效價在術日均≤1∶16,并給予常規術前備皮、灌腸。在全身麻醉下行ABO 血型不相容親屬活體腎移植術。術前預處理情況見表2。
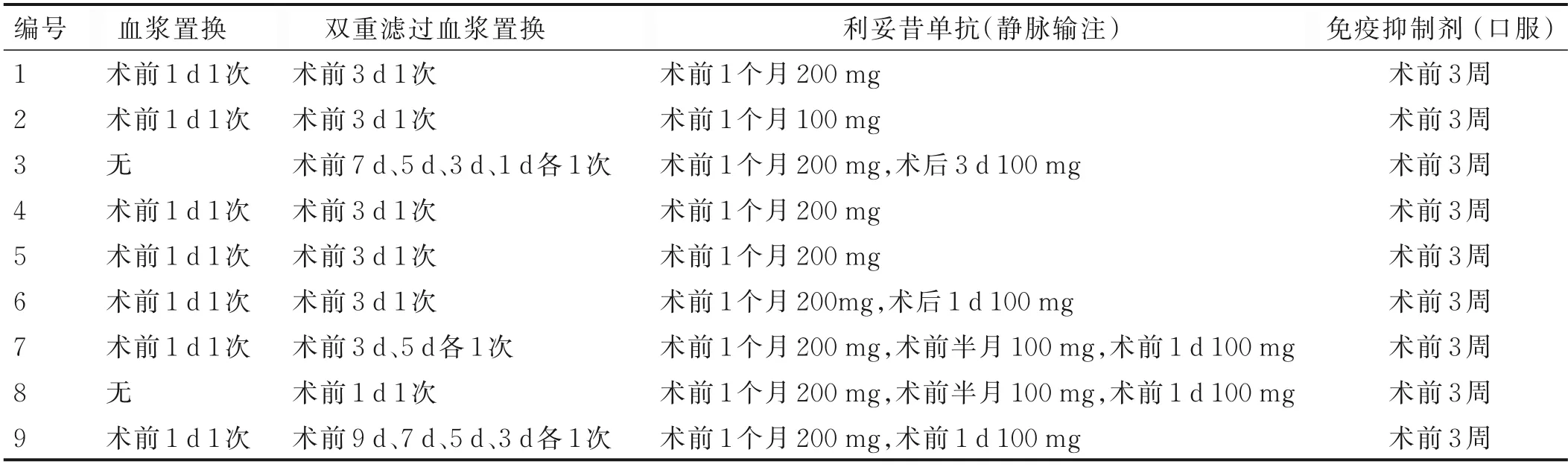
表2 9 例ABO 血型不相容受者預處理
2 結果
9 例病人在術日血型抗體效價水平≤1∶16,術后2 周均未出現血型抗體效價的反彈。病例1~病例7 于術后21 d 痊愈出院,另2 例病人于術后1 個月痊愈出院。其中,病例6 術后1 d 發生低氧血癥,經床旁血液濾過2 次及高流量氧療后好轉;病例8 在術后8 d 發生排異反應,給予血漿置換、兔抗人胸腺細胞免疫球蛋白抗排異治療后,肌酐逐漸下降。病例3 和病例4 在術后4 個月發生肺部感染,其中,病例3 因呼吸衰竭死亡,病例4 治愈;病例9 于術后78 d 因移植腎排異,行移植腎摘除術;其余病人隨訪腎功能正常。
3 精細化護理
3.1 心理護理 病人術后最主要的心理反應是焦慮。首先,供者與受者血型不相容,會承擔比一般親屬活體腎移植術更大的風險。其次,供者是自己的親屬,萬一手術失敗,會增加自己對家庭的內疚感。護理人員應耐心與病人溝通,引用國外此類手術的數據減輕病人的焦慮情緒。Takahashi 等[3]對日本1989 年―2010 年的1 878 例ABO 血型不相容活體腎移植進行總結表明,與同期的ABO 血型相容腎移植療效相近。
3.2 病室管理 嚴格執行院內各項感染防控規章制度,建立健全醫院管理制度及消毒隔離制度。病人由于使用免疫抑制劑,免疫力低下,術后轉入監護室,每例病人固定責任護士,減少人員流動。監護室每日用循環風紫外線空氣消毒機進行空氣消毒,室溫保持在22~25 ℃,濕度在50%~60%。做好病室內物品、床單元、治療臺、地面的消毒工作,用500 mg/L 含氯消毒液每日擦拭2 次,每月對物體表面、工作人員手、空氣進行細菌菌落總數監測,保證空氣細菌菌落總數≤4 cfu/(15 min·直 徑9 cm 平 皿),物 體 表 面 細 菌 菌 落數≤5 cfu/cm2,工作人員手≤5 cfu/cm2。
3.3 生命體征觀察及補液 術后7 d 內采用心電監護儀持續監護血壓、脈搏、呼吸等生命體征。術后監護期保持相對高的血壓[高于病人術前血壓5~10 mmHg(1 mmHg=0.133 kPa )],以利于移植腎的血液灌注[4]。尿量是腎移植術后最重要的觀察指標,術后每小時記錄1 次尿量至術后5 d 拔除尿管后,每隔2 h 記錄1 次尿量直到出院,準確記錄24 h 出入量,根據尿量對補液量及補液速度進行調整。補液方案:0.9% 氯化鈉注射液1 000 mL 與5% 葡萄糖注射液500 mL 交替補液;術后5 d 內每日監測電解質2 次或3 次,根據血清鉀離子水平補液中可加入10%氯化鉀注射液;病人排氣前每隔3 h 監測血糖1 次,根據血糖水平調整補液糖中胰島素用量。我科應用DASH 3000 無創血流動力學監測系統(美國通用電氣公司)監測病人術后早期的血流動力學變化,在指導術后補液方面取得了良好效果。
3.4 溶血現象的觀察 ABO 血型不相容腎移植術后易出現溶血,術后每日化驗血、尿常規和腎功能、凝血、血型抗體滴度等,密切觀察皮膚是否有出血點或瘀斑及皮膚的顏色、尿液的顏色,并觀察血氧飽和度變化。
3.5 抗體滴度的監測 ABO 血型不相容腎移植術前靜脈輸注利妥昔單抗前后、口服免疫抑制劑前后、血漿置換或雙重濾過血漿置換前后監測抗體滴度。術后2周內每日監測抗A-IgG、抗A-IgM、抗B-IgG、抗B-IgM血型抗體的變化。
3.6 術后并發癥管理
3.6.1 出血 術后病人一般需在腎周留置2 根引流管(上極引流管、下極引流管),應保持引流管通暢,防止受壓、折疊、扭曲,觀察引流液的顏色、性質和量,并做好記錄。密切觀察血壓趨勢、切口敷料滲血情況,經常檢查移植腎區有無腫脹、壓痛,在排除排斥反應后應警惕出血的可能。
3.6.2 尿瘺 術后早期有引流管者表現為引流液較正常情況下明顯增多,顏色呈淡紅或淡黃色,尿管引流尿液明顯減少。留置導尿管期間,保持尿管通暢,防止導尿管的扭曲、折疊、脫落。拔除尿管后囑病人勿憋尿,每小時督促病人排尿,并密切觀察切口敷料滲液情況。
3.6.3 排斥反應 排斥反應包括超急性排斥反應、加速排斥反應、急性排斥反應、慢性排斥反應4 種。其中,急性排斥反應最常見,多發生在移植術后早期,由于各種新型免疫抑制劑的不斷推出,其發生率逐漸下降,目前1 年內急性排斥反應發生率低于15%[5]。臨床表現為尿量突然減少、血壓升高、體溫升高、移植腎區腫脹壓痛、血肌酐升高等,腎移植術后應合理使用免疫抑制劑,加強監測病人他克莫司血藥濃度,及時調整免疫抑制劑的用量,注意觀察病情、傾聽病人主訴、及時發現排斥反應的先兆癥狀,盡早采取抗排斥措施,并做好移植術后健康宣教。
3.6.4 感染預防 腎移植術后各種感染是導致手術失敗和病人死亡最常見的原因之一,早期感染率為40%~78%[6]。
3.6.4.1 肺部感染 體溫是監測感染的敏感性指標,術后4 h 測1 次體溫。病人術后5 d 內需臥床休息,給予鹽酸氨溴索注射液(30 mg,每日2 次)靜脈輸注及0.9%氯化鈉注射液(5 mL,每日3 次)霧化吸入,并給予電按摩治療促進排痰,并指導病人臥床期間適當的床上活動,預防墜積性肺炎的發生。術后5 d 下床稱體重,在護士協助下適當活動,循序漸進。做好口腔護理,采用益口漱口液含漱,每日3 次,定期行痰培養、咽拭子培養。
3.6.4.2 尿路感染 尿路感染是術后最常見的感染并發癥,病人術后第1 年的發生率達74%[7],且術后第1個月內首發尿路感染多源于醫院獲得性感染[8]。術后常規使用抗生素預防感染,注意觀察固定輸尿管支架管的牽線有無脫出,如脫出應及時剪掉拖出尿道外口的縫線,以防逆行感染。帶線的移植腎腎盂輸尿管支架管一般于術后2~3 周拔除,無線的于術后2 個月在膀胱鏡下拔除。留置尿管期間做好尿道口的護理,定期行尿常規檢查、尿培養,及時發現和診斷泌尿系統感染。腎功能恢復良好者,應盡早拔除尿管,我中心通常在術后第5 日拔除尿管。
3.6.4.3 切口感染 腎移植術后免疫力低下,使得病人切口愈合及抗感染能力下降,注意保持切口敷料清潔干燥,嚴格執行換藥流程及無菌操作,拔除引流管前定期行引流液培養,行床旁彩色多普勒超聲檢查時預防切口交叉感染。
3.7 飲食管理 病人術后常規禁飲食,待腸蠕動恢復、肛門排氣后可進流食、半流食過渡到普食。由于激素的應用可影響血糖水平,術后應嚴格限制糖的攝入。飲食宜清淡易消化,給予適當優質蛋白質,加強營養,促進切口愈合。禁食菌類(如香菇、木耳等)、紅棗、人參、海參等提高免疫力食物及提高鈣調磷酸酶抑制劑血藥濃度的水果,如柑橘類。每日稱體重,注意維持體重在標準范圍內,有利于維持血中他克莫司濃度。
3.8 延續護理 延續護理的關鍵是降低病人出院后并發癥發生率,提高病人的生活質量。我院利用醫院信息系統建立病人隨訪信息庫,對腎移植病人實施延續護理,病人出院當天將病人信息導入隨訪系統,設置隨訪提醒時間,分別于第1 周、第2 周、第3 周、第5 周、第7 周、第10 周、第13 周各1 次,以后每個月1 次,1 年半后每2 個月1 次。可根據病人病情需要隨時調整隨訪時間。
4 小結
ABO 血型不相容腎移植術關鍵是術前盡可能清除體內的抗A、抗B 血型抗體,并抑制血型抗體的反彈。由于ABO 血型不相容腎移植術受者多次行血漿置換或雙重濾過血漿置換,導致凝血因子丟失,因此,術前血漿處理過程中、術中、術后要嚴密監測血漿鈣離子水平、血常規及凝血功能相關指標[9]。ABO 血型不相容腎移植在擴大供者的范圍和減少移植的等待時間等方面的優勢,將成為尿毒癥病人解決供腎來源的又一新的途徑。我院從心理護理、病室管理、術后監護、溶血現象觀察、抗體滴度監測、術后并發癥管理、飲食管理及延續護理等方面進行全方位、個體化、精細化的護理管理,取得了良好的效果。

