廣東省中藥配方顆粒抽檢結果的質量和相關分析*
胡碧波,黃俊忠,張 莉,陳 旻,李杏芳,劉敏敏
(廣東省藥品檢驗所,廣東 廣州 510663)
中藥配方顆粒是用符合炮制規范的傳統中藥飲片作為原料經水提、分離、濃縮、干燥、制粒而成的一種顆粒狀制劑,其性味、功效與原中藥飲片一致,可根據臨床復方配伍,調劑定量分裝,又稱為“免煎顆粒”[1-3]。截止目前,國家中醫藥管理局一共批準了6家企業全國試點單位,共開展了600余個品種的配方顆粒研制,在臨床中的應用越來越廣泛。本研究以廣東省中藥配方顆粒抽驗數據為基礎,結合對10個品種的探索性研究進行了質量分析,并提出了相關建議,以更好地發揮中藥配方顆粒的效用。
1 資料與方法
1.1研究對象 2016—2018年廣東省藥品抽檢中藥配方顆粒266批次,涉及54個品種,4家生產企業,均在醫療機構進行抽樣,2018年為廣東省第1次開展中藥配方顆粒專項抽檢工作。2016—2018年廣東省中藥配方顆粒各企業抽檢基本信息見圖1。
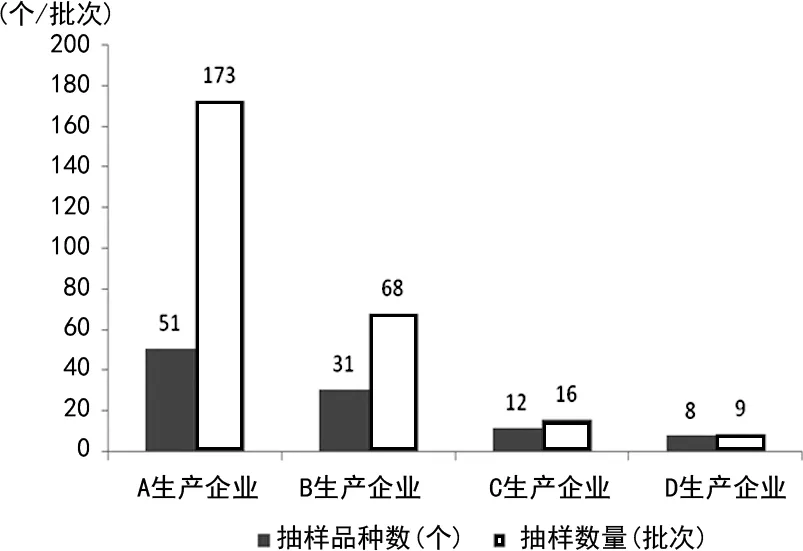
圖1 2016—2018年廣東省中藥配方顆粒各企業抽檢基本信息
1.2方法
1.2.1標準檢驗 標準檢驗是按各企業執行標準開展檢驗。標準檢驗結果雖然可在一定程度上反映產品質量,但難以發現產品中潛在的質量問題,也無法全面評價產品質量。
1.2.2探索性研究檢驗 探索性研究檢驗是對未執行《廣東省中藥配方顆粒標準》的生產企業品種按《廣東省中藥配方顆粒標準》進行評價,同時根據實際情況對含量測定按實驗室擬定方法進一步研究。2018年專項抽檢工作除按標準檢驗外,還選取了白芍配方顆粒等10個品種進行探索性研究檢驗。
2 結 果
2.1抽檢結果 266批樣品中符合規定259批,合格率為97.37%,不合格7 批,不合格率為2.63%。2018年專項抽檢工作檢驗的10個品種、80批次樣品均符合規定,合格率為100.0%;按實驗室擬定方法進行標準提高檢驗,新增含量測定方法,19批樣品不符合規定,不合格率為23.8%。
2.2存在問題 中藥配方顆粒存在現行標準相對較簡單,且同一品種存在多個檢驗標準和制劑規格相差較大等現象,臨床推薦劑量不同、中藥飲片質量和制備工藝等問題。見表1、2。

表1 不合格樣品信息

表2 不合格樣品規格(臨床推薦劑量)
3 討 論
3.1發現的主要問題 本研究通過對白芍配方顆粒等10個品種探索性研究的結果進行分析發現,中藥配方顆粒存在質量標準相對簡單且不統一、臨床推薦劑量不同、中藥飲片質量和制備工藝等問題。
3.1.1標準不統一 目前,中藥配方顆粒標準多為企業自己或委托科研單位參照《中國藥典》所制定,各自執行企業標準或地方標準,出現同一品種執行多個質量標準的現象。如本研究抽檢的黃芩配方顆粒,涉及4個生產企業,執行3個不同標準,分別為《廣東省中藥配方顆粒標準》(第一冊)、《廣西壯族自治區中藥配方顆粒質量標準》(第一卷)和生產企業中藥配方顆粒質量標準。沒有全國統一質量標準、無法對各品種產品質量進行統一評價。
3.1.2標準相對簡單 目前,中藥配方顆粒質量標準多采用薄層色譜法、高效液相色譜法測定中藥配方顆粒的指標成分,與中藥材比較,配方顆粒的質量標準相對簡單,單純的指標成分的定性和定量無法有效控制配方顆粒的質量[4];而有些品種甚至無指標成分含量的測定項目。
3.1.3制備工藝問題 中藥配方顆粒生產企業多依據自身條件與生產經驗探索生產工藝,采用的生產工藝千變萬化,不同的工藝參數,不同的輔料用量,使不同生產企業生產的產品質量存在較大差異[5-6]。由于不同企業生產工藝的不同必將引起產品成分的差異,難以保證臨床療效的一致性、穩定性[7-8]。
3.1.4制劑規格不一致,臨床推薦劑量不同 不同中藥配方顆粒生產企業生產的包裝規格不同,臨床推薦劑量也不同,甚至同一生產企業不同規格其臨床推薦劑量也有差別。如本研究抽檢的黃芩配方顆粒,4家生產企業的制劑規格與臨床推薦劑量:(1)每袋1.8 g,相當于臨床使用飲片量10.0 g(1.0 g顆粒相當于臨床使用飲片量5.6 g);(2)每袋1.0 g,相當于臨床使用飲片量10 g(1.0 g顆粒相當于臨床使用飲片量10.0 g);(3)1.0 g配方顆粒相當于臨床使用飲片量6.7 g;(4)每克濃縮顆粒相當于黃芩3.0 g(1.0 g配方顆粒相當于臨床使用飲片量3.0 g);(5)每袋2.0 g,相當于飲片10.0 g(10 g顆粒相當于臨床使用飲片量5.0 g)。(2)項的臨床推薦劑量是(4)項的3.3倍。制劑規格不統一,臨床推薦劑量不同,不便于醫生與患者準確地掌握藥物使用劑量[3]。
3.1.5中藥飲片的質量問題 中藥飲片是中藥配方顆粒生產的原料藥,其質量的好壞將會直接影響產品質量[9-11]。本研究在探索性研究檢驗中發現,不同生產企業間同一品種按自行擬定方法進行含量測定,結果相差較大,與不同企業原料藥來源不同有著重要的關系。中藥配方顆粒的生產需嚴格控制原料藥的來源,以保證中藥飲片質量。
3.2建議
3.2.1建立統一規范的國家標準,開展提高配方顆粒標準研究 中藥配方顆粒的質量標準研究已有20余年,但至今尚未正式出臺中藥配方顆粒國家標準。2019年11月國家藥監局綜合司公開征求《中藥配方顆粒質量控制與標準制定技術要求(征求意見稿)》意見,全面啟動了中藥配方顆粒國家標準研究,規定了原輔料、生產工藝和標準制定的要求。要求應建立與藥效相關的活性成分或指標成分的含量測定項,并采用指紋圖譜或特征圖譜等方法進行整體質量評價,必要時可建立生物活性評價方法。這對于補充現行質量標準的缺失、促進標準統一、提高產品質量均具有重要作用。
3.2.2開展臨床療效一致性研究 中藥配方顆粒作為傳統中藥飲片的補充,給患者帶來了更多的選擇和方便。多項臨床研究表明,中藥配方顆粒在治療多種疾病方面與傳統中藥飲片具有更好或同等療效[3,12-14]。但仍是醫務人員與患者最關心的問題。目前,爭議較大的問題在于中藥配方顆粒單煎與中藥湯劑合煎在化學成分和臨床療效方面是否一致[15-16]。中藥煎煮方式多樣,各種中藥飲片混合煎煮是否會產生新的有效成分。因此,建議中藥配方顆粒生產企業開展臨床療效一致性研究,解決在臨床使用方面的困惑。
3.2.3加強生產過程控制 中藥配方顆粒質量與其生產工藝密切相關,在配方顆粒制備過程中應以標準湯劑作為對照,采用主成分含量、指紋圖譜相似度評價系統等進行質量一致性評價,對中藥材、中藥飲片、中間體、中藥配方顆粒指紋圖譜的整體信息(包括色譜峰的峰數、峰位及峰高或峰面積比值等)進行分析,并明確各環節相似度量值傳遞規律。嚴格監管從原材料至成品整個生產環節的質量,從而保證中藥配方顆粒質量的可控與穩定。
綜上所述,中藥配方顆粒是傳統飲片改革的一項科研成果,比服用傳統中藥湯劑更方便,但在今后的發展中需更多地關注其不足之處,建議改進工藝,嚴格對每個環節進行質量控制,開展提高標準研究,建立統一國家標準,逐步實現生產的標準化、產業化和國際化。

