Rho激酶抑制劑聯合葛根素通過抑制TGF?β1/Smads信號通路和炎癥反應來減輕缺氧誘導肺動脈高壓對肺血管的損傷
陳晨 張妍蓓
1安徽醫科大學第一附屬醫院老年呼吸與危重癥(合肥230022);2安徽省胸科醫院結核科(合肥230022)
許多肺部疾病均能引起肺部持續性的低氧環境,從而發展為缺氧性肺動脈高壓[1-3],死亡率極高[4]。研究發現通過抑制TGF?β1/Smads 通路相關因子的表達能夠緩解缺氧性肺動脈高壓[5],炎癥和重塑會使血管發生永久性的結構改變,而半乳糖凝集素?3(galectin?3,Gal?3)的高表達能夠增加平滑肌細胞的非自然增殖和存活[6]。近年來研究發現Rho 激酶抑制劑法舒地爾在慢性阻塞性肺疾病相關性肺動脈高壓中有一定作用[7]。國內對于中藥治療缺氧性肺動脈高壓的研究越來越多,研究發現黃酮類槲皮素能減輕肺動脈高壓的嚴重程度[8],丹參通過抑制肺動脈平滑肌細胞過度增殖和過度激活RhoA/Rho 信號通路來預防大鼠缺氧性肺動脈高壓[9],葛根素誘導人肺動脈平滑肌細胞線粒體依賴性凋亡[10],但是對于Rho 激酶抑制劑法舒地爾聯合葛根素治療缺氧性肺動脈高壓的研究未見報道。因此研究Rho 激酶抑制劑法舒地爾聯合葛根素通過TGF?β1/Smads 通路和炎癥反應來減輕缺氧誘導肺動脈高壓對肺血管的損傷程度具有重要的意義,對于臨床治療缺氧性肺動脈高壓提供理論依據。
1 材料與方法
1.1 實驗動物與分組選取體質量為180~200 g的SD 大鼠60 只(最后納入實驗的例數,HPH 模型成功率為72%),隨機分成5 組:正常對照組、模型組、葛根素組、法舒地爾組和法舒地爾與葛根素聯合治療組。
將模型組、葛根素組、法舒地爾組和法舒地爾與葛根素聯合治療組大鼠分別放入常壓缺氧艙內缺氧,缺氧期間艙內氧濃度控制在10%,每天缺氧8 h,連續21 d[11]。各組大鼠缺氧放置前30 min進行腹腔注射,葛根素組大鼠注射葛根素注射液20 mg/kg,法舒地爾組大鼠注射法舒地爾注射液15 mg/kg,聯合治療組大鼠注射葛根素注射液20 mg/kg+法舒地爾注射液15 mg/kg,對照組和模型注射相當體積的0.9%NaCl 溶液。
1.2 實驗方法
1.2.1 血流動力學指標的測定將麻醉后的大鼠仰臥位固定在手術板上,用測壓導管沿著大鼠勁外靜脈經右心房插入至右心室及肺動脈,記錄右心室收縮壓(RVSP)、平均肺動脈壓(mPAP)、肺動脈收縮壓(PASP)和肺小動脈楔壓(PAWP)。
1.2.2 右心室肥厚指數的測定開胸取心臟,采集并稱取右心室(RV)和左心室加室間隔(LV+S)的重量,計算右心室肥厚指數(RVHI)=RV/(LV+S)。
1.2.3 HE 染色法將石蠟切片脫蠟至水后,沒入Harris 蘇木素染液,蒸餾水洗后用1%的鹽酸酒精分化,0.6%氨水返藍,伊紅染液中染色。脫水透明后,用中性樹膠封片保存。用光學顯微鏡鏡觀察肺血管形態學變化。
1.2.4 qPCR 檢測法肺組織被迅速分離后放于液氮中。采用Trizol 法提取樣品中總RNA。根據逆轉錄試劑盒說明書進行反轉錄后,擴增目的基因(表1)。
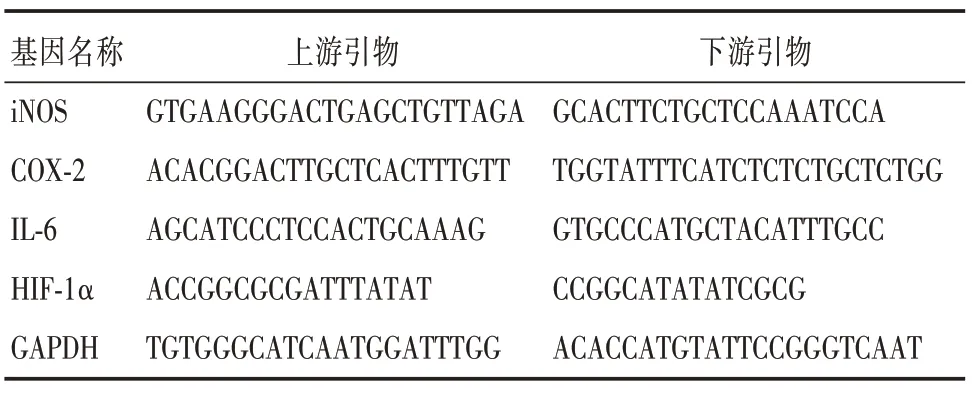
表1 引物序列Tab.1 Primer sequence
1.2.5 Western blot檢測法提取總蛋白,采用SDS?PAGE 分離蛋白。隨后轉印蛋白到PVDF 膜上。5%的脫脂奶粉室溫封閉1 h,一抗(兔抗鼠TGF?β1、Smad2、Smad4 和Smad7 多克隆抗體)4 ℃孵育過夜,二抗(HRP 標記的山羊抗兔)室溫孵育1 h。采用ECL顯色法掃描獲得圖片。通過Image J 軟件對目的條帶進行灰度分析,做統計學分析。
1.2.6 免疫組化檢測法將肺組織放入4 ℃4%多聚甲醛中固定6 h,再放入30%蔗糖4 ℃過夜,然后將組織包埋成石蠟塊,切片、爬片、脫臘后按照免疫組化試劑盒進行免疫組化,置于倒置顯微鏡下觀察。
1.3 統計學方法采用SPSS 20.0 進行統計學分析,值以均數±標準差表示。組間多重比較采用單因素方差分析,采用最小顯著性差異(LSD)檢驗作為多重比較的事后分析。方差不整齊時進行Dunnett′t 檢驗。以P<0.05 為差異有統計學意義。
2 結果
2.1 法舒地爾聯合葛根素對HPH大鼠血流動力學和右心室重構指標的影響模型組RVSP、mPAP、PASP、PAWP和RVHI值明顯高于Sham組(P<0.05)。與模型組、葛根素組和法舒地爾組比較,聯合治療組的RVSP、mPAP、PASP、PAWP 和RVHI 值顯著降低(P<0.05)。見表2。
2.2 法舒地爾聯合葛根素對HPH 大鼠肺動脈血管壁的影響見圖1,對照組組肺動脈血管壁清晰、管壁薄、管腔大、細胞分布均勻、血管周圍無炎性浸潤。與對照組相比,模型組肺動脈血管壁明顯增厚、平滑肌增生、管腔變狹窄、細胞核增多、血管周圍出現炎性浸潤。與模型組相比,葛根素組、法舒地爾組和聯合治療組肺動脈血管壁厚度下降、管腔變小、細胞形態趨于正常、血管周圍炎性浸潤程度下降。
表2 各組大鼠血流動力學和右心室重構指標比較Tab.2 Comparison of hemodynamics and right ventricular remodeling in each group ±s
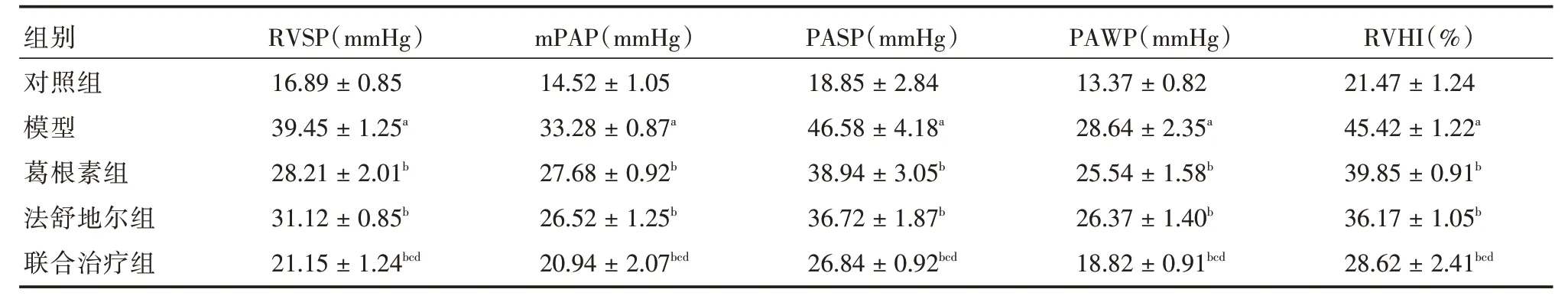
表2 各組大鼠血流動力學和右心室重構指標比較Tab.2 Comparison of hemodynamics and right ventricular remodeling in each group ±s
注:與對照組比較,aP <0.05;與模型組比較,bP <0.05;與葛根素組比較,cP <0.05;與法舒地爾組比較,dP <0.05
組別對照組模型葛根素組法舒地爾組聯合治療組RVSP(mmHg)16.89±0.85 39.45±1.25a 28.21±2.01b 31.12±0.85b 21.15±1.24bcd mPAP(mmHg)14.52±1.05 33.28±0.87a 27.68±0.92b 26.52±1.25b 20.94±2.07bcd PASP(mmHg)18.85±2.84 46.58±4.18a 38.94±3.05b 36.72±1.87b 26.84±0.92bcd PAWP(mmHg)13.37±0.82 28.64±2.35a 25.54±1.58b 26.37±1.40b 18.82±0.91bcd RVHI(%)21.47±1.24 45.42±1.22a 39.85±0.91b 36.17±1.05b 28.62±2.41bcd
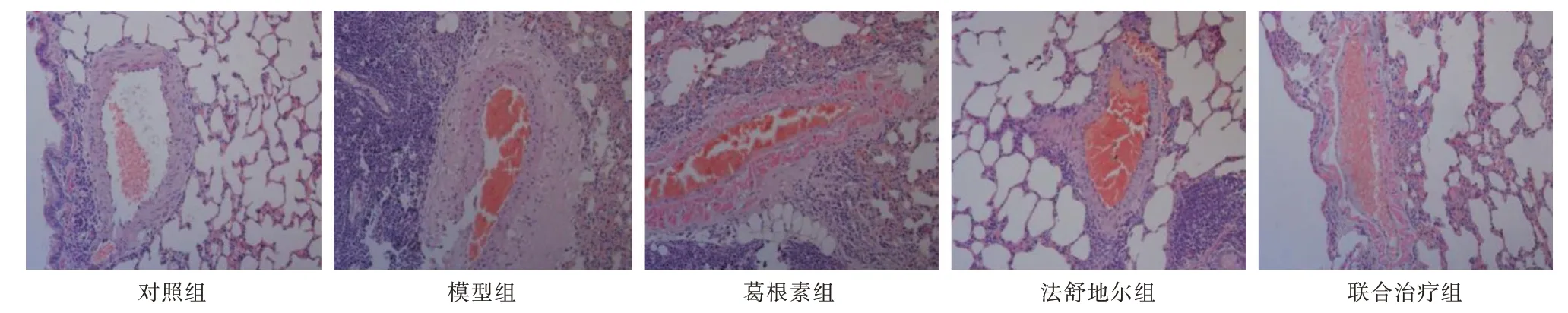
圖1 法舒地爾聯合葛根素對HPH 大鼠肺動脈血管壁的影響Fig.1 Effect of fasudil combined with puerarin on pulmonary artery wall in HPH rats
2.3 法舒地爾聯合葛根素對HPH 大鼠TGF?β1/Smads 通路的影響見圖2,與模型組、葛根素組和法舒地爾組相比較,聯合治療組TGF?β1、Smad2、Smad4 和Smad7 蛋白的表達量顯著下降(P<0.05)。

圖2 法舒地爾聯合葛根素對HPH 大鼠TGF?β1/Smad2/Smad4/Smad7 的影響Fig.2 Effects of fasudil combined with puerarin on TGF? β1/Smad2/Smad4/Smad7 in HPH rats
2.4 法舒地爾聯合葛根素對HPH 大鼠炎癥因子的影響見圖3,與模型組、葛根素組和法舒地爾組相比較,聯合治療組iNOS、COX?2、IL?6 和HIF?1α mRNA 的表達量顯著下降(P<0.05)。
2.5 法舒地爾聯合葛根素對HPH 大鼠Gal?3 的影響見圖4,與模型組、葛根素組和法舒地爾組相比較,聯合治療組Gal?3 蛋白的表達量顯著下降(P<0.01)。
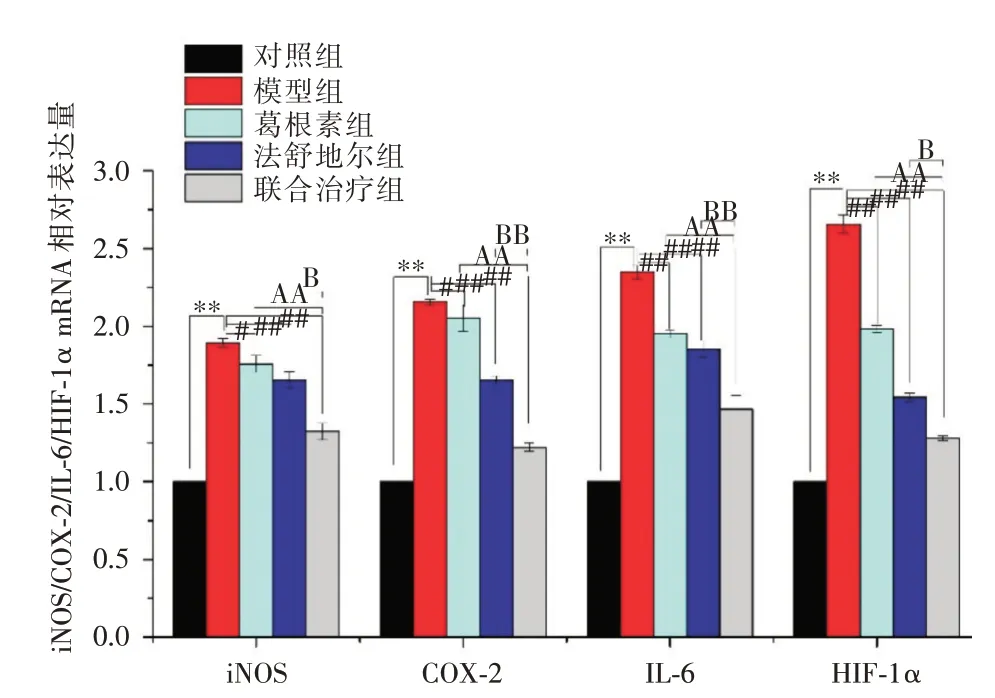
圖3 法舒地爾聯合葛根素對HPH 大鼠iNOS/COX?2/IL?6/HIF?1α mRNA 的影響Fig.3 Effects of fasudil combined with puerarin on iNOS/COX?2/IL?6/HIF?1α mRNA in HPH rats
3 討論
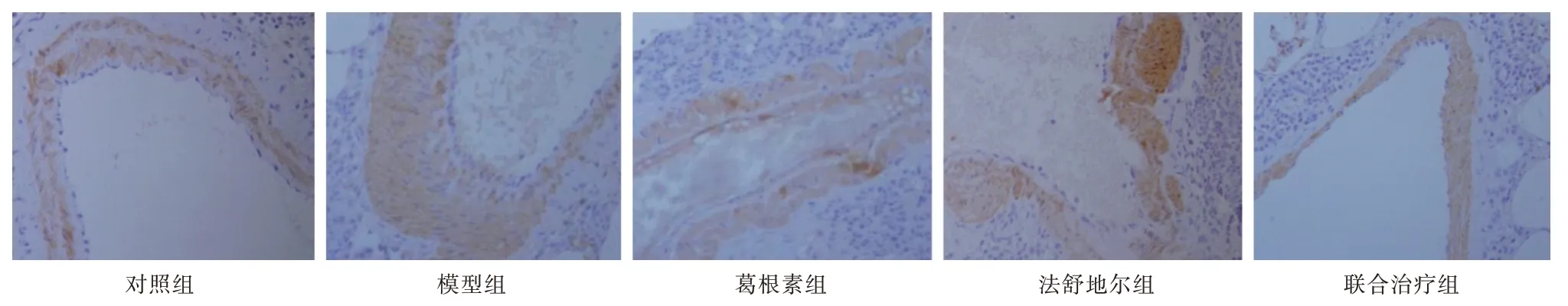
圖4 法舒地爾聯合葛根素對HPH 大鼠Gal?3 蛋白的影響Fig.4 Effects of fasudil combined with puerarin on Gal?3 protein in HPH rats
本研究發現與對照組相比,模型組右心室收縮壓和右心肥厚指數顯著升高,且肺動脈血管壁明顯增厚、平滑肌增生、管腔變狹窄、細胞核增多、血管周圍出現炎性浸潤等,說明缺氧誘導的肺動脈高壓會改變心臟右心室壓力,加重右心室負荷[12-13]的同時,導致肺循環阻力增大[14],這與AGARWAL等[15]的研究結果相似。本研究還發現與模型組、葛根素組和法舒地爾組相比較,聯合治療組HPH大鼠RVSP、mPAP、PASP、PAWP、PVHI 和Gal?3 蛋白的表達量下降、脈血管壁厚度下降、管腔變小、細胞形態趨于正常、血管周圍炎性浸潤程度下降,提示法舒地爾聯合葛根素對大鼠缺氧誘導的肺血管損傷具有很好的修護作用,且效果優于法舒地爾和葛根素單獨治療。Gal?3 的相對表達量能夠預測心血管疾病的發生風險及治療效果[16],其高表達能夠增加平滑肌細胞的非自然增值和存活[17]。
進一步檢測了炎癥相關因子的表達情況,發現模型組炎癥相關因子iNOS、COX?2、IL?6 和HIF?1α mRNA 等炎癥因子的相對表達量顯著升高,而聯合治療組炎癥因子的相對表達量顯著下降,提示模型組大鼠為了保護機體免受低氧誘導肺動脈高壓的損傷炎性因子水平迅速上升[18],而法舒地爾聯合葛根素具有免疫調節和抗炎作用,保護肺血管免受缺氧誘導的肺動脈高壓的損傷[19]。本研究檢測了TGF?β1/Smads 通路相關蛋白的表達,結果顯示聯合治療組TGF?β1/Smads 通路相關蛋白相對表達量下降。缺氧誘導的肺動脈高壓可激活TGF?β1,激活的TGF?β1 首先與受體結合使其活化,受體活化后激活絲/蘇氨酸激酶從而磷酸化其下游信號蛋白Smad2[20],磷酸化的Smad2 與Smad4 結合形成異二聚體,轉入細胞核調節靶基因的表達,即Smad2 與Smad4 復合物的形成及核轉位是該通路活化的標志[21-22]。受體激活性Smad 被激活以后,相對應的靶基因的產物開始調控抑制性Smad7 的表達,構成負反饋調節環路從而抑制Smad 通路信號的轉導,即Smad7 表達的上調也是該通路活化的標志[23]。以上提示,缺氧誘導肺動脈高壓促進TGF?β1/Smads 通路活化來增大肺血管損傷程度,而法舒地爾聯合葛根素通過促進TGF?β1/Smads 通路負反饋調節來保護缺氧性肺血管損傷。
綜上所述,缺氧性肺動脈高壓可促使肺血管重建、導致肺損傷,法舒地爾聯合葛根素能保護肺動脈血管緩解缺氧誘發的肺動脈高壓引起一系列肺血管收縮失常、重建及肺血管壁病理變化,并通過調節TGF?β1/Smads 信號通路和緩解炎癥反應來保護機體減輕損傷,為缺氧性肺動脈高壓的臨床治療提供參考。

