檸檬酸改性白酒糟對Cu、Cd、Cr和Pb的吸附特性研究
張強,劉哲,董威,張萌,陸青
(湖北省環境科學研究院,湖北 武漢 430072)
吸附法是廣泛應用的處理重金屬廢水的一種方法,近年來對稻米殼、花生殼、玉米芯、酒糟、藻類等非傳統吸附劑的研究也日益增多[1-6]。白酒糟,是白酒生產中主要的副產物,具有廣泛來源、環境友好和價格低廉等特點。白酒糟內含有豐富的纖維素、粗纖維和氨基酸,其表面含有羥基、羰基等活性官能團,十分利于物質的吸附,理論上具備了優質生物吸附劑材料的特點[7]。因此,本研究擬以白酒糟為吸附劑材料,并采用檸檬酸對其進行改性,針對工業廢水中常見的重金屬Cu、Cd、Cr和Pb,研究檸檬酸改性白酒糟對模擬廢水中共存的四種重金屬的吸附特性。
1 實驗部分
1.1 試劑與儀器
本研究中配制模擬重金屬廢水替代工業廢水進行實驗,分別采用Cu、Cd、Cr和Pb的單標溶液(國家有色金屬及電子材料分析測試中心)分別配制1 000 mg/L的Cu、Cd、Cr和Pb標準儲備液,然后根據實驗需求用去離子水配制重金屬使用液;檸檬酸、硝酸等均為分析純;白酒糟,取自湖北省十堰市某白酒廠。
PerkinElmer NexlON 350電感耦合等離子體質譜儀;FE20 pH計;PWC214電子天平;DHG-9010電熱恒溫鼓風干燥箱;SHA-C水浴恒溫振蕩器等。
1.2 吸附材料的制備
用自來水清洗白酒糟,然后用去離子水浸泡 24 h,進一步去除其表面殘留的可溶性物質,在 80 ℃ 烘干。以固液比1∶25 g/mL的比例將白酒糟浸入5%的檸檬酸溶液中,在150 r/min條件下攪拌反應4 h。過濾,棄掉上清液,用去離子水反復沖洗,直至改性酒糟至中性,在80 ℃下烘干至恒重,置于干燥器內備用。
1.3 實驗方法
用1 mol/L HNO3的溶液調節反應液的初始pH值,采用200 mL容量的三角瓶作為反應容器,分別加入濃度50 mg/L的4種目標重金屬溶液100 mL和 2 g/L 檸檬酸改性白酒糟吸附劑,放置在25 ℃恒溫水浴中振蕩反應,120 r/min條件下反應4 h。取上清液測定重金屬濃度,每組均進行3個平行實驗。計算檸檬酸改性白酒糟對各重金屬的吸附容量(qe)。
式中qe——改性白酒糟對各重金屬的平衡吸附容量,mg/g;
Ce——達到吸附平衡時各重金屬的濃度,mg/L;
C0——吸附質的初始投加濃度,mg/L;
m——投加的改性白酒糟質量,g;
V——吸附質溶液體積,mL。
2 結果與討論
2.1 pH值的影響
一般而言,pH值對吸附材料活性位點和重金屬離子吸附質化學形態有較大影響。Cu、Cd、Cr和Pb初始濃度均為50 mg/L的模擬廢水,用1 mol/L HNO3調節溶液pH,考察pH值對檸檬酸改性白酒糟吸附性能的影響。改性白酒糟投加量均為2 g/L,吸附反應4 h。改性白酒糟對4種重金屬的吸附去除效果見圖1和圖2。
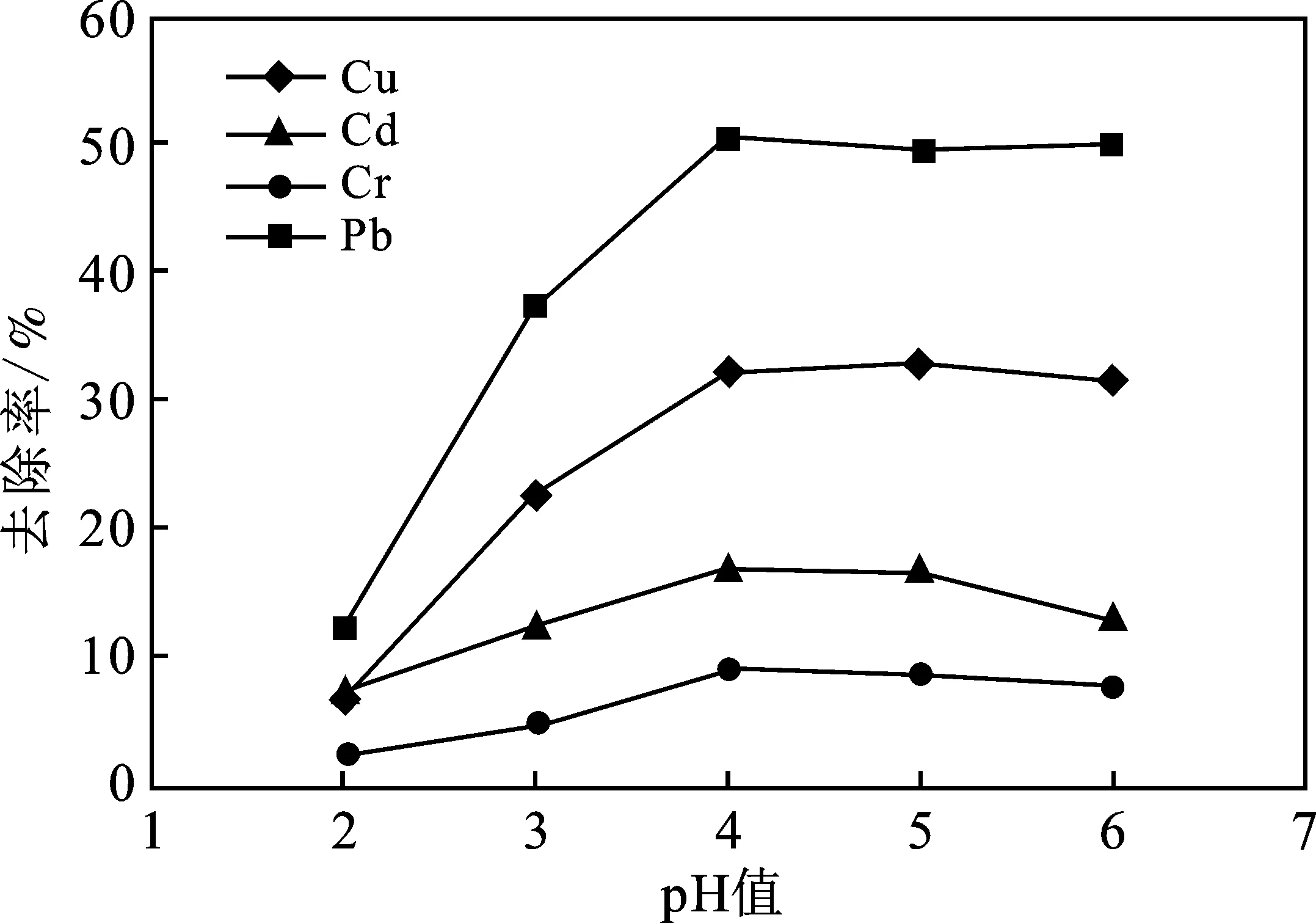
圖1 pH值對去除率的影響Fig.1 Effect of pH on the removal efficiency
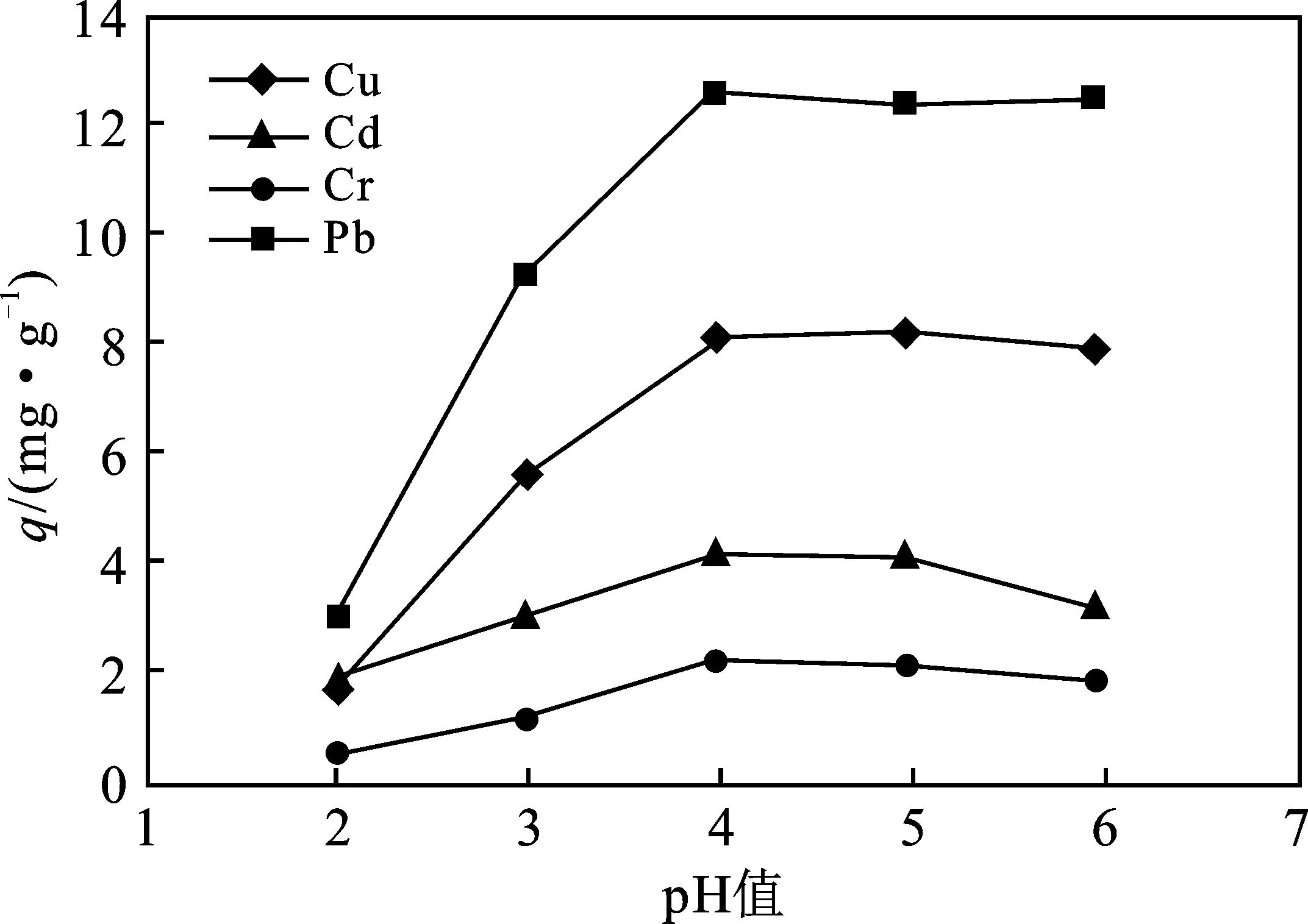
圖2 pH值對吸附量的影響Fig.2 Effect of pH on the adsorption capacity
由圖1可知,隨著pH從2上升,吸附劑檸檬酸改性白酒糟對4種目標重金屬Cu、Cd、Cr和Pb的去除率表現出急速增大而后趨緩或稍降的趨勢,吸附量表現出與去除率相同規律。主要原因在于,當pH值較低時,溶液中大量存在的氫離子可與Cu、Cd、Cr、Pb等重金屬離子產生競爭吸附作用,爭奪占據改性白酒糟表面與孔隙內有限的吸附活性位點,導致對重金屬離子的吸附效果不佳[8]。但隨著pH值繼續增大,除Cu在pH=5時吸附有極微增加,隨即呈略下降趨勢外,Cd、Cr、Pb均在pH=4后即呈略下降趨勢。綜合考慮,將pH均設置為相對較佳時的4。
2.2 吸附質投加量的影響
模擬廢水中重金屬Cu、Cd、Cr和Pb初始濃度均為50 mg/L,以1 mol/L HNO3調節吸附質溶液初始pH至4,投加檸檬酸改性白酒糟,反應4 h。改性白酒糟對4種重金屬的吸附去除效果見圖3和圖4。
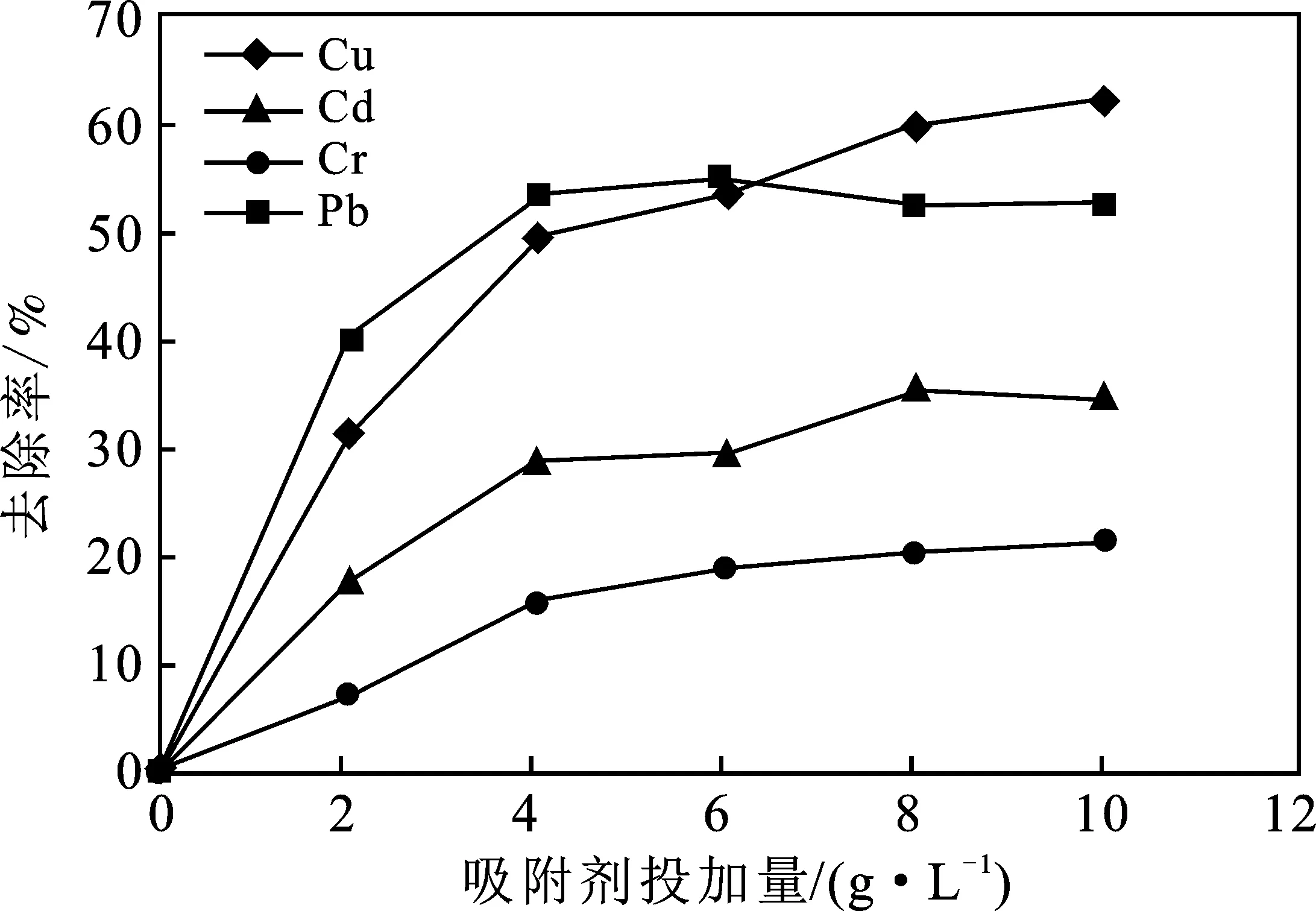
圖3 吸附劑的投加量對去除率的影響Fig.3 Effect of adsorbent dose on the removal efficiency
由圖3可知,隨著吸附劑投加量增大,4種重金屬的吸附去除率均呈上升趨勢,吸附劑投加量 ≥4 g/L時,4種重金屬的吸附率增幅較緩慢或呈略下降趨勢,最終Cu、Cd、Cr、Pb的去除率分別為62%,34.4%,21.2%,52.6%。分析認為,在一定量的重金屬離子情況下,改性白酒糟投加量增大即意味著吸附劑材料總比表面積的絕對增大,隨之其表面與內部可提供的吸附活性位點的絕對數量也就越多,同時由于其吸附行為不具有選擇性,因此在此種條件下4種目標重金屬的吸附率也就隨之相應地升高。
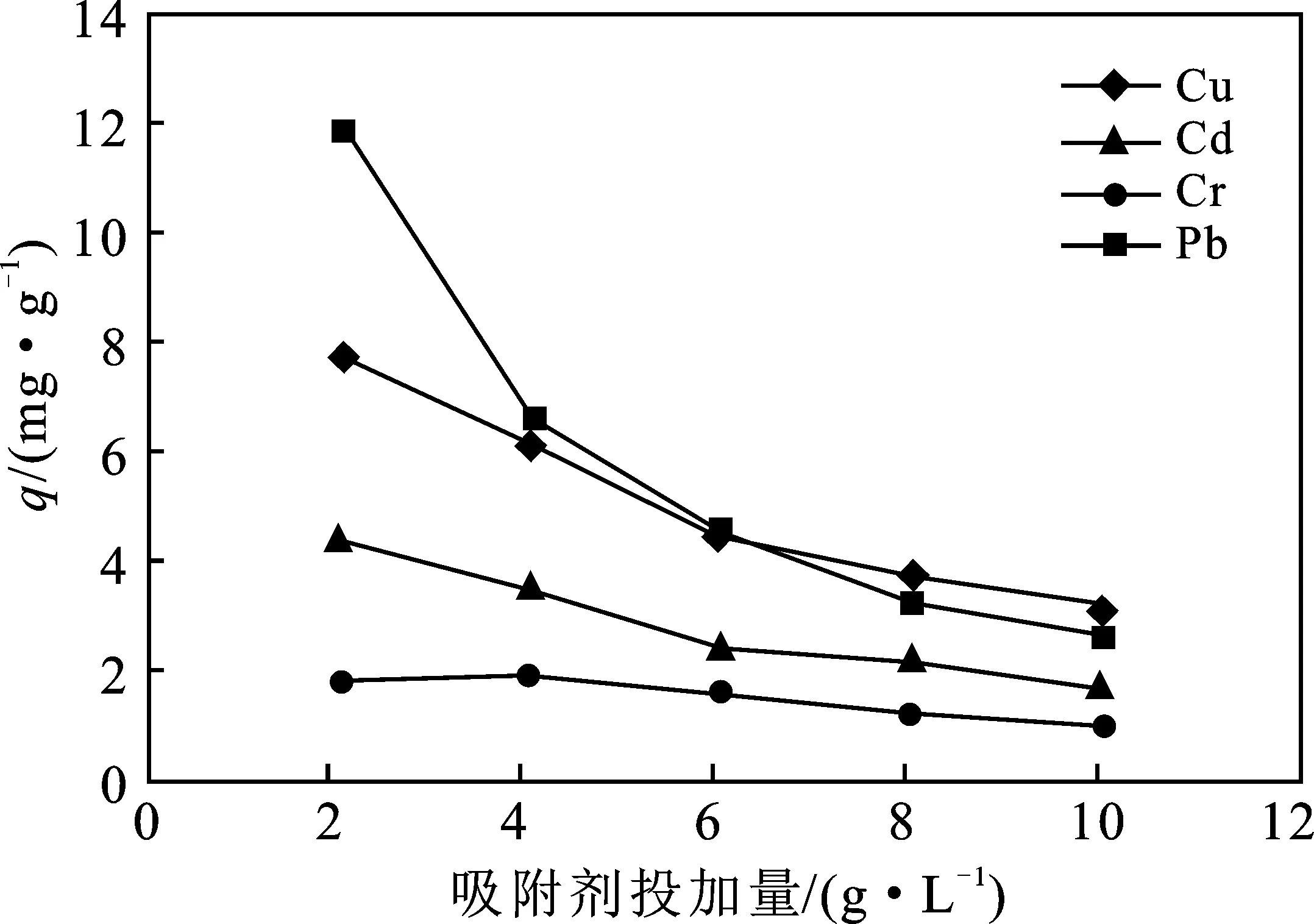
圖4 吸附劑的投加量對吸附量的影響Fig.4 Effect of adsorbent dose on the adsorption capacity
由圖4可知,隨著吸附劑的增加,單位質量的改性白酒糟材料對4種目標重金屬的吸附量均呈現出不同程度的降低。分析認為,在重金屬離子一定的情況下,增大吸附劑的投加量,即意味著單位質量吸附劑表面上可分配吸附的金屬離子量減少,即導致吸附量相對減小。4種重金屬中,Cr相對保持平穩偏緩降趨勢,Cu、Cd、Pb則下降趨勢較為明顯。分析認為,改性白酒糟對Cr的初始吸附效率相對較低,在逐漸增大吸附劑投加量后,大量增加的吸附活性位點與溶液中仍大量存在的Cr發生吸附作用,因此總體上保持了單位質量改性白酒糟對Cr的穩定吸附。而Cu、Cd、Pb則在較低的吸附劑投加量條件下即可被有效吸附去除,增大吸附劑的投加量反而相對降低了單位質量吸附劑所吸附的重金屬量。
綜上,在改性白酒糟投加量>4 g/L以后,其對Cu、Cd、Cr、Pb等4種重金屬的吸附率增長總體趨于平緩,且其對4種目標重金屬的吸附量是一直呈下降的趨勢。因此,在后續的優化實驗中檸檬酸改性白酒糟的投加量均設置為4 g/L。
2.3 吸附動力學[9]
Cu、Cd、Cr、Pb初始質量濃度均為50 mg/L,改性白酒糟投加量均為4 g/L,反應時間對吸附效果的影響見圖5和圖6。

圖5 反應時間對去除率的影響Fig.5 Effect of react time on the removal efficiency
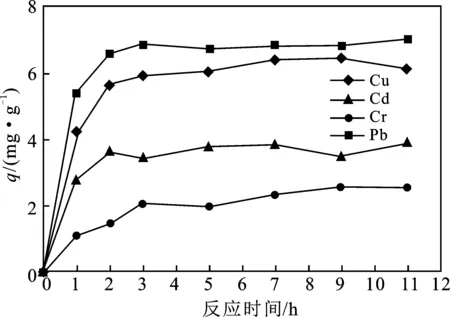
圖6 反應時間對吸附量的影響Fig.6 Effect of react time on adsorption capacity
由圖5和圖6可知,改性白酒糟對Cu、Pb、Cd、Cr的吸附均在1~2 h內快速發生,反應3 h時,4種重金屬的吸附反應均幾乎達到平衡。改性白酒糟對Cu、Cd、Cr、Pb的吸附在前2 h內應是在改性酒糟表面快速發生,隨著其表面上活性吸附位點被重金屬離子占據而快速達到飽和狀態。隨后溶液中大量存在的重金屬離子進一步進入酒糟內部的孔隙結構中,由于受粒子內部傳質阻力的影響,此時發生擴散與吸附的作用變緩,直至逐漸達到平衡。因此,吸附反應時間取3 h。
一般常用準一級吸附動力學模型和準二級吸附動力學模型來研究固相吸附的動力學原理。就模型原理而言,前者是基于擴散是吸附反應的速控步驟的假設,吸附速率與平衡吸附量和瞬時吸附量之間的差值成正比。而后者則是基于固相吸附反應的吸附速率主要是受到化學吸附機理控制的假設,而這個過程往往都會涉及到固相吸附劑與液相吸附質之間的電子轉移或共用等機理[10]。本研究采用準一級和準二級模型對實驗數據進行擬合,研究檸檬酸改性白酒糟對目標重金屬的吸附機理。
準一級動力學方程[11]:
ln(qe-qt)=lnqe-k1t
準二級動力學方程[12]:
式中qe——平衡吸附容量,mg/g;
qt——t時刻吸附容量,mg/g;
k1——準一級吸附速率常數,min-1;
k2——準二級吸附速率常數,g/(mg·min)。
分別以ln(qe-qt)對t、t/qt對t作圖,并對所有數據進行線性回歸分析,計算動力學參數和其它參數,結果見表1。
由表1可知,檸檬酸改性白酒糟對Cu、Pb、Cd、Cr的吸附過程用準二級動力學模型擬合效果相對更好,其相關系數幾乎都在0.99以上(除Cr的R2為0.987 6外),均優于準一級動力學模型擬合的相關系數。故可用準二級動力學模型來描述改性酒糟對Cu、Pb、Cd、Cr的吸附過程,理論平衡吸附量(qe2)分別為6.43,3.84,2.96,7.02 mg/g,與實驗得到的平衡吸附量(qea)較為一致和接近。基于兩模型的基本原理可知,準一級動力學模型一般更適合用于表征固相吸附反應的初始階段,而準二級動力學方程則能更好地模擬描述吸附反應的全過程,因而采用準二級動力學方程取得更好的擬合結果,并且可進一步推測認為物理擴散與化學吸附作用應是共存于檸檬酸改性白酒糟吸附Cu、Pb、Cd、Cr的過程中,而且該過程應當是以化學吸附反應為主的。
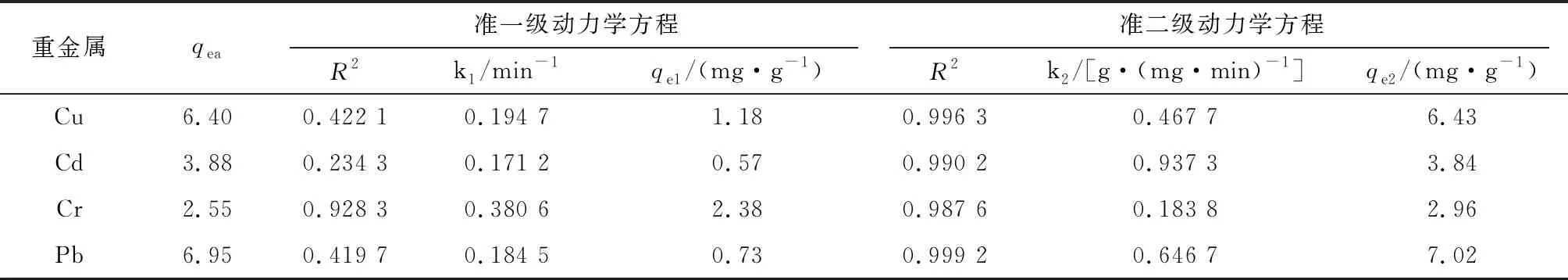
表1 動力學參數擬合結果Table 1 The kinetic parameters of adsorption process
2.4 吸附等溫線
Cu、Cd、Cr、Pb初始質量濃度分別為20,40,60,80,100,120 mg/L,改性白酒糟投加量為4 g/L,反應時間為3 h。吸附質初始濃度對吸附效果的影響見圖7和圖8。
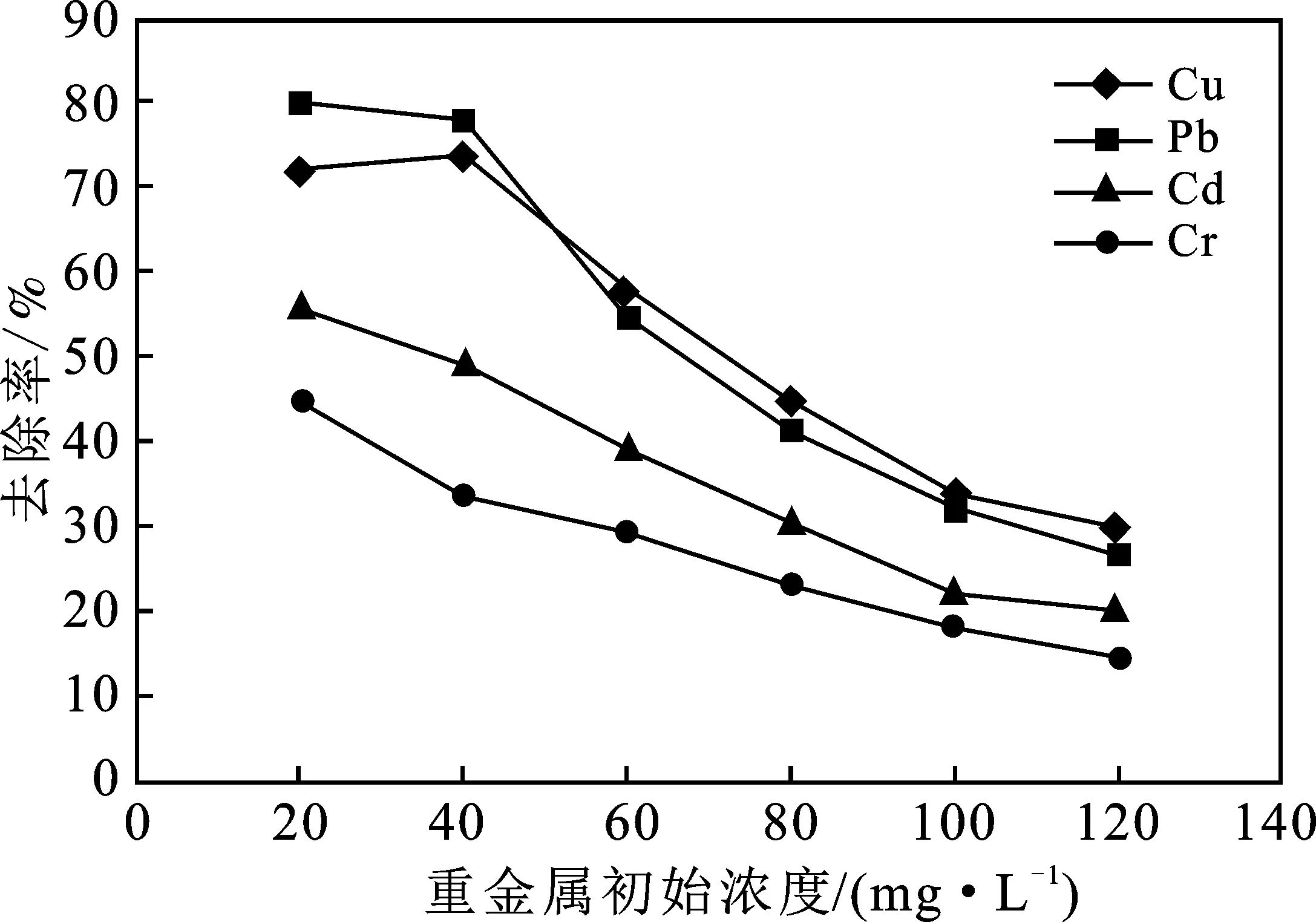
圖7 重金屬吸附質初始濃度對去除率的影響Fig.7 Effect of initial adsorbate concentration on removal efficiency
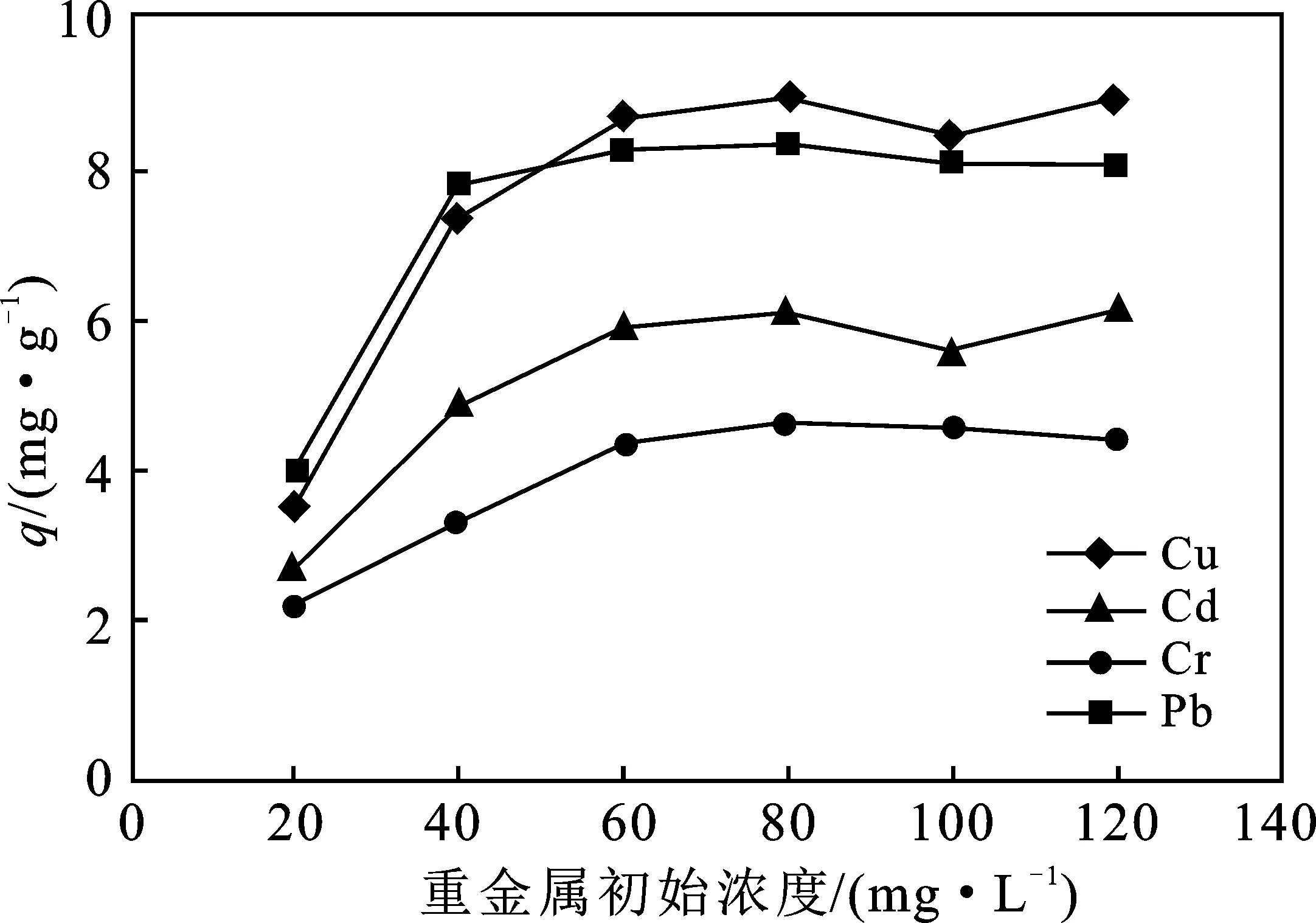
圖8 重金屬吸附質初始濃度對吸附量的影響Fig.8 Effect of initial adsorbate concentration on adsorption capacity
由圖可知,隨著Cu、Cd、Cr、Pb初始濃度增加,吸附劑檸檬酸改性白酒糟對4種重金屬的吸附量呈快速增加狀態。一方面是由于吸附劑的活性位點大量富余,有利于吸附的快速發生;另一方面也可能是較高的重金屬離子初始濃度可減小吸附劑與吸附質之間的傳質阻力,從而增加吸附量[13]。而當重金屬離子的初始濃度>60 mg/L時,改性白酒糟對4種重金屬的吸附量則由于吸附劑活性位點的飽和而趨于平穩。
對實驗數據分別進行Langmuir和Freundlich吸附等溫線擬合,并計算相關參數,結果見表2。
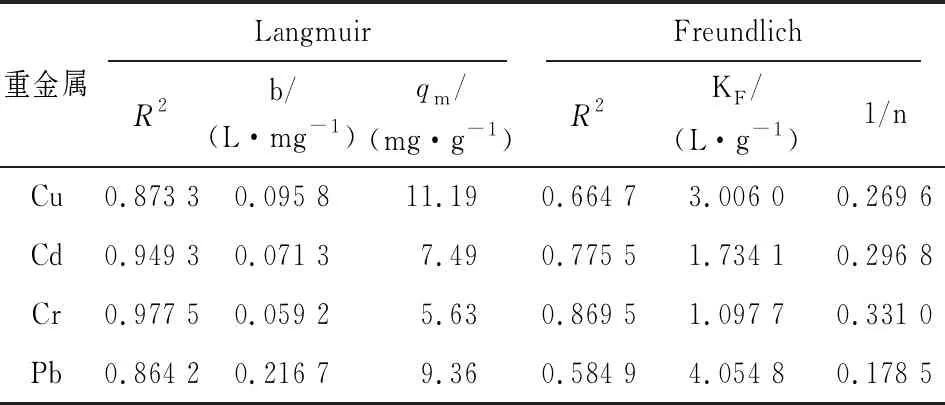
表2 等溫吸附模型參數Table 2 The isotherm parameters of adsorption
式中qe——平衡吸附量,mg/g;
qm——理論飽和吸附容量,mg/g;
Ce——平衡濃度,mg/L;
b——朗格繆爾吸附常數,L/mg;
KF——弗蘭德里希吸附常數,L/g;
n——弗蘭德里希模型常數。
由表2可知,檸檬酸改性白酒糟對Cu、Cd、Cr、Pb的吸附更符合Langmuir等溫線方程,其相關系數R2均相對更高,表明改性白酒糟對4種重金屬的吸附應主要是發生于吸附劑表面的單分子層吸附[16]。在Langmuir方程式,b值一般表示的是吸附劑材料表面及空隙內部的活性吸附位點對吸附質的親和力的大小,由表2可知,幾種目標重金屬中Pb的b值最大,說明檸檬酸改性白酒糟的活性吸附位點與Pb的結合力相較于其他幾種重金屬更強,這與實驗中Pb取得相對更高吸附量的結果一致。此外,通過Langmuir模型擬合得到Cu、Cd、Cr、Pb最大理論吸附量(qm)分別為11.19,7.49,5.63,9.36 mg/g。
在Freundlich方程式中,n值表征的是吸附強度。一般而言,當1/n<1時有利于吸附,1/n值越小,吸附反應越容易正向發生。由表2可知,Cu、Cd、Cr、Pb 4種重金屬的1/n值均在0.1~0.5范圍內,表明檸檬酸改性白酒糟可很好地吸附4種目標重金屬。在Freundlich方程式中,KF可表征吸附能力,表2中Pb和Cu的KF值相對更大,說明改性白酒糟對二者的吸附能力應當更強。
3 結論
(1)改性白酒糟對Cu、Pb、Cd、Cr吸附反應相對最優的條件為:pH值為4,吸附劑投加量4 g/L,反應時間3 h,吸附質初始濃度60 mg/L。
(2)準二級動力學模型可更好地模擬檸檬酸改性白酒糟對Cu、Pb、Cd、Cr的吸附全過程,物理擴散與化學吸附共存于該過程,而且其中以化學吸附反應為主。
(3)Langmuir等溫線可更好地擬合檸檬酸改性白酒糟對4種重金屬的吸附,該過程應為酒糟表面的單分子層吸附,計算得到Cu、Cd、Cr、Pb理論最大吸附量分別為11.19,7.49,5.63,9.36 mg/g。

