西番蓮果皮可溶性膳食纖維對金屬離子的吸附
李晗,馬歆芳,范方宇*,楊代勇,王振興,劉云
1(西南林業大學 林學院,云南 昆明,650224) 2(西南林業大學 生命科學學院,云南 昆明,650224) 3(云南省昆明市生產力促進中心,云南 昆明,650224)
近年來,隨著工業技術的不斷發展,工業廢水排放量增多,Hg2+、Cu2+、Pb2+、Cd2+、Zn2+等重金屬離子向環境中的釋放量不斷增加[1]。這些有害金屬離子易在生物體內富集、不易排出,能通過食物鏈進入人體,積累量達到一定程度時會對人體健康造成危害[1-2]。據報道,Cu2+過量會導致黃疸胰腺炎和貧血癥等,還能引發皮炎和濕疹,嚴重者出現皮膚壞死等;Pb2+過量可導致兒童智力下降,腎病、麻風病和神經痛等;Cd2+過量主要損害腎臟、肝臟等人體代謝器官,導致骨骼變形和紅血球病變等[3]。
膳食纖維(dietary fiber,DF)是從植物細胞壁中提取的一系列非消化營養物質,分為可溶性膳食纖維(soluble dietary fiber,SDF)和不溶性膳食纖維(insoluble dietary fiber,IDF)2大類[4]。研究表明,DF的攝入可有效吸附部分金屬離子。GUO等[4]對大蒜皮SDF體內結合Pb2+能力進行了研究,發現經喂食大蒜皮SDF的小鼠糞便和尿液中鉛排泄量顯著增加,表明大蒜皮SDF對Pb2+結合有積極作用。單平陽等[5]對不同方法提取的花生殼SDF重金屬(Pb2+、As3+、Cu2+)吸附力進行了研究,結果表明花生殼SDF在腸環境吸附重金屬離子效果更好,且經乳酸菌發酵和擠壓膨化處理后的金屬離子吸附力更高。YAN等[6]采用麥麩DF為食品添加劑制作餅干,并對其在小鼠體內結合Cd2+和Pb2+的能力進行了研究,發現與未添加DF的餅干相比,小鼠糞便中Cd2+和Pb2+排泄量分別增加了27.4%和25.2%,表明DF功能餅干在一定程度上能有效吸附金屬離子。
很多果蔬食品加工過程中產生的副產品可用于提取生物活性物質或制備DF,以減少廢棄物污染和資源浪費[7-8]。基于此,本研究以西番蓮果皮為原料,制備西番蓮果皮可溶性膳食纖維(passion fruit peel soluble dietary fiber,PSDF)。探討了PSDF在體外模擬胃腸條件下,PSDF質量、吸附時間、金屬離子初始濃度3個因素對Cu2+、Pb2+、Cd2+三種金屬離子吸附性能的影響,并結合吸附動力學模型(準一級、準二級動力學模型)和等溫吸附模型(Langmuir、Freundlich等溫吸附模型)對吸附機理進行了研究。旨在模擬胃腸環境下為PSDF對Cu2+、Pb2+、Cd2+的吸附性能提供理論支撐。
1 材料與方法
1.1 材料與儀器
西番蓮,云南昆明農貿市場;檸檬酸(分析純),天津市風船化學試劑科技有限公司;α-淀粉酶(10 000 U/g),邢臺萬達生物工程有限公司;木瓜蛋白酶(100 000 U/g),南寧龐博生物工程有限公司;體積分數95%乙醇,天津市致遠化學試劑有限公司;胰蛋白酶(牛胰)、胃蛋白酶(豬胃粘膜),南京都萊生物技術有限公司;硫酸、硝酸,均為分析純,云南楊林工業開發區汕滇藥業有限公司;硝酸銅、硝酸鉛、硝酸鎘,均為分析純,天津大茂化學試劑廠。
DHG-9240A電熱恒溫鼓風干燥箱,上海齊欣科學儀器有限公司;CRT-400高速多功能粉碎機,永康市超然電器有限公司;SB25-12DTDS超聲波清洗器,寧波新藝超聲設備有限公司;DZKW-4電熱恒溫水浴鍋,北京中興偉業儀器有限公司;IKA RV10立式旋轉蒸發儀,南京榮華科學器材有限公司;5804R臺式冷凍離心機,德國艾本德股份公司;AA100型火焰原子吸收分光光度計,美國PerkinElmer公司;SHZ-82恒溫振蕩器,常州智博瑞儀器制造有限公司。
1.2 實驗方法
1.2.1 膳食纖維的制備
參照文獻[9]的方法制備PSDF。西番蓮果皮經洗凈、干燥、粉碎并過60目篩備用。取一定量果皮粉于燒杯中,按料液比1∶26(g∶mL)加入質量分數0.2%檸檬酸溶液,40 ℃、250 W超聲波提取30 min后,加入質量分數0.6%混合酶(α-淀粉酶∶木瓜蛋白酶質量比為1∶1),70 ℃水浴酶解1 h,沸水浴滅酶10 min,5 500 r/min離心10 min。收集上清液,于50 ℃旋轉蒸發儀中濃縮至原體積的1/3,加入濃縮液4倍體積且預熱至60 ℃的95%乙醇醇沉30 min,5 500 r/min離心20 min,沉淀于50 ℃烘干、粉碎過60目篩,得PSDF。
1.2.2 試劑配制
(1)模擬胃液的配制[10]:取1 mol/L HCl溶液16.4 mL,加入10 g胃蛋白酶和800 mL蒸餾水,搖勻,加水定容至1 L。
(2)模擬腸液的配制[10]:取KH2PO46.8 g,加500 mL水溶解,用0.1 mol/L NaOH溶液調pH值至6.8,取胰蛋白酶10 g,加少量水溶解,將上述溶液混合,加水定容至1 L。
(3)金屬離子溶液的配制:分別以Cu(NO3)2、Pb(NO3)2、Cd(NO3)2為溶質,模擬胃液、模擬腸液為溶劑,配制成質量濃度為1 000 mg/L的Cu2+、Pb2+、Cd2+溶液,用于后續實驗。
1.2.3 吸附實驗
吸附實驗分別在模擬胃液和模擬腸液2種體系下進行。
(1)PSDF質量:將一定質量的PSDF放入150 mL錐形瓶中,分別加入20 mL 100 mg/L的Cu2+、Pb2+、Cd2+溶液,37 ℃下120 r/min振蕩吸附120 min。設置PSDF質量為0.10、0.15、0.20、0.25、0.30 g。
(2)吸附時間:將0.1 g PSDF放入150 mL錐形瓶中,分別加入20 mL 100 mg/L的Cu2+、Pb2+、Cd2+溶液,37 ℃下120 r/min振蕩吸附。設置吸附時間為5、10、20、30、60、90、120 min。
(3)金屬離子初始濃度:將0.1 g PSDF放入150 mL錐形瓶中,分別加入20 mL不同質量濃度的Cu2+、Pb2+、Cd2+溶液,37 ℃下120 r/min振蕩吸附120 min。設置Cu2+、Pb2+、Cd2+溶液初始質量濃度為25、50、75、100、125、150 mg/L。
1.2.4 金屬離子濃度測定
吸附后的溶液用0.45 μm微孔濾膜過濾,采用火焰原子吸收儀測定濾液中Cu2+、Pb2+、Cd2+的濃度。吸附量和吸附率分別按公式(1)、(2)計算。
(1)
(2)
式中:q,吸附量,mg/g;Q,吸附率,%;co、c分別為吸附前后溶液中金屬離子的質量濃度,mg/L;v,金屬離子溶液體積,L;m,PSDF質量,g。
1.3 吸附模型
1.3.1 吸附動力學模型研究
準一級和準二級動力學方程假定t時刻PSDF對Cu2+、Pb2+、Cd2+的吸附量qt與吸附達到平衡狀態時的吸附量qe之間的差值是吸附原發力[11]。研究采用準一級和準二級動力學模型描述PSDF吸附Cu2+、Pb2+、Cd2+的動力學過程。準一級、準二級動力學模型的線性形式分別用公式(3)、(4)表示[12]。
ln(qe-qt)=lnqe-k1t
(3)
(4)
式中:qe,平衡吸附量,mg/g;qt,t時刻的吸附量,mg/g;t,吸附時間,min;k1,準一級吸附速率常數,min-1;k2,準二級吸附速率常數,g/(mg·min)。
1.3.2 等溫吸附模型研究
等溫吸附模型可用于描述恒定溫度下PSDF吸附量與不同金屬離子濃度吸附量之間的關系[11]。因此,研究采用Langmuir方程和Freundlich方程來描述PSDF對Cu2+、Pb2+、Cd2+的吸附等溫線。Langmuir方程和Freundlich方程的線性形式如公式(5)、(6)[13-14]所示。
(5)
(6)
式中:qe,平衡吸附量,mg/g;qm,PSDF最大吸附量,mg/g;ce,吸附平衡時溶液中金屬離子質量濃度,mg/L;kL,吸附速率常數,L/mg;kf,PSDF吸附能力的量度;n,吸附強度的量度。
1.4 數據處理
采用Excel 2010軟件進行數據分析和表格繪制,Origin 2017軟件進行模型擬合和圖形繪制。
2 結果與分析
2.1 PSDF質量對吸附量的影響
由圖1可見,模擬胃腸環境中,隨PSDF質量的增加,其對Cu2+、Pb2+、Cd2+的吸附量逐漸減小,但吸附率均呈逐漸增大后趨于平衡趨勢。與PSDF質量為0.10 g相比,PSDF質量為0.30 g時對3種金屬離子的吸附量在模擬胃環境中分別降低了46.47%、41.38%、53.56%,模擬腸環境中分別降低了50.54%、56.67%、62.58%。這是因為金屬離子濃度與PSDF質量之間的比值對其吸附過程產生一定影響[10]。

a-模擬胃環境;b-模擬腸環境圖1 PSDF質量對吸附量和吸附率的影響Fig.1 Effect of PSDF dosage on adsorptive capacities and adsorption rate
PSDF質量較少時,比值較大,PSDF的表面吸附位點有限,更易被金屬離子充分占滿,單位質量的PSDF吸附量增加,但吸附率相對較低。PSDF質量為0.30 g時,在胃腸環境中對Cu2+、Pb2+、Cd2+的吸附率均較高,在模擬胃環境中分別為52.32%、74.73%、17.10%,模擬腸環境中分別為94.38%、85.51%、94.16%。這是因PSDF質量增加時,有更多的吸附位點結合金屬離子[12],從而提高了PSDF對金屬離子的吸附率;同時吸附位置出現空余,導致單位質量的PSDF吸附量出現下降趨勢,造成了PSDF的浪費。
2.2 吸附時間對吸附量的影響
由圖2可見,模擬胃腸環境中,PSDF與Cu2+、Pb2+、Cd2+開始接觸的前5 min吸附速率較快,其吸附量和吸附率隨吸附時間增加均呈現先增大后平緩的趨勢,對金屬離子的吸附均在30 min左右達到平衡狀態。30 min時,PSDF在胃環境中對Cu2+、Pb2+、Cd2+的吸附率分別為32.10%、42.82%、13.30%,平衡吸附量分別為6.206、8.930、2.781 mg/g;腸環境中吸附率分別為62.87%、66.71%、83.50%,平衡吸附量分別為12.554、13.292、16.352 mg/g。30 min后PSDF表面吸附位點均已被金屬離子占據,吸附過程基本達到平衡狀態,此時PSDF可發揮最大限度的吸附效果。
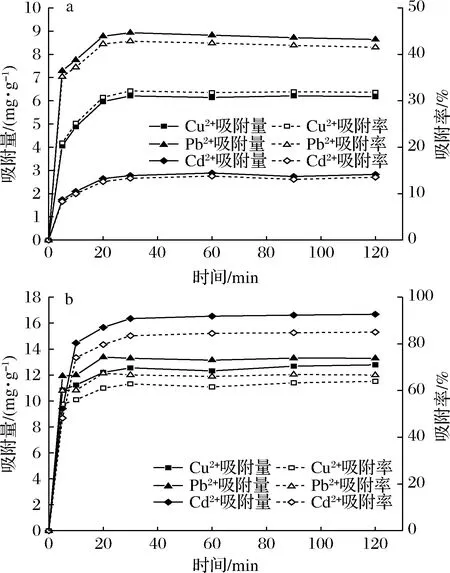
a-模擬胃環境;b-模擬腸環境圖2 吸附時間對吸附量和吸附率的影響Fig.2 Effect of adsorption time on adsorptive capacities and adsorption rate
吸附是一個緩慢進行的過程。吸附初期,金屬離子在PSDF上的吸附主要發生在纖維表面,隨時間延長,金屬離子吸附逐漸由溶液擴散控制轉為內部擴散控制,即金屬離子通過PSDF表面大孔逐漸擴散至其微孔內部[10],且吸附阻力隨PSDF表面吸附金屬離子的增多而增大,致使吸附速率逐級減小[15],吸附量和吸附率緩慢增加直至吸附平衡。
2.3 金屬離子初始濃度對吸附量的影響
由圖3可見,隨著金屬離子初始濃度的增大,PSDF對Cu2+、Pb2+、Cd2+的吸附量呈逐漸增加的趨勢,而吸附率則逐漸下降。初始質量濃度為25 mg/L時,PSDF對Cu2+、Pb2+、Cd2+的吸附量均較小,模擬胃環境中分別為2.355、2.394、0.782 mg/g,模擬腸環境中分別為4.292、2.869、3.695 mg/g,但吸附率均較高。這是因為初始濃度較低時,金屬離子總量較少,能較快與PSDF表面豐富的吸附位點結合[16],提高了利用率,但吸附量相對較低。金屬離子初始質量濃度增至150 mg/L時,吸附量增加,但相較于25 mg/L時,胃環境中吸附率分別降低了22.97%、29.06%、14.84%,腸環境中分別降低了9.56%、10.30%、6.26%。這是因為濃度增加后,PSDF表面吸附位點被占據,吸附能力趨于飽和,吸附過程受到阻礙[16],因此吸附率呈逐漸下降的趨勢。
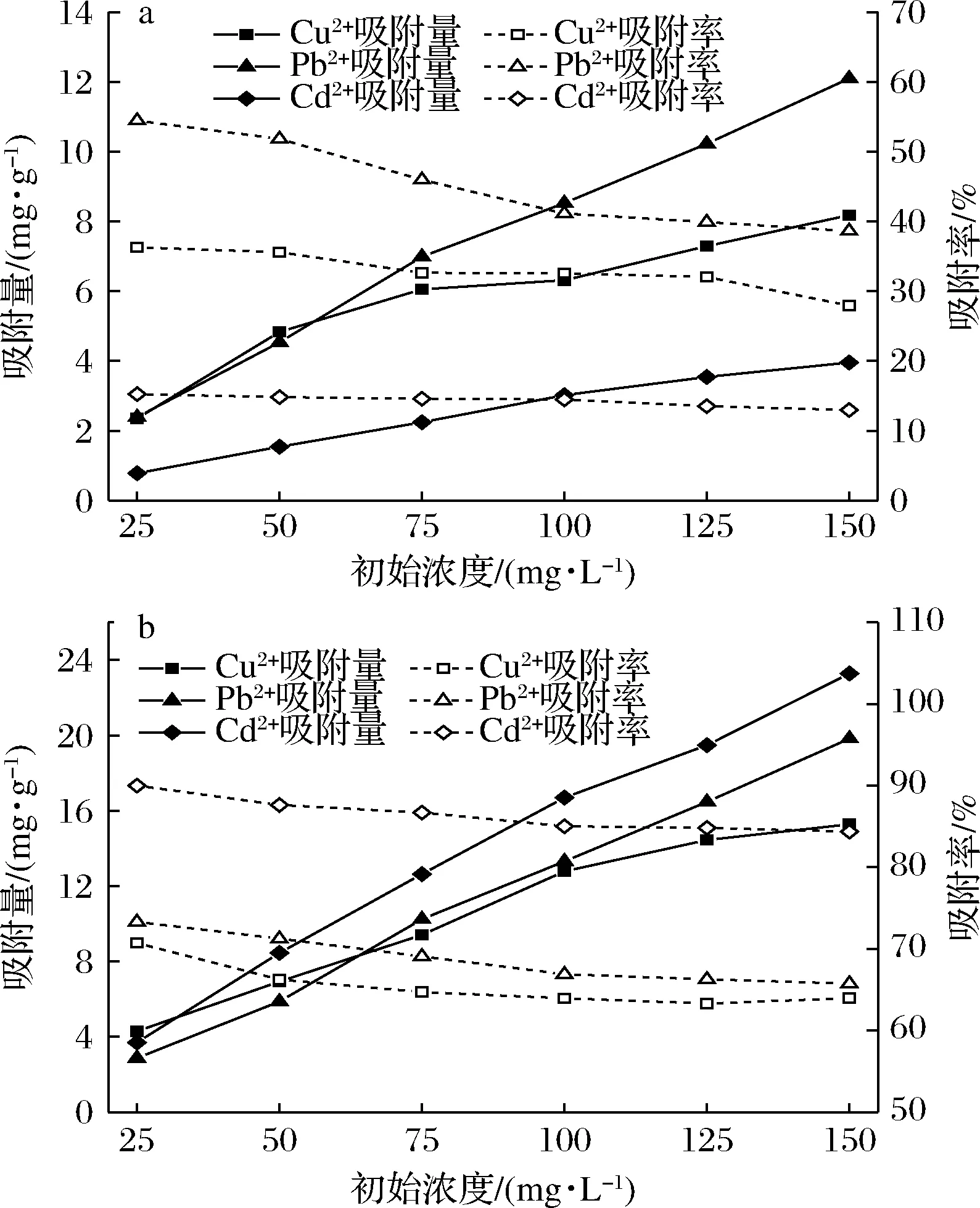
a-模擬胃環境;b-模擬腸環境圖3 金屬離子初始濃度對吸附量和吸附率的影響Fig.3 Effect of initial concentration on adsorptive capacities and adsorption rate
由上述結果可見,PSDF在模擬腸環境中對Cu2+、Pb2+、Cd2+的吸附量均高于胃環境,這與李楊等[17]、單平陽等[5]的研究結果相似,說明腸環境更適合PSDF對金屬離子的吸附。這是因為大部分PSDF在pH 6.8時對金屬離子的吸附能力較強,且金屬離子在腸環境體系下與OH-形成了不溶性沉淀[1]。此外,PSDF對金屬離子的吸附主要依靠化學吸附,也存在物理吸附,而化學吸附主要依靠PSDF中的羧基、糖醛酸的羥基、結合于PSDF上的酚酸和氨基酸等親水基團[17],這些羧基的解離程度與PSDF對金屬離子的束縛有很大的關系[18]。模擬腸環境中,羧基上質子解離增多并帶負電,增大了金屬離子束縛量[19];而模擬胃環境中,羧基質子解離減少,金屬離子束縛量下降。PSDF在胃環境中對金屬離子的吸附可能是金屬離子與溶液中質子共同爭奪羧基、羥基等活性基團[19],兩者占有羧基的量與它們的解離常數和相對濃度有關。
2.4 吸附動力學模型擬合
吸附動力學模型可用于吸附過程中速率變化的研究,并確定吸附的速率控制步驟[20]。為進一步了解PSDF吸附機制,研究對PSDF的吸附效率進行了評價,將模擬胃腸環境下PSDF于不同吸附時間對Cu2+、Pb2+、Cd2+的吸附量分別采用準一級動力學方程和準二級動力學方程進行了擬合。這些模型可通過所作直線的線性驗證擬合效果[21]。
以ln(qe-qt)對t作線性擬合得到準一級動力學線性圖(圖4),以t/qt對t作線性擬合得到準二級動力學線性圖(圖5),并通過相關系數R2判斷PSDF對Cu2+、Pb2+、Cd2+的吸附是否符合動力學模型。
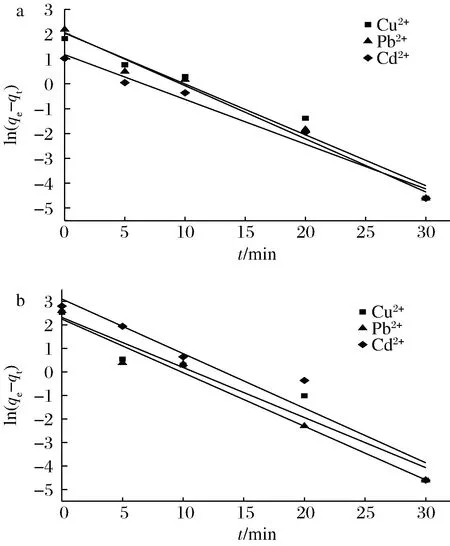
a-模擬胃環境;b-模擬腸環境圖4 PSDF吸附Cu2+、Pb2+、Cd2+的準一級動力學模型擬合線性圖Fig.4 Plot of pseudo first-order adsorption kinetics model of Cu2+,Pb2+,and Cd2+ adsorption on PSDF

a-模擬胃環境;b-模擬腸環境圖5 PSDF吸附Cu2+、Pb2+、Cd2+的準二級動力學模型擬合線性圖Fig.5 Plot of pseudo second-order adsorption kinetics model of Cu2+,Pb2+,and Cd2+ adsorption on PSDF
根據斜率和截距可得到準一級和準二級動力學模型中的未知參數[22],擬合后得到的動力學相關參數見表1。
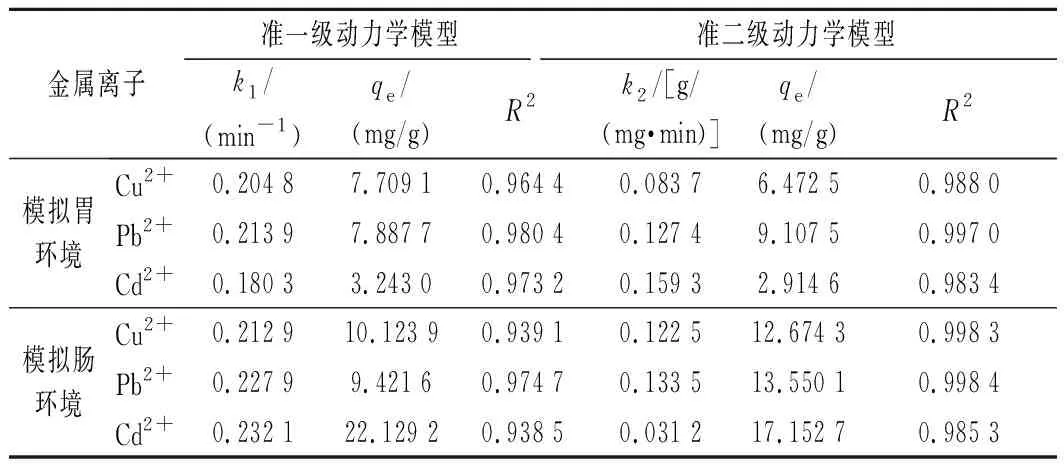
表1 PSDF吸附Cu2+、Pb2+、Cd2+的動力學模型相關參數Table 1 Parameters of kinetics models for Cu2+,Pb2+,and Cd2+ adsorption on PSDF
由圖4、圖5和表1可知,模擬胃腸環境中,PSDF對Cu2+、Pb2+、Cd2+吸附的準一級動力學模型R2范圍為0.938 5~0.980 4,準二級動力學模型R2范圍為0.983 4~0.998 4,這表明準二級動力學模型對吸附實驗數據擬合效果較好。且由該模型計算出吸附平衡時PSDF在胃中對Cu2+、Pb2+、Cd2+的理論吸附量(qe)分別為6.472 5、9.107 5、2.914 6 mg/g,腸中分別為12.674 3、13.550 1、17.152 7 mg/g,與圖2吸附時間對吸附量影響的實驗值更接近,進一步表明其吸附機理符合準二級動力學模型。準一級動力學模型中的吸附為非化學吸附的不穩定吸附;準二級動力學模型則是基于假定吸附速率是受化學吸附機理的控制,吸附劑和吸附質間通過電子共享或交換的化學吸附[12,23]。因此,可以推測Cu2+、Pb2+、Cd2+在PSDF表面活性位點的速率控制步驟主要為化學吸附。綜上可知,PSDF對Cu2+、Pb2+、Cd2+的吸附過程符合準二級動力學模型,且吸附速率控制步驟主要為化學吸附。
2.5 等溫吸附模型
為探究PSDF吸附Cu2+、Pb2+、Cd2+的機理,研究將模擬胃腸環境下PSDF對不同金屬離子初始濃度的吸附量進行了Langmuir和Freundlich等溫線模型擬合。Langmuir方程中以ce/qe對ce作線性擬合得到直線(圖6),1/qm和1/kLqm分別為直線的斜率和截距。Freundlich方程中以lnqe對lnce作線性擬合得到直線(圖7),1/n和lnkf分別為直線的斜率和截距,由此可得到Freundlich方程中的其他參數。Langmuir和Freundlich方程的相關參數見表2。
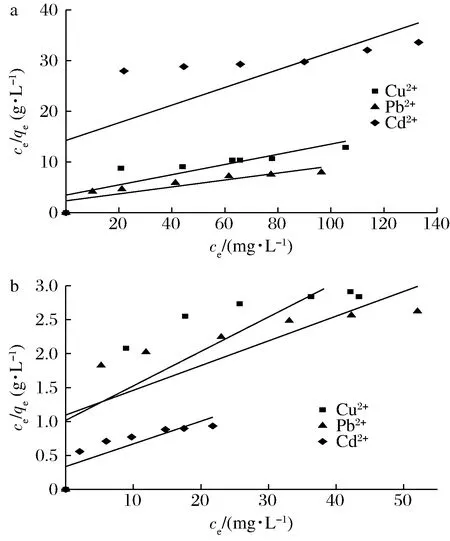
a-模擬胃環境;b-模擬腸環境圖6 PSDF吸附Cu2+、Pb2+、Cd2+的Langmuir等溫式線性圖Fig.6 Plot of Langmuir isothermal equation of Cu2+,Pb2+ and Cd2+ adsorption on PSDF
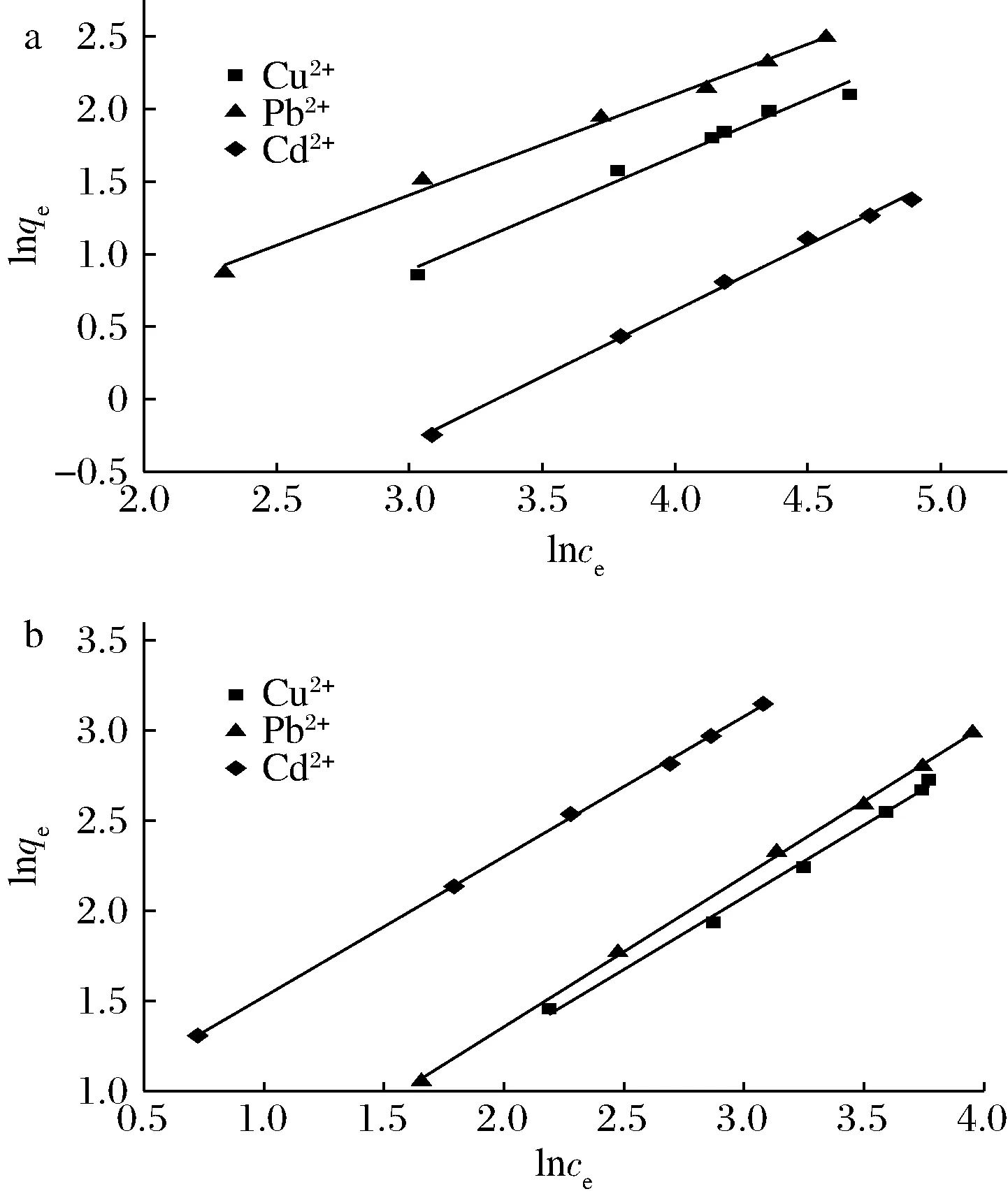
a-模擬胃環境;b-模擬腸環境圖7 PSDF吸附Cu2+、Pb2+、Cd2+的Freundlich等溫式線性圖Fig.7 Plot of Freundlich isothermal equation of Cu2+,Pb2+ and Cd2+ adsorption on PSDF

表2 PSDF吸附Cu2+、Pb2+、Cd2+的等溫吸附模型相關參數Table 2 Parameters of isothermal adsorption models for Cu2+, Pb2+, and Cd2+ adsorption on PSDF
由圖6、圖7和表2可知,Langmuir等溫模型的擬合相關系數R2為0.530 8~0.793 1,Freundlich等溫模型的擬合相關系數R2為0.981 6~0.999 6。因此,PSDF對Cu2+、Pb2+、Cd2+三種金屬離子的吸附行為更符合Freundlich等溫吸附模型。Freundlich模型中,一般認為1/n是一個濃度指數,表示線性程度及吸附機理的差異。n值常用于吸附過程優惠性判斷[21-23]:n>1為優惠吸附;n=1為線性吸附;n<1為非優惠吸附。因此,胃腸環境中PSDF對Cu2+、Pb2+、Cd2+的吸附均為優惠吸附,而腸中的吸附較胃中更接近線性吸附。此外,Freundlich等溫線中的kf值可表示吸附能力強弱。PSDF在胃中對Cu2+、Pb2+、Cd2+吸附的kf值分別為0.230 5、0.510 5、0.048 7,其kf值與圖3胃中PSDF對不同初始濃度金屬離子的吸附量大小順序相同,均為Pb2+>Cu2+>Cd2+。表明PSDF在胃中對Pb2+的吸附能力強于Cu2+和Cd2+。而腸中Cu2+、Pb2+、Cd2+吸附的kf值分別為0.720 8、0.731 3、2.107 3,圖3腸中吸附量大小順序為Cd2+>Pb2+>Cu2+,表明PSDF在腸中對Cd2+的吸附能力更強,對Pb2+和Cd2+的吸附能力則相差不大。且PSDF在腸中吸附Cu2+和Cd2+的kf值均高于胃中,表明PSDF在腸中的吸附能力更好。綜上可知,Freundlich等溫吸附模型對PSDF吸附金屬離子的擬合效果更好,表明PSDF的吸附行為不是簡單的單分子層吸附,其吸附機制既有物理吸附、靜電相互作用,又有金屬離子與PSDF中羧基等活性基團的螯合作用[23-24]。
3 結論
研究對PSDF吸附Cu2+、Pb2+、Cd2+三種金屬離子的機理進行了探索,探討了PSDF質量、吸附時間、金屬離子初始濃度3個因素對吸附過程的影響。結果表明,PSDF對Cu2+、Pb2+、Cd2+的吸附量隨PSDF質量增加而減少,吸附率則先增大后趨于平衡,適當的PSDF質量既可提高PSDF利用率,又可避免PSDF的浪費。PSDF對Cu2+、Pb2+、Cd2+的吸附均在30 min左右達到飽和狀態,在胃環境中的吸附率分別為32.10%、42.82%、13.30%,平衡吸附量分別為6.206、8.930、2.781 mg/g;腸環境中吸附率分別為62.87%、66.71%、83.50%,平衡吸附量分別為12.554、13.292、16.352 mg/g。PSDF吸附量分別隨Cu2+、Pb2+、Cd2+初始濃度增加而增大,吸附率則隨初始濃度增加逐漸下降。PSDF在模擬腸環境中對Cu2+、Pb2+、Cd2+的吸附優于胃環境,吸附量和吸附率更高。吸附動力學和等溫吸附模型擬合結果表明,PSDF對Cu2+、Pb2+、Cd2+的吸附過程符合準二級動力學模型,表明其吸附的速率控制步驟主要為化學吸附;PSDF吸附平衡符合Freundlich等溫模型,相關性良好。

