轉人溶菌酶牛乳營養成分及食用安全研究
程靜然 宋榮榮 戴蘊平 趙春江
摘要 [目的]探究轉人溶菌酶牛乳和非轉基因牛乳的營養成分差異,以及重組人溶菌酶的食用安全性。[方法]通過測定轉基因和非轉基因組2種乳樣乳常規、氨基酸和脂肪酸的含量,比較其成分差異。通過大鼠、小鼠急性經口毒性試驗以及模擬胃腸液消化穩定性試驗檢測重組人溶菌酶的食用安全性。[結果]營養成分檢測結果表明,轉人溶菌酶牛乳和非轉基因牛乳相比,細菌總數偏高,脂肪含量偏低,其他營養成分無明顯的變化;食品安全評估說明重組人溶菌酶屬于實際無毒蛋白,且無潛在的致敏性。[結論]該試驗驗證了轉人溶菌酶牛乳的食用安全性。
關鍵詞 轉基因牛;重組人溶菌酶;牛乳;營養成分;食用安全性
中圖分類號 TS-201? 文獻標識碼 A? 文章編號 0517-6611(2021)11-0147-04
doi:10.3969/j.issn.0517-6611.2021.11.041
開放科學(資源服務)標識碼(OSID):
Study on Nutritional Components and Edible Safety of Milk of Transgenic Cloned Cows Expressing Human Lysozyme
CHENG Jing-ran1, SONG Rong-rong1, DAI Yun-ping2 et al
( 1.College of Animal Science and Technology, China Agricultural University, Beijing 100193;2. College of Biology, China Agricultural University, Beijing 100193)
Abstract [Objective] To explore the nutritional differences between transgenic and non-transgenic milk and the food safety of recombinant human lysozyme.[Method] By measuring the contents of routine, amino acid and fatty acid of two kinds of milk, the difference in composition was compared. The food safety of recombinant human lysozyme was determined by acute oral toxicity test and simulated gastroenteric fluid digestion stability test in rats and mice.[Result]The results of nutritional component detection showed that compared with milk of non-transgenic cows, the milk of transgenic cows has larger number bacteria and lower fat content, but other nutrients have no significant change.Food safety assessment showed that recombinant human lysozyme was a non-toxic protein and had no potential sensitization. [Conclusion]This experiment verified the edible safety of recombinant human lysozyme.
Key words Transgenic cows;Recombinant human lysozyme;Milk;Nutritional components;Edible safety
人溶菌酶(lysozyme)是一種存在于人體正常體液及組織中的堿性多肽,由130個氨基酸組成,對生物體的自身防御起著重要作用[1]。人乳中溶菌酶的含量高、活性強,也是人乳不易敗壞的主要原因。人乳中溶菌酶含量約0.5 mg/mL,比牛、綿羊和山羊乳含量高出1 500~4 000倍,破壞和溶解細菌的能力約為牛乳的300倍,是人乳中的重要抗菌因子,也是動物乳“人乳化”的主要研究對象。人乳中的溶菌酶可破壞大多數革蘭氏陽性菌和少量陰性菌的細胞壁[2-3],有利于嬰兒腸道正常菌群的建立和提高抗病能力。隨著對奶制品消費需求的增加,奶制品的品質也越來越受到人們的關注。利用乳腺生物反應器的方法表達重組人溶菌酶,使生產出的奶含有高抑菌活性的溶菌酶,既有營養功能,又有藥用功能[4]。隨著對轉基因動物的研究越來越廣泛,人們越來越重視轉基因制品的安全性。筆者以先前成功獲得的轉人溶菌酶基因奶牛為研究對象,通過與普通奶牛(非轉基因牛)對照的方式,探明轉基因牛乳與普通牛乳的營養成分及代謝組差異,并對重組人溶菌酶進行了毒理學試驗,進一步探究重組人溶菌酶的安全性。
1 材料與方法
1.1 材料
乳樣采集自中國農業大學試驗基地的1頭轉人溶菌酶奶牛和3頭非轉基因奶牛。重組人溶菌酶由轉基因奶牛乳中純化得到。
1.2 方法
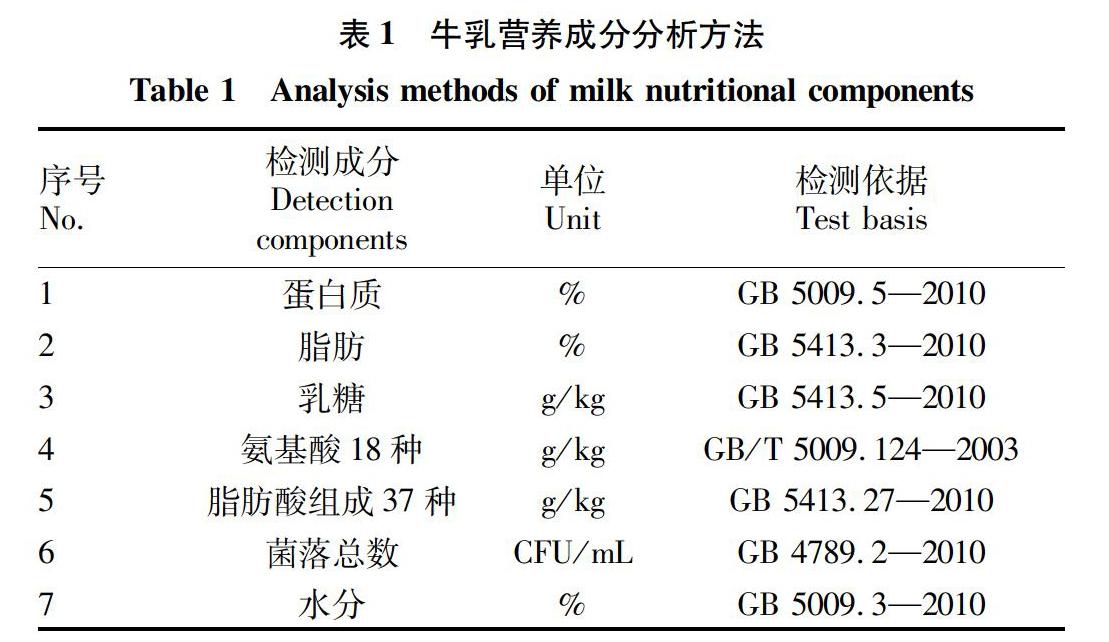
1.2.1 牛乳營養成分分析。牛乳營養成分分析方法見表1。
1.2.2 牛乳代謝組。
乳樣離心(4 ℃,3 000 r/min,5 min),棄沉淀。上清液離心(4 ℃,12 000 r/min,15 min),棄沉淀,重復3次。吸取100 μL上清液,加入新的1.5 mL EP管中,并加入350 μL預冷甲醇。加入10 μL核糖醇,漩渦30 s,冰水浴5 min,離心(4 ℃,12 000 r/min,15 min)。將上清液在真空壓縮器中干燥,將80 μL氧胺鹽試劑加入干燥后的代謝物中,攪拌混勻,在80 ℃烘箱中孵育30 min。加入100 μL BSTFA,70 ℃進行孵育1.5 h,隨機順序上機檢測。結合數據庫LECO-Fiehn-Rtx5,通過ChromaTOF(v4.3x,LECO)軟件對質譜數據進行分析。
1.2.3 重組人溶菌酶急性經口毒性試驗。
1.2.3.1 大鼠急性經口毒性試驗。
依據《食品安全國家標準急性經口毒性試驗》(GB 15193.3—2014)進行重組人溶菌酶的大鼠經口毒性試驗。依據預試驗的結果并且以霍恩氏法進行試驗設計,共設計4個劑量組,劑量分別為2 150、4 640、10 000和21 500 mg/kg。按照體重隨機二步法對大鼠進行分組,雌、雌大鼠各2組,每組各10只大鼠。
在灌胃之前,大鼠需要進行16 h禁食,飲水自由。重組溶菌酶灌胃大鼠時,需要分2次進行,間隔時間為4 h,之后再進行3 h禁食,連續進行14 d的觀察。重組人溶菌酶灌胃大鼠之后,需要對大鼠的臨床情況進行觀察和記錄(如中毒情況、死亡情況等),觀察終點為灌胃后第14天。觀察期間,及時對死亡大鼠進行尸體解剖及組織病理學檢查。試驗終點后,對所有試驗大鼠進行脫頸椎處死,并進行全身解剖進行組織病理學檢查。
試驗結束時統計不同性別大鼠的存活數量、中毒癥狀的嚴重程度和可逆性、死亡、存活及解剖檢查中各種病變的發生頻率。分別計算上述各因素的發生率和灌胃第0、7、14天的平均體重和標準差。
1.2.3.2 小鼠急性經口毒性試驗。
依據《食品安全國家標準急性經口毒性試驗》(GB 15193.3—2014)進行重組人溶菌酶的小鼠經口毒性試驗。依據預試驗結果并且以霍恩氏法進行試驗設計,共設計4個劑量組,劑量分別為4 640、10 000、21 500和46 400 mg/kg。按照體重隨機二步法將小鼠進行分組,雌、雌小鼠各2組,每2組各10只小鼠。在灌胃之前,小鼠需要進行6 h禁食,飲水自由。4 640、10 000、21 500 mg/kg劑量組一次性灌胃小鼠,46 400 mg/kg劑量組分2次灌胃小鼠,間隔時間為4 h,之后再進行1 h禁食,連續進行14 d的觀察。
觀察、記錄和統計方法同“1.2.3.1”。
1.2.4 重組人溶菌酶模擬胃腸液消化穩定性試驗。
依據《轉基因生物及其產品食用安全性檢測模擬胃腸液外源蛋白質消化穩定性試驗方法》(農業部869號公告-2-2007)進行試驗。
按照 19∶1(V/V)的比例將模擬胃(腸)液與重組溶菌酶樣品溶液(對照樣品或受試蛋白)進行混合,并且進行快速旋渦振蕩混勻,在37 ℃下進行水浴并準確計時。分別在0、15 s和2、30、60 min時,迅速轉移200 μL反應液至1.5 mL離心管(含有碳酸氫鈉溶液)中。再加蛋白上樣緩沖液70 μL,進行5 min沸水浴,在室溫下冷卻,進行SDS-PAGE電泳,將電泳后的凝膠進行考馬斯藍染色,脫色,待條帶變清晰,取出凝膠并對圖像進行保存。分別用模擬的胃、腸液對樣品進行消化,消化后的蛋白進行電泳,然后進行蛋白印跡,并保存圖像。
2 結果與分析
2.1 牛乳營養成分分析
轉人溶菌酶牛乳營養成分測定主要包括乳常規、16種氨基酸、25種脂肪酸的測定。
2.1.1 乳常規。
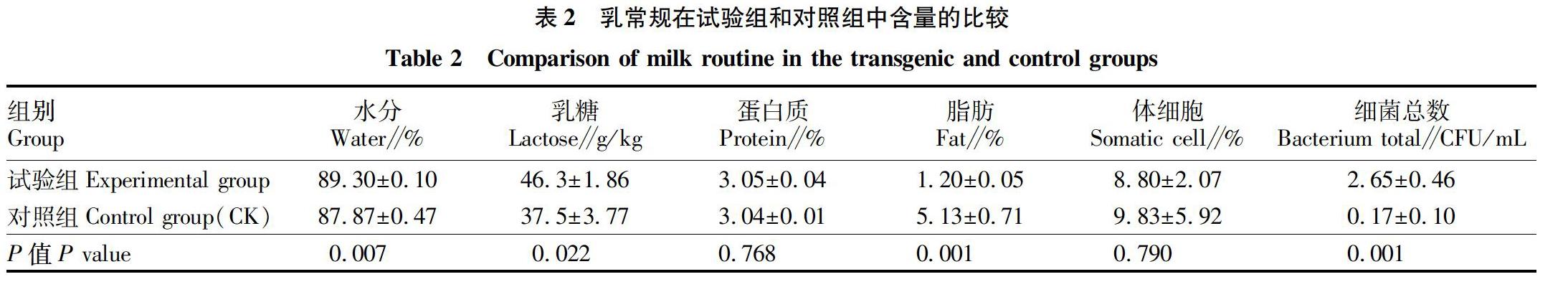
乳常規的測定包括乳中水分、乳糖、蛋白質總量以及體細胞和細菌總數。比較轉人溶菌酶牛乳(試驗組)和非轉基因牛乳(CK)的乳常規測定值,由表2可知,這2組的水分、乳糖、蛋白質含量以及體細胞的數量均無明顯變化,而試驗組的脂肪含量低于CK(P>0.05),其細菌總數則高于CK(P>0.05)。
2.1.2 乳中氨基酸。
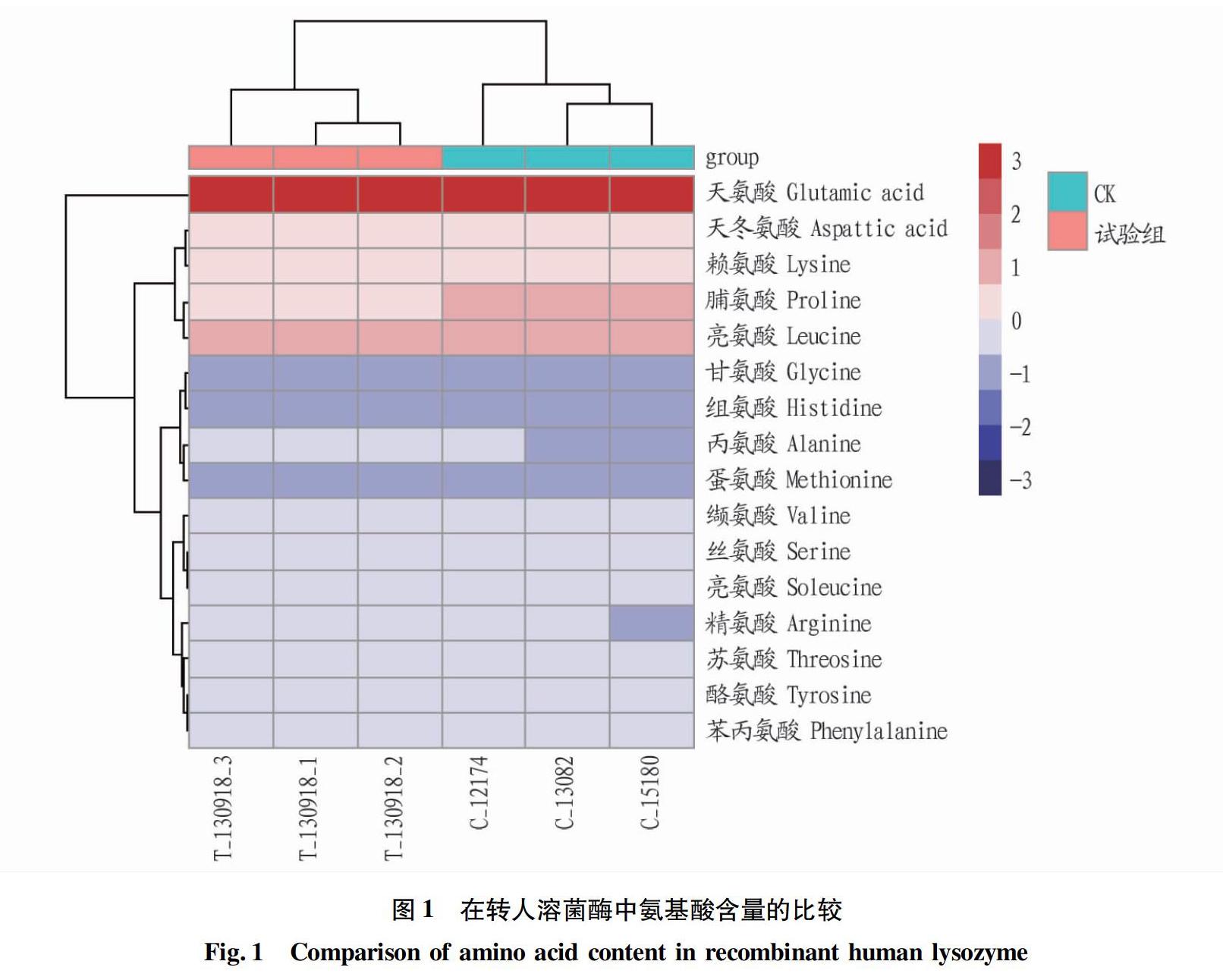
對轉人溶菌酶牛乳(試驗組)和非轉基因牛乳(CK)的16種氨基酸進行測定,結果見圖1。從圖1可見,這16種氨基酸除了脯氨酸(Proline)、丙氨酸(Alanine)含量略有差異外,其他氨基酸含量接近或者相同,這16種氨基酸含量在2組間總體上差異不顯著(P>0.05)。
2.1.3 乳中脂肪酸。
對轉人溶菌酶牛乳(試驗組)和非轉基因牛乳(CK)的牛乳中飽和脂肪酸和不飽和脂肪酸共25種脂肪酸進行測定,結果見圖2。從圖2可以看出,除了飽和脂肪酸C14∶0、C16∶0、C18∶0以及不飽和脂肪酸C18∶ln9c在2組之間存在差異,其他脂肪酸則在2組之間則無明顯變化,說明脂肪酸含量在2組間總體上差異不顯著(P>0.05)。
2.2 轉人溶菌酶牛乳代謝組結果與分析
基于GC-TOF-MS平臺在轉人溶菌酶牛乳與非轉基因牛乳組(CK)總共檢測出472種代謝物,對所有的代謝組進行主成分分析,從圖3發現,試驗組和CK并沒有明顯的聚類現象,且2組之間沒有顯著差異(P>0.05)。
2.3 重組人溶菌酶急性經口毒性試驗
2.3.1 大鼠急性經口毒性試驗。
給予大鼠重組人溶菌酶處理后,2 150 mg/kg組和4 640 mg/kg組大鼠均未見明顯中毒癥狀,試驗結束時未見有死亡的大鼠。在10 000 mg/kg劑量組,大鼠在最后一次灌胃后出現活動減少和精神不適癥狀。共死亡6只大鼠,其中雌、雄各3只。在觀察終點,存活4只大鼠,其中雌、雄各2只。21 500 mg/kg劑量組大鼠在第1次灌胃后出現活動減少、精神萎靡的癥狀,末次灌胃后1 h開始有死亡大鼠,24 h內全部死亡。觀察期間,對死亡大鼠進行大體解剖,主要觀察到胃發生腫脹,其他主要臟器未發現明顯異常。試驗結束時,對處死的大鼠進行解剖,未發生明顯的毒理學變化。
觀察期內動物體重呈增長相。至觀察終點時,10 000 mg/kg劑量組雌、雄性大鼠死亡率均為60%;21 500 mg/kg劑量組大鼠全部死亡,死亡率100%。經統計,重組人溶菌酶的大鼠急性經口毒性試驗的雌雄LD50均為9 260 mg/kg,95% MNDG可信區間為6 360~13 500 mg/kg[5]。
2.3.2 小鼠急性經口毒性試驗。
給予小鼠重組人溶菌酶處理后,4 640 mg/kg劑量組未發現明顯中毒癥狀及死亡的小鼠;10 000 mg/kg劑量組小鼠出現活動減少、精神萎靡等癥狀,24 h內雌、雄小鼠各有1只死亡,試驗結束時,雌、雄小鼠各有4只存活。21 500 mg/kg劑量組,小鼠出現活動減少、精神萎靡等癥狀,1 h后出現死亡,在24 h內所有受試小鼠出現死亡。46 400 mg/kg劑量組,小鼠首次灌胃重組人溶菌酶后出現活動減少、精神萎靡等癥狀,1 h后出現死亡,4 h后最后一次灌胃重組人溶菌酶,在24 h內所有受試小鼠死亡。觀察期間,小鼠尸體解剖觀察到胃腫脹,其他主要器官未發現明顯異常。試驗結束時,小鼠死亡后的尸體解剖未發現明顯的毒理學變化。
觀察期內動物體重呈增長相。至觀察終點時,10 000 mg/kg劑量組,雌、雄小鼠各有1只死亡,死亡率均為20%;21 500 mg/kg劑量組,小鼠全部死亡,死亡率100%;至觀察終點時46 400 mg/kg 劑量組,小鼠全部死亡,死亡率100%。經過統計計算,重組人溶菌酶的小鼠急性經口毒性雌雄LD50為12 600 mg/kg,95%可信區間為9 260~17 100 mg/kg。
2.4 模擬胃腸液消化穩定性
2.4.1 模擬胃腸液試驗。SDS-PAGE 顯示(圖4),在模擬的胃液中重組人溶菌酶及其可見降解片段在2~30 min 內全部消化(3~7 孔道)。蛋白免疫印跡結果(圖5)顯示,重組人溶菌酶及其可見降解片段在模擬胃液(4~8 孔道)中 2~30 min 內全部消化。
2.4.2 重組人溶菌酶模擬腸液消化試驗 。
SDS-PAGE 結果顯示(圖4),在模擬腸液中重組人溶菌酶及其可見降解片段在0~15 s內全部消化(11~15 孔道)。蛋白免疫印跡結果顯示(圖6),重組人溶菌酶及其可見降解片段在模擬腸液(4~8 孔道)中0~15 s內全部消化。
3 結論與討論
在乳常規方面,轉基因牛乳的水分、乳糖、蛋白質含量和體細胞數等與非轉基因組無明顯變化,但脂肪含量試驗組低于CK,菌落總數高于對照組;轉基因牛乳中所測的16種氨基酸及25種脂肪酸含量在2組之間無明顯差異。在牛乳代謝組方面,轉人溶菌酶牛乳和非轉基因牛乳無明顯差異。
Laible等[6]研究表明,牛乳的乳成分容易發生變化。楊鵬華等[7]關于人乳鐵蛋白基因對牛乳成分影響的研究結果表明,轉基因牛乳與常乳在乳脂、總蛋白、乳糖和干物質的含量上無明顯變化,且外源蛋白的表達水平穩定。
毒理學研究決定是否能夠將新藥應用于臨床,并提供有關藥物的毒性劑量和治療指數的信息。同時科學、道德和法
規要求在將任何潛在的新藥供人類使用之前,必須在動物中研究其安全性以定義安全的人類劑量[8]。溶菌酶在醫藥、食品行業以及畜牧領域都有著比較廣泛的應用[9],而轉基因得到的重組人溶菌酶在投入應用之前,則需要進行毒理學方面的試驗,為今后的應用提供試驗支持。食品安全是指符合人體的營養需求,且不會對人體健康造成急性、亞慢性和慢性危害[10]。該研究通過大鼠和小鼠急性經口毒性試驗,結果表明,重組人溶菌酶屬于實際無毒蛋白;重組人溶菌酶模擬胃腸液消化穩定性試驗表明,重組人溶菌酶在胃腸液中都可消化。
周興華[11]對轉雙反義分支酶基因大米的急性毒性試驗研究表明,轉基因大米的LD50>21.50 g/kg,試驗期間,動物狀態良好,無死亡和異常現象。因此,轉雙反義分支酶基因大米屬無毒級別。
根據《食品安全國家標準急性經口毒性試驗》(GB 15193.3—2014)急性毒性(LD50)分級標準,大鼠和小鼠急性經口毒性試驗表明,重組人溶菌酶是一種實際無毒蛋白。模擬胃腸液消化穩定性試驗結果表明,重組人溶菌酶在模擬的胃液中可消化,在模擬的腸液中極易消化,初步說明重組人溶菌酶無潛在的致敏性。
參考文獻
[1] 王佃亮.重組人溶菌酶研究進展[J].中國生物工程雜志,2003,23(9):59-63.
[2] ITO Y,YAMADA H,IMOTO T.Colorimetric assay for lysozyme using Micrococcus luteus labeled with a blue dye,Remazol brilliant blue R,as a substrate[J].Chemical & pharmaceutical bulletin,1992,40(6):1523-1526.
[3] WANG C S,KLOER H U.Purification of human lysozyme from milk and pancreatic juice[J].Analytical biochemistry,1984,139(1):224-227.
[4] TAKAI I,ODA O,SHINZATO T,et al.Effective method for purification of lysozyme from human urine[J].Journal of chromatography B:Biomedical applications,1996,685(1):21-25.
[5]李亭,黃詩淇.急性經口毒性試驗方法研究進展[J].吉林化工學院學報,2019,36(1):11-14.
[6] LAIBLE G,BROPHY B,KNIGHTON D,et al.Compositional analysis of dairy products derived from clones and cloned transgenic cattle[J].Theriogenology,2007,67(1):166-177.
[7] 楊鵬華,倪鳳娥,李寧.利用轉基因牛生產重組人乳鐵蛋白研究[J].安徽農業科學,2008,36(35):15507-15509.
[8] AL-AFIFI N A,ALABSI A M,BAKRI M M,et al.Acute and sub-acute oral toxicity of Dracaena cinnabari resin methanol extract in rats[J].BMC complementary & alternative medicine,2018,18:1-14.
[9] 宋娟.溶菌酶的分離方法及進展[J].河南化工,2017,34(7):16-18.
[10] 李州霞.我國食品安全檢測主要應用技術的研究及現狀[J].食品界,2019(4):24-25.
[11] 周興華.兩種轉基因大米食用安全性的毒理學研究[D].鎮江:江蘇大學,2012.

